鲁教版化学九年级下册 第八单元 第二节 海水“制碱”课件(共15张PPT)
文档属性
| 名称 | 鲁教版化学九年级下册 第八单元 第二节 海水“制碱”课件(共15张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-21 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
第二节 海水“制碱”
反应后溶液中溶质成分的探究
想一想
实验室有两瓶失去标签的无色溶液,分别是碳酸钠溶液和氯化钡溶液,你能用什么方法将其区分呢?
加入氯化钡溶液
碳酸钠溶液
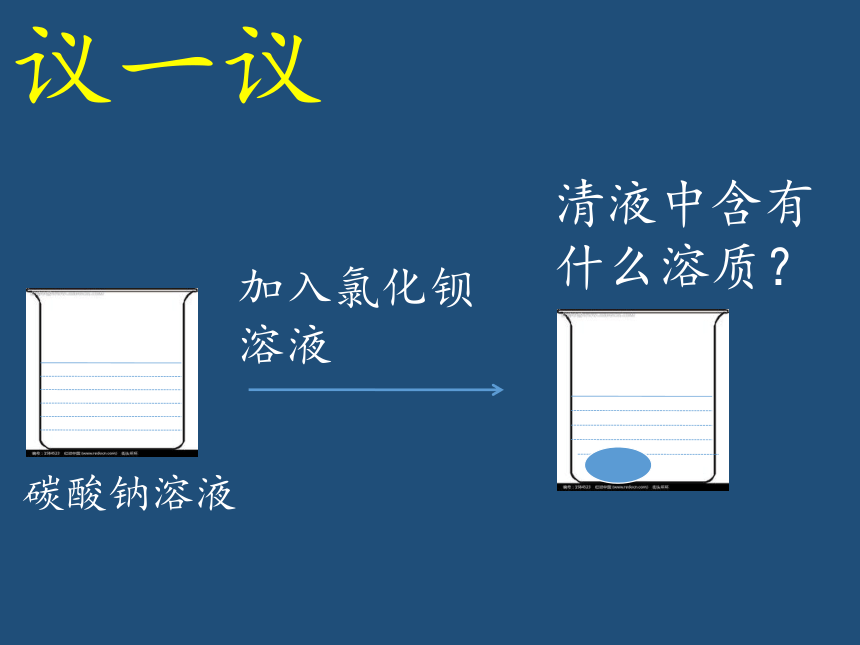
清液中含有什么溶质?
议一议
加入氯化钡溶液
碳酸钠溶液
清液中含有的溶质可能有三种情况
①NaCl
②NaCl和Na2CO3
③NaCl和BaCl2
你能总结出:反应后溶质成分的探究步骤吗?
反应后溶液中溶质成分的探究步骤:
1、读题,写出有关反应的化学方程式(一写)
2、找出产物和反应物 (二找)
3、判断各物质的溶解性,猜想溶质成分(溶质不含难溶性物质) (三猜)
思考:溶质成分能否是生成物和两种反应物同时存在?
不能,因为两种反应物同时存在就会继续反应直到其中一种反应物完全反应
①只含有生成物
②含生成物和一种反应物
③含生成物和另一种反应物
(有一种反应物过量)
(恰好完全反应)
试一试
1、过量铁粉与稀盐酸反应后的溶质成分是
FeCl2
2、铁粉与稀盐酸反应后的溶质成分是
FeCl2
或FeCl2和HCl
加入氯化钡溶液
碳酸钠溶液
清液中含有的溶质可能有三种情况
①NaCl
②NaCl和Na2CO3
③NaCl和BaCl2
如何来确定废液中的溶质到底是什么?
反应后溶液中溶质成分的探究步骤:
1、读题,写出有关反应的化学方程式(一写)
2、找出产物和反应物 (二找)
3、判断各物质的溶解性,猜测溶质成分(溶质不含难溶性物质) (三猜)
①只含有生成物
②含生成物和一种反应物
③含生成物和另一种反应物
(有一种反应物
过量)
(恰好完全反应)
4、分析猜想,确定溶质成分。生成物一定有,反应物可能有,再根据反应物的性质确定其是否存在。 (四定)
3. 甲、乙同学在学完酸的化学性质后,做了如下实验:
【观察与讨论1】甲同学在做实验时没有观察到明显现象,于是对氢氧化钙溶液和稀盐酸能发生反 应表示怀疑。但乙同学认为,甲同学实验时向氢氧化钙溶液中应先滴几滴酚酞试液,再加入稀盐酸,当观察到(1)
,就可以说明两种物质能发生反应,写出甲试管中发生反应的化学方程式:
Ca(OH)2+2HCl=CaCl2+2H2O
变为无色时
溶液由红色
【观察与讨论2】实验结束,先将甲试管中的废液倒入废液缸中,然后将乙试管中的废液沿废液缸内壁缓慢倒入,观察到废液缸中先有气泡产生,然后又出现白色沉淀。由该现象可知:甲、乙试管废液中的溶质分别为
【提出问题】废液缸中的废液最终含有什么溶质?
【猜想与假设】猜想(1):废液中只含有氯化钠;猜想(2):废液中含有氯化钠、氯化钙;猜想(3)
甲:HCl和CaCl2、乙:Na2CO3和NaCl
废液中含有氯化钠、
碳酸钠
【活动与探究】取少量废液缸中的废液于试管中,滴加适量的
观察到 , , 则猜想3成立。
【表达与交流】甲、乙同学确认了最终废液中溶质的成分。你认为实验结束后,应该如何处理这些废液?
(4)______________________________。
BaCl2溶液
产生白色沉淀,
向废液缸中加入稀盐酸至不再产生气泡
,然后在排放这些废液。
本节课你学到了什么?
1. 反应后溶液中溶质成分的确定方法——“一写二找三猜四定”;
2、Na2CO3、BaCl2等常见盐的检验方法
3、“溶质成分的探究”类题目的审题、解题方法,
5、对反应产生的废液进行化学处理,增强环保意识。
4、 合作探究的学习方式。
再 见
谢 谢
第二节 海水“制碱”
反应后溶液中溶质成分的探究
想一想
实验室有两瓶失去标签的无色溶液,分别是碳酸钠溶液和氯化钡溶液,你能用什么方法将其区分呢?
加入氯化钡溶液
碳酸钠溶液
清液中含有什么溶质?
议一议
加入氯化钡溶液
碳酸钠溶液
清液中含有的溶质可能有三种情况
①NaCl
②NaCl和Na2CO3
③NaCl和BaCl2
你能总结出:反应后溶质成分的探究步骤吗?
反应后溶液中溶质成分的探究步骤:
1、读题,写出有关反应的化学方程式(一写)
2、找出产物和反应物 (二找)
3、判断各物质的溶解性,猜想溶质成分(溶质不含难溶性物质) (三猜)
思考:溶质成分能否是生成物和两种反应物同时存在?
不能,因为两种反应物同时存在就会继续反应直到其中一种反应物完全反应
①只含有生成物
②含生成物和一种反应物
③含生成物和另一种反应物
(有一种反应物过量)
(恰好完全反应)
试一试
1、过量铁粉与稀盐酸反应后的溶质成分是
FeCl2
2、铁粉与稀盐酸反应后的溶质成分是
FeCl2
或FeCl2和HCl
加入氯化钡溶液
碳酸钠溶液
清液中含有的溶质可能有三种情况
①NaCl
②NaCl和Na2CO3
③NaCl和BaCl2
如何来确定废液中的溶质到底是什么?
反应后溶液中溶质成分的探究步骤:
1、读题,写出有关反应的化学方程式(一写)
2、找出产物和反应物 (二找)
3、判断各物质的溶解性,猜测溶质成分(溶质不含难溶性物质) (三猜)
①只含有生成物
②含生成物和一种反应物
③含生成物和另一种反应物
(有一种反应物
过量)
(恰好完全反应)
4、分析猜想,确定溶质成分。生成物一定有,反应物可能有,再根据反应物的性质确定其是否存在。 (四定)
3. 甲、乙同学在学完酸的化学性质后,做了如下实验:
【观察与讨论1】甲同学在做实验时没有观察到明显现象,于是对氢氧化钙溶液和稀盐酸能发生反 应表示怀疑。但乙同学认为,甲同学实验时向氢氧化钙溶液中应先滴几滴酚酞试液,再加入稀盐酸,当观察到(1)
,就可以说明两种物质能发生反应,写出甲试管中发生反应的化学方程式:
Ca(OH)2+2HCl=CaCl2+2H2O
变为无色时
溶液由红色
【观察与讨论2】实验结束,先将甲试管中的废液倒入废液缸中,然后将乙试管中的废液沿废液缸内壁缓慢倒入,观察到废液缸中先有气泡产生,然后又出现白色沉淀。由该现象可知:甲、乙试管废液中的溶质分别为
【提出问题】废液缸中的废液最终含有什么溶质?
【猜想与假设】猜想(1):废液中只含有氯化钠;猜想(2):废液中含有氯化钠、氯化钙;猜想(3)
甲:HCl和CaCl2、乙:Na2CO3和NaCl
废液中含有氯化钠、
碳酸钠
【活动与探究】取少量废液缸中的废液于试管中,滴加适量的
观察到 , , 则猜想3成立。
【表达与交流】甲、乙同学确认了最终废液中溶质的成分。你认为实验结束后,应该如何处理这些废液?
(4)______________________________。
BaCl2溶液
产生白色沉淀,
向废液缸中加入稀盐酸至不再产生气泡
,然后在排放这些废液。
本节课你学到了什么?
1. 反应后溶液中溶质成分的确定方法——“一写二找三猜四定”;
2、Na2CO3、BaCl2等常见盐的检验方法
3、“溶质成分的探究”类题目的审题、解题方法,
5、对反应产生的废液进行化学处理,增强环保意识。
4、 合作探究的学习方式。
再 见
谢 谢
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
