第2节 分子晶体和原子晶体
图片预览






文档简介
课件24张PPT。2 分子晶体和原子晶体交流·讨论雪花、冰糖、食盐、水晶和电木(酚醛树脂)这些固体是否属于晶体?若不是晶体,请说明理由。
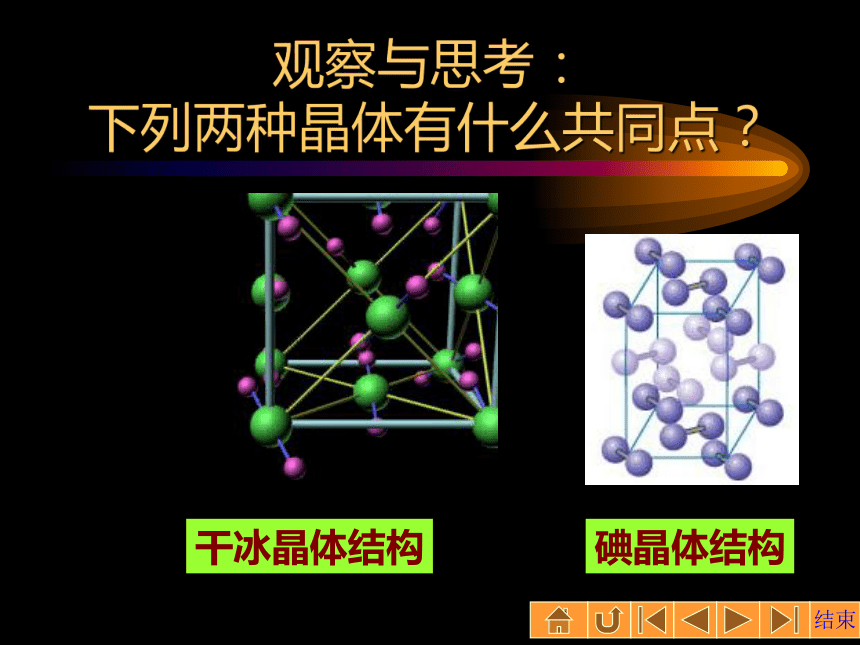
为什么不同的晶体,它们的物理性质各不相同?观察与思考: 下列两种晶体有什么共同点?碘晶体结构干冰晶体结构一、分子晶体概念
分子间以分子间作用力(范德华力,氢键)相结合的晶体叫分子晶体。
构成分子晶体的粒子是分子,粒子间的相互作用是分子间作用力。分子晶体有哪些物理特性,为什么?思考与交流一、分子晶体分子晶体的物理特性:
较低的熔点和沸点
较小的硬度
一般都是绝缘体,熔融状态也不导电。
原因:分子间作用力很弱一、分子晶体典型的分子晶体:
非金属氢化物:H2O,H2S,NH3,CH4,HX
酸:H2SO4,HNO3,H3PO4
部分非金属单质:X2,O2,H2, S8,P4, C60
部分非金属氧化物: CO2, SO2, NO2, P4O6, P4O10
大多数有机物:乙醇,冰醋酸,蔗糖一、分子晶体分子晶体结构特征
只有范德华力,无分子间氢键——分子密堆积
每个分子周围有12个紧邻的分子,如:C60、干冰 、I2、O2
有分子间氢键——不具有分子密堆积特征
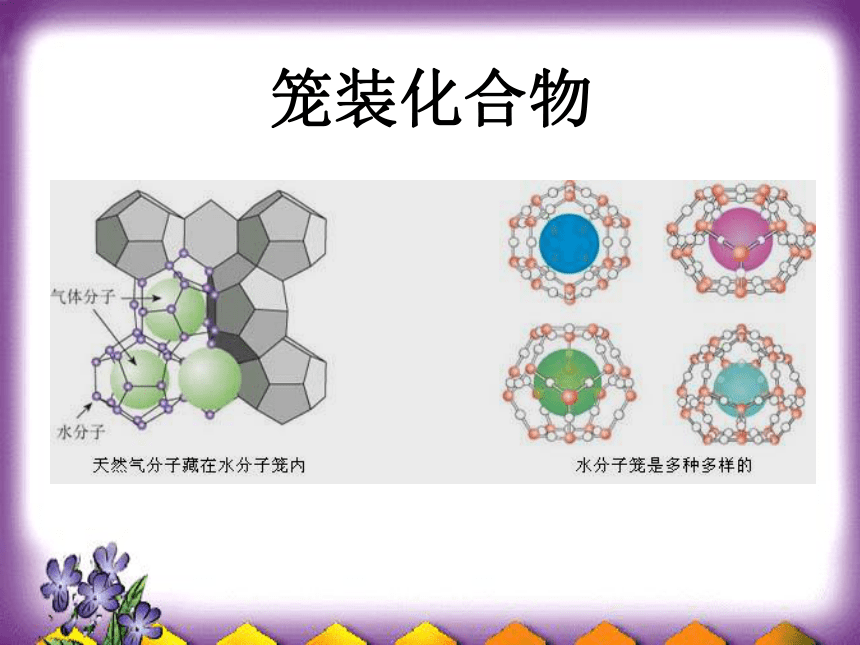
如:HF 、冰、NH3 笼装化合物思考与交流CO2和SiO2的一些物理性质如下表所示,通过比较试判断SiO2晶体是否属于分子晶体。
碳元素和硅元素处于元素周期表中同一主族,为什么CO2晶体的熔、沸点很低,而SiO2晶体的熔沸点很高?180o109o28′SiO共价键二氧化硅晶体结构示意图109o28′共价键金刚石的晶体结构示意图二.原子晶体(共价晶体)概念:
相邻原子间以共价键相结合而形成空间立体网状结构的晶体。
构成原子晶体的粒子是原子,原子间以较强的共价键相结合。金刚石观察·思考对比分子晶体和原子晶体的数据,原子晶体有何物理特性?原子晶体的物理特性在原子晶体中,由于原子间以较强的共价键相结合,而且形成空间立体网状结构,所以原子晶体的
熔点和沸点高
硬度大
一般不导电
且难溶于一些常见的溶剂常见的原子晶体某些非金属单质:
金刚石(C)、晶体硅(Si)、晶体硼(B)、晶体锗(Ge)等
某些非金属化合物:
碳化硅(SiC)晶体、氮化硼(BN)晶体
某些氧化物:
二氧化硅( SiO2)晶体、Al2O3解释:结构相似的原子晶体,原子半径越小,键长越短,键能越大,晶体熔点越高
金刚石>硅>锗交流与研讨1、怎样从原子结构角度理解金刚石、硅和锗的熔点和硬度依次下降?2、“具有共价键的晶体叫做原子晶体”。这种说法对吗?为什么?石墨晶体结构知识拓展-石墨石墨石墨为什么很软?
石墨为层状结构,各层之间是范德华力结合,容易滑动,所以石墨很软。
石墨的熔沸点为什么很高(高于金刚石)?
石墨各层均为平面网状结构,碳原子之间存在很强的共价键(大π键),故熔沸点很高。
石墨属于哪类晶体?为什么?
石墨为混合键型晶体讨论·总结分子晶体有什么特点?
哪些晶体是分子晶体?
原子晶体有什么特点?哪些晶体是原子晶体?
氢键对分子晶体的结构与性质有何影响?
总结对比原子晶体和分子晶体的差异。原子晶体和分子晶体的差异分子的密堆积(与每个分子距离最近的相同分子共有12个 )氧(O2)的晶体结构碳60的晶胞分子的密堆积(与CO2分子距离最近的CO2分子共有12个 )干冰的晶体结构图冰中1个水分子周围有4个水分子冰的结构氢键具有方向性分子的非密堆积
为什么不同的晶体,它们的物理性质各不相同?观察与思考: 下列两种晶体有什么共同点?碘晶体结构干冰晶体结构一、分子晶体概念
分子间以分子间作用力(范德华力,氢键)相结合的晶体叫分子晶体。
构成分子晶体的粒子是分子,粒子间的相互作用是分子间作用力。分子晶体有哪些物理特性,为什么?思考与交流一、分子晶体分子晶体的物理特性:
较低的熔点和沸点
较小的硬度
一般都是绝缘体,熔融状态也不导电。
原因:分子间作用力很弱一、分子晶体典型的分子晶体:
非金属氢化物:H2O,H2S,NH3,CH4,HX
酸:H2SO4,HNO3,H3PO4
部分非金属单质:X2,O2,H2, S8,P4, C60
部分非金属氧化物: CO2, SO2, NO2, P4O6, P4O10
大多数有机物:乙醇,冰醋酸,蔗糖一、分子晶体分子晶体结构特征
只有范德华力,无分子间氢键——分子密堆积
每个分子周围有12个紧邻的分子,如:C60、干冰 、I2、O2
有分子间氢键——不具有分子密堆积特征
如:HF 、冰、NH3 笼装化合物思考与交流CO2和SiO2的一些物理性质如下表所示,通过比较试判断SiO2晶体是否属于分子晶体。
碳元素和硅元素处于元素周期表中同一主族,为什么CO2晶体的熔、沸点很低,而SiO2晶体的熔沸点很高?180o109o28′SiO共价键二氧化硅晶体结构示意图109o28′共价键金刚石的晶体结构示意图二.原子晶体(共价晶体)概念:
相邻原子间以共价键相结合而形成空间立体网状结构的晶体。
构成原子晶体的粒子是原子,原子间以较强的共价键相结合。金刚石观察·思考对比分子晶体和原子晶体的数据,原子晶体有何物理特性?原子晶体的物理特性在原子晶体中,由于原子间以较强的共价键相结合,而且形成空间立体网状结构,所以原子晶体的
熔点和沸点高
硬度大
一般不导电
且难溶于一些常见的溶剂常见的原子晶体某些非金属单质:
金刚石(C)、晶体硅(Si)、晶体硼(B)、晶体锗(Ge)等
某些非金属化合物:
碳化硅(SiC)晶体、氮化硼(BN)晶体
某些氧化物:
二氧化硅( SiO2)晶体、Al2O3解释:结构相似的原子晶体,原子半径越小,键长越短,键能越大,晶体熔点越高
金刚石>硅>锗交流与研讨1、怎样从原子结构角度理解金刚石、硅和锗的熔点和硬度依次下降?2、“具有共价键的晶体叫做原子晶体”。这种说法对吗?为什么?石墨晶体结构知识拓展-石墨石墨石墨为什么很软?
石墨为层状结构,各层之间是范德华力结合,容易滑动,所以石墨很软。
石墨的熔沸点为什么很高(高于金刚石)?
石墨各层均为平面网状结构,碳原子之间存在很强的共价键(大π键),故熔沸点很高。
石墨属于哪类晶体?为什么?
石墨为混合键型晶体讨论·总结分子晶体有什么特点?
哪些晶体是分子晶体?
原子晶体有什么特点?哪些晶体是原子晶体?
氢键对分子晶体的结构与性质有何影响?
总结对比原子晶体和分子晶体的差异。原子晶体和分子晶体的差异分子的密堆积(与每个分子距离最近的相同分子共有12个 )氧(O2)的晶体结构碳60的晶胞分子的密堆积(与CO2分子距离最近的CO2分子共有12个 )干冰的晶体结构图冰中1个水分子周围有4个水分子冰的结构氢键具有方向性分子的非密堆积
