粤教版化学九年级上册同步课时练习:2.1 空气的成分 第1课时 空气中氧气含量的测定、空气的成分(Word 含答案)
文档属性
| 名称 | 粤教版化学九年级上册同步课时练习:2.1 空气的成分 第1课时 空气中氧气含量的测定、空气的成分(Word 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 234.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-22 00:00:00 | ||
图片预览


文档简介
2.1 空气的成分
第1课时 空气中氧气含量的测定、空气的成分
知识点 1 氧气含量的测定
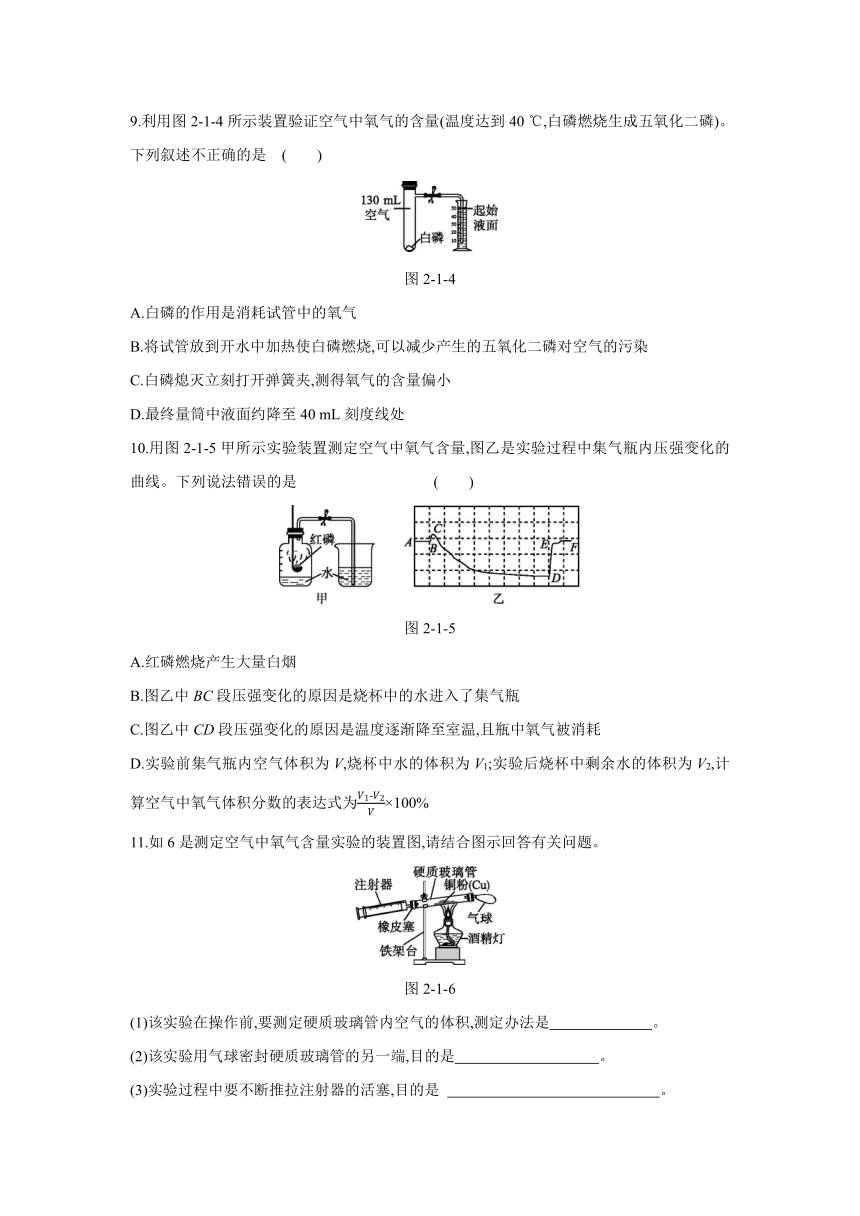
1.[2020·广州] 测定空气中氧气含量的实验装置如1,步骤如图下(已完成装置气密性检查):①在集气瓶内加入少量水,并将水面上方空间分为5等份;②用弹簧夹夹紧胶皮管;③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;④红磷熄灭后,立即打开弹簧夹,观察现象。其中有错误的实验步骤是 ( )
图2-1-1
A.① B.② C.③ D.④
2.如2为实验室用于测定空气中氧气体积分数的常用装置。请回答下列问题。
图2-1-2
(1)燃烧匙内放过量的红磷目的是 。
(2)红磷燃烧的文字表达式为 ,该反应的现象是 ,打开止水夹观察到的现象为 。
(3)该实验得出的结论是 。
(4)该实验后瓶中剩余气体主要为氮气(N2),请推测氮气的物理性质和化学性质各一条: 、 。
知识点 2 空气的成分
3.下列物质中,不属于空气成分的是 ( )
A.二氧化碳(CO2) B.氮气(N2)
C.氦气(He) D.二氧化硫(SO2)
4.下列关于空气中各成分含量的描述错误的是( )
A.氧气占空气总体积的21%
B.氮气占空气总体积的78%
C.稀有气体占空气总体积的0.03%
D.二氧化碳占空气总体积的0.03%
5.到云南省迪庆州梅里雪山旅游时,有人常常会感到呼吸困难,这是因为空气成分中 ( )
A.氧气的体积分数远大于21%
B.氮气的体积分数远小于78%
C.氧气的体积分数仍为21%,主要是由于高原空气稀薄
D.二氧化碳的含量太高
6.请用事实说明空气中含有下列成分。
(1) ,说明空气中含有氧气。
(2) ,说明空气中含有水蒸气。
(3) ,说明空气中含有二氧化碳。
7.如3为空气成分示意图(按体积分数计算),其中“X”代表的是 ( )
图2-1-3
A.氧气(O2)
B.二氧化碳(CO2)
C.氮气(N2)
D.稀有气体
8.下列对空气的叙述正确的是 ( )
A.按质量分数计,空气中含氧气约21%,含氮气约78%
B.空气的成分是固定不变的
C.空气的成分是相对稳定的,主要是由氮气和氧气组成的
D.空气中的氧气可以供给呼吸,所以浓度越高越好,其他成分含量高低无关紧要
9.利用图2-1-4所示装置验证空气中氧气的含量(温度达到40 ℃,白磷燃烧生成五氧化二磷)。下列叙述不正确的是 ( )
图2-1-4
A.白磷的作用是消耗试管中的氧气
B.将试管放到开水中加热使白磷燃烧,可以减少产生的五氧化二磷对空气的污染
C.白磷熄灭立刻打开弹簧夹,测得氧气的含量偏小
D.最终量筒中液面约降至40 mL刻度线处
10.用图2-1-5甲所示实验装置测定空气中氧气含量,图乙是实验过程中集气瓶内压强变化的曲线。下列说法错误的是 ( )
图2-1-5
A.红磷燃烧产生大量白烟
B.图乙中BC段压强变化的原因是烧杯中的水进入了集气瓶
C.图乙中CD段压强变化的原因是温度逐渐降至室温,且瓶中氧气被消耗
D.实验前集气瓶内空气体积为V,烧杯中水的体积为V1;实验后烧杯中剩余水的体积为V2,计算空气中氧气体积分数的表达式为×100%
11.如6是测定空气中氧气含量实验的装置图,请结合图示回答有关问题。
图2-1-6
(1)该实验在操作前,要测定硬质玻璃管内空气的体积,测定办法是 。
(2)该实验用气球密封硬质玻璃管的另一端,目的是 。
(3)实验过程中要不断推拉注射器的活塞,目的是 。
(4)实验前,若硬质玻璃管中空气的体积为25 mL,注射器中空气的体积为15 mL,反应结束后,测得注射器中气体的体积为9 mL,则该实验测得空气中氧气的体积分数为 。
(5)该实验测得的结果偏小,可能的原因: 、 (列举两条)。
考|题|展|示
12.[2020·张家界改编] 空气是一种宝贵的自然资源。下列有关空气的说法中不正确的是 ( )
A.稀有气体在空气中的体积分数为0.94%
B.氧气在空气中的体积分数为78%
C.氦气、氖气都属于稀有气体
D.空气中二氧化碳的含量是相对稳定的
13.[2020·嘉兴] 为提高测定空气中氧气含量实验的精确度,化学兴趣小组对教材实验进行了创新改进(如7)。
图2-1-7
[实验步骤] ①取一根玻璃管,用橡皮塞将一端密封;②将食品脱氧剂粉末装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端标为A,弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为O,如图图甲所示;③水平滚动玻璃管,使食品脱氧剂粉末平铺在玻璃管中,静置至水滴不再移动时,水滴的右端标为B,如图图乙所示;④用刻度尺测量出AO段和AB段的长度,并计算出AB与AO的比值,将数据记录在表格中。
实验次数 AO/mm AB/mm
1 523.5 109.5 0.2092
2 525.5 110.0 0.2093
3 527.0 110.5 0.2097
[得出结论] 根据表格中的实验数据,可知空气中氧气含量为 (用百分数表示)。
[思考讨论]
(1)实验步骤③中,将食品脱氧剂粉末平铺在玻璃管中的目的是 。
(2)实验步骤②中,如图果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因是 。
答案
1.D ①在集气瓶内加入少量水可以起到降温、吸收五氧化二磷的作用;为了观察进入瓶中水的体积,将水面上方空间分为5等份; ②用弹簧夹夹紧胶皮管,防止受热时瓶内气体逸出; ③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,防止红磷燃烧放热使气体逸出,可减小误差; ④红磷熄灭后,没有冷却至室温就打开弹簧夹,会使测定结果偏小。
2.(1)使瓶内的氧气完全反应
(2)红磷+氧气五氧化二磷 放出热量,产生大量白烟 水沿导管进入集气瓶且进入水的体积约占集气瓶内原空气体积的
(3)氧气约占空气体积的
(4)难溶于水 不能燃烧(或不支持燃烧)
3.D 空气的成分有氧气、氮气、二氧化碳、稀有气体等,但不包括二氧化硫。
4.C 5.C
6.(1)蜡烛可以在空气中燃烧(合理即可)
(2)酥脆的饼干放在空气中变软(合理即可)
(3)澄清石灰水在空气中放置一段时间后,表面出现一层白膜(合理即可)
7.C
8.C 按体积分数计,空气中含氧气约21%,含氮气约78%,不是质量分数;空气的成分一般是不变的,但不是固定不变的;空气中的氧气可以供给呼吸,但含量要在一定的范围内,不是浓度越高越好,其他成分含量也都要在一定范围内。
9.D 130 mL空气中氧气的含量为26 mL,则最终量筒中液面约降至24 mL刻度线处。
10.B 图乙中BC段压强变化的原因是红磷燃烧放热,导致气体膨胀,压强增大;CD段压强变化的原因是温度逐渐降至室温,且瓶中氧气被消耗;DE段是因为水进入集气瓶补充消耗的氧气的体积,压强慢慢恢复至大气压。
11.(1)利用注射器向硬质玻璃管内注水,注满时水的体积就是硬质玻璃管内空气的体积(合理即可)
(2)缓冲,防止加热时橡皮塞飞出
(3)使空气中的氧气与铜粉充分反应
(4)15%
(5)装置漏气 铜粉的量不足(合理即可)
(1)注射器上有刻度,要测定硬质玻璃管内空气的体积,可利用注射器向硬质玻璃管内注水,注满时水的体积就是硬质玻璃管内空气的体积。(2)在实验加热过程中,硬质玻璃管内气体膨胀,小气球的作用是缓冲,防止橡皮塞飞出。(3)实验过程中要不断推拉注射器的活塞,目的是使空气中的氧气与铜粉充分反应。(4)硬质玻璃管中空气的体积为25 mL,注射器中空气的体积为15 mL,反应结束后,测得注射器中气体体积为9 mL,则氧气的体积分数为×100%=15%。(5)该实验测得的结果偏小,可能的原因是装置漏气、铜粉的量不足等。
12.B 空气中各成分的含量都是相对稳定的,氧气的体积分数为21%,氮气的体积分数为78%,稀有气体的体积分数为0.94%。
13.[得出结论] 20.94%
[思考讨论] (1)增大接触面积,使氧气被脱氧剂粉末充分吸收 (2)粉末分布不够紧密,导致空气柱(AO段的长度)测量值偏小
根据实验设计,AO的长度代表空气体积大小,AB的长度代表氧气体积大小,即为空气中氧气含量,通过计算三次实验的平均值,即可求出空气中氧气的含量为:×100%=20.94%。
第1课时 空气中氧气含量的测定、空气的成分
知识点 1 氧气含量的测定
1.[2020·广州] 测定空气中氧气含量的实验装置如1,步骤如图下(已完成装置气密性检查):①在集气瓶内加入少量水,并将水面上方空间分为5等份;②用弹簧夹夹紧胶皮管;③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;④红磷熄灭后,立即打开弹簧夹,观察现象。其中有错误的实验步骤是 ( )
图2-1-1
A.① B.② C.③ D.④
2.如2为实验室用于测定空气中氧气体积分数的常用装置。请回答下列问题。
图2-1-2
(1)燃烧匙内放过量的红磷目的是 。
(2)红磷燃烧的文字表达式为 ,该反应的现象是 ,打开止水夹观察到的现象为 。
(3)该实验得出的结论是 。
(4)该实验后瓶中剩余气体主要为氮气(N2),请推测氮气的物理性质和化学性质各一条: 、 。
知识点 2 空气的成分
3.下列物质中,不属于空气成分的是 ( )
A.二氧化碳(CO2) B.氮气(N2)
C.氦气(He) D.二氧化硫(SO2)
4.下列关于空气中各成分含量的描述错误的是( )
A.氧气占空气总体积的21%
B.氮气占空气总体积的78%
C.稀有气体占空气总体积的0.03%
D.二氧化碳占空气总体积的0.03%
5.到云南省迪庆州梅里雪山旅游时,有人常常会感到呼吸困难,这是因为空气成分中 ( )
A.氧气的体积分数远大于21%
B.氮气的体积分数远小于78%
C.氧气的体积分数仍为21%,主要是由于高原空气稀薄
D.二氧化碳的含量太高
6.请用事实说明空气中含有下列成分。
(1) ,说明空气中含有氧气。
(2) ,说明空气中含有水蒸气。
(3) ,说明空气中含有二氧化碳。
7.如3为空气成分示意图(按体积分数计算),其中“X”代表的是 ( )
图2-1-3
A.氧气(O2)
B.二氧化碳(CO2)
C.氮气(N2)
D.稀有气体
8.下列对空气的叙述正确的是 ( )
A.按质量分数计,空气中含氧气约21%,含氮气约78%
B.空气的成分是固定不变的
C.空气的成分是相对稳定的,主要是由氮气和氧气组成的
D.空气中的氧气可以供给呼吸,所以浓度越高越好,其他成分含量高低无关紧要
9.利用图2-1-4所示装置验证空气中氧气的含量(温度达到40 ℃,白磷燃烧生成五氧化二磷)。下列叙述不正确的是 ( )
图2-1-4
A.白磷的作用是消耗试管中的氧气
B.将试管放到开水中加热使白磷燃烧,可以减少产生的五氧化二磷对空气的污染
C.白磷熄灭立刻打开弹簧夹,测得氧气的含量偏小
D.最终量筒中液面约降至40 mL刻度线处
10.用图2-1-5甲所示实验装置测定空气中氧气含量,图乙是实验过程中集气瓶内压强变化的曲线。下列说法错误的是 ( )
图2-1-5
A.红磷燃烧产生大量白烟
B.图乙中BC段压强变化的原因是烧杯中的水进入了集气瓶
C.图乙中CD段压强变化的原因是温度逐渐降至室温,且瓶中氧气被消耗
D.实验前集气瓶内空气体积为V,烧杯中水的体积为V1;实验后烧杯中剩余水的体积为V2,计算空气中氧气体积分数的表达式为×100%
11.如6是测定空气中氧气含量实验的装置图,请结合图示回答有关问题。
图2-1-6
(1)该实验在操作前,要测定硬质玻璃管内空气的体积,测定办法是 。
(2)该实验用气球密封硬质玻璃管的另一端,目的是 。
(3)实验过程中要不断推拉注射器的活塞,目的是 。
(4)实验前,若硬质玻璃管中空气的体积为25 mL,注射器中空气的体积为15 mL,反应结束后,测得注射器中气体的体积为9 mL,则该实验测得空气中氧气的体积分数为 。
(5)该实验测得的结果偏小,可能的原因: 、 (列举两条)。
考|题|展|示
12.[2020·张家界改编] 空气是一种宝贵的自然资源。下列有关空气的说法中不正确的是 ( )
A.稀有气体在空气中的体积分数为0.94%
B.氧气在空气中的体积分数为78%
C.氦气、氖气都属于稀有气体
D.空气中二氧化碳的含量是相对稳定的
13.[2020·嘉兴] 为提高测定空气中氧气含量实验的精确度,化学兴趣小组对教材实验进行了创新改进(如7)。
图2-1-7
[实验步骤] ①取一根玻璃管,用橡皮塞将一端密封;②将食品脱氧剂粉末装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端标为A,弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为O,如图图甲所示;③水平滚动玻璃管,使食品脱氧剂粉末平铺在玻璃管中,静置至水滴不再移动时,水滴的右端标为B,如图图乙所示;④用刻度尺测量出AO段和AB段的长度,并计算出AB与AO的比值,将数据记录在表格中。
实验次数 AO/mm AB/mm
1 523.5 109.5 0.2092
2 525.5 110.0 0.2093
3 527.0 110.5 0.2097
[得出结论] 根据表格中的实验数据,可知空气中氧气含量为 (用百分数表示)。
[思考讨论]
(1)实验步骤③中,将食品脱氧剂粉末平铺在玻璃管中的目的是 。
(2)实验步骤②中,如图果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因是 。
答案
1.D ①在集气瓶内加入少量水可以起到降温、吸收五氧化二磷的作用;为了观察进入瓶中水的体积,将水面上方空间分为5等份; ②用弹簧夹夹紧胶皮管,防止受热时瓶内气体逸出; ③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,防止红磷燃烧放热使气体逸出,可减小误差; ④红磷熄灭后,没有冷却至室温就打开弹簧夹,会使测定结果偏小。
2.(1)使瓶内的氧气完全反应
(2)红磷+氧气五氧化二磷 放出热量,产生大量白烟 水沿导管进入集气瓶且进入水的体积约占集气瓶内原空气体积的
(3)氧气约占空气体积的
(4)难溶于水 不能燃烧(或不支持燃烧)
3.D 空气的成分有氧气、氮气、二氧化碳、稀有气体等,但不包括二氧化硫。
4.C 5.C
6.(1)蜡烛可以在空气中燃烧(合理即可)
(2)酥脆的饼干放在空气中变软(合理即可)
(3)澄清石灰水在空气中放置一段时间后,表面出现一层白膜(合理即可)
7.C
8.C 按体积分数计,空气中含氧气约21%,含氮气约78%,不是质量分数;空气的成分一般是不变的,但不是固定不变的;空气中的氧气可以供给呼吸,但含量要在一定的范围内,不是浓度越高越好,其他成分含量也都要在一定范围内。
9.D 130 mL空气中氧气的含量为26 mL,则最终量筒中液面约降至24 mL刻度线处。
10.B 图乙中BC段压强变化的原因是红磷燃烧放热,导致气体膨胀,压强增大;CD段压强变化的原因是温度逐渐降至室温,且瓶中氧气被消耗;DE段是因为水进入集气瓶补充消耗的氧气的体积,压强慢慢恢复至大气压。
11.(1)利用注射器向硬质玻璃管内注水,注满时水的体积就是硬质玻璃管内空气的体积(合理即可)
(2)缓冲,防止加热时橡皮塞飞出
(3)使空气中的氧气与铜粉充分反应
(4)15%
(5)装置漏气 铜粉的量不足(合理即可)
(1)注射器上有刻度,要测定硬质玻璃管内空气的体积,可利用注射器向硬质玻璃管内注水,注满时水的体积就是硬质玻璃管内空气的体积。(2)在实验加热过程中,硬质玻璃管内气体膨胀,小气球的作用是缓冲,防止橡皮塞飞出。(3)实验过程中要不断推拉注射器的活塞,目的是使空气中的氧气与铜粉充分反应。(4)硬质玻璃管中空气的体积为25 mL,注射器中空气的体积为15 mL,反应结束后,测得注射器中气体体积为9 mL,则氧气的体积分数为×100%=15%。(5)该实验测得的结果偏小,可能的原因是装置漏气、铜粉的量不足等。
12.B 空气中各成分的含量都是相对稳定的,氧气的体积分数为21%,氮气的体积分数为78%,稀有气体的体积分数为0.94%。
13.[得出结论] 20.94%
[思考讨论] (1)增大接触面积,使氧气被脱氧剂粉末充分吸收 (2)粉末分布不够紧密,导致空气柱(AO段的长度)测量值偏小
根据实验设计,AO的长度代表空气体积大小,AB的长度代表氧气体积大小,即为空气中氧气含量,通过计算三次实验的平均值,即可求出空气中氧气的含量为:×100%=20.94%。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
