粤教版化学九年级下册同步课件:7.3 溶液浓稀的表示(第1课时)(共24张PPT)
文档属性
| 名称 | 粤教版化学九年级下册同步课件:7.3 溶液浓稀的表示(第1课时)(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-24 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
第七章 溶液
7.3 溶液浓稀的表示
第1课时 溶质质量分数及其简单计算
学习目标
1.明确溶液浓度的含义。
2.掌握溶液浓度的一种定量表示方式——溶质质量分数。
新知导入
如果把一只鸡蛋放入半杯水中,不断加食盐搅拌,你会看到什么?为什么会出现这样的现象呢?
新知导入
生理盐水对大家来说并不陌生,它是不是溶液?你知道标签上的这个0.9%是什么意思吗?
生理盐水标签上的这个0.9%是指的氯化钠溶液的浓度,它能准确地反应氯化钠溶液是浓还是稀。
那么溶液的浓度指的是什么?它应该如何计算呢?
新知探究
知道有色溶液颜色的深浅与溶液浓稀有关
新知探究
实验结论
有色溶液颜色的深浅,可粗略反映溶液的浓、稀。颜色越深,溶液越浓,颜色越浅,溶液越稀
新知探究
溶质的质量分数
定义
计算公式
含义
溶液中溶质的质量分数是溶质质量与溶液质量之比
=
每100g某溶液中溶质的质量。如某氯化钠溶液中溶质的质量分数为26.5%,其含义是100g该溶液中氯化钠的质量为26.5g。
新知探究
①溶质的质量指的是形成溶液的那部分溶质的质量,未溶解的不计算在内。
②溶液的质量 = 溶质的质量 + 溶剂的质量。
③计算时上下质量单位要统一,不要忘记×100%,最后结果要写成百分数。
④溶液中的溶质可以是一种或多种,物质的质量分数要在不超过其最大溶解量的范围时才有意义。
⑤溶液具有稳定性,只要外界条件不变,其溶质的质量分数不变。
新知探究
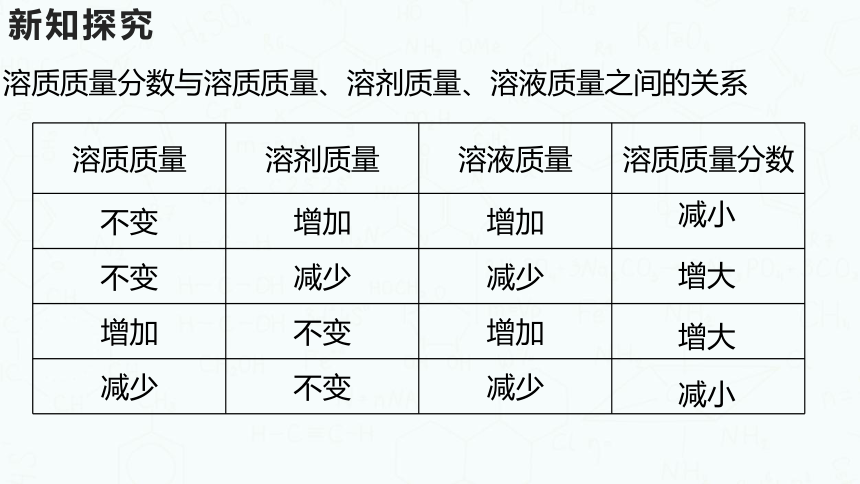
溶质质量分数与溶质质量、溶剂质量、溶液质量之间的关系
溶质质量 溶剂质量 溶液质量 溶质质量分数
不变 增加 增加
不变 减少 减少
增加 不变 增加
减少 不变 减少
减小
减小
增大
增大
新知探究
小试牛刀
溶质质量/g 溶剂质量/g 溶液质量/g 溶质质量分数
10 200
96 100
150 16%
20 80
190
5%
4%
24
126
100
20%
4
新知探究
质量分数与溶解度的区别与联系
溶解度 溶质质量分数
条件
溶剂量要求
溶液是否饱和
单位
在一定的温度下
不受外界条件的影响
100g
无要求
一定达到饱和
不一定
克(g)
是一个比值,单位为1
新知探究
饱和溶液的
溶质质量分数
溶解度S
100g+溶解度S
=
×100%
新知探究
典例训练
某氯化钠溶液的溶质质量分数为16%,它表示的含义是 ( )
A.溶液中含有氯化钠16g
B.溶液质量为100g
C.每100g溶液中含氯化钠16g
D.每100g水中溶解了16g氯化钠
C
新知探究
有关溶质质量分数的简单计算
=
溶质质量=溶液质量 x 溶质的质量分数
溶剂质量=溶液质量 – 溶质质量
溶液质量=
新知探究
小试牛刀
1.在20 C时,CuSO4的溶解度为25g,求20 C时CuSO4饱和溶液溶质的质量分数。
硫酸铜溶液溶质的质量分数= ×100%
= ×100%=20%
新知探究
有关溶液稀释、增浓问题的计算
1.稀释方法:加溶剂;用稀溶液稀释
2.稀释依据:稀释前后溶液中溶质的质量不变
3.关系式:A×a%=(A+m溶剂)×b%
A×a%+B×b%=(A+B)×c%
溶
液
稀
释
问
题
新知探究
典例训练
现在实验室只有溶质质量分数为37%的浓盐酸,要配制148g溶质质量分数为5%的稀盐酸,需要加水的质量为( )
A.20g B.25g
C.140.6g D.128g
D
新知探究
1.增浓方法:加溶质;蒸发溶剂;加浓溶液
2.关系式:A×a%+B=(A+B)×c%
A×a%=(A-B)×c%
A×a%+B×b% =(A+B)×c%
溶液增浓问题
新知探究
典例训练
有40g溶质质量分数为5%的氯化钙溶液,若将其溶质的质量分数增大到10%,求需加入氯化钙的质量。
解:设需加入氯化钙的质量为x
x≈2.22g
答:需加入氯化钙的质量为2.22g。
(40 g+x)
(40 g×5%+x)
×100%=10%
新知探究
有40g溶质质量分数为5%的氯化钙溶液,若将其溶质的质量分数增大到10%,需加入15%的CaCl2溶液的质量为多少?
解:需加入15%的CaCl2溶液的质量为z
z=40g
答:需加入15%的CaCl2溶液的质量为40g。
(40g+z)
(40g×5%)+(z×15%)
×100%=10%
典例训练
课堂小结
1.直接套用公式或变形公式
2.溶液稀释问题的计算(依据:稀释前后溶质的质量不变)
3.溶液增浓问题的计算
溶质的质量分数= ×100%
溶质的质量分数
计算公式
简单计算
溶质质量
溶液质量
课堂达标
1.常温下,把20 g氯化钠放在100 g水中,搅拌后氯化钠全部溶解。溶液中氯化钠的质量分数为( )
A.16.7%
B.20%
C.25%
D.18.5%
A
课堂达标
2.现有一杯20 ℃的硝酸钾饱和溶液,采取下列方法能改变其溶质的质量分数的是( )
A.加入一定量的固体硝酸钾
B.恒温蒸发部分水
C.将温度升高到60℃
D.加入一定量的水
D
谢 谢 观 看
第七章 溶液
7.3 溶液浓稀的表示
第1课时 溶质质量分数及其简单计算
学习目标
1.明确溶液浓度的含义。
2.掌握溶液浓度的一种定量表示方式——溶质质量分数。
新知导入
如果把一只鸡蛋放入半杯水中,不断加食盐搅拌,你会看到什么?为什么会出现这样的现象呢?
新知导入
生理盐水对大家来说并不陌生,它是不是溶液?你知道标签上的这个0.9%是什么意思吗?
生理盐水标签上的这个0.9%是指的氯化钠溶液的浓度,它能准确地反应氯化钠溶液是浓还是稀。
那么溶液的浓度指的是什么?它应该如何计算呢?
新知探究
知道有色溶液颜色的深浅与溶液浓稀有关
新知探究
实验结论
有色溶液颜色的深浅,可粗略反映溶液的浓、稀。颜色越深,溶液越浓,颜色越浅,溶液越稀
新知探究
溶质的质量分数
定义
计算公式
含义
溶液中溶质的质量分数是溶质质量与溶液质量之比
=
每100g某溶液中溶质的质量。如某氯化钠溶液中溶质的质量分数为26.5%,其含义是100g该溶液中氯化钠的质量为26.5g。
新知探究
①溶质的质量指的是形成溶液的那部分溶质的质量,未溶解的不计算在内。
②溶液的质量 = 溶质的质量 + 溶剂的质量。
③计算时上下质量单位要统一,不要忘记×100%,最后结果要写成百分数。
④溶液中的溶质可以是一种或多种,物质的质量分数要在不超过其最大溶解量的范围时才有意义。
⑤溶液具有稳定性,只要外界条件不变,其溶质的质量分数不变。
新知探究
溶质质量分数与溶质质量、溶剂质量、溶液质量之间的关系
溶质质量 溶剂质量 溶液质量 溶质质量分数
不变 增加 增加
不变 减少 减少
增加 不变 增加
减少 不变 减少
减小
减小
增大
增大
新知探究
小试牛刀
溶质质量/g 溶剂质量/g 溶液质量/g 溶质质量分数
10 200
96 100
150 16%
20 80
190
5%
4%
24
126
100
20%
4
新知探究
质量分数与溶解度的区别与联系
溶解度 溶质质量分数
条件
溶剂量要求
溶液是否饱和
单位
在一定的温度下
不受外界条件的影响
100g
无要求
一定达到饱和
不一定
克(g)
是一个比值,单位为1
新知探究
饱和溶液的
溶质质量分数
溶解度S
100g+溶解度S
=
×100%
新知探究
典例训练
某氯化钠溶液的溶质质量分数为16%,它表示的含义是 ( )
A.溶液中含有氯化钠16g
B.溶液质量为100g
C.每100g溶液中含氯化钠16g
D.每100g水中溶解了16g氯化钠
C
新知探究
有关溶质质量分数的简单计算
=
溶质质量=溶液质量 x 溶质的质量分数
溶剂质量=溶液质量 – 溶质质量
溶液质量=
新知探究
小试牛刀
1.在20 C时,CuSO4的溶解度为25g,求20 C时CuSO4饱和溶液溶质的质量分数。
硫酸铜溶液溶质的质量分数= ×100%
= ×100%=20%
新知探究
有关溶液稀释、增浓问题的计算
1.稀释方法:加溶剂;用稀溶液稀释
2.稀释依据:稀释前后溶液中溶质的质量不变
3.关系式:A×a%=(A+m溶剂)×b%
A×a%+B×b%=(A+B)×c%
溶
液
稀
释
问
题
新知探究
典例训练
现在实验室只有溶质质量分数为37%的浓盐酸,要配制148g溶质质量分数为5%的稀盐酸,需要加水的质量为( )
A.20g B.25g
C.140.6g D.128g
D
新知探究
1.增浓方法:加溶质;蒸发溶剂;加浓溶液
2.关系式:A×a%+B=(A+B)×c%
A×a%=(A-B)×c%
A×a%+B×b% =(A+B)×c%
溶液增浓问题
新知探究
典例训练
有40g溶质质量分数为5%的氯化钙溶液,若将其溶质的质量分数增大到10%,求需加入氯化钙的质量。
解:设需加入氯化钙的质量为x
x≈2.22g
答:需加入氯化钙的质量为2.22g。
(40 g+x)
(40 g×5%+x)
×100%=10%
新知探究
有40g溶质质量分数为5%的氯化钙溶液,若将其溶质的质量分数增大到10%,需加入15%的CaCl2溶液的质量为多少?
解:需加入15%的CaCl2溶液的质量为z
z=40g
答:需加入15%的CaCl2溶液的质量为40g。
(40g+z)
(40g×5%)+(z×15%)
×100%=10%
典例训练
课堂小结
1.直接套用公式或变形公式
2.溶液稀释问题的计算(依据:稀释前后溶质的质量不变)
3.溶液增浓问题的计算
溶质的质量分数= ×100%
溶质的质量分数
计算公式
简单计算
溶质质量
溶液质量
课堂达标
1.常温下,把20 g氯化钠放在100 g水中,搅拌后氯化钠全部溶解。溶液中氯化钠的质量分数为( )
A.16.7%
B.20%
C.25%
D.18.5%
A
课堂达标
2.现有一杯20 ℃的硝酸钾饱和溶液,采取下列方法能改变其溶质的质量分数的是( )
A.加入一定量的固体硝酸钾
B.恒温蒸发部分水
C.将温度升高到60℃
D.加入一定量的水
D
谢 谢 观 看
