粤教版化学九年级下册同步课件:7.4 结晶现象(共21张PPT)
文档属性
| 名称 | 粤教版化学九年级下册同步课件:7.4 结晶现象(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 38.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-24 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
第七章 溶液
7.4 结晶现象
学习目标
1.通过观察常见晶体的形成等活动,了解晶体和结晶的概念;
2.通过观察实验现象,知道因溶质溶解度随温度升降变化程度不同,分别采用降温结晶法和蒸发结晶法;
3.通过分析,学会过滤和结晶两种混合物分离方法的其适用范围;
4.通过分离混合物的活动,掌握粗盐中难溶杂质的实验方法。
新知导入
你喜欢清纯浪漫的雪景吗?大家对雪花了解多少?
雪花大都呈六角形,是一种晶体,每一片雪花都是一副精美的图案。
新知导入
美丽的化学
新知探究
什么是晶体呢?它是如何形成的?
晶体具有规则的形状,不同的晶体具有不同的形状。
新知探究
结晶
概念:热的溶液冷却后,不饱和溶液变成了饱和溶液,温度继续降低,
已溶解在溶液中的溶质会从溶液中以晶体的形式析出,这一过
程叫做结晶。
析出晶体后的溶液叫母液,母液对于析出的溶质来说,仍然是
饱和溶液。
条件:①溶液达到饱和状态②温度改变或溶剂减少
新知探究
我们知道氯化钠的溶解度随温度变化不大,那么氯化钠能用该方法结晶吗?
新知探究
冬天湖面上漂浮的纯碱晶体
夏天湖滩上晒出的食盐
“夏天晒盐,冬天捞碱”
新知探究
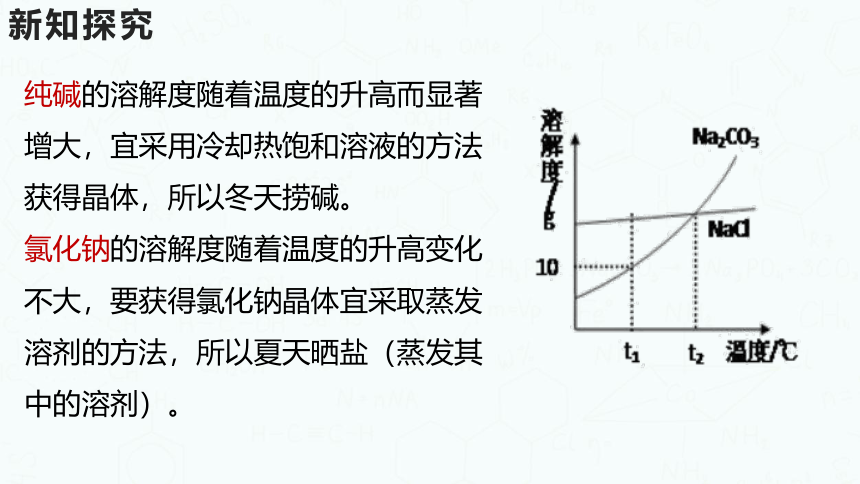
纯碱的溶解度随着温度的升高而显著增大,宜采用冷却热饱和溶液的方法获得晶体,所以冬天捞碱。
氯化钠的溶解度随着温度的升高变化不大,要获得氯化钠晶体宜采取蒸发溶剂的方法,所以夏天晒盐(蒸发其中的溶剂)。
新知探究
如何从含有少量NaCl的KNO3固体混合物中提纯KNO3 ?
高温下制成热饱和溶液(KNO3、NaCl)
冷却
大部分KNO3结晶析出
大部分NaCl仍留在溶液中
过滤
滤纸上有KNO3晶体
滤液中含大量的NaCl
转移固体
蒸发结晶
新知探究
结晶的方法
结晶方法 原理 应用举例
冷却热饱和溶液法 (降温结晶法) 将溶液制成较高温度下的饱和溶液,再降温冷却,析出晶体,过滤得到晶体 从KNO3饱和溶液中得到KNO3晶体
蒸发溶剂法(蒸发结晶法) 将溶液加热蒸发溶剂,使其达到饱和后,继续蒸发溶剂,溶质会结晶析出 海水晒盐
结晶
蒸发结晶
降温结晶
新知探究
海水晒盐
新知探究
结晶的应用——海水晒盐
海水
贮水池
蒸发池
结晶池
粗盐
母液
氯化钠
多种化工产品
原理:利用风吹和日晒使水分蒸发,食盐从海水中结晶析出
(将泥沙沉降)
(也叫苦卤,是氯化钠的饱和溶液)
新知探究
粗盐中有很多难溶性泥沙,如何除去氯化钠中的泥沙?
新知探究
在溶解、过滤、蒸发操作中都用到了玻璃棒,分别起什么作用
溶解:
玻璃棒起搅拌作用,目的是加速溶解。
过滤:
玻璃棒起引流作用。
蒸发:
玻璃棒起搅拌作用,防止液体局部过热造成液滴飞溅。
新知探究
典例训练
下列分析正确的是_____(填序号)。
A.海水进入贮水池,氯化钠的质量分数基本不变
B.在①的溶液中氯化钠的质量分数不改变
C.海洋中蕴藏着丰富的资源
D.析出晶体后的母液是食盐的不饱和溶液
海水提取食盐的方法主要为“盐田法”,其过程如下:
AC
课堂小结
结晶现象
晶体与结晶
什么是结晶
冷却结晶法:
蒸发溶剂结晶法:
粗盐的提纯
溶解
过滤
蒸发
原理
操作要领
玻璃棒的作用
课堂达标
1.下列关于结晶和晶体的说法,错误的是( )
A.饱和溶液降温析出晶体后的溶液仍是饱和溶液
B.降低饱和溶液的温度,不一定有晶体析出
C.溶液析出晶体后溶质质量分数一定增大
D.降温和蒸发是结晶的常用方法
C
课堂达标
2.如图是“粗盐中难溶性杂质的去除”的实验操作示意图。
(1)图中部分操作有错误,其中有的错误会导致精盐的产率明显偏低,其原因是_____________________________________
__________________。
蒸发时没有用玻璃棒搅拌,会导致液滴外
溅,造成氯化钠的流失
课堂达标
(2)仪器a的名称:__________。
(3)操作A中两个托盘各放一张干净的大小相同的纸片,其作用是_______________________________________。
(4)操作B中还需用到的仪器是________________。
(5)操作C中,倒入液体时液面要低于滤纸边缘主要是为了防止________(填序号)。
A.过滤速度慢 B.滤纸破损 C.杂质未经过滤就进入滤液
铁架台
防止粗盐腐蚀托盘,同时能使称量更准确
胶头滴管
C
谢 谢 观 看
第七章 溶液
7.4 结晶现象
学习目标
1.通过观察常见晶体的形成等活动,了解晶体和结晶的概念;
2.通过观察实验现象,知道因溶质溶解度随温度升降变化程度不同,分别采用降温结晶法和蒸发结晶法;
3.通过分析,学会过滤和结晶两种混合物分离方法的其适用范围;
4.通过分离混合物的活动,掌握粗盐中难溶杂质的实验方法。
新知导入
你喜欢清纯浪漫的雪景吗?大家对雪花了解多少?
雪花大都呈六角形,是一种晶体,每一片雪花都是一副精美的图案。
新知导入
美丽的化学
新知探究
什么是晶体呢?它是如何形成的?
晶体具有规则的形状,不同的晶体具有不同的形状。
新知探究
结晶
概念:热的溶液冷却后,不饱和溶液变成了饱和溶液,温度继续降低,
已溶解在溶液中的溶质会从溶液中以晶体的形式析出,这一过
程叫做结晶。
析出晶体后的溶液叫母液,母液对于析出的溶质来说,仍然是
饱和溶液。
条件:①溶液达到饱和状态②温度改变或溶剂减少
新知探究
我们知道氯化钠的溶解度随温度变化不大,那么氯化钠能用该方法结晶吗?
新知探究
冬天湖面上漂浮的纯碱晶体
夏天湖滩上晒出的食盐
“夏天晒盐,冬天捞碱”
新知探究
纯碱的溶解度随着温度的升高而显著增大,宜采用冷却热饱和溶液的方法获得晶体,所以冬天捞碱。
氯化钠的溶解度随着温度的升高变化不大,要获得氯化钠晶体宜采取蒸发溶剂的方法,所以夏天晒盐(蒸发其中的溶剂)。
新知探究
如何从含有少量NaCl的KNO3固体混合物中提纯KNO3 ?
高温下制成热饱和溶液(KNO3、NaCl)
冷却
大部分KNO3结晶析出
大部分NaCl仍留在溶液中
过滤
滤纸上有KNO3晶体
滤液中含大量的NaCl
转移固体
蒸发结晶
新知探究
结晶的方法
结晶方法 原理 应用举例
冷却热饱和溶液法 (降温结晶法) 将溶液制成较高温度下的饱和溶液,再降温冷却,析出晶体,过滤得到晶体 从KNO3饱和溶液中得到KNO3晶体
蒸发溶剂法(蒸发结晶法) 将溶液加热蒸发溶剂,使其达到饱和后,继续蒸发溶剂,溶质会结晶析出 海水晒盐
结晶
蒸发结晶
降温结晶
新知探究
海水晒盐
新知探究
结晶的应用——海水晒盐
海水
贮水池
蒸发池
结晶池
粗盐
母液
氯化钠
多种化工产品
原理:利用风吹和日晒使水分蒸发,食盐从海水中结晶析出
(将泥沙沉降)
(也叫苦卤,是氯化钠的饱和溶液)
新知探究
粗盐中有很多难溶性泥沙,如何除去氯化钠中的泥沙?
新知探究
在溶解、过滤、蒸发操作中都用到了玻璃棒,分别起什么作用
溶解:
玻璃棒起搅拌作用,目的是加速溶解。
过滤:
玻璃棒起引流作用。
蒸发:
玻璃棒起搅拌作用,防止液体局部过热造成液滴飞溅。
新知探究
典例训练
下列分析正确的是_____(填序号)。
A.海水进入贮水池,氯化钠的质量分数基本不变
B.在①的溶液中氯化钠的质量分数不改变
C.海洋中蕴藏着丰富的资源
D.析出晶体后的母液是食盐的不饱和溶液
海水提取食盐的方法主要为“盐田法”,其过程如下:
AC
课堂小结
结晶现象
晶体与结晶
什么是结晶
冷却结晶法:
蒸发溶剂结晶法:
粗盐的提纯
溶解
过滤
蒸发
原理
操作要领
玻璃棒的作用
课堂达标
1.下列关于结晶和晶体的说法,错误的是( )
A.饱和溶液降温析出晶体后的溶液仍是饱和溶液
B.降低饱和溶液的温度,不一定有晶体析出
C.溶液析出晶体后溶质质量分数一定增大
D.降温和蒸发是结晶的常用方法
C
课堂达标
2.如图是“粗盐中难溶性杂质的去除”的实验操作示意图。
(1)图中部分操作有错误,其中有的错误会导致精盐的产率明显偏低,其原因是_____________________________________
__________________。
蒸发时没有用玻璃棒搅拌,会导致液滴外
溅,造成氯化钠的流失
课堂达标
(2)仪器a的名称:__________。
(3)操作A中两个托盘各放一张干净的大小相同的纸片,其作用是_______________________________________。
(4)操作B中还需用到的仪器是________________。
(5)操作C中,倒入液体时液面要低于滤纸边缘主要是为了防止________(填序号)。
A.过滤速度慢 B.滤纸破损 C.杂质未经过滤就进入滤液
铁架台
防止粗盐腐蚀托盘,同时能使称量更准确
胶头滴管
C
谢 谢 观 看
