粤教版化学九年级下册同步课时练习:7.3 第2课时 配制一定溶质质量分数的溶液(word版有答案)
文档属性
| 名称 | 粤教版化学九年级下册同步课时练习:7.3 第2课时 配制一定溶质质量分数的溶液(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 148.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-24 00:00:00 | ||
图片预览

文档简介
第2课时 配制一定溶质质量分数的溶液
知识点 1 配制一定溶质质量分数的溶液的操作步骤
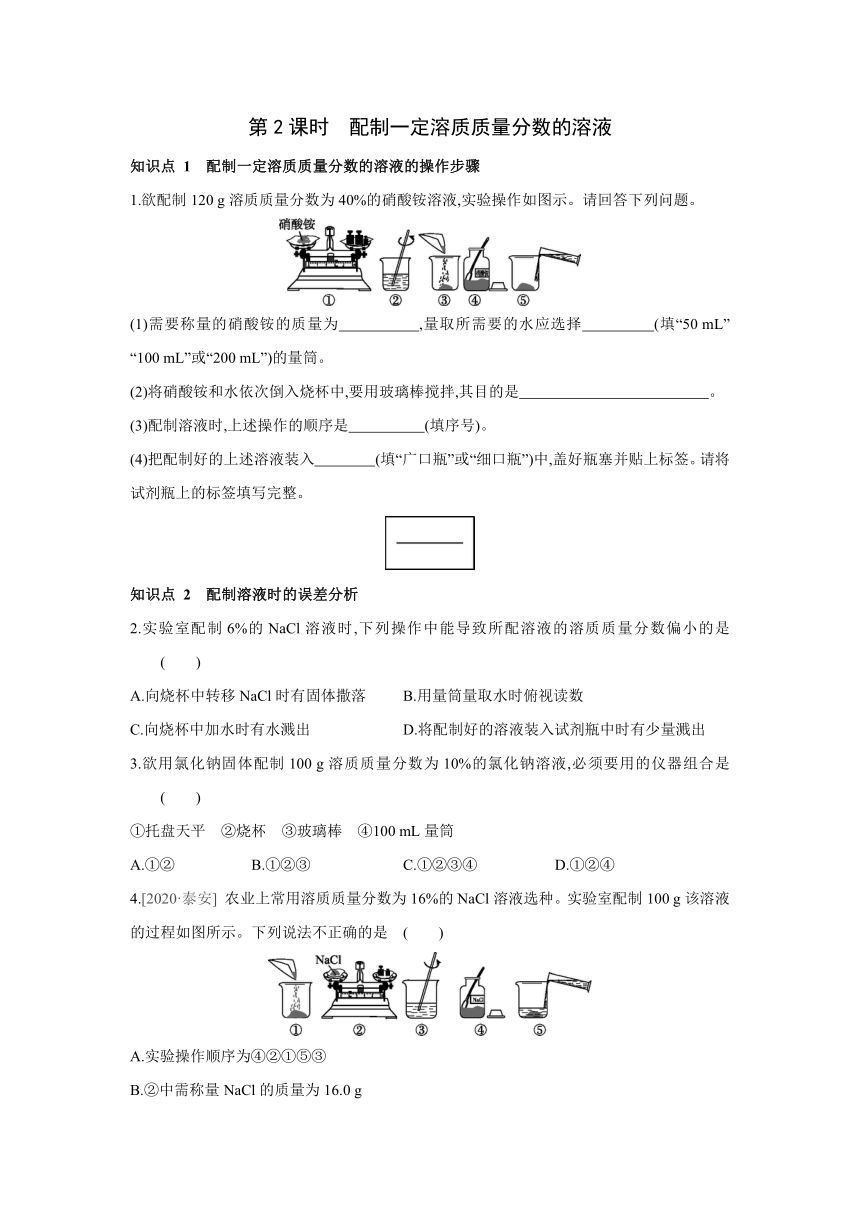
1.欲配制120 g溶质质量分数为40%的硝酸铵溶液,实验操作如图示。请回答下列问题。
(1)需要称量的硝酸铵的质量为 ,量取所需要的水应选择 (填“50 mL” “100 mL”或“200 mL”)的量筒。
(2)将硝酸铵和水依次倒入烧杯中,要用玻璃棒搅拌,其目的是 。
(3)配制溶液时,上述操作的顺序是 (填序号)。
(4)把配制好的上述溶液装入 (填“广口瓶”或“细口瓶”)中,盖好瓶塞并贴上标签。请将试剂瓶上的标签填写完整。
知识点 2 配制溶液时的误差分析
2.实验室配制6%的NaCl溶液时,下列操作中能导致所配溶液的溶质质量分数偏小的是 ( )
A.向烧杯中转移NaCl时有固体撒落 B.用量筒量取水时俯视读数
C.向烧杯中加水时有水溅出 D.将配制好的溶液装入试剂瓶中时有少量溅出
3.欲用氯化钠固体配制100 g溶质质量分数为10%的氯化钠溶液,必须要用的仪器组合是 ( )
①托盘天平 ②烧杯 ③玻璃棒 ④100 mL量筒
A.①② B.①②③ C.①②③④ D.①②④
4.[2020·泰安] 农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100 g该溶液的过程如图所示。下列说法不正确的是 ( )
A.实验操作顺序为④②①⑤③
B.②中需称量NaCl的质量为16.0 g
C.选用100 mL量筒量取所需水
D.用量筒量取水时仰视读数,所得溶液的溶质质量分数偏大
5.用固体氯化钠配制120 g溶质质量分数为10%的氯化钠溶液,下列说法中正确的是 ( )
A.称量时,左盘放10 g砝码,游码移到2 g处
B.量取所需水时,仰视读数会导致所配溶液浓度偏大
C.实验过程中,用到的玻璃仪器仅有烧杯和量筒
D.将所配溶液转移至贴有标签的试剂瓶中保存
6.配制一定溶质质量分数的氯化钠溶液常按以下操作顺序进行。请回答下列问题。
(1)配制100 g溶质质量分数为7.5%的氯化钠溶液需要氯化钠 g,水 g。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 (填字母)。
A.增加适量氯化钠固体 B.减少适量氯化钠固体
C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌的目的是 。
(4)下列情况会导致所配溶液中溶质的质量分数偏大的是 (填字母)。
A.氯化钠中混有少量杂质
B.称量时氯化钠和砝码位置放反了(使用了游码)
C.用量筒量取水时,俯视读数
D.将配制好的溶液装入未干燥的细口瓶中
7.[2021·安徽] 某同学配制100 g质量分数为11%的葡萄糖溶液,下列操作会导致所配溶液浓度偏高的是 ( )
A.用托盘天平称葡萄糖时,砝码放在左盘
B.转移葡萄糖时,纸上有少量残留
C.用量筒量取水时,俯视液面
D.配好溶液装入试剂瓶时,有少量洒出
第2课时 配制一定溶质质量分数的溶液
1.(1)48 g 100 mL (2)加速硝酸铵的溶解
(3)④①③⑤②
(4)细口瓶
2.A 用量筒量取水时俯视读数,会造成实际量取的水的体积偏小,则使溶质质量分数偏大;向烧杯中加水时有水溅出,会造成实际取用的水的体积偏小,则使溶质质量分数偏大;将溶液装入试剂瓶中时有少量溅出,溶液具有均一性,溶质质量分数不变。
3.C 配制一定溶质质量分数的溶液的基本步骤:计算、称量(量取)、溶解、装瓶存放。其中需要用到的仪器有托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒等。
4.D 配制100 g溶质质量分数为16%的NaCl溶液,所需NaCl的质量为100 g× 16%=16.0 g;所需水的质量为100 g-16.0 g=84.0 g,即需量取水84.0 mL,故配制100 g该溶液应选用100 mL量筒量取所需水;用量筒量取水时仰视读数,实际量取的水偏多,所得溶液的溶质质量分数偏小。
5.D 称量时,应该是右盘放10 g砝码,游码移到2 g处;量取所需水时,仰视读数会导致实际量取的水偏多,所配溶液的浓度偏小;实验过程中,用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管等。
6.(1)7.5 92.5 (2)B
(3)加快氯化钠的溶解速率 (4)C
(4)氯化钠中混有少量杂质,会使氯化钠偏少,溶质质量分数偏小;称量时氯化钠和砝码位置放反了(使用了游码),会使氯化钠质量偏少,溶质质量分数偏小;量取水时俯视读数,使实际量取水的体积偏小,溶质质量分数偏大;将配制好的溶液装入未干燥的细口瓶中,细口瓶中有水,导致溶质的质量分数偏小。
7.C 用量筒量取液体时,量筒要放平,读数时视线应与液体凹液面的最低处相平;如图果俯视液面,读数偏大,实际量取水的体积偏小,导致所配溶液浓度偏高。
知识点 1 配制一定溶质质量分数的溶液的操作步骤
1.欲配制120 g溶质质量分数为40%的硝酸铵溶液,实验操作如图示。请回答下列问题。
(1)需要称量的硝酸铵的质量为 ,量取所需要的水应选择 (填“50 mL” “100 mL”或“200 mL”)的量筒。
(2)将硝酸铵和水依次倒入烧杯中,要用玻璃棒搅拌,其目的是 。
(3)配制溶液时,上述操作的顺序是 (填序号)。
(4)把配制好的上述溶液装入 (填“广口瓶”或“细口瓶”)中,盖好瓶塞并贴上标签。请将试剂瓶上的标签填写完整。
知识点 2 配制溶液时的误差分析
2.实验室配制6%的NaCl溶液时,下列操作中能导致所配溶液的溶质质量分数偏小的是 ( )
A.向烧杯中转移NaCl时有固体撒落 B.用量筒量取水时俯视读数
C.向烧杯中加水时有水溅出 D.将配制好的溶液装入试剂瓶中时有少量溅出
3.欲用氯化钠固体配制100 g溶质质量分数为10%的氯化钠溶液,必须要用的仪器组合是 ( )
①托盘天平 ②烧杯 ③玻璃棒 ④100 mL量筒
A.①② B.①②③ C.①②③④ D.①②④
4.[2020·泰安] 农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100 g该溶液的过程如图所示。下列说法不正确的是 ( )
A.实验操作顺序为④②①⑤③
B.②中需称量NaCl的质量为16.0 g
C.选用100 mL量筒量取所需水
D.用量筒量取水时仰视读数,所得溶液的溶质质量分数偏大
5.用固体氯化钠配制120 g溶质质量分数为10%的氯化钠溶液,下列说法中正确的是 ( )
A.称量时,左盘放10 g砝码,游码移到2 g处
B.量取所需水时,仰视读数会导致所配溶液浓度偏大
C.实验过程中,用到的玻璃仪器仅有烧杯和量筒
D.将所配溶液转移至贴有标签的试剂瓶中保存
6.配制一定溶质质量分数的氯化钠溶液常按以下操作顺序进行。请回答下列问题。
(1)配制100 g溶质质量分数为7.5%的氯化钠溶液需要氯化钠 g,水 g。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 (填字母)。
A.增加适量氯化钠固体 B.减少适量氯化钠固体
C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌的目的是 。
(4)下列情况会导致所配溶液中溶质的质量分数偏大的是 (填字母)。
A.氯化钠中混有少量杂质
B.称量时氯化钠和砝码位置放反了(使用了游码)
C.用量筒量取水时,俯视读数
D.将配制好的溶液装入未干燥的细口瓶中
7.[2021·安徽] 某同学配制100 g质量分数为11%的葡萄糖溶液,下列操作会导致所配溶液浓度偏高的是 ( )
A.用托盘天平称葡萄糖时,砝码放在左盘
B.转移葡萄糖时,纸上有少量残留
C.用量筒量取水时,俯视液面
D.配好溶液装入试剂瓶时,有少量洒出
第2课时 配制一定溶质质量分数的溶液
1.(1)48 g 100 mL (2)加速硝酸铵的溶解
(3)④①③⑤②
(4)细口瓶
2.A 用量筒量取水时俯视读数,会造成实际量取的水的体积偏小,则使溶质质量分数偏大;向烧杯中加水时有水溅出,会造成实际取用的水的体积偏小,则使溶质质量分数偏大;将溶液装入试剂瓶中时有少量溅出,溶液具有均一性,溶质质量分数不变。
3.C 配制一定溶质质量分数的溶液的基本步骤:计算、称量(量取)、溶解、装瓶存放。其中需要用到的仪器有托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒等。
4.D 配制100 g溶质质量分数为16%的NaCl溶液,所需NaCl的质量为100 g× 16%=16.0 g;所需水的质量为100 g-16.0 g=84.0 g,即需量取水84.0 mL,故配制100 g该溶液应选用100 mL量筒量取所需水;用量筒量取水时仰视读数,实际量取的水偏多,所得溶液的溶质质量分数偏小。
5.D 称量时,应该是右盘放10 g砝码,游码移到2 g处;量取所需水时,仰视读数会导致实际量取的水偏多,所配溶液的浓度偏小;实验过程中,用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管等。
6.(1)7.5 92.5 (2)B
(3)加快氯化钠的溶解速率 (4)C
(4)氯化钠中混有少量杂质,会使氯化钠偏少,溶质质量分数偏小;称量时氯化钠和砝码位置放反了(使用了游码),会使氯化钠质量偏少,溶质质量分数偏小;量取水时俯视读数,使实际量取水的体积偏小,溶质质量分数偏大;将配制好的溶液装入未干燥的细口瓶中,细口瓶中有水,导致溶质的质量分数偏小。
7.C 用量筒量取液体时,量筒要放平,读数时视线应与液体凹液面的最低处相平;如图果俯视液面,读数偏大,实际量取水的体积偏小,导致所配溶液浓度偏高。
