北京课改版化学九年级上册同步练习:第3章 构成物质的微粒 单元复习(word含答案)
文档属性
| 名称 | 北京课改版化学九年级上册同步练习:第3章 构成物质的微粒 单元复习(word含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 195.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-24 00:00:00 | ||
图片预览


文档简介
本章知识清单
一、原子的结构
1.原子的结构
原子
2.在原子中,核电荷数= = 。
3.相对原子质量≈ 数+ 数
4.两个决定
二、离子
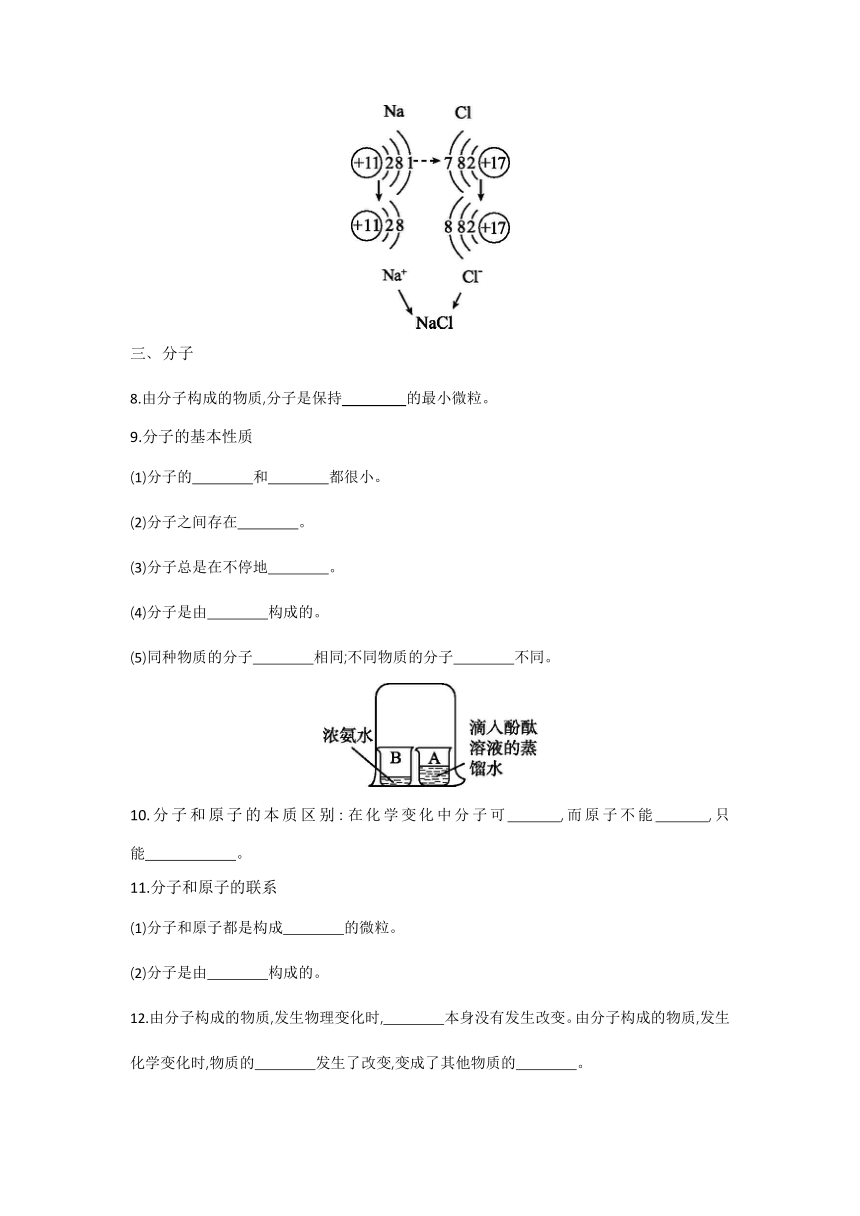
5.概念:带电的 或 叫作离子。
6.表示方法及意义:如Fe3+表示 。
7.离子结构示意图与原子结构示意图的区别
质子数 (填“>”“=”或“<”,下同)电子数为原子;质子数 电子数为阳离子;质子数 电子数为阴离子。
三、分子
8.由分子构成的物质,分子是保持 的最小微粒。
9.分子的基本性质
(1)分子的 和 都很小。
(2)分子之间存在 。
(3)分子总是在不停地 。
(4)分子是由 构成的。
(5)同种物质的分子 相同;不同物质的分子 不同。
10.分子和原子的本质区别:在化学变化中分子可 ,而原子不能 ,只能 。
11.分子和原子的联系
(1)分子和原子都是构成 的微粒。
(2)分子是由 构成的。
12.由分子构成的物质,发生物理变化时, 本身没有发生改变。由分子构成的物质,发生化学变化时,物质的 发生了改变,变成了其他物质的 。
四、物质的组成与构成
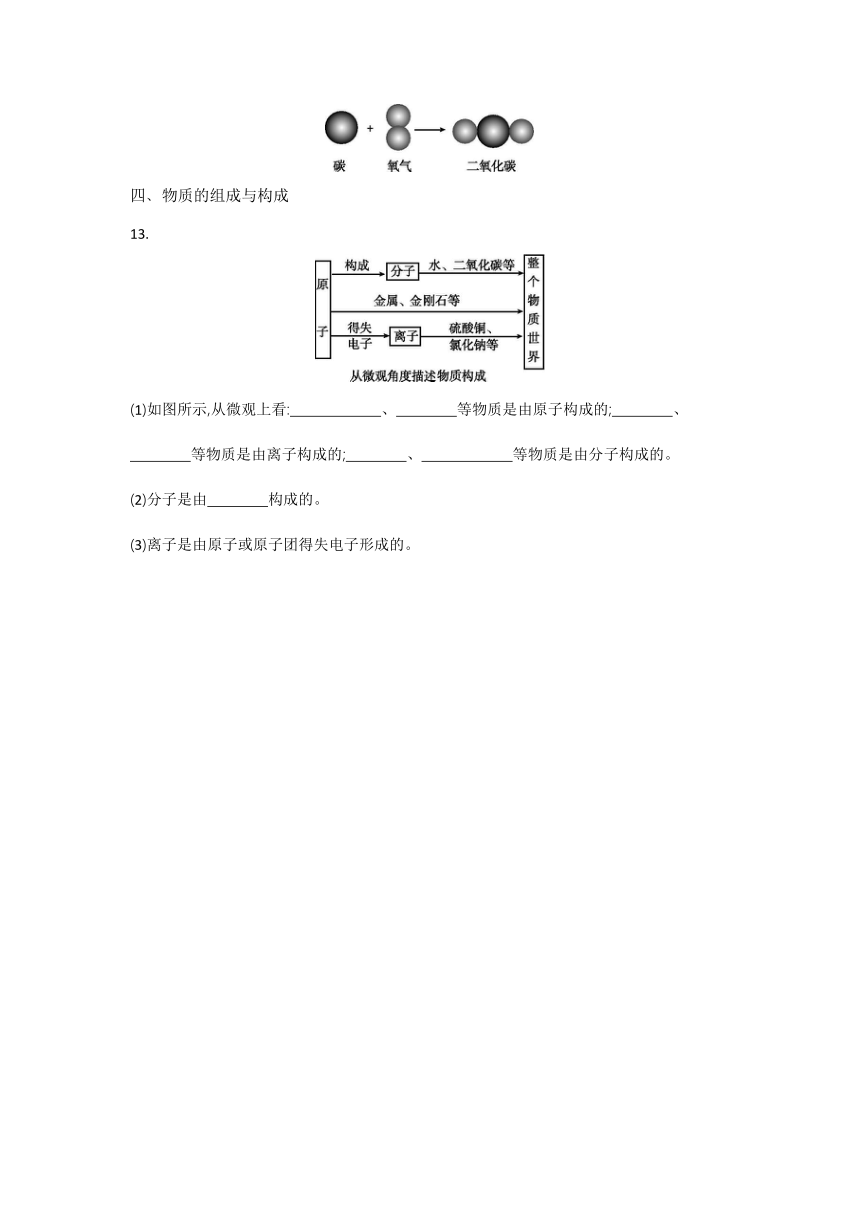
13.
(1)如图所示,从微观上看: 、 等物质是由原子构成的; 、
等物质是由离子构成的; 、 等物质是由分子构成的。
(2)分子是由 构成的。
(3)离子是由原子或原子团得失电子形成的。
易错易混辨析
易错点 1 对分子、原子、离子的认识
1.判断正误:(正确的打“√”,错误的打“×”)
对分子、原子、离子的典型认识 判断正误
(1)分子的体积一定比原子的大
(2)构成物质的微粒只有分子和原子
(3)相同的原子只能构成相同的分子
(4)分子保持物质的化学性质,原子不保持物质的化学性质
(5)保持二氧化硫化学性质的最小微粒是二氧化硫分子
(6)分子是保持物质性质的最小微粒
(7)原子失去电子带负电荷
易错点 2 对微粒性质的认识
2.判断正误:(正确的打“√”,错误的打“×”)
对微粒性质的典型认识 判断正误
(1)升高温度,分子的体积变大
(2)水结成冰以后,水分子的运动停止了
(3)在剪刀将铜丝剪开的过程中,有可能将铜原子剪开
(4)物体受热膨胀,从微观上看是温度越高,微粒之间的空隙越大
(5)水银温度计的工作原理是分子之间的空隙随温度升高而增大
易错点 3 对物质及微粒构成的认识
3.判断正误:(正确的打“√”,错误的打“×”)
对物质构成的典型认识 判断正误
(1)最外层电子数为8的微粒一定是稀有气体元素的原子
(2)氦原子与镁原子最外层电子数相同,它们的化学性质相似
(3)白糖水是混合物,是由不同种分子构成的
(4)水是由2个氢原子和1个氧原子构成的
易错点 4 微粒观解释物质的化学变化和物质的分类
4.小青和同学们一起完成了氢气燃烧的实验,并绘制了该反应的微观示意图(如图所示)。请回答下列问题。
(1)图中①的微观实质是 ,②的微观实质是 。
(2)图中方框内表示纯净物的是 (填字母)。
(3)由分子构成的物质在发生化学变化时,一定改变的微粒是 ,不发生改变的微粒是 。
[我来当老师] 检测一下自己的复习效果吧,请评价一下这位同学的答案是否正确,正确的打“√”,错误的打“×”,并给出你的正确答案以及讲评。
5.“超临界水”因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的物质。请你判断下列有关“超临界水”的认识是否正确(正确的打“√”,错误的打“×”),错误的请说明理由。
(1)它是一种不同于水的新物质,化学性质与普通水不同 (√)
(2)它的分子不再运动 (√)
(3)它的分子之间没有空隙 (√)
(4)它的1个分子由4个氢原子和2个氧原子构成 (√)
我的答案:
(1)( )
(2)( )
(3)( )
(4)( )
我的讲评:
教师详解详析
1.质子 正 不带电 核外电子 负 质子数
原子核 7
2.质子数 核外电子数
3.质子 中子
4.最外层电子数 原子核(质子和中子)
5.原子 原子团
6.1个铁离子带3个单位的正电荷
7.= > <
8.物质化学性质
9.(1)质量 体积
(2)空隙
(3)运动
(4)原子
(5)化学性质 化学性质
10.分 再分 重新组合
11.(1)物质
(2)原子
12.分子 分子 分子
13.(1)金属 金刚石 硫酸铜 氯化钠 水
二氧化碳
(2)原子
教师详解详析
1.(1)× (2)× (3)× (4)× (5)√
(6)× (7)×
2.(1)× (2)× (3)× (4)√ (5)×
3.(1)× (2)× (3)√ (4)×
4.(1)氢分子分解成氢原子,氧分子分解成氧原子 氢原子和氧原子重新结合成水分子
(2)C (3)分子 原子
[易错点] 由分子构成的物质,发生化学反应的微观实质是分子分成原子,原子重新组合成新的分子,所以分子一定发生改变,原子一定不变;由同种分子构成的物质属于纯净物。
5.我的答案:(1)× “超临界水”由水分子构成,分子是保持该物质化学性质的最小微粒,化学性质和普通水相同
(2)× 分子在永不停息地运动
(3)× 分子之间有空隙
(4)× “超临界水”仍然是水,水分子构成没有改变
我的讲评:(1)“超临界水”是水的一种新状态,仍然由水分子构成,因此化学性质和普通水相同。(2)分子总是在不停地运动。(3)分子之间的空隙永远存在。(4)每个水分子均由2个氢原子和1个氧原子构成。
一、原子的结构
1.原子的结构
原子
2.在原子中,核电荷数= = 。
3.相对原子质量≈ 数+ 数
4.两个决定
二、离子
5.概念:带电的 或 叫作离子。
6.表示方法及意义:如Fe3+表示 。
7.离子结构示意图与原子结构示意图的区别
质子数 (填“>”“=”或“<”,下同)电子数为原子;质子数 电子数为阳离子;质子数 电子数为阴离子。
三、分子
8.由分子构成的物质,分子是保持 的最小微粒。
9.分子的基本性质
(1)分子的 和 都很小。
(2)分子之间存在 。
(3)分子总是在不停地 。
(4)分子是由 构成的。
(5)同种物质的分子 相同;不同物质的分子 不同。
10.分子和原子的本质区别:在化学变化中分子可 ,而原子不能 ,只能 。
11.分子和原子的联系
(1)分子和原子都是构成 的微粒。
(2)分子是由 构成的。
12.由分子构成的物质,发生物理变化时, 本身没有发生改变。由分子构成的物质,发生化学变化时,物质的 发生了改变,变成了其他物质的 。
四、物质的组成与构成
13.
(1)如图所示,从微观上看: 、 等物质是由原子构成的; 、
等物质是由离子构成的; 、 等物质是由分子构成的。
(2)分子是由 构成的。
(3)离子是由原子或原子团得失电子形成的。
易错易混辨析
易错点 1 对分子、原子、离子的认识
1.判断正误:(正确的打“√”,错误的打“×”)
对分子、原子、离子的典型认识 判断正误
(1)分子的体积一定比原子的大
(2)构成物质的微粒只有分子和原子
(3)相同的原子只能构成相同的分子
(4)分子保持物质的化学性质,原子不保持物质的化学性质
(5)保持二氧化硫化学性质的最小微粒是二氧化硫分子
(6)分子是保持物质性质的最小微粒
(7)原子失去电子带负电荷
易错点 2 对微粒性质的认识
2.判断正误:(正确的打“√”,错误的打“×”)
对微粒性质的典型认识 判断正误
(1)升高温度,分子的体积变大
(2)水结成冰以后,水分子的运动停止了
(3)在剪刀将铜丝剪开的过程中,有可能将铜原子剪开
(4)物体受热膨胀,从微观上看是温度越高,微粒之间的空隙越大
(5)水银温度计的工作原理是分子之间的空隙随温度升高而增大
易错点 3 对物质及微粒构成的认识
3.判断正误:(正确的打“√”,错误的打“×”)
对物质构成的典型认识 判断正误
(1)最外层电子数为8的微粒一定是稀有气体元素的原子
(2)氦原子与镁原子最外层电子数相同,它们的化学性质相似
(3)白糖水是混合物,是由不同种分子构成的
(4)水是由2个氢原子和1个氧原子构成的
易错点 4 微粒观解释物质的化学变化和物质的分类
4.小青和同学们一起完成了氢气燃烧的实验,并绘制了该反应的微观示意图(如图所示)。请回答下列问题。
(1)图中①的微观实质是 ,②的微观实质是 。
(2)图中方框内表示纯净物的是 (填字母)。
(3)由分子构成的物质在发生化学变化时,一定改变的微粒是 ,不发生改变的微粒是 。
[我来当老师] 检测一下自己的复习效果吧,请评价一下这位同学的答案是否正确,正确的打“√”,错误的打“×”,并给出你的正确答案以及讲评。
5.“超临界水”因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的物质。请你判断下列有关“超临界水”的认识是否正确(正确的打“√”,错误的打“×”),错误的请说明理由。
(1)它是一种不同于水的新物质,化学性质与普通水不同 (√)
(2)它的分子不再运动 (√)
(3)它的分子之间没有空隙 (√)
(4)它的1个分子由4个氢原子和2个氧原子构成 (√)
我的答案:
(1)( )
(2)( )
(3)( )
(4)( )
我的讲评:
教师详解详析
1.质子 正 不带电 核外电子 负 质子数
原子核 7
2.质子数 核外电子数
3.质子 中子
4.最外层电子数 原子核(质子和中子)
5.原子 原子团
6.1个铁离子带3个单位的正电荷
7.= > <
8.物质化学性质
9.(1)质量 体积
(2)空隙
(3)运动
(4)原子
(5)化学性质 化学性质
10.分 再分 重新组合
11.(1)物质
(2)原子
12.分子 分子 分子
13.(1)金属 金刚石 硫酸铜 氯化钠 水
二氧化碳
(2)原子
教师详解详析
1.(1)× (2)× (3)× (4)× (5)√
(6)× (7)×
2.(1)× (2)× (3)× (4)√ (5)×
3.(1)× (2)× (3)√ (4)×
4.(1)氢分子分解成氢原子,氧分子分解成氧原子 氢原子和氧原子重新结合成水分子
(2)C (3)分子 原子
[易错点] 由分子构成的物质,发生化学反应的微观实质是分子分成原子,原子重新组合成新的分子,所以分子一定发生改变,原子一定不变;由同种分子构成的物质属于纯净物。
5.我的答案:(1)× “超临界水”由水分子构成,分子是保持该物质化学性质的最小微粒,化学性质和普通水相同
(2)× 分子在永不停息地运动
(3)× 分子之间有空隙
(4)× “超临界水”仍然是水,水分子构成没有改变
我的讲评:(1)“超临界水”是水的一种新状态,仍然由水分子构成,因此化学性质和普通水相同。(2)分子总是在不停地运动。(3)分子之间的空隙永远存在。(4)每个水分子均由2个氢原子和1个氧原子构成。
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
