沪教版(全国)化学九年级上册同步课时练习:第2章 单元复习小结(word版有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册同步课时练习:第2章 单元复习小结(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 232.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-26 00:00:00 | ||
图片预览



文档简介
单元复习小结
本章知识清单
一、空气的成分
空气中各组分气体的体积分数:氮气 %、氧气 %、稀有气体 %、二氧化碳 %、其他气体和杂质 %。
二、氧气的性质和用途
1.氧气的物理性质
(1)通常状况下,氧气是一种 色、 气味的气体,密度稍 空气, 溶于水。
(2)氧气有三态变化。在外界条件改变时,可以变成 色液体和固体。
2.氧气的化学性质
氧气是一种化学性质 的气体,能与许多物质发生化学反应,在反应中提供氧,具有
性。
(1)碳+氧气 ; C+O2 。
(2)铁+氧气 ; Fe+O2 。
(3)石蜡+氧气 + 。
3.氧气的用途
供给呼吸和支持燃烧是氧气的重要用途。如图潜水、太空飞行、 、
等。
三、氧气的制法
1.工业制氧气
利用液态氧和液态氮的 不同,采用分离液态空气法制氧气,该过程发生 (填“物理”或“化学”)变化。
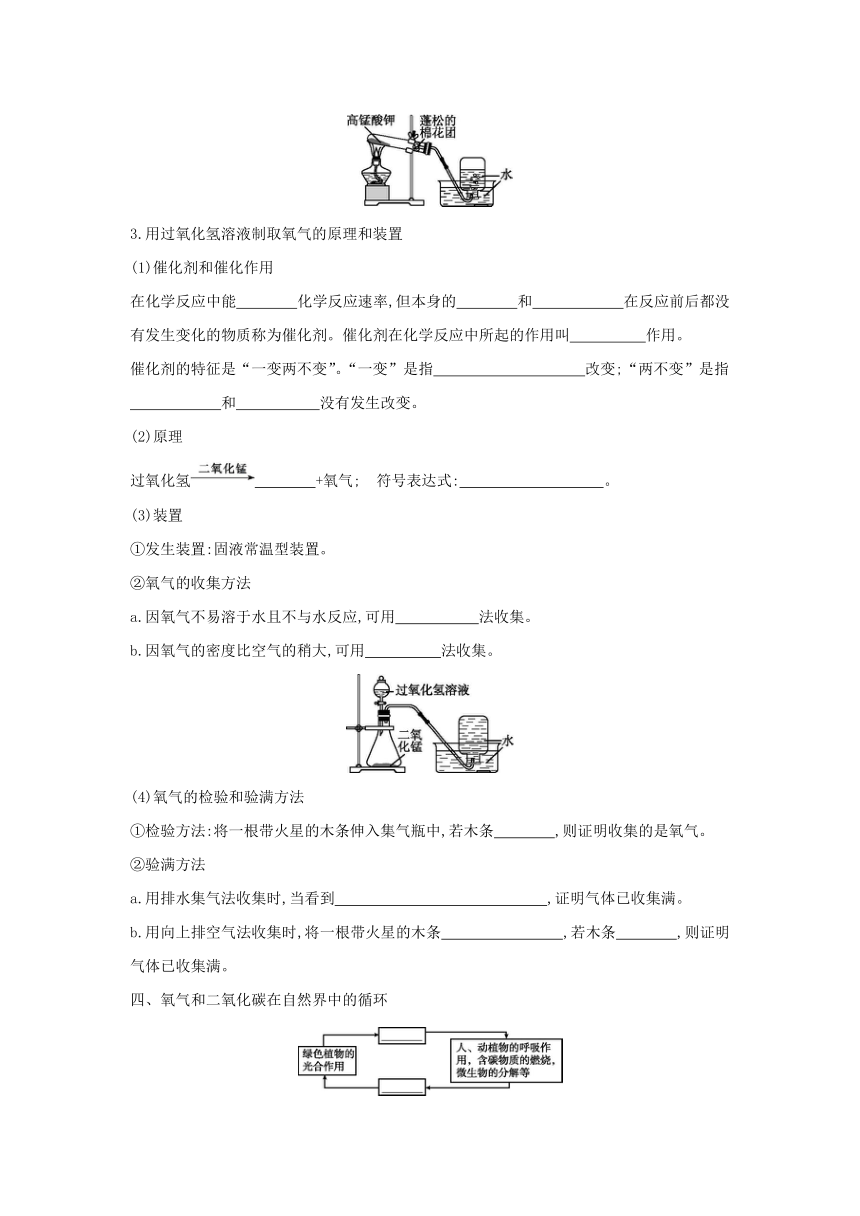
2.用高锰酸钾制取氧气的原理和装置
(1)原理
用高锰酸钾制取氧气的文字表达式: ;符号表达式: 。
(2)发生装置:固体加热型装置。
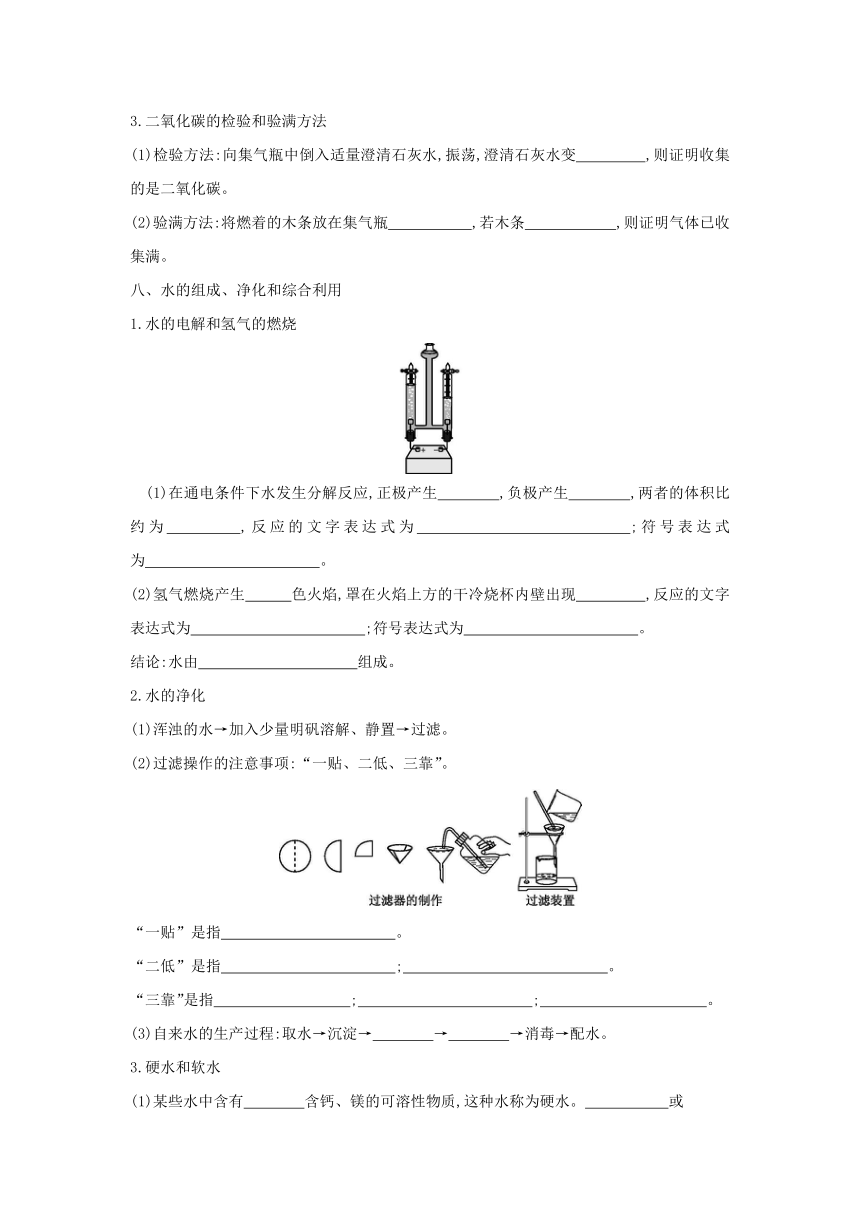
3.用过氧化氢溶液制取氧气的原理和装置
(1)催化剂和催化作用
在化学反应中能 化学反应速率,但本身的 和 在反应前后都没有发生变化的物质称为催化剂。催化剂在化学反应中所起的作用叫 作用。
催化剂的特征是“一变两不变”。“一变”是指 改变;“两不变”是指
和 没有发生改变。
(2)原理
过氧化氢 +氧气; 符号表达式: 。
(3)装置
①发生装置:固液常温型装置。
②氧气的收集方法
a.因氧气不易溶于水且不与水反应,可用 法收集。
b.因氧气的密度比空气的稍大,可用 法收集。
(4)氧气的检验和验满方法
①检验方法:将一根带火星的木条伸入集气瓶中,若木条 ,则证明收集的是氧气。
②验满方法
a.用排水集气法收集时,当看到 ,证明气体已收集满。
b.用向上排空气法收集时,将一根带火星的木条 ,若木条 ,则证明气体已收集满。
四、氧气和二氧化碳在自然界中的循环
五、二氧化碳的性质和用途
1.物理性质
通常情况下,二氧化碳是 色、 气味的气体,密度比空气的 ,能溶于水,固体二氧化碳的俗称是 。
2.化学性质
(1)一般情况下,既不能燃烧也不支持燃烧。
(2)能跟水反应:二氧化碳+水 。
符号表达式: 。
(3)能跟氢氧化钙反应:
二氧化碳+氢氧化钙 + 。
符号表达式: 。
3.用途
(1)二氧化碳既不能燃烧也不支持燃烧,密度比空气大,可用于 。
(2)干冰可用于 等。
(3)二氧化碳是化工原料,可用于制汽水等。
六、化合反应和分解反应
由两种或两种以上物质生成一种新物质的反应叫作 。由一种物质生成两种或两种以上新物质的反应叫作 。化合反应的特征是“多变一”,分解反应的特征是“ ”。
七、二氧化碳的实验室制法
1.原理
碳酸钙+盐酸 + + ;
符号表达式: 。
2.装置
(1)制取二氧化碳的发生装置:“固+液”常温型装置。
(2)通常状况下,二氧化碳的密度比空气的大,所以用 法收集。
3.二氧化碳的检验和验满方法
(1)检验方法:向集气瓶中倒入适量澄清石灰水,振荡,澄清石灰水变 ,则证明收集的是二氧化碳。
(2)验满方法:将燃着的木条放在集气瓶 ,若木条 ,则证明气体已收集满。
八、水的组成、净化和综合利用
1.水的电解和氢气的燃烧
(1)在通电条件下水发生分解反应,正极产生 ,负极产生 ,两者的体积比约为 ,反应的文字表达式为 ;符号表达式为 。
(2)氢气燃烧产生 色火焰,罩在火焰上方的干冷烧杯内壁出现 ,反应的文字表达式为 ;符号表达式为 。
结论:水由 组成。
2.水的净化
(1)浑浊的水→加入少量明矾溶解、静置→过滤。
(2)过滤操作的注意事项:“一贴、二低、三靠”。
“一贴”是指 。
“二低”是指 ; 。
“三靠”是指 ; ; 。
(3)自来水的生产过程:取水→沉淀→ → →消毒→配水。
3.硬水和软水
(1)某些水中含有 含钙、镁的可溶性物质,这种水称为硬水。 或
含钙、镁的可溶性物质的水叫软水。
(2)硬水和软水的检验方法: 。
(3)硬水软化的方法:生活中常用 的方法。在实验和科研中通常用 的方法获取蒸馏水。
4.节约用水
地球上水的总储量较大,但是可以利用的淡水资源非常有限,我国的人均水资源占有量仅为世界人均水平的四分之一。保护水资源、节约用水是我们义不容辞的责任。
易错易混辨析
易错点 1 物质在氧气中燃烧的现象
1.下列实验现象的描述中正确的是 ( )
A.铁丝在空气中燃烧,火星四射,生成黑色固体 B.木炭在氧气中燃烧发出白光
C.镁条在空气中燃烧,生成氧化镁 D.红磷在空气中燃烧,产生大量白雾
易错点 2 氧气的性质和用途
2.下列关于氧气的说法中不正确的是 ( )
A.氧气能支持燃烧,所以氧气可作燃料 B.氧气能使带火星的木条复燃
C.氧气不易溶于水 D.氧气是一种化学性质比较活泼的气体
易错点 3 二氧化碳的性质和用途
3.如图将充满二氧化碳的试管倒扣在滴有紫色石蕊试液的水中,一段时间后,下列实验现象描述正确的是 ( )
①试管内液面上升 ②液体变红 ③试管内液面不上升 ④液体变蓝 ⑤液体不变色
A.①② B.①④ C.②③ D.③⑤
4.二氧化碳之所以能够灭火,是因为 ( )
①密度比空气大;②能溶于水;③一般情况下,它不能燃烧;④一般情况下,它不支持燃烧;⑤能使紫色石蕊试液变色
A.②③④ B.①④⑤ C.③④⑤ D.①③④
易错点 4 化合反应、分解反应和氧化反应
5.写出下列反应的符号表达式,并在括号内写出反应的基本类型。
(1)铁在氧气中燃烧: ( )。
(2)二氧化碳与水反应: ( )。
(3)加热氯酸钾和二氧化锰的混合物: ( )。
易错点 5 电解水实验
6.判断正误:(正确的打“√”,错误的打“×”)
对电解水和水的组成的典型认识 判断正误
(1)水是由氢气和氧气组成的
(2)水是由氢元素和氧元素组成的
(3)水电解后正极产生氧气,负极产生氢气,氢气的质量是氧气质量的2倍
易错点 6 水的净化、软水和硬水
7.下列有关水的说法正确的是 ( )
A.净化水的过程中发生的都是物理变化
B.用肥皂水不可以区分硬水和软水
C.用滤纸过滤可以除去水中的所有杂质
D.将黄河水进行沉降、过滤、吸附、灭菌等净化操作后,可作为人们的生活用水
易错点 7 气体的制取
8.根据示装置图,回答有关问题。
(1)图中仪器①的名称为 。
(2)用装置F收集一瓶氧气,气体应从 (填“a”或“b”)管通入,验满的方法是
。
(3)实验室没有大理石和石灰石,只有碳酸钠粉末和盐酸,为了顺利制取一瓶二氧化碳,来验证二氧化碳不能使干燥的紫色石蕊试纸变红。你选择的最佳装置组合是 (填字母),选择该气体发生装置的理由是 。
易错点 8 气体的区分
9.能够区分氧气、空气、二氧化碳这三种无色、无味气体的简便方法是 ( )
A.用带火星的木条 B.用燃着的木条
C.通入澄清石灰水 D.通入紫色石蕊试液
答案
一、78 21 0.94 0.03 0.03
二、1.(1)无 无 大于 不易
(2)淡蓝
2.比较活泼 氧化
(1)二氧化碳 CO2
(2)四氧化三铁 Fe3O4
(3)二氧化碳 水
3.焊接和切割金属 炼钢(合理即可)
三、1.沸点 物理
2.(1)高锰酸钾锰酸钾+二氧化锰+氧气 KMnO4K2MnO4+MnO2+O2
3.(1)增大 质量 化学性质 催化
反应速率 质量 化学性质
(2)水 H2O2H2O+O2
(3)②a.排水集气 b.向上排空气
(4)①复燃 ②a.集气瓶口有大气泡冒出 b.伸至集气瓶口 复燃
四、氧气 二氧化碳
五、1.无 无 大 干冰
2.(2)碳酸 CO2 +H2OH2CO3
(3)碳酸钙 水
CO2 +Ca(OH)2CaCO3+H2O
3.(1)灭火 (2)人工降雨
六、化合反应 分解反应 一变多
七、1.氯化钙 水 二氧化碳
CaCO3+HClCaCl2+H2O+CO2
2.(2)向上排空气
3.(1)浑浊
(2)口 熄灭
八、1.(1)氧气 氢气 1∶2 水氢气+氧气
H2OH2+O2
(2)淡蓝 小水珠 氢气+氧气水
H2+O2 H2O
氢元素和氧元素
2.(2)滤纸紧贴漏斗内壁 滤纸边缘低于漏斗边缘 漏斗中液体的液面低于滤纸边缘 盛待过滤液的烧杯口紧靠玻璃棒 玻璃棒下端轻靠三层滤纸一边 漏斗下端管口紧靠盛接滤液的烧杯内壁
(3)过滤 吸附
3.(1)较多 不含 含有少量
(2)取等量水样品,分别加入等量肥皂水,搅拌,产生泡沫多的(或产生垢状物少的)为软水,产生泡沫少或不产生泡沫的(或产生垢状物多的)为硬水
(3)煮沸 蒸馏
答案
1.B 铁丝在空气中不燃烧,在氧气中燃烧,火星四射,生成黑色固体;生成氧化镁是结论而非实验现象;红磷在空气中燃烧,产生大量白烟而非白雾。
2.A [易错点] 氧气能支持燃烧,能使带火星的木条复燃,但它不具有可燃性,不能作燃料。
3.A 二氧化碳与水反应生成碳酸,碳酸显酸性,能使紫色石蕊试液变红;在通常情况下,一体积水能溶解一体积二氧化碳,所以试管中气体体积会减小,气压降低,液面会上升。
[易错点] 紫色石蕊试液的变色情况,学生容易混淆;学生对气压的变化容易忽略,导致对试管中液面高度的变化视而不见。
4.D
5.(1)Fe+O2Fe3O4 化合反应 (2)CO2+H2OH2CO3 化合反应
(3)KClO3KCl+O2 分解反应
[易错点] 学生易把氧化反应当作基本反应类型,容易把催化剂当作反应物或生成物。
6.(1)× (2)√ (3)×
7.D [易错点] 水的净化措施很多,需根据实际情况进行取舍,这一点学生比较容易出错,另外沉降、过滤、吸附等操作的先后顺序也是易错点。 最常见的一个错误就是认为过滤能将硬水变成软水。
8.(1)水槽 (2)a 将带火星的木条放在b导管口处,若木条复燃,则已收集满,否则不满
(3)AF 装置A可以控制反应的速率
(3)用碳酸钠粉末和稀盐酸来制取二氧化碳,反应速率较快,不便于控制,所以可用分液漏斗控制液体的滴加速率,从而控制反应速率。二氧化碳的密度比空气大,用向上排空气法可以收集干燥的二氧化碳气体;二氧化碳能溶于水,一般不用排水集气法收集,且用排水集气法收集不符合本实验要求。
[易错点] 仪器名称容易写错。选择装置有三种要求:发生装置、收集装置、制取装置,学生容易混淆,对应装置的仪器容易漏选。气体发生装置的选择应该依据反应物的状态和反应条件,收集装置要考虑气体的密度、水溶性、化学性质等,学生容易考虑不全面,从而导致选择错误。二氧化碳能溶于水,且与水反应生成碳酸,如图果要收集干燥的二氧化碳气体,只能用向上排空气法收集。
9.B 燃着的木条在氧气中燃烧更旺,在空气中正常燃烧,在二氧化碳中熄灭。
本章知识清单
一、空气的成分
空气中各组分气体的体积分数:氮气 %、氧气 %、稀有气体 %、二氧化碳 %、其他气体和杂质 %。
二、氧气的性质和用途
1.氧气的物理性质
(1)通常状况下,氧气是一种 色、 气味的气体,密度稍 空气, 溶于水。
(2)氧气有三态变化。在外界条件改变时,可以变成 色液体和固体。
2.氧气的化学性质
氧气是一种化学性质 的气体,能与许多物质发生化学反应,在反应中提供氧,具有
性。
(1)碳+氧气 ; C+O2 。
(2)铁+氧气 ; Fe+O2 。
(3)石蜡+氧气 + 。
3.氧气的用途
供给呼吸和支持燃烧是氧气的重要用途。如图潜水、太空飞行、 、
等。
三、氧气的制法
1.工业制氧气
利用液态氧和液态氮的 不同,采用分离液态空气法制氧气,该过程发生 (填“物理”或“化学”)变化。
2.用高锰酸钾制取氧气的原理和装置
(1)原理
用高锰酸钾制取氧气的文字表达式: ;符号表达式: 。
(2)发生装置:固体加热型装置。
3.用过氧化氢溶液制取氧气的原理和装置
(1)催化剂和催化作用
在化学反应中能 化学反应速率,但本身的 和 在反应前后都没有发生变化的物质称为催化剂。催化剂在化学反应中所起的作用叫 作用。
催化剂的特征是“一变两不变”。“一变”是指 改变;“两不变”是指
和 没有发生改变。
(2)原理
过氧化氢 +氧气; 符号表达式: 。
(3)装置
①发生装置:固液常温型装置。
②氧气的收集方法
a.因氧气不易溶于水且不与水反应,可用 法收集。
b.因氧气的密度比空气的稍大,可用 法收集。
(4)氧气的检验和验满方法
①检验方法:将一根带火星的木条伸入集气瓶中,若木条 ,则证明收集的是氧气。
②验满方法
a.用排水集气法收集时,当看到 ,证明气体已收集满。
b.用向上排空气法收集时,将一根带火星的木条 ,若木条 ,则证明气体已收集满。
四、氧气和二氧化碳在自然界中的循环
五、二氧化碳的性质和用途
1.物理性质
通常情况下,二氧化碳是 色、 气味的气体,密度比空气的 ,能溶于水,固体二氧化碳的俗称是 。
2.化学性质
(1)一般情况下,既不能燃烧也不支持燃烧。
(2)能跟水反应:二氧化碳+水 。
符号表达式: 。
(3)能跟氢氧化钙反应:
二氧化碳+氢氧化钙 + 。
符号表达式: 。
3.用途
(1)二氧化碳既不能燃烧也不支持燃烧,密度比空气大,可用于 。
(2)干冰可用于 等。
(3)二氧化碳是化工原料,可用于制汽水等。
六、化合反应和分解反应
由两种或两种以上物质生成一种新物质的反应叫作 。由一种物质生成两种或两种以上新物质的反应叫作 。化合反应的特征是“多变一”,分解反应的特征是“ ”。
七、二氧化碳的实验室制法
1.原理
碳酸钙+盐酸 + + ;
符号表达式: 。
2.装置
(1)制取二氧化碳的发生装置:“固+液”常温型装置。
(2)通常状况下,二氧化碳的密度比空气的大,所以用 法收集。
3.二氧化碳的检验和验满方法
(1)检验方法:向集气瓶中倒入适量澄清石灰水,振荡,澄清石灰水变 ,则证明收集的是二氧化碳。
(2)验满方法:将燃着的木条放在集气瓶 ,若木条 ,则证明气体已收集满。
八、水的组成、净化和综合利用
1.水的电解和氢气的燃烧
(1)在通电条件下水发生分解反应,正极产生 ,负极产生 ,两者的体积比约为 ,反应的文字表达式为 ;符号表达式为 。
(2)氢气燃烧产生 色火焰,罩在火焰上方的干冷烧杯内壁出现 ,反应的文字表达式为 ;符号表达式为 。
结论:水由 组成。
2.水的净化
(1)浑浊的水→加入少量明矾溶解、静置→过滤。
(2)过滤操作的注意事项:“一贴、二低、三靠”。
“一贴”是指 。
“二低”是指 ; 。
“三靠”是指 ; ; 。
(3)自来水的生产过程:取水→沉淀→ → →消毒→配水。
3.硬水和软水
(1)某些水中含有 含钙、镁的可溶性物质,这种水称为硬水。 或
含钙、镁的可溶性物质的水叫软水。
(2)硬水和软水的检验方法: 。
(3)硬水软化的方法:生活中常用 的方法。在实验和科研中通常用 的方法获取蒸馏水。
4.节约用水
地球上水的总储量较大,但是可以利用的淡水资源非常有限,我国的人均水资源占有量仅为世界人均水平的四分之一。保护水资源、节约用水是我们义不容辞的责任。
易错易混辨析
易错点 1 物质在氧气中燃烧的现象
1.下列实验现象的描述中正确的是 ( )
A.铁丝在空气中燃烧,火星四射,生成黑色固体 B.木炭在氧气中燃烧发出白光
C.镁条在空气中燃烧,生成氧化镁 D.红磷在空气中燃烧,产生大量白雾
易错点 2 氧气的性质和用途
2.下列关于氧气的说法中不正确的是 ( )
A.氧气能支持燃烧,所以氧气可作燃料 B.氧气能使带火星的木条复燃
C.氧气不易溶于水 D.氧气是一种化学性质比较活泼的气体
易错点 3 二氧化碳的性质和用途
3.如图将充满二氧化碳的试管倒扣在滴有紫色石蕊试液的水中,一段时间后,下列实验现象描述正确的是 ( )
①试管内液面上升 ②液体变红 ③试管内液面不上升 ④液体变蓝 ⑤液体不变色
A.①② B.①④ C.②③ D.③⑤
4.二氧化碳之所以能够灭火,是因为 ( )
①密度比空气大;②能溶于水;③一般情况下,它不能燃烧;④一般情况下,它不支持燃烧;⑤能使紫色石蕊试液变色
A.②③④ B.①④⑤ C.③④⑤ D.①③④
易错点 4 化合反应、分解反应和氧化反应
5.写出下列反应的符号表达式,并在括号内写出反应的基本类型。
(1)铁在氧气中燃烧: ( )。
(2)二氧化碳与水反应: ( )。
(3)加热氯酸钾和二氧化锰的混合物: ( )。
易错点 5 电解水实验
6.判断正误:(正确的打“√”,错误的打“×”)
对电解水和水的组成的典型认识 判断正误
(1)水是由氢气和氧气组成的
(2)水是由氢元素和氧元素组成的
(3)水电解后正极产生氧气,负极产生氢气,氢气的质量是氧气质量的2倍
易错点 6 水的净化、软水和硬水
7.下列有关水的说法正确的是 ( )
A.净化水的过程中发生的都是物理变化
B.用肥皂水不可以区分硬水和软水
C.用滤纸过滤可以除去水中的所有杂质
D.将黄河水进行沉降、过滤、吸附、灭菌等净化操作后,可作为人们的生活用水
易错点 7 气体的制取
8.根据示装置图,回答有关问题。
(1)图中仪器①的名称为 。
(2)用装置F收集一瓶氧气,气体应从 (填“a”或“b”)管通入,验满的方法是
。
(3)实验室没有大理石和石灰石,只有碳酸钠粉末和盐酸,为了顺利制取一瓶二氧化碳,来验证二氧化碳不能使干燥的紫色石蕊试纸变红。你选择的最佳装置组合是 (填字母),选择该气体发生装置的理由是 。
易错点 8 气体的区分
9.能够区分氧气、空气、二氧化碳这三种无色、无味气体的简便方法是 ( )
A.用带火星的木条 B.用燃着的木条
C.通入澄清石灰水 D.通入紫色石蕊试液
答案
一、78 21 0.94 0.03 0.03
二、1.(1)无 无 大于 不易
(2)淡蓝
2.比较活泼 氧化
(1)二氧化碳 CO2
(2)四氧化三铁 Fe3O4
(3)二氧化碳 水
3.焊接和切割金属 炼钢(合理即可)
三、1.沸点 物理
2.(1)高锰酸钾锰酸钾+二氧化锰+氧气 KMnO4K2MnO4+MnO2+O2
3.(1)增大 质量 化学性质 催化
反应速率 质量 化学性质
(2)水 H2O2H2O+O2
(3)②a.排水集气 b.向上排空气
(4)①复燃 ②a.集气瓶口有大气泡冒出 b.伸至集气瓶口 复燃
四、氧气 二氧化碳
五、1.无 无 大 干冰
2.(2)碳酸 CO2 +H2OH2CO3
(3)碳酸钙 水
CO2 +Ca(OH)2CaCO3+H2O
3.(1)灭火 (2)人工降雨
六、化合反应 分解反应 一变多
七、1.氯化钙 水 二氧化碳
CaCO3+HClCaCl2+H2O+CO2
2.(2)向上排空气
3.(1)浑浊
(2)口 熄灭
八、1.(1)氧气 氢气 1∶2 水氢气+氧气
H2OH2+O2
(2)淡蓝 小水珠 氢气+氧气水
H2+O2 H2O
氢元素和氧元素
2.(2)滤纸紧贴漏斗内壁 滤纸边缘低于漏斗边缘 漏斗中液体的液面低于滤纸边缘 盛待过滤液的烧杯口紧靠玻璃棒 玻璃棒下端轻靠三层滤纸一边 漏斗下端管口紧靠盛接滤液的烧杯内壁
(3)过滤 吸附
3.(1)较多 不含 含有少量
(2)取等量水样品,分别加入等量肥皂水,搅拌,产生泡沫多的(或产生垢状物少的)为软水,产生泡沫少或不产生泡沫的(或产生垢状物多的)为硬水
(3)煮沸 蒸馏
答案
1.B 铁丝在空气中不燃烧,在氧气中燃烧,火星四射,生成黑色固体;生成氧化镁是结论而非实验现象;红磷在空气中燃烧,产生大量白烟而非白雾。
2.A [易错点] 氧气能支持燃烧,能使带火星的木条复燃,但它不具有可燃性,不能作燃料。
3.A 二氧化碳与水反应生成碳酸,碳酸显酸性,能使紫色石蕊试液变红;在通常情况下,一体积水能溶解一体积二氧化碳,所以试管中气体体积会减小,气压降低,液面会上升。
[易错点] 紫色石蕊试液的变色情况,学生容易混淆;学生对气压的变化容易忽略,导致对试管中液面高度的变化视而不见。
4.D
5.(1)Fe+O2Fe3O4 化合反应 (2)CO2+H2OH2CO3 化合反应
(3)KClO3KCl+O2 分解反应
[易错点] 学生易把氧化反应当作基本反应类型,容易把催化剂当作反应物或生成物。
6.(1)× (2)√ (3)×
7.D [易错点] 水的净化措施很多,需根据实际情况进行取舍,这一点学生比较容易出错,另外沉降、过滤、吸附等操作的先后顺序也是易错点。 最常见的一个错误就是认为过滤能将硬水变成软水。
8.(1)水槽 (2)a 将带火星的木条放在b导管口处,若木条复燃,则已收集满,否则不满
(3)AF 装置A可以控制反应的速率
(3)用碳酸钠粉末和稀盐酸来制取二氧化碳,反应速率较快,不便于控制,所以可用分液漏斗控制液体的滴加速率,从而控制反应速率。二氧化碳的密度比空气大,用向上排空气法可以收集干燥的二氧化碳气体;二氧化碳能溶于水,一般不用排水集气法收集,且用排水集气法收集不符合本实验要求。
[易错点] 仪器名称容易写错。选择装置有三种要求:发生装置、收集装置、制取装置,学生容易混淆,对应装置的仪器容易漏选。气体发生装置的选择应该依据反应物的状态和反应条件,收集装置要考虑气体的密度、水溶性、化学性质等,学生容易考虑不全面,从而导致选择错误。二氧化碳能溶于水,且与水反应生成碳酸,如图果要收集干燥的二氧化碳气体,只能用向上排空气法收集。
9.B 燃着的木条在氧气中燃烧更旺,在空气中正常燃烧,在二氧化碳中熄灭。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
