2021-2022学年高二上学期化学人教版(2019)选择性必修3第一章有机化合物的结构特点与研究方法单元测试(word版含解析)
文档属性
| 名称 | 2021-2022学年高二上学期化学人教版(2019)选择性必修3第一章有机化合物的结构特点与研究方法单元测试(word版含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 431.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-29 00:00:00 | ||
图片预览




文档简介
第一章《有机化合物的结构特点与研究方法》测试题
一、单选题(共12题)
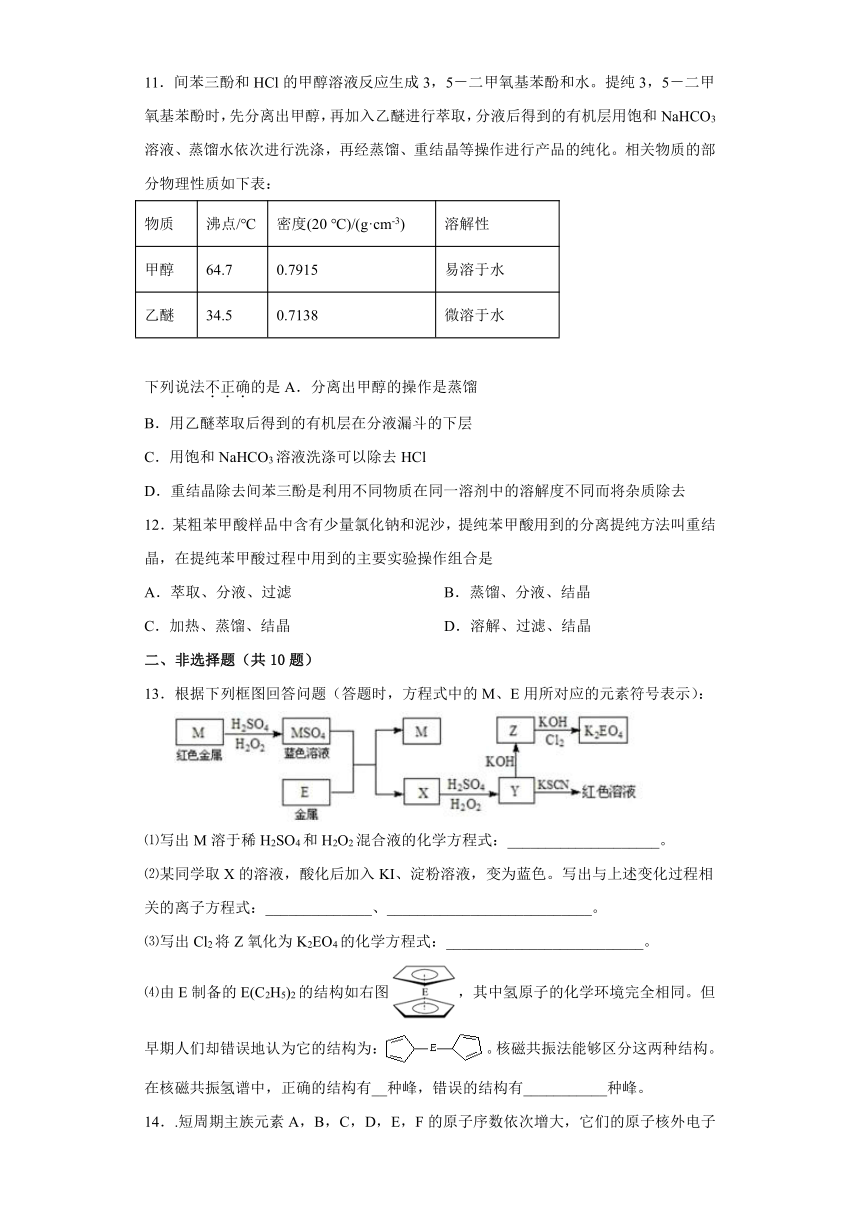
1.核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的吸收峰(信号),根据吸收峰可以确定分子中氢原子的种类和数目。例如氯甲基甲醚(ClCH2OCH3)的核磁共振氢谱如图甲所示,两个吸收峰的面积之比为3:2。金刚烷的分子立体结构如图乙所示,它的核磁共振氢谱图中吸收峰数目与峰面积之比分别为
A.5,1:6:2:3:4 B.3,1:3:12 C.4,1:6:3:6 D.2,1:3
2.已知某有机物A的核磁共振氢谱如图所示,下列说法中不正确的是
A.若分子式为,则其结构简式可能为
B.分子中不同化学环境的氢原子个数之比为1:2:3
C.该分子中氢原子个数一定为6
D.若A的化学式为,则其为丙烯
3.对如图所示两种化合物的结构或性质描述正确的是
A.均含有σ键和π键且均存在碳原子的sp3和sp2杂化
B.均为芳香族化合物
C.二者的分子式均为C10H12O
D.可用红外光谱区分,但不能用核磁共振氢谱区分
4.下列化合物的核磁共振氢谱中出现三组峰的是:
A.2,2,3,3-四甲基丁烷 B.2,3,4-三甲基戊烷 C.3,4-二甲基己烷 D.2,5-二甲基己烷
5.具有下列结构的化合物,其核磁共振氢谱中有2个峰的是
A.CH3CH2OH B.CH3CH3 C.CH3OCH3 D.HOCH2CH2OH
6.下列有机物中,一氯取代物不止一种的是
A.新戊烷 B.环己烷() C.立方烷() D.对二甲苯
7.下列关于同分异构体异构方式的说法中,不正确的是
A.CH3CH2CH2CH3和CH3CH(CH3)2属于碳架异构
B.H3CC≡CCH3和CH2=CHCH=CH2属于官能团异构
C.CH2=C(CH3)2和CH3CH=CHCH3属于官能团异构
D.和属于位置异构
8.我们已经学习过有机化合物的分类,用已有的知识对下列有机物的分类其正确的是
A.是脂环化合物 B.是芳香族化合物
C.是链状化合物 D.乙烯、苯、环己烷都属于脂肪烃
9.某烃的相对分子质量为134,该烃的所有的可能结构中属于芳香烃且苯环上只有1条交链的有
A.10种 B.8种 C.6种 D.4种
10.下列说法正确的是
A.和互为同位素
B.和互为同分异构体
C.和是同一种物质
D.与互为同系物
11.间苯三酚和HCl的甲醇溶液反应生成3,5-二甲氧基苯酚和水。提纯3,5-二甲氧基苯酚时,先分离出甲醇,再加入乙醚进行萃取,分液后得到的有机层用饱和NaHCO3溶液、蒸馏水依次进行洗涤,再经蒸馏、重结晶等操作进行产品的纯化。相关物质的部分物理性质如下表:
物质 沸点/℃ 密度(20 ℃)/(g·cm-3) 溶解性
甲醇 64.7 0.7915 易溶于水
乙醚 34.5 0.7138 微溶于水
下列说法不正确的是A.分离出甲醇的操作是蒸馏
B.用乙醚萃取后得到的有机层在分液漏斗的下层
C.用饱和NaHCO3溶液洗涤可以除去HCl
D.重结晶除去间苯三酚是利用不同物质在同一溶剂中的溶解度不同而将杂质除去
12.某粗苯甲酸样品中含有少量氯化钠和泥沙,提纯苯甲酸用到的分离提纯方法叫重结晶,在提纯苯甲酸过程中用到的主要实验操作组合是
A.萃取、分液、过滤 B.蒸馏、分液、结晶
C.加热、蒸馏、结晶 D.溶解、过滤、结晶
二、非选择题(共10题)
13.根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式:____________________。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式:______________、___________________________。
⑶写出Cl2将Z氧化为K2EO4的化学方程式:__________________________。
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有__种峰,错误的结构有___________种峰。
14..短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)E2D2的电子式:___。
(2)B与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为___,Q与水反应的化学方程式为___。
(3)A,C,D,E的原子半径由大到小的顺序是___(用元素符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性___于F(填“强”或“弱”),并用化学方程式证明上述结论___。
15.有A、B两种有机物,按要求回答下列问题:
(1)取有机物A3.0g,测得完全燃烧后生成3.6gH2O和3.36LCO2 (标准状况),已知相同条件下,该有机物的蒸气密度是氢气的30倍,则该有机物的分子式为___。
(2)有机物B的分子式为C4H8O2,其红外光谱图如图:
又测得其核磁共振氢谱图中有3组峰,且峰面积比为6:1:1,试推测该有机物的结构:___。
(3)主链含6个碳原子,有甲基、乙基2个支链的烷烃有__(不考虑立体异构)(填序号)。
A.2种 B.3种 C.4种 D.5种
(4)维生素C的结构简式为,丁香油酚的结构简式为。
下列关于二者所含官能团的说法正确的是___(填序号)。
A.均含酯基 B.均含羟基 C.均含碳碳双键
16.有下列几种有机化合物的结构简式:
①;②;③;④;⑤;⑥;⑦;⑧;⑨;⑩
(1)互为同分异构体的是_______(填序号,下同);
(2)互为同系物的是_______;
(3)官能团位置不同的同分异构体是_______;
(4)官能团类型不同的同分异构体是_______。
17.现有下列各组物质:
①和 ②和
③ 和 ④和
⑤和 ⑥和质量数为238、中子数为146的原子
⑦和
按要求用序号填空:
(1)互为同系物的是___________。
(2)互为同分异构体的是___________。
(3)互为同位素的是___________。
(4)互为同素异形体的是___________。
(5)属于同种物质的是___________。
18.按要求回答下列问题:
(1)乙烷的结构式为____。
(2)丙烷的结构简式为_____。
(3)分子中含有30个氢原子的饱和链状烷烃的分子式为____。
(4)相对分子质量为58的饱和链状烷烃的结构有____种,分别写出它们的结构简式:_____。
(5)分子式为C5H12的直链烷烃的习惯命名为____,其一氯代物只有一种的同分异构体的结构简式为___。
19.某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90,有C-O键、C=O键、C-H键、O-H键,核磁共振氢谱图有四种类型的氢原子,峰面积之比为3:1:1:1。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求:
(1)该有机物的分子式____
(2)该有机物的结构简式_____
20.为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:
(1)有机物A的相对分子质量是_______;
(2)有机物A的最简式分子式是_______,分子式是_______
(3)写出有机物A的结构简式:_______。
(4)写出有机物A的一种同分异构体结构简式:_______。
21.某研究性学习小组为了解有机物A的性质,对A的结构进行了如下实验。
实验一:通过质谱分析仪分析得知有机物A的相对分子质量为90
实验二:用_______分析发现有机物A中含有-COOH和-OH
实验三:取1.8g有机物A完全燃烧后,测得生成物为和
实验四:经_______检测发现有机物A的谱图中H原子峰值比为
(1)实验二中使用的分析仪器是_______,实验四中使用的分析仪器为_______
(2)有机物A的结构简式为_______
(3)有机物A在一定条件下可以发生的反应有_______
a.消去反应 b.取代反应 c.聚合反应 d.加成反应 e.氧化反应
(4)有机物A在浓硫酸作用下可生成多种产物。其中一种产物B的分子式为,B能和溴发生加成反应,则B的结构简式为_______另一种产物C是一种六元环状酯,则C的结构简式为:_______
(5)写出与A具有相同官能团的A的同分异构体的结构简式:_______
22.香蕉水主要用作喷漆的溶剂和稀释剂,其主要成分乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
++H2O
物质名称 相对分子质量 密度/(g·cm-3) 沸点/℃ 水中溶解性
异戊醇 88 0.8123 131 微溶
乙酸 60 1.0492 118 溶
乙酸异戊酯 130 0.8670 142 难溶
实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A(加热和夹持装置略),回流50min。反应液冷至室温后倒入分液漏斗中,先用少量水、饱和碳酸氢钠溶液洗,再用水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集得乙酸异戊酯3.9g。
回答下列问题:
(1)仪器B的名称是___________,加入碎瓷片的作用是___________。
(2)在洗涤操作中第一次用水洗的主要目的是___________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后粗产品应从分液漏斗的___________(填“上”或“下”)口分离出。
(4)实验中加入少量无水MgSO4的目的是___________。
(5)在蒸馏操作中,仪器选择及安装都正确的是___________(填标号)。
a. b. c. d.
(6)在蒸馏操作中,收集乙酸异戊酯时应控制的温度范围___________。A.115℃~125℃ B.118℃~130℃ C.130℃~140℃ D.140~143℃
(7)本实验的产率是___________。
试卷第1页,共8页
参考答案:
1.D
【解析】
由金刚烷的键线式可知,分子中的氢原子分为2类,即4个CH和6个CH2中氢原子,所以它的核磁共振氢谱图中吸收峰数目为2,峰面积之比为(4×1):(6×2)=1:3。
故选D。
2.C
【解析】
分子式为,则其结构简式可能为,含3种H,且氢原子个数之比为1:2:3,故A正确;
B.由图可知,分子中不同化学环境的氢原子个数之比为1:2:3,故B正确;
C.无法确定该有机物中H原子个数,故C错误;
D.若A的化学式为,丙烯的结构简式为,含3种H,且氢原子个数之比为1:2:3,故D正确;
故选:C。
3.A
【解析】
A.两种化合物中,前者存在苯环、碳碳单键、碳氢键,后者存在碳碳双键、碳碳单键、碳氢键,苯环和碳碳双键中含有π键和σ键,碳碳单键和碳氢键属于σ键;其中苯环和碳碳双键中的碳原子为杂化、甲基中的碳原子为杂化,故A正确;
B.芳香族化合物是指含有苯环的有机化合物,其中的结构中不含苯环结构,不属于芳香族化合物,故B错误;
C.的分子式为,的分子式为,故C错误;
D.核磁共振氢谱可以确定有机物的结构,也可以区分有机物,故D错误;
故选A。
4.D
【解析】
A. 该分子的结构简式为:,只含一种H原子,其核磁共振氢谱中只显示一组峰,A错误;
B. 该分子的结构简式为:,含四种H原子,其核磁共振氢谱中只显示四组峰,B错误;
C. 该分子的结构简式为:,含四种H原子,其核磁共振氢谱中只显示四组峰,C错误;
D. 该分子的结构简式为:,含三种H原子,其核磁共振氢谱中只显示三组峰,D正确;
故合理选项为D。
5.D
【解析】
A.乙醇分子中含有3类氢原子,核磁共振氢谱中有3个不同的吸收峰,故A不符合题意;
B.甲烷分子中含有1类氢原子,核磁共振氢谱中有1个不同的吸收峰,故B不符合题意;
C.二甲醚分子中含有1类氢原子,核磁共振氢谱中有1个不同的吸收峰,故C不符合题意;
D.乙二醇分子中含有2类氢原子,核磁共振氢谱中有2个不同的吸收峰,故D符合题意;
故选D。
6.D
【解析】
A.新戊烷分子为C(CH3)4为对称结构,只有1种氢原子,一氯取代物只有1种,故A不符合题意;
B.环己烷()的分子为对称结构,只有1种氢原子,一氯取代物只有1种,故B不符合题意;
C.立方烷()的分子为对称结构,只有1种氢原子,一氯取代物只有1种,故C不符合题意;
D.对二甲苯()分子中有2种氢原子,如图中数字,其一氯取代物有2种,故D符合题意;
答案选D。
7.C
【解析】
A.CH3CH2CH2CH3和CH3CH(CH3)2,二者的碳骨架不同,前者没有支链,后者有支链,属于碳架异构,故A正确;
B.H3CC≡CCH3的官能团为碳碳三键,CH2=CHCH=CH2的官能团为碳碳双键,二者的官能团不同,分子式相同,属于官能团异构,故B正确;
C.CH2=C(CH3)2和CH3CH=CHCH3,二者官能团相同,不属于官能团异构,前者有支链,后者没有支链,属于碳链异构,故C错误;
D.和,前者羟基在甲基的邻位,后者羟基在甲基的对位,属于位置异构,故D正确;
故选C。
8.C
【解析】
A.该结构中含有的是苯环,是芳香环化合物,故A错误;
B.该结构中不含苯环不属于芳香族化合物,故B错误;
C.由结构简式可知该结构中不含环状结构,属于链状化合物,故C正确;
D.苯属于芳香化合物,故D错误;
故选:C。
9.D
【解析】
烃只有C、H元素组成,相对分子质量为134,,分子式为C10H14的单取代芳烃,不饱和度为=4,故分子中含有一个苯环,侧链是烷基,为-C4H9,-C4H9的异构体有:-CH2CH2CH2CH3、-CH(CH3)CH2CH3、-CH2CH(CH3)2、-C(CH3)3,故符合条件的结构有4种,故选:D。
10.C
【解析】
A.H2和D2均为氢元素构成的单质,且均为双原子分子,为同种物质,故A错误;
B.甲烷为正四面体构型,则二溴甲烷只有一种结构,即和是同一种物质,故B错误;
C.和 都是异戊烷,故C正确;
D.属于酚,属于醇,结构不相似,不是同系物,故D错误;
答案选C。
11.B
【解析】
A.根据图表知,甲醇和乙醚的能互溶,但沸点不同,所以可以采用蒸馏的方法分离出甲醇,A正确;
B.根据密度知,有机层的密度小于水,是在上方,B错误;
C.混合物中含有氯化氢,氯化氢能和碳酸氢钠反应,所以为除去氯化氢用饱和NaHCO3 溶液洗涤,C正确;
D.重结晶除去间苯三酚是利用不同物质在同一溶剂中的溶解度不同而将杂质除去,从而提纯,D正确;
故选:B。
12.D
【解析】
苯甲酸的溶解度随温度的升高而增大,提纯苯甲酸的操作过程为在加热条件下将样品充分溶解,用漏斗趁热过滤得到苯甲酸溶液,待溶液缓慢冷却结晶后过滤得到苯甲酸晶体,则提纯过程的主要实验操作组合为溶解、过滤、结晶,故选D。
13. Cu+H2O2+H2SO4═CuSO4+2H2O 4Fe2++O2+4H+=4Fe3++2H2O 2Fe3++2I =2Fe2++I2 10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O 1 3
【解析】
M是红色金属,M和稀硫酸、双氧水反应生成硫酸盐,溶液呈蓝色,则M为Cu,MSO4为CuSO4;金属E和硫酸铜反应生成Cu和X,X和氯气反应生成Y,Y和KSCN溶液混合得到红色溶液,则Y为Fe2(SO4)3,X为FeSO4,E为Fe,Z和KOH、Cl2反应生成K2EO4,Z为K2FeO4,Z为Fe(OH)3,再结合题目分析解答。
(1)Cu、双氧水和稀硫酸发生氧化还原反应生成硫酸铜和水,反应方程式为Cu+H2O2+H2SO4═CuSO4+2H2O;
(2)X中含有亚铁离子,先被氧气氧化为铁离子后,酸化后加入KI、淀粉溶液,变为蓝色,说明碘离子被氧化生成碘单质,同时铁离子又被还原生成亚铁离子,离子方程式为分别是:4Fe2++O2+4H+=4Fe3++2H2O;2Fe3++2I =2Fe2++I2;
(3)氯气和KOH、氢氧化铁反应生成高铁酸钾、氯化钾和水,反应方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O;
(4)正确的结构是对称的结构,所以核磁共振氢谱中含有的吸收峰1种;而错误的结构中有与E相连的2个C、与之相邻的2个C、与之相间的2个C上有三种氢原子,所以其的核磁共振氢谱中含有的吸收峰3种,故答案为1:3。
14.(1)
(2) Mg2C3+4H2O=2Mg(OH)2+C3H4↑
(3)Na>N>O>H
(4) 弱 Na2CO3+2HClO4=CO2↑+H2O+2NaClO4或NaHCO3+HClO4=CO2↑+H2O+NaClO4
【解析】
C,D是空气中含量最多的两种元素,且原子序数C小于D,则C为氮元素,D为氧元素;B的化合物种类繁多,数目庞大,且原子序数小于氮,则应为碳元素;D,E两种元素的单质反应可以生成两种不同的离子化合物,且E的原子序数大于氧,则E为钠元素;F应位于第三周期,且为同周期半径最小的元素,则为氯元素;原子核外电子层数之和为13,则A核外有13-3-3-2-2-2=1层电子,应为氢元素。
(1)
E2D2即为Na2O2,由钠离子和过氧根构成,电子式为;
(2)
B为碳元素,与镁形成的化合物Q应为Mg3C2,烃分子中碳氢质量比为9∶1,则碳氢的个数比为=3:4,则与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑;C3H4的电子式为;
(3)
核外电子层数越多原子半径越大,电子层数相同时核电荷数越小半径越大,所以四种元素原子半径由大到小为Na>N>O>H;
(4)
高氯酸的酸性强于碳酸,所以碳的非金属性弱于氯元素,相关方程式为Na2CO3+2HClO4=CO2↑+H2O+2NaClO4或NaHCO3+HClO4=CO2↑+H2O+NaClO4。
15. C3H8O C B、C
【解析】
(1)相同条件下,该有机物的蒸气密度是氢气的30倍,则该有机物的相对分子质量为30×2=60,该有机物的物质的量为,完全燃烧后生成3.6g水和(标准状况),,,则该有机物分子中含C原子数为,含H原子数为,含O原子数为,该有机物的分子式为;
(2)由红外光谱可知有机物B中含有C=O、C-O-C结构,结合有机物B的分子式及B的核磁共振氢谱图可知其有6个氢原子处于相同化学环境,即分子中含有2个相同的甲基,则该有机物的结构为;
(3)主链含6个碳原子,对主链碳原子进行编号:,有甲基、乙基2个支链,则乙基只能连在3号碳原子上,3号碳原子上连有乙基后,分子结构不对称,甲基可以连在2、3、4、5号碳原子上,则共有4种结构,答案选C;
(4)由二者的结构简式可知,维生素C分子中含有碳碳双键、羟基、酯基;丁香油酚分子中含有羟基和碳碳双键,答案选B、C。
16. ②⑧、④⑤⑨、③⑥⑦、①⑩ ①②、②⑩ ①⑩、③⑥、④⑤ ③⑦、⑥⑦、④⑨、⑤⑨
【解析】
①的分子式为,②的分子式为,③的分子式为,④的分子式为,⑤的分子式为,⑥的分子式为,⑦的分子式为,⑧的分子式为,⑨的分子式为,⑩的分子式为。
(1)互为同分异构体的有机物必须分子式相同,且结构不同,故互为同分异构体的为①②、②⑩、④⑤⑨、③⑥⑦。
(2)同系物必须结构相似,在分子组成上相差一个或若干个原子团,①②、②⑩的官能团种类及数目相同,结构彼此相似,在分子组成上相差一个,故彼此互为同系物。
(3)官能团位置不同的同分异构体,即分子式相同,官能团种类及数目相同,官能团的位置不同,符合条件的有①⑩、③⑥、④⑤。
(4)官能团类型不同的同分异构体有③⑦、⑥⑦、④⑨、⑤⑨。
17. ⑤ ⑦ ⑥ ① ③④
【解析】
(1)的结构相似,分子组成上相差2个,二者互为同系物,故填⑤;
(2)的分子式相同,均是,结构不同,互为同分异构体,故填⑦;
(3)质量数为238、中子数为146的原子的质子数为238-146=92,与的质子数相同,中子数不同,二者互为同位素,故填⑥;
(4),是由氧元素形成的不同单质,二者互为同素异形体,故填①;
(5) 和均表示二氯甲烷,是同种物质,均表示水分子,属于同种物质,故填③④。
18.(1)
(2)CH3CH2CH3
(3)C14H30
(4) 2 CH3CH2CH2CH3、
(5) 正戊烷 C(CH3)4
【解析】
(1)
乙烷的分子式为,其结构式为;
(2)
丙烷的分子式为,其结构简式为;
(3)
由烷烃的分子通式(n为正整数)可知,,,其分子式为;
(4)
由烷烃的分子通式可知,,,的同分异构体有2种,分别为和;
(5)
分子式为的直链烷烃的习惯命名为正戊烷, 其一氯代物只有一种的同分异构体则其分子中只有一种化学环境的氢原子,其结构简式为C(CH3)4。
19. C3H6O3 CH2(OH)CH2COOH
【解析】
(1)已知m(H)=1.08g×2÷18=0.12g,m(C)=2.64g×12÷44=0.72g,则m(O)=1.8g-0.12g-0.72g=0.96g,则n(C)∶n(H)∶n(O)=0.72÷12∶0.12÷1∶0.96÷16=1∶2∶1,则其实验式为CH2O;故可设其分子式为 (CH2O)n,则有30n=90,解之得:n=3,故分子式为C3H6O3。
(2)根据有机物有C-O键、C=O键、C-H键、O-H键,其中C=O键说明可能含有醛基、羰基、羧基中一种,O-H键说明有羟基,且核磁共振氢谱图有4种类型的氢原子,峰面积之比为3:1:1:1,可以确定有机物含羧基和羟基,其结构简式为:CH2(OH)CH2COOH。
20. 46 C2H6O C2H6O CH3CH2OH CH3OCH3
【解析】
(1)由A的质谱图中最大质荷比为46可知,有机物A的相对分子质量是46,故答案为:46;
(2)由二氧化碳的物质的量和水的质量可知,2.3g有机物A中碳原子的质量为0.1mol×12g/mol=1.2g,氢原子的质量为×2×1g/mol=0.3g,则有机物A中氧原子的物质的量为=0.05mol,由碳原子、氢原子和氧原子的物质的量比为0.1mol:0.3mol:0.05mol=2:6:1可知,有机物A的最简式为C2H6O,由有机物A的相对分子质量是46可知,有机物A的分子式为C2H6O,故答案为:C2H6O;C2H6O;
(3) 分子式为C2H6O的有机物可能为CH3CH2OH和CH3OCH3,由有机物A的核磁共振氢谱有3组峰,三个峰的面积之比是1:2:3可知,A的结构简式为CH3CH2OH,故答案为:CH3CH2OH;
(4) CH3CH2OH和CH3OCH3的分子式相同,结构不同,互为同分异构体,则A的同分异构体结构简式为CH3OCH3,故答案为:CH3OCH3。
21.(1) 红外光谱仪 核磁共振氢谱仪
(2)
(3)abce
(4)
(5)
【解析】
用红外光谱分析有机物中的官能团,通过核磁共振氢谱检测有机物中含有的H原子,根据有机物燃烧后的产物计算分子中含有的元素及其个数比,根据相对分子质量确定其分子式,再结合有机物分子中含有的官能团和氢原子种类和数目确定其结构简式;2.64gCO2和1.08gH2O 中碳元素、氢元素的物质的量分别是×1=0.06mol、×2=0.12mol,根据质量守恒,1.8g有机物A中氧元素的物质的量是=0.06mol,A的最简式是CH2O,A的相对分子质量是90,所以A的分子式是C3H6O3。
(1)
实验二发现该有机物中含有羧基和羟基,即确定了有机物中的官能团,分析官能团所用的分析仪器是红外光谱仪;实验四是检测发现有机物A的谱图中H原子峰值比为3:1:1:1,分析H原子的仪器是核磁共振氢谱仪,故答案为:红外光谱仪;核磁共振氢谱仪;
(2)
由上述分析可知,A的分子式是C3H6O3,A中含有—COOH和 —OH ,核磁共振检测发现有机物A的谱图中H原子峰值比为3:1:1:1,则A的结构简式是;故答案为:;
(3)
a. 含有羟基,能发生消去反应生成CH2=CHCOOH,故a符合题意;
b. 含有羟基、羧基能发生酯化反应,酯化反应属于取代反应,故b符合题意;
c. 含有羟基、羧基能发生缩聚反应,故c符合题意;
d. 不含能加成的官能团,不能发生加成反应,故d不符合题意;
e. 含有羟基,能发生氧化反应,故e符合题意;
答案选abce,故答案为:abce;
(4)
B的分子式为C3H4O2,B能和溴发生加成反应,说明B含有碳碳双键,则B的结构简式为CH2=CHCOOH;另一种产物C是一种六元环状酯,C是一个A分子的羧基和另一个A分子的羟基之间发生酯化反应形成的,则C是,故答案为:CH2=CHCOOH;;
(5)
与A具有相同官能团,即分子中含有羟基和羧基,则符合条件的同分异构体为,故答案为:。
22.(1) 球形冷凝管或冷凝管 防止暴沸
(2)洗去大部分的硫酸和乙酸
(3)上
(4)干燥、吸水
(5)b
(6)D
(7)60%(或0.6)
【解析】
(1)
根据装置图可知:仪器B是球形冷凝管或冷凝管,加入碎瓷片的作用是防止暴沸,故答案:球形冷凝管;防止暴沸。
(2)
因为乙酸和浓硫酸都易溶于水,在洗涤操作中第一次用水洗的主要目的是除去大部分的硫酸和乙酸,故答案:洗去大部分的硫酸和乙酸。
(3)
乙酸异戊酯的密度小于水的密度,分液时在上层,待分层后粗产品应从分液漏斗的上口分离出,故答案为:上;
(4)
无水MgSO4可以吸收水分,起到干燥的作用,故答案为:干燥吸水;
(5)
在蒸馏操作中,为了获得更多的馏分,选择b装置,故答案:b。
(6)
在蒸馏操作中,乙酸异戊酯的沸点为142℃,异戊醇的沸点为131℃,乙酸的沸点为18℃,所以收集乙酸异戊酯时应控制的温度范围140~143℃,故D符合题意;
(7)
乙酸的物质的量为:n=,异戊醇的物质的量为:n=,根据++H2O反应可知,乙酸和异戊醇是按照1:1进行反应,所以乙酸过量,生成乙酸异戊酯的量要按照异戊醇的物质的量计算,即理论上生成0.05mol乙酸异戊酯;实际上生成的乙酸异戊酯的物质的量为=,所以实验中乙酸异戊酯的产率为,故答案:60%(或0.6)。
答案第1页,共2页
一、单选题(共12题)
1.核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的吸收峰(信号),根据吸收峰可以确定分子中氢原子的种类和数目。例如氯甲基甲醚(ClCH2OCH3)的核磁共振氢谱如图甲所示,两个吸收峰的面积之比为3:2。金刚烷的分子立体结构如图乙所示,它的核磁共振氢谱图中吸收峰数目与峰面积之比分别为
A.5,1:6:2:3:4 B.3,1:3:12 C.4,1:6:3:6 D.2,1:3
2.已知某有机物A的核磁共振氢谱如图所示,下列说法中不正确的是
A.若分子式为,则其结构简式可能为
B.分子中不同化学环境的氢原子个数之比为1:2:3
C.该分子中氢原子个数一定为6
D.若A的化学式为,则其为丙烯
3.对如图所示两种化合物的结构或性质描述正确的是
A.均含有σ键和π键且均存在碳原子的sp3和sp2杂化
B.均为芳香族化合物
C.二者的分子式均为C10H12O
D.可用红外光谱区分,但不能用核磁共振氢谱区分
4.下列化合物的核磁共振氢谱中出现三组峰的是:
A.2,2,3,3-四甲基丁烷 B.2,3,4-三甲基戊烷 C.3,4-二甲基己烷 D.2,5-二甲基己烷
5.具有下列结构的化合物,其核磁共振氢谱中有2个峰的是
A.CH3CH2OH B.CH3CH3 C.CH3OCH3 D.HOCH2CH2OH
6.下列有机物中,一氯取代物不止一种的是
A.新戊烷 B.环己烷() C.立方烷() D.对二甲苯
7.下列关于同分异构体异构方式的说法中,不正确的是
A.CH3CH2CH2CH3和CH3CH(CH3)2属于碳架异构
B.H3CC≡CCH3和CH2=CHCH=CH2属于官能团异构
C.CH2=C(CH3)2和CH3CH=CHCH3属于官能团异构
D.和属于位置异构
8.我们已经学习过有机化合物的分类,用已有的知识对下列有机物的分类其正确的是
A.是脂环化合物 B.是芳香族化合物
C.是链状化合物 D.乙烯、苯、环己烷都属于脂肪烃
9.某烃的相对分子质量为134,该烃的所有的可能结构中属于芳香烃且苯环上只有1条交链的有
A.10种 B.8种 C.6种 D.4种
10.下列说法正确的是
A.和互为同位素
B.和互为同分异构体
C.和是同一种物质
D.与互为同系物
11.间苯三酚和HCl的甲醇溶液反应生成3,5-二甲氧基苯酚和水。提纯3,5-二甲氧基苯酚时,先分离出甲醇,再加入乙醚进行萃取,分液后得到的有机层用饱和NaHCO3溶液、蒸馏水依次进行洗涤,再经蒸馏、重结晶等操作进行产品的纯化。相关物质的部分物理性质如下表:
物质 沸点/℃ 密度(20 ℃)/(g·cm-3) 溶解性
甲醇 64.7 0.7915 易溶于水
乙醚 34.5 0.7138 微溶于水
下列说法不正确的是A.分离出甲醇的操作是蒸馏
B.用乙醚萃取后得到的有机层在分液漏斗的下层
C.用饱和NaHCO3溶液洗涤可以除去HCl
D.重结晶除去间苯三酚是利用不同物质在同一溶剂中的溶解度不同而将杂质除去
12.某粗苯甲酸样品中含有少量氯化钠和泥沙,提纯苯甲酸用到的分离提纯方法叫重结晶,在提纯苯甲酸过程中用到的主要实验操作组合是
A.萃取、分液、过滤 B.蒸馏、分液、结晶
C.加热、蒸馏、结晶 D.溶解、过滤、结晶
二、非选择题(共10题)
13.根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式:____________________。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式:______________、___________________________。
⑶写出Cl2将Z氧化为K2EO4的化学方程式:__________________________。
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有__种峰,错误的结构有___________种峰。
14..短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)E2D2的电子式:___。
(2)B与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为___,Q与水反应的化学方程式为___。
(3)A,C,D,E的原子半径由大到小的顺序是___(用元素符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性___于F(填“强”或“弱”),并用化学方程式证明上述结论___。
15.有A、B两种有机物,按要求回答下列问题:
(1)取有机物A3.0g,测得完全燃烧后生成3.6gH2O和3.36LCO2 (标准状况),已知相同条件下,该有机物的蒸气密度是氢气的30倍,则该有机物的分子式为___。
(2)有机物B的分子式为C4H8O2,其红外光谱图如图:
又测得其核磁共振氢谱图中有3组峰,且峰面积比为6:1:1,试推测该有机物的结构:___。
(3)主链含6个碳原子,有甲基、乙基2个支链的烷烃有__(不考虑立体异构)(填序号)。
A.2种 B.3种 C.4种 D.5种
(4)维生素C的结构简式为,丁香油酚的结构简式为。
下列关于二者所含官能团的说法正确的是___(填序号)。
A.均含酯基 B.均含羟基 C.均含碳碳双键
16.有下列几种有机化合物的结构简式:
①;②;③;④;⑤;⑥;⑦;⑧;⑨;⑩
(1)互为同分异构体的是_______(填序号,下同);
(2)互为同系物的是_______;
(3)官能团位置不同的同分异构体是_______;
(4)官能团类型不同的同分异构体是_______。
17.现有下列各组物质:
①和 ②和
③ 和 ④和
⑤和 ⑥和质量数为238、中子数为146的原子
⑦和
按要求用序号填空:
(1)互为同系物的是___________。
(2)互为同分异构体的是___________。
(3)互为同位素的是___________。
(4)互为同素异形体的是___________。
(5)属于同种物质的是___________。
18.按要求回答下列问题:
(1)乙烷的结构式为____。
(2)丙烷的结构简式为_____。
(3)分子中含有30个氢原子的饱和链状烷烃的分子式为____。
(4)相对分子质量为58的饱和链状烷烃的结构有____种,分别写出它们的结构简式:_____。
(5)分子式为C5H12的直链烷烃的习惯命名为____,其一氯代物只有一种的同分异构体的结构简式为___。
19.某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90,有C-O键、C=O键、C-H键、O-H键,核磁共振氢谱图有四种类型的氢原子,峰面积之比为3:1:1:1。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求:
(1)该有机物的分子式____
(2)该有机物的结构简式_____
20.为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:
(1)有机物A的相对分子质量是_______;
(2)有机物A的最简式分子式是_______,分子式是_______
(3)写出有机物A的结构简式:_______。
(4)写出有机物A的一种同分异构体结构简式:_______。
21.某研究性学习小组为了解有机物A的性质,对A的结构进行了如下实验。
实验一:通过质谱分析仪分析得知有机物A的相对分子质量为90
实验二:用_______分析发现有机物A中含有-COOH和-OH
实验三:取1.8g有机物A完全燃烧后,测得生成物为和
实验四:经_______检测发现有机物A的谱图中H原子峰值比为
(1)实验二中使用的分析仪器是_______,实验四中使用的分析仪器为_______
(2)有机物A的结构简式为_______
(3)有机物A在一定条件下可以发生的反应有_______
a.消去反应 b.取代反应 c.聚合反应 d.加成反应 e.氧化反应
(4)有机物A在浓硫酸作用下可生成多种产物。其中一种产物B的分子式为,B能和溴发生加成反应,则B的结构简式为_______另一种产物C是一种六元环状酯,则C的结构简式为:_______
(5)写出与A具有相同官能团的A的同分异构体的结构简式:_______
22.香蕉水主要用作喷漆的溶剂和稀释剂,其主要成分乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
++H2O
物质名称 相对分子质量 密度/(g·cm-3) 沸点/℃ 水中溶解性
异戊醇 88 0.8123 131 微溶
乙酸 60 1.0492 118 溶
乙酸异戊酯 130 0.8670 142 难溶
实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A(加热和夹持装置略),回流50min。反应液冷至室温后倒入分液漏斗中,先用少量水、饱和碳酸氢钠溶液洗,再用水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集得乙酸异戊酯3.9g。
回答下列问题:
(1)仪器B的名称是___________,加入碎瓷片的作用是___________。
(2)在洗涤操作中第一次用水洗的主要目的是___________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后粗产品应从分液漏斗的___________(填“上”或“下”)口分离出。
(4)实验中加入少量无水MgSO4的目的是___________。
(5)在蒸馏操作中,仪器选择及安装都正确的是___________(填标号)。
a. b. c. d.
(6)在蒸馏操作中,收集乙酸异戊酯时应控制的温度范围___________。A.115℃~125℃ B.118℃~130℃ C.130℃~140℃ D.140~143℃
(7)本实验的产率是___________。
试卷第1页,共8页
参考答案:
1.D
【解析】
由金刚烷的键线式可知,分子中的氢原子分为2类,即4个CH和6个CH2中氢原子,所以它的核磁共振氢谱图中吸收峰数目为2,峰面积之比为(4×1):(6×2)=1:3。
故选D。
2.C
【解析】
分子式为,则其结构简式可能为,含3种H,且氢原子个数之比为1:2:3,故A正确;
B.由图可知,分子中不同化学环境的氢原子个数之比为1:2:3,故B正确;
C.无法确定该有机物中H原子个数,故C错误;
D.若A的化学式为,丙烯的结构简式为,含3种H,且氢原子个数之比为1:2:3,故D正确;
故选:C。
3.A
【解析】
A.两种化合物中,前者存在苯环、碳碳单键、碳氢键,后者存在碳碳双键、碳碳单键、碳氢键,苯环和碳碳双键中含有π键和σ键,碳碳单键和碳氢键属于σ键;其中苯环和碳碳双键中的碳原子为杂化、甲基中的碳原子为杂化,故A正确;
B.芳香族化合物是指含有苯环的有机化合物,其中的结构中不含苯环结构,不属于芳香族化合物,故B错误;
C.的分子式为,的分子式为,故C错误;
D.核磁共振氢谱可以确定有机物的结构,也可以区分有机物,故D错误;
故选A。
4.D
【解析】
A. 该分子的结构简式为:,只含一种H原子,其核磁共振氢谱中只显示一组峰,A错误;
B. 该分子的结构简式为:,含四种H原子,其核磁共振氢谱中只显示四组峰,B错误;
C. 该分子的结构简式为:,含四种H原子,其核磁共振氢谱中只显示四组峰,C错误;
D. 该分子的结构简式为:,含三种H原子,其核磁共振氢谱中只显示三组峰,D正确;
故合理选项为D。
5.D
【解析】
A.乙醇分子中含有3类氢原子,核磁共振氢谱中有3个不同的吸收峰,故A不符合题意;
B.甲烷分子中含有1类氢原子,核磁共振氢谱中有1个不同的吸收峰,故B不符合题意;
C.二甲醚分子中含有1类氢原子,核磁共振氢谱中有1个不同的吸收峰,故C不符合题意;
D.乙二醇分子中含有2类氢原子,核磁共振氢谱中有2个不同的吸收峰,故D符合题意;
故选D。
6.D
【解析】
A.新戊烷分子为C(CH3)4为对称结构,只有1种氢原子,一氯取代物只有1种,故A不符合题意;
B.环己烷()的分子为对称结构,只有1种氢原子,一氯取代物只有1种,故B不符合题意;
C.立方烷()的分子为对称结构,只有1种氢原子,一氯取代物只有1种,故C不符合题意;
D.对二甲苯()分子中有2种氢原子,如图中数字,其一氯取代物有2种,故D符合题意;
答案选D。
7.C
【解析】
A.CH3CH2CH2CH3和CH3CH(CH3)2,二者的碳骨架不同,前者没有支链,后者有支链,属于碳架异构,故A正确;
B.H3CC≡CCH3的官能团为碳碳三键,CH2=CHCH=CH2的官能团为碳碳双键,二者的官能团不同,分子式相同,属于官能团异构,故B正确;
C.CH2=C(CH3)2和CH3CH=CHCH3,二者官能团相同,不属于官能团异构,前者有支链,后者没有支链,属于碳链异构,故C错误;
D.和,前者羟基在甲基的邻位,后者羟基在甲基的对位,属于位置异构,故D正确;
故选C。
8.C
【解析】
A.该结构中含有的是苯环,是芳香环化合物,故A错误;
B.该结构中不含苯环不属于芳香族化合物,故B错误;
C.由结构简式可知该结构中不含环状结构,属于链状化合物,故C正确;
D.苯属于芳香化合物,故D错误;
故选:C。
9.D
【解析】
烃只有C、H元素组成,相对分子质量为134,,分子式为C10H14的单取代芳烃,不饱和度为=4,故分子中含有一个苯环,侧链是烷基,为-C4H9,-C4H9的异构体有:-CH2CH2CH2CH3、-CH(CH3)CH2CH3、-CH2CH(CH3)2、-C(CH3)3,故符合条件的结构有4种,故选:D。
10.C
【解析】
A.H2和D2均为氢元素构成的单质,且均为双原子分子,为同种物质,故A错误;
B.甲烷为正四面体构型,则二溴甲烷只有一种结构,即和是同一种物质,故B错误;
C.和 都是异戊烷,故C正确;
D.属于酚,属于醇,结构不相似,不是同系物,故D错误;
答案选C。
11.B
【解析】
A.根据图表知,甲醇和乙醚的能互溶,但沸点不同,所以可以采用蒸馏的方法分离出甲醇,A正确;
B.根据密度知,有机层的密度小于水,是在上方,B错误;
C.混合物中含有氯化氢,氯化氢能和碳酸氢钠反应,所以为除去氯化氢用饱和NaHCO3 溶液洗涤,C正确;
D.重结晶除去间苯三酚是利用不同物质在同一溶剂中的溶解度不同而将杂质除去,从而提纯,D正确;
故选:B。
12.D
【解析】
苯甲酸的溶解度随温度的升高而增大,提纯苯甲酸的操作过程为在加热条件下将样品充分溶解,用漏斗趁热过滤得到苯甲酸溶液,待溶液缓慢冷却结晶后过滤得到苯甲酸晶体,则提纯过程的主要实验操作组合为溶解、过滤、结晶,故选D。
13. Cu+H2O2+H2SO4═CuSO4+2H2O 4Fe2++O2+4H+=4Fe3++2H2O 2Fe3++2I =2Fe2++I2 10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O 1 3
【解析】
M是红色金属,M和稀硫酸、双氧水反应生成硫酸盐,溶液呈蓝色,则M为Cu,MSO4为CuSO4;金属E和硫酸铜反应生成Cu和X,X和氯气反应生成Y,Y和KSCN溶液混合得到红色溶液,则Y为Fe2(SO4)3,X为FeSO4,E为Fe,Z和KOH、Cl2反应生成K2EO4,Z为K2FeO4,Z为Fe(OH)3,再结合题目分析解答。
(1)Cu、双氧水和稀硫酸发生氧化还原反应生成硫酸铜和水,反应方程式为Cu+H2O2+H2SO4═CuSO4+2H2O;
(2)X中含有亚铁离子,先被氧气氧化为铁离子后,酸化后加入KI、淀粉溶液,变为蓝色,说明碘离子被氧化生成碘单质,同时铁离子又被还原生成亚铁离子,离子方程式为分别是:4Fe2++O2+4H+=4Fe3++2H2O;2Fe3++2I =2Fe2++I2;
(3)氯气和KOH、氢氧化铁反应生成高铁酸钾、氯化钾和水,反应方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O;
(4)正确的结构是对称的结构,所以核磁共振氢谱中含有的吸收峰1种;而错误的结构中有与E相连的2个C、与之相邻的2个C、与之相间的2个C上有三种氢原子,所以其的核磁共振氢谱中含有的吸收峰3种,故答案为1:3。
14.(1)
(2) Mg2C3+4H2O=2Mg(OH)2+C3H4↑
(3)Na>N>O>H
(4) 弱 Na2CO3+2HClO4=CO2↑+H2O+2NaClO4或NaHCO3+HClO4=CO2↑+H2O+NaClO4
【解析】
C,D是空气中含量最多的两种元素,且原子序数C小于D,则C为氮元素,D为氧元素;B的化合物种类繁多,数目庞大,且原子序数小于氮,则应为碳元素;D,E两种元素的单质反应可以生成两种不同的离子化合物,且E的原子序数大于氧,则E为钠元素;F应位于第三周期,且为同周期半径最小的元素,则为氯元素;原子核外电子层数之和为13,则A核外有13-3-3-2-2-2=1层电子,应为氢元素。
(1)
E2D2即为Na2O2,由钠离子和过氧根构成,电子式为;
(2)
B为碳元素,与镁形成的化合物Q应为Mg3C2,烃分子中碳氢质量比为9∶1,则碳氢的个数比为=3:4,则与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑;C3H4的电子式为;
(3)
核外电子层数越多原子半径越大,电子层数相同时核电荷数越小半径越大,所以四种元素原子半径由大到小为Na>N>O>H;
(4)
高氯酸的酸性强于碳酸,所以碳的非金属性弱于氯元素,相关方程式为Na2CO3+2HClO4=CO2↑+H2O+2NaClO4或NaHCO3+HClO4=CO2↑+H2O+NaClO4。
15. C3H8O C B、C
【解析】
(1)相同条件下,该有机物的蒸气密度是氢气的30倍,则该有机物的相对分子质量为30×2=60,该有机物的物质的量为,完全燃烧后生成3.6g水和(标准状况),,,则该有机物分子中含C原子数为,含H原子数为,含O原子数为,该有机物的分子式为;
(2)由红外光谱可知有机物B中含有C=O、C-O-C结构,结合有机物B的分子式及B的核磁共振氢谱图可知其有6个氢原子处于相同化学环境,即分子中含有2个相同的甲基,则该有机物的结构为;
(3)主链含6个碳原子,对主链碳原子进行编号:,有甲基、乙基2个支链,则乙基只能连在3号碳原子上,3号碳原子上连有乙基后,分子结构不对称,甲基可以连在2、3、4、5号碳原子上,则共有4种结构,答案选C;
(4)由二者的结构简式可知,维生素C分子中含有碳碳双键、羟基、酯基;丁香油酚分子中含有羟基和碳碳双键,答案选B、C。
16. ②⑧、④⑤⑨、③⑥⑦、①⑩ ①②、②⑩ ①⑩、③⑥、④⑤ ③⑦、⑥⑦、④⑨、⑤⑨
【解析】
①的分子式为,②的分子式为,③的分子式为,④的分子式为,⑤的分子式为,⑥的分子式为,⑦的分子式为,⑧的分子式为,⑨的分子式为,⑩的分子式为。
(1)互为同分异构体的有机物必须分子式相同,且结构不同,故互为同分异构体的为①②、②⑩、④⑤⑨、③⑥⑦。
(2)同系物必须结构相似,在分子组成上相差一个或若干个原子团,①②、②⑩的官能团种类及数目相同,结构彼此相似,在分子组成上相差一个,故彼此互为同系物。
(3)官能团位置不同的同分异构体,即分子式相同,官能团种类及数目相同,官能团的位置不同,符合条件的有①⑩、③⑥、④⑤。
(4)官能团类型不同的同分异构体有③⑦、⑥⑦、④⑨、⑤⑨。
17. ⑤ ⑦ ⑥ ① ③④
【解析】
(1)的结构相似,分子组成上相差2个,二者互为同系物,故填⑤;
(2)的分子式相同,均是,结构不同,互为同分异构体,故填⑦;
(3)质量数为238、中子数为146的原子的质子数为238-146=92,与的质子数相同,中子数不同,二者互为同位素,故填⑥;
(4),是由氧元素形成的不同单质,二者互为同素异形体,故填①;
(5) 和均表示二氯甲烷,是同种物质,均表示水分子,属于同种物质,故填③④。
18.(1)
(2)CH3CH2CH3
(3)C14H30
(4) 2 CH3CH2CH2CH3、
(5) 正戊烷 C(CH3)4
【解析】
(1)
乙烷的分子式为,其结构式为;
(2)
丙烷的分子式为,其结构简式为;
(3)
由烷烃的分子通式(n为正整数)可知,,,其分子式为;
(4)
由烷烃的分子通式可知,,,的同分异构体有2种,分别为和;
(5)
分子式为的直链烷烃的习惯命名为正戊烷, 其一氯代物只有一种的同分异构体则其分子中只有一种化学环境的氢原子,其结构简式为C(CH3)4。
19. C3H6O3 CH2(OH)CH2COOH
【解析】
(1)已知m(H)=1.08g×2÷18=0.12g,m(C)=2.64g×12÷44=0.72g,则m(O)=1.8g-0.12g-0.72g=0.96g,则n(C)∶n(H)∶n(O)=0.72÷12∶0.12÷1∶0.96÷16=1∶2∶1,则其实验式为CH2O;故可设其分子式为 (CH2O)n,则有30n=90,解之得:n=3,故分子式为C3H6O3。
(2)根据有机物有C-O键、C=O键、C-H键、O-H键,其中C=O键说明可能含有醛基、羰基、羧基中一种,O-H键说明有羟基,且核磁共振氢谱图有4种类型的氢原子,峰面积之比为3:1:1:1,可以确定有机物含羧基和羟基,其结构简式为:CH2(OH)CH2COOH。
20. 46 C2H6O C2H6O CH3CH2OH CH3OCH3
【解析】
(1)由A的质谱图中最大质荷比为46可知,有机物A的相对分子质量是46,故答案为:46;
(2)由二氧化碳的物质的量和水的质量可知,2.3g有机物A中碳原子的质量为0.1mol×12g/mol=1.2g,氢原子的质量为×2×1g/mol=0.3g,则有机物A中氧原子的物质的量为=0.05mol,由碳原子、氢原子和氧原子的物质的量比为0.1mol:0.3mol:0.05mol=2:6:1可知,有机物A的最简式为C2H6O,由有机物A的相对分子质量是46可知,有机物A的分子式为C2H6O,故答案为:C2H6O;C2H6O;
(3) 分子式为C2H6O的有机物可能为CH3CH2OH和CH3OCH3,由有机物A的核磁共振氢谱有3组峰,三个峰的面积之比是1:2:3可知,A的结构简式为CH3CH2OH,故答案为:CH3CH2OH;
(4) CH3CH2OH和CH3OCH3的分子式相同,结构不同,互为同分异构体,则A的同分异构体结构简式为CH3OCH3,故答案为:CH3OCH3。
21.(1) 红外光谱仪 核磁共振氢谱仪
(2)
(3)abce
(4)
(5)
【解析】
用红外光谱分析有机物中的官能团,通过核磁共振氢谱检测有机物中含有的H原子,根据有机物燃烧后的产物计算分子中含有的元素及其个数比,根据相对分子质量确定其分子式,再结合有机物分子中含有的官能团和氢原子种类和数目确定其结构简式;2.64gCO2和1.08gH2O 中碳元素、氢元素的物质的量分别是×1=0.06mol、×2=0.12mol,根据质量守恒,1.8g有机物A中氧元素的物质的量是=0.06mol,A的最简式是CH2O,A的相对分子质量是90,所以A的分子式是C3H6O3。
(1)
实验二发现该有机物中含有羧基和羟基,即确定了有机物中的官能团,分析官能团所用的分析仪器是红外光谱仪;实验四是检测发现有机物A的谱图中H原子峰值比为3:1:1:1,分析H原子的仪器是核磁共振氢谱仪,故答案为:红外光谱仪;核磁共振氢谱仪;
(2)
由上述分析可知,A的分子式是C3H6O3,A中含有—COOH和 —OH ,核磁共振检测发现有机物A的谱图中H原子峰值比为3:1:1:1,则A的结构简式是;故答案为:;
(3)
a. 含有羟基,能发生消去反应生成CH2=CHCOOH,故a符合题意;
b. 含有羟基、羧基能发生酯化反应,酯化反应属于取代反应,故b符合题意;
c. 含有羟基、羧基能发生缩聚反应,故c符合题意;
d. 不含能加成的官能团,不能发生加成反应,故d不符合题意;
e. 含有羟基,能发生氧化反应,故e符合题意;
答案选abce,故答案为:abce;
(4)
B的分子式为C3H4O2,B能和溴发生加成反应,说明B含有碳碳双键,则B的结构简式为CH2=CHCOOH;另一种产物C是一种六元环状酯,C是一个A分子的羧基和另一个A分子的羟基之间发生酯化反应形成的,则C是,故答案为:CH2=CHCOOH;;
(5)
与A具有相同官能团,即分子中含有羟基和羧基,则符合条件的同分异构体为,故答案为:。
22.(1) 球形冷凝管或冷凝管 防止暴沸
(2)洗去大部分的硫酸和乙酸
(3)上
(4)干燥、吸水
(5)b
(6)D
(7)60%(或0.6)
【解析】
(1)
根据装置图可知:仪器B是球形冷凝管或冷凝管,加入碎瓷片的作用是防止暴沸,故答案:球形冷凝管;防止暴沸。
(2)
因为乙酸和浓硫酸都易溶于水,在洗涤操作中第一次用水洗的主要目的是除去大部分的硫酸和乙酸,故答案:洗去大部分的硫酸和乙酸。
(3)
乙酸异戊酯的密度小于水的密度,分液时在上层,待分层后粗产品应从分液漏斗的上口分离出,故答案为:上;
(4)
无水MgSO4可以吸收水分,起到干燥的作用,故答案为:干燥吸水;
(5)
在蒸馏操作中,为了获得更多的馏分,选择b装置,故答案:b。
(6)
在蒸馏操作中,乙酸异戊酯的沸点为142℃,异戊醇的沸点为131℃,乙酸的沸点为18℃,所以收集乙酸异戊酯时应控制的温度范围140~143℃,故D符合题意;
(7)
乙酸的物质的量为:n=,异戊醇的物质的量为:n=,根据++H2O反应可知,乙酸和异戊醇是按照1:1进行反应,所以乙酸过量,生成乙酸异戊酯的量要按照异戊醇的物质的量计算,即理论上生成0.05mol乙酸异戊酯;实际上生成的乙酸异戊酯的物质的量为=,所以实验中乙酸异戊酯的产率为,故答案:60%(或0.6)。
答案第1页,共2页
