2022秋人教化学九上第六单元 碳和碳的氧化物习题(word版有答案)
文档属性
| 名称 | 2022秋人教化学九上第六单元 碳和碳的氧化物习题(word版有答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 688.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-07 00:00:00 | ||
图片预览




文档简介
2022秋人教化学九上第六单元 碳和碳的氧化物习题含答案
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、对下列事实的微观解释正确的是( )
选项 事 实 解 释
A 湿衣服被晒干 分子是不断运动的
B 1L芝麻与1L大米混合,总体积小于2L 微粒之间有一定的空隙
C 金刚石、石墨性质存在明显差异 碳原子的内部结构不同
D 水蒸发为水蒸气 有其他分子生成
A.A B.B C.C D.D
2、下列物质的用途与该物质的化学性质有关的是( )
A.用铜丝作导电线 B.金刚石用于制造切割工具
C.活性炭用于冰箱除臭 D.食品包装中充氮气以防腐
3、下列图示实验操作中,错误的是( )
A.倾倒液体 B.检验二氧化碳是否集满
C.加热液体 D.采取一定质量的
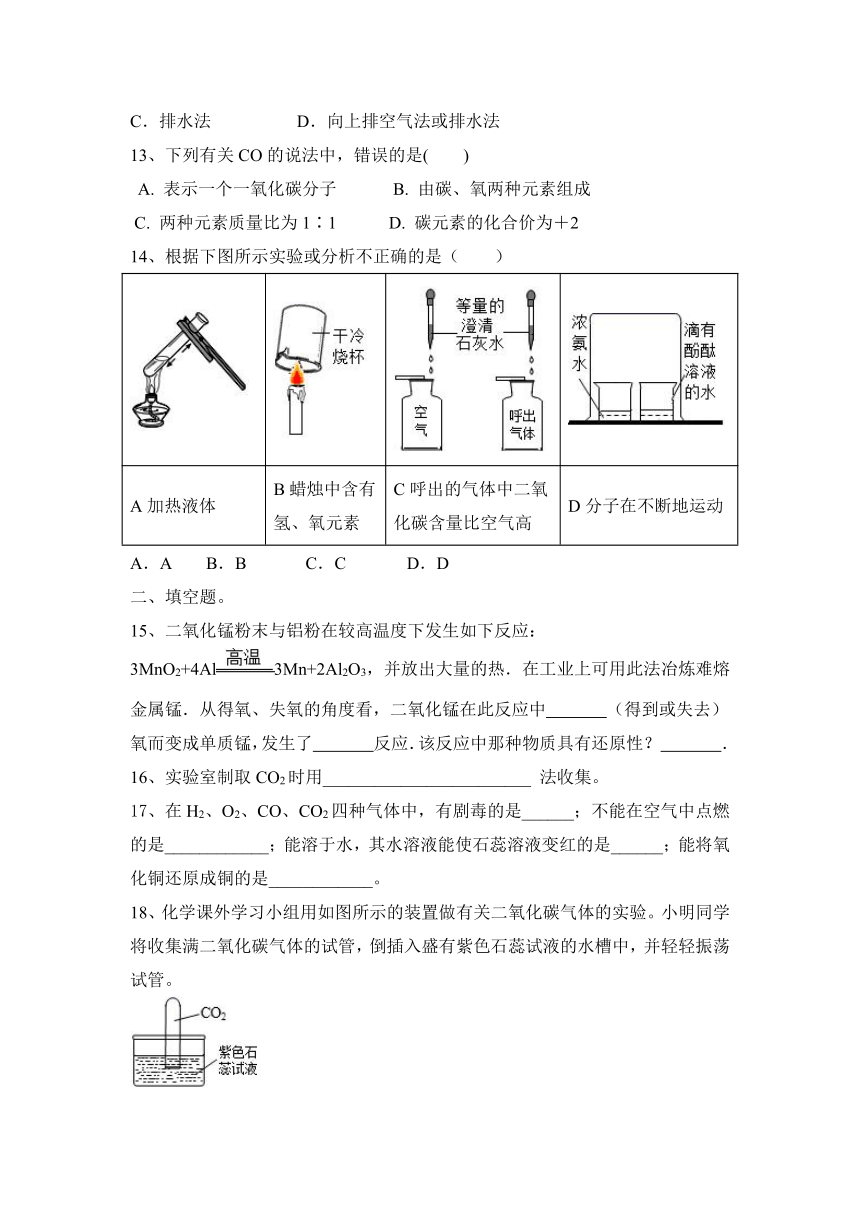
4、如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球。下列说法正确的是( )
A.①②③④都变红
B.③不变红、④变红,说明CO2密度较大
C.实验中的CO2可通过块状大理石和稀硫酸制取
D.①④变红、②③不变红,说明CO2与水反应生成酸
5、下列关于二氧化碳的描述正确的是( )
A. 向紫色石蕊溶液里通入CO2,溶液变蓝
B. 在温室中适量补充CO2可提高农作物产量
C. 空气里CO2浓度过大,会使人中毒死亡
D. CO2是气体,不能像液体一样从一个容器倒入另一个容器
6、下图是某同学探究二氧化碳的制取和性质的创新装置。下列关于该实验的叙述正确的是( )
A.浸有紫色石蕊试液的棉花会变蓝
B.实验过程中装置内会出现大量沉淀
C.上下移动的粗铜丝能控制反应的发生和停止
D.能验证二氧化碳的密度比空气大
7、下列解释不合理的是( )
A.金刚石与石墨的性质不同与它们的结构有关
B.铁丝在空气中不能被点燃与空气中氧气的体积分数有关
C.二氧化碳通入水中能使紫色石蕊试液变红与生成碳酸有关
D.过氧化氢溶液与二氧化锰混合制氧气时一开始速率变快与反应中过氧化氢浓度变化有关
8、由图可知,大气中浓度大约从1800年起急剧增加,下列解释合理的是( )
大气中浓度随时间变化图
A.大量火山的喷发 B.气候的自然波动
C.浮游生物的光合作用 D.人类大量使用化石燃料
9、教育部发布关于在全国各级各类学校禁烟事项的通知,提倡“无烟学校”,香烟的烟气中含有几百种有毒物质,其中一种物质极易与血液中的血红蛋白结合,该物质是( )
A. CO2 B. CO C. SO2 D. NO2
10、下列实验方案中,能达到预期目的的是( )
A.用稀盐酸除去盛过石灰水的试剂瓶壁上的白膜
B.将混合气体通过澄清的石灰水除去二氧化碳中混有的一氧化碳
C.用点燃的方法除去CO2中混有的少量CO
D.将气体通过红热的木炭粉除去CO2中混有的少量O2,得到纯净的CO2
11、O4是意大利的一位科学家合成的一种新型的氧分子,可以与黄金反应,该气体在振荡时会发生爆炸,产生氧气: 。下列关于这种气体的说法正确的是( )
A.O4这种气体与氧气都是由氧元素组成的,所以性质相同
B.同种元素可以组成不同的单质
C.O4这种气体是由2个氧分子构成的
D.O4这种气体化学性质比较稳定
12、实验室欲制备一氧化氮气体。已知该气体的密度比空气大,难溶于水,常温下一氧化氮与空气中的氧气发生反应,生成二氧化氮。收集一氧化氮气体的方法是( )
A.向下排空气法 B.向上排空气法
C.排水法 D.向上排空气法或排水法
13、下列有关CO的说法中,错误的是( )
A. 表示一个一氧化碳分子 B. 由碳、氧两种元素组成
C. 两种元素质量比为1∶1 D. 碳元素的化合价为+2
14、根据下图所示实验或分析不正确的是( )
A加热液体 B蜡烛中含有氢、氧元素 C呼出的气体中二氧化碳含量比空气高 D分子在不断地运动
A.A B.B C.C D.D
二、填空题。
15、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
16、实验室制取CO2时用________________________ 法收集。
17、在H2、O2、CO、CO2四种气体中,有剧毒的是______;不能在空气中点燃的是____________;能溶于水,其水溶液能使石蕊溶液变红的是______;能将氧化铜还原成铜的是____________。
18、化学课外学习小组用如图所示的装置做有关二氧化碳气体的实验。小明同学将收集满二氧化碳气体的试管,倒插入盛有紫色石蕊试液的水槽中,并轻轻振荡试管。
(1)描述上述实验产生的现象_____;
(2)写出有关反应的化学方程式_____,该化学反应类型为_____。
19、早在20世纪30年代,就有了生产人造金刚石的工厂,所用的原料是石墨,这个转化需要高温高压和催化剂,请同学们回答下列有关问题:
(1)请写出金刚石的一个用途: .
(2)金刚石和石墨的物理性质有很大差异,原因是 不同.
(3)用石墨来制金刚石,所发生的变化属于 (填“物理”或“化学”)变化.
(4)中国科学技术大学化学家在440℃和高压下,利用金属钠与二氧化碳作用得到了金刚石和碳酸钠.请写出这一反应的化学方程式 .
20、实验室制取CO2时用 _________________________ 来检验CO2,而验满的方法是_______________ 。
21、如图所示是一个正在燃烧的煤炉示意图,请回答下列问题。
(1)煤炉中煤层上方的蓝色火焰是________在燃烧,其反应的化学方程式为__________________ 。
(2)煤炉的进气口在煤炉的下方,在进气口,煤的燃烧一般都很充分,其反应的化学方程式为__________________。
(3)煤炉中CO有两个来源:①是煤的不充分燃烧,反应的化学方程式为____________________;②是____________________(写化学方程式)。
三、实验题。
22、木炭作为还原剂用于金属冶炼已有几千年历史。教材用下图实验介绍这一知识。
(1)木炭与氧化铜反应的化学方程式是_______ 。
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是__ ;
(3)酒精灯火焰处加有铁丝网罩,其作用是_______ ;
(4)不能把石灰水变浑法作为木炭跟CuO反应的充分依据。因为试管中还可能发生的反应是____ ;(写化学方程式),也可能使石灰水变浑浊。
(5)极高温下,如果木炭不足量,氧化铜还可能部分被还原为氧化亚铜,为使该反应生成亮红色的铜,氧化铜和碳的质量比可选择:(________)
A 32:3 B 40:3 C 48:3
四、计算题。
23、高温煅烧贝壳(主要成分是碳酸钙)可以生成氧化钙和二氧化碳。现有10 t贝壳煅烧后质量减少了2.2 t,可制得氧化钙的质量是多少 (假设其他成分不参加反应)
2022秋人教化学九上第六单元 碳和碳的氧化物习题含答案
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、对下列事实的微观解释正确的是( )
选项 事 实 解 释
A 湿衣服被晒干 分子是不断运动的
B 1L芝麻与1L大米混合,总体积小于2L 微粒之间有一定的空隙
C 金刚石、石墨性质存在明显差异 碳原子的内部结构不同
D 水蒸发为水蒸气 有其他分子生成
A.A B.B C.C D.D
【答案】A
2、下列物质的用途与该物质的化学性质有关的是( )
A.用铜丝作导电线 B.金刚石用于制造切割工具
C.活性炭用于冰箱除臭 D.食品包装中充氮气以防腐
【答案】D
3、下列图示实验操作中,错误的是( )
A.倾倒液体 B.检验二氧化碳是否集满
C.加热液体 D.采取一定质量的
【答案】A
4、如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球。下列说法正确的是( )
A.①②③④都变红
B.③不变红、④变红,说明CO2密度较大
C.实验中的CO2可通过块状大理石和稀硫酸制取
D.①④变红、②③不变红,说明CO2与水反应生成酸
【答案】D
5、下列关于二氧化碳的描述正确的是( )
A. 向紫色石蕊溶液里通入CO2,溶液变蓝
B. 在温室中适量补充CO2可提高农作物产量
C. 空气里CO2浓度过大,会使人中毒死亡
D. CO2是气体,不能像液体一样从一个容器倒入另一个容器
【答案】B
6、下图是某同学探究二氧化碳的制取和性质的创新装置。下列关于该实验的叙述正确的是( )
A.浸有紫色石蕊试液的棉花会变蓝
B.实验过程中装置内会出现大量沉淀
C.上下移动的粗铜丝能控制反应的发生和停止
D.能验证二氧化碳的密度比空气大
【答案】C
7、下列解释不合理的是( )
A.金刚石与石墨的性质不同与它们的结构有关
B.铁丝在空气中不能被点燃与空气中氧气的体积分数有关
C.二氧化碳通入水中能使紫色石蕊试液变红与生成碳酸有关
D.过氧化氢溶液与二氧化锰混合制氧气时一开始速率变快与反应中过氧化氢浓度变化有关
【答案】D
8、由图可知,大气中浓度大约从1800年起急剧增加,下列解释合理的是( )
大气中浓度随时间变化图
A.大量火山的喷发 B.气候的自然波动
C.浮游生物的光合作用 D.人类大量使用化石燃料
【答案】D
9、教育部发布关于在全国各级各类学校禁烟事项的通知,提倡“无烟学校”,香烟的烟气中含有几百种有毒物质,其中一种物质极易与血液中的血红蛋白结合,该物质是( )
A. CO2 B. CO C. SO2 D. NO2
【答案】B
10、下列实验方案中,能达到预期目的的是( )
A.用稀盐酸除去盛过石灰水的试剂瓶壁上的白膜
B.将混合气体通过澄清的石灰水除去二氧化碳中混有的一氧化碳
C.用点燃的方法除去CO2中混有的少量CO
D.将气体通过红热的木炭粉除去CO2中混有的少量O2,得到纯净的CO2
【答案】A
11、O4是意大利的一位科学家合成的一种新型的氧分子,可以与黄金反应,该气体在振荡时会发生爆炸,产生氧气: 。下列关于这种气体的说法正确的是( )
A.O4这种气体与氧气都是由氧元素组成的,所以性质相同
B.同种元素可以组成不同的单质
C.O4这种气体是由2个氧分子构成的
D.O4这种气体化学性质比较稳定
【答案】B
12、实验室欲制备一氧化氮气体。已知该气体的密度比空气大,难溶于水,常温下一氧化氮与空气中的氧气发生反应,生成二氧化氮。收集一氧化氮气体的方法是( )
A.向下排空气法 B.向上排空气法
C.排水法 D.向上排空气法或排水法
【答案】C
13、下列有关CO的说法中,错误的是( )
A. 表示一个一氧化碳分子 B. 由碳、氧两种元素组成
C. 两种元素质量比为1∶1 D. 碳元素的化合价为+2
【答案】C
14、根据下图所示实验或分析不正确的是( )
A加热液体 B蜡烛中含有氢、氧元素 C呼出的气体中二氧化碳含量比空气高 D分子在不断地运动
A.A B.B C.C D.D
【答案】B
二、填空题。
15、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
【答案】失去;还原;Al.
16、实验室制取CO2时用________________________ 法收集。
【答案】向上排空气
17、在H2、O2、CO、CO2四种气体中,有剧毒的是______;不能在空气中点燃的是____________;能溶于水,其水溶液能使石蕊溶液变红的是______;能将氧化铜还原成铜的是____________。
【答案】CO O2和CO2 CO2 H2和CO
18、化学课外学习小组用如图所示的装置做有关二氧化碳气体的实验。小明同学将收集满二氧化碳气体的试管,倒插入盛有紫色石蕊试液的水槽中,并轻轻振荡试管。
(1)描述上述实验产生的现象_____;
(2)写出有关反应的化学方程式_____,该化学反应类型为_____。
【答案】(1)试管内液面上升,同时试管内液体变成红色
(2)CO2+H2O═H2CO3 化合反应
19、早在20世纪30年代,就有了生产人造金刚石的工厂,所用的原料是石墨,这个转化需要高温高压和催化剂,请同学们回答下列有关问题:
(1)请写出金刚石的一个用途: .
(2)金刚石和石墨的物理性质有很大差异,原因是 不同.
(3)用石墨来制金刚石,所发生的变化属于 (填“物理”或“化学”)变化.
(4)中国科学技术大学化学家在440℃和高压下,利用金属钠与二氧化碳作用得到了金刚石和碳酸钠.请写出这一反应的化学方程式 .
【答案】(1)故填:切割大理石; (2)碳原子的排列方式;
(3)化学; (4)3CO2+4Na2Na2CO3+C.
20、实验室制取CO2时用 _________________________ 来检验CO2,而验满的方法是_______________ 。
【答案】澄清的石灰水 用一根燃着的木条放在瓶口,看木条是否熄灭
21、如图所示是一个正在燃烧的煤炉示意图,请回答下列问题。
(1)煤炉中煤层上方的蓝色火焰是________在燃烧,其反应的化学方程式为__________________ 。
(2)煤炉的进气口在煤炉的下方,在进气口,煤的燃烧一般都很充分,其反应的化学方程式为__________________。
(3)煤炉中CO有两个来源:①是煤的不充分燃烧,反应的化学方程式为____________________;②是____________________(写化学方程式)。
【答案】(1)CO(或一氧化碳) 2CO+O22CO2
(2)C+O2CO2 (3)2C+O22CO C+CO22CO
三、实验题。
22、木炭作为还原剂用于金属冶炼已有几千年历史。教材用下图实验介绍这一知识。
(1)木炭与氧化铜反应的化学方程式是_______ 。
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是__ ;
(3)酒精灯火焰处加有铁丝网罩,其作用是_______ ;
(4)不能把石灰水变浑法作为木炭跟CuO反应的充分依据。因为试管中还可能发生的反应是____ ;(写化学方程式),也可能使石灰水变浑浊。
(5)极高温下,如果木炭不足量,氧化铜还可能部分被还原为氧化亚铜,为使该反应生成亮红色的铜,氧化铜和碳的质量比可选择:(________)
A 32:3 B 40:3 C 48:3
【答案】(1)
(2)增大反应物的接触面积,使反应更充分
(3)使火焰集中并提高温度 (4) (5)A
四、计算题。
23、高温煅烧贝壳(主要成分是碳酸钙)可以生成氧化钙和二氧化碳。现有10 t贝壳煅烧后质量减少了2.2 t,可制得氧化钙的质量是多少 (假设其他成分不参加反应)
【答案】解:设可制得氧化钙的质量为x
CaCO3CaO+ CO2↑
56 44
x 2.2 t
56:44=x:2.2 t 解得x=2.8 t
答:可制得氧化钙为2.8 t。
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、对下列事实的微观解释正确的是( )
选项 事 实 解 释
A 湿衣服被晒干 分子是不断运动的
B 1L芝麻与1L大米混合,总体积小于2L 微粒之间有一定的空隙
C 金刚石、石墨性质存在明显差异 碳原子的内部结构不同
D 水蒸发为水蒸气 有其他分子生成
A.A B.B C.C D.D
2、下列物质的用途与该物质的化学性质有关的是( )
A.用铜丝作导电线 B.金刚石用于制造切割工具
C.活性炭用于冰箱除臭 D.食品包装中充氮气以防腐
3、下列图示实验操作中,错误的是( )
A.倾倒液体 B.检验二氧化碳是否集满
C.加热液体 D.采取一定质量的
4、如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球。下列说法正确的是( )
A.①②③④都变红
B.③不变红、④变红,说明CO2密度较大
C.实验中的CO2可通过块状大理石和稀硫酸制取
D.①④变红、②③不变红,说明CO2与水反应生成酸
5、下列关于二氧化碳的描述正确的是( )
A. 向紫色石蕊溶液里通入CO2,溶液变蓝
B. 在温室中适量补充CO2可提高农作物产量
C. 空气里CO2浓度过大,会使人中毒死亡
D. CO2是气体,不能像液体一样从一个容器倒入另一个容器
6、下图是某同学探究二氧化碳的制取和性质的创新装置。下列关于该实验的叙述正确的是( )
A.浸有紫色石蕊试液的棉花会变蓝
B.实验过程中装置内会出现大量沉淀
C.上下移动的粗铜丝能控制反应的发生和停止
D.能验证二氧化碳的密度比空气大
7、下列解释不合理的是( )
A.金刚石与石墨的性质不同与它们的结构有关
B.铁丝在空气中不能被点燃与空气中氧气的体积分数有关
C.二氧化碳通入水中能使紫色石蕊试液变红与生成碳酸有关
D.过氧化氢溶液与二氧化锰混合制氧气时一开始速率变快与反应中过氧化氢浓度变化有关
8、由图可知,大气中浓度大约从1800年起急剧增加,下列解释合理的是( )
大气中浓度随时间变化图
A.大量火山的喷发 B.气候的自然波动
C.浮游生物的光合作用 D.人类大量使用化石燃料
9、教育部发布关于在全国各级各类学校禁烟事项的通知,提倡“无烟学校”,香烟的烟气中含有几百种有毒物质,其中一种物质极易与血液中的血红蛋白结合,该物质是( )
A. CO2 B. CO C. SO2 D. NO2
10、下列实验方案中,能达到预期目的的是( )
A.用稀盐酸除去盛过石灰水的试剂瓶壁上的白膜
B.将混合气体通过澄清的石灰水除去二氧化碳中混有的一氧化碳
C.用点燃的方法除去CO2中混有的少量CO
D.将气体通过红热的木炭粉除去CO2中混有的少量O2,得到纯净的CO2
11、O4是意大利的一位科学家合成的一种新型的氧分子,可以与黄金反应,该气体在振荡时会发生爆炸,产生氧气: 。下列关于这种气体的说法正确的是( )
A.O4这种气体与氧气都是由氧元素组成的,所以性质相同
B.同种元素可以组成不同的单质
C.O4这种气体是由2个氧分子构成的
D.O4这种气体化学性质比较稳定
12、实验室欲制备一氧化氮气体。已知该气体的密度比空气大,难溶于水,常温下一氧化氮与空气中的氧气发生反应,生成二氧化氮。收集一氧化氮气体的方法是( )
A.向下排空气法 B.向上排空气法
C.排水法 D.向上排空气法或排水法
13、下列有关CO的说法中,错误的是( )
A. 表示一个一氧化碳分子 B. 由碳、氧两种元素组成
C. 两种元素质量比为1∶1 D. 碳元素的化合价为+2
14、根据下图所示实验或分析不正确的是( )
A加热液体 B蜡烛中含有氢、氧元素 C呼出的气体中二氧化碳含量比空气高 D分子在不断地运动
A.A B.B C.C D.D
二、填空题。
15、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
16、实验室制取CO2时用________________________ 法收集。
17、在H2、O2、CO、CO2四种气体中,有剧毒的是______;不能在空气中点燃的是____________;能溶于水,其水溶液能使石蕊溶液变红的是______;能将氧化铜还原成铜的是____________。
18、化学课外学习小组用如图所示的装置做有关二氧化碳气体的实验。小明同学将收集满二氧化碳气体的试管,倒插入盛有紫色石蕊试液的水槽中,并轻轻振荡试管。
(1)描述上述实验产生的现象_____;
(2)写出有关反应的化学方程式_____,该化学反应类型为_____。
19、早在20世纪30年代,就有了生产人造金刚石的工厂,所用的原料是石墨,这个转化需要高温高压和催化剂,请同学们回答下列有关问题:
(1)请写出金刚石的一个用途: .
(2)金刚石和石墨的物理性质有很大差异,原因是 不同.
(3)用石墨来制金刚石,所发生的变化属于 (填“物理”或“化学”)变化.
(4)中国科学技术大学化学家在440℃和高压下,利用金属钠与二氧化碳作用得到了金刚石和碳酸钠.请写出这一反应的化学方程式 .
20、实验室制取CO2时用 _________________________ 来检验CO2,而验满的方法是_______________ 。
21、如图所示是一个正在燃烧的煤炉示意图,请回答下列问题。
(1)煤炉中煤层上方的蓝色火焰是________在燃烧,其反应的化学方程式为__________________ 。
(2)煤炉的进气口在煤炉的下方,在进气口,煤的燃烧一般都很充分,其反应的化学方程式为__________________。
(3)煤炉中CO有两个来源:①是煤的不充分燃烧,反应的化学方程式为____________________;②是____________________(写化学方程式)。
三、实验题。
22、木炭作为还原剂用于金属冶炼已有几千年历史。教材用下图实验介绍这一知识。
(1)木炭与氧化铜反应的化学方程式是_______ 。
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是__ ;
(3)酒精灯火焰处加有铁丝网罩,其作用是_______ ;
(4)不能把石灰水变浑法作为木炭跟CuO反应的充分依据。因为试管中还可能发生的反应是____ ;(写化学方程式),也可能使石灰水变浑浊。
(5)极高温下,如果木炭不足量,氧化铜还可能部分被还原为氧化亚铜,为使该反应生成亮红色的铜,氧化铜和碳的质量比可选择:(________)
A 32:3 B 40:3 C 48:3
四、计算题。
23、高温煅烧贝壳(主要成分是碳酸钙)可以生成氧化钙和二氧化碳。现有10 t贝壳煅烧后质量减少了2.2 t,可制得氧化钙的质量是多少 (假设其他成分不参加反应)
2022秋人教化学九上第六单元 碳和碳的氧化物习题含答案
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、对下列事实的微观解释正确的是( )
选项 事 实 解 释
A 湿衣服被晒干 分子是不断运动的
B 1L芝麻与1L大米混合,总体积小于2L 微粒之间有一定的空隙
C 金刚石、石墨性质存在明显差异 碳原子的内部结构不同
D 水蒸发为水蒸气 有其他分子生成
A.A B.B C.C D.D
【答案】A
2、下列物质的用途与该物质的化学性质有关的是( )
A.用铜丝作导电线 B.金刚石用于制造切割工具
C.活性炭用于冰箱除臭 D.食品包装中充氮气以防腐
【答案】D
3、下列图示实验操作中,错误的是( )
A.倾倒液体 B.检验二氧化碳是否集满
C.加热液体 D.采取一定质量的
【答案】A
4、如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球。下列说法正确的是( )
A.①②③④都变红
B.③不变红、④变红,说明CO2密度较大
C.实验中的CO2可通过块状大理石和稀硫酸制取
D.①④变红、②③不变红,说明CO2与水反应生成酸
【答案】D
5、下列关于二氧化碳的描述正确的是( )
A. 向紫色石蕊溶液里通入CO2,溶液变蓝
B. 在温室中适量补充CO2可提高农作物产量
C. 空气里CO2浓度过大,会使人中毒死亡
D. CO2是气体,不能像液体一样从一个容器倒入另一个容器
【答案】B
6、下图是某同学探究二氧化碳的制取和性质的创新装置。下列关于该实验的叙述正确的是( )
A.浸有紫色石蕊试液的棉花会变蓝
B.实验过程中装置内会出现大量沉淀
C.上下移动的粗铜丝能控制反应的发生和停止
D.能验证二氧化碳的密度比空气大
【答案】C
7、下列解释不合理的是( )
A.金刚石与石墨的性质不同与它们的结构有关
B.铁丝在空气中不能被点燃与空气中氧气的体积分数有关
C.二氧化碳通入水中能使紫色石蕊试液变红与生成碳酸有关
D.过氧化氢溶液与二氧化锰混合制氧气时一开始速率变快与反应中过氧化氢浓度变化有关
【答案】D
8、由图可知,大气中浓度大约从1800年起急剧增加,下列解释合理的是( )
大气中浓度随时间变化图
A.大量火山的喷发 B.气候的自然波动
C.浮游生物的光合作用 D.人类大量使用化石燃料
【答案】D
9、教育部发布关于在全国各级各类学校禁烟事项的通知,提倡“无烟学校”,香烟的烟气中含有几百种有毒物质,其中一种物质极易与血液中的血红蛋白结合,该物质是( )
A. CO2 B. CO C. SO2 D. NO2
【答案】B
10、下列实验方案中,能达到预期目的的是( )
A.用稀盐酸除去盛过石灰水的试剂瓶壁上的白膜
B.将混合气体通过澄清的石灰水除去二氧化碳中混有的一氧化碳
C.用点燃的方法除去CO2中混有的少量CO
D.将气体通过红热的木炭粉除去CO2中混有的少量O2,得到纯净的CO2
【答案】A
11、O4是意大利的一位科学家合成的一种新型的氧分子,可以与黄金反应,该气体在振荡时会发生爆炸,产生氧气: 。下列关于这种气体的说法正确的是( )
A.O4这种气体与氧气都是由氧元素组成的,所以性质相同
B.同种元素可以组成不同的单质
C.O4这种气体是由2个氧分子构成的
D.O4这种气体化学性质比较稳定
【答案】B
12、实验室欲制备一氧化氮气体。已知该气体的密度比空气大,难溶于水,常温下一氧化氮与空气中的氧气发生反应,生成二氧化氮。收集一氧化氮气体的方法是( )
A.向下排空气法 B.向上排空气法
C.排水法 D.向上排空气法或排水法
【答案】C
13、下列有关CO的说法中,错误的是( )
A. 表示一个一氧化碳分子 B. 由碳、氧两种元素组成
C. 两种元素质量比为1∶1 D. 碳元素的化合价为+2
【答案】C
14、根据下图所示实验或分析不正确的是( )
A加热液体 B蜡烛中含有氢、氧元素 C呼出的气体中二氧化碳含量比空气高 D分子在不断地运动
A.A B.B C.C D.D
【答案】B
二、填空题。
15、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
【答案】失去;还原;Al.
16、实验室制取CO2时用________________________ 法收集。
【答案】向上排空气
17、在H2、O2、CO、CO2四种气体中,有剧毒的是______;不能在空气中点燃的是____________;能溶于水,其水溶液能使石蕊溶液变红的是______;能将氧化铜还原成铜的是____________。
【答案】CO O2和CO2 CO2 H2和CO
18、化学课外学习小组用如图所示的装置做有关二氧化碳气体的实验。小明同学将收集满二氧化碳气体的试管,倒插入盛有紫色石蕊试液的水槽中,并轻轻振荡试管。
(1)描述上述实验产生的现象_____;
(2)写出有关反应的化学方程式_____,该化学反应类型为_____。
【答案】(1)试管内液面上升,同时试管内液体变成红色
(2)CO2+H2O═H2CO3 化合反应
19、早在20世纪30年代,就有了生产人造金刚石的工厂,所用的原料是石墨,这个转化需要高温高压和催化剂,请同学们回答下列有关问题:
(1)请写出金刚石的一个用途: .
(2)金刚石和石墨的物理性质有很大差异,原因是 不同.
(3)用石墨来制金刚石,所发生的变化属于 (填“物理”或“化学”)变化.
(4)中国科学技术大学化学家在440℃和高压下,利用金属钠与二氧化碳作用得到了金刚石和碳酸钠.请写出这一反应的化学方程式 .
【答案】(1)故填:切割大理石; (2)碳原子的排列方式;
(3)化学; (4)3CO2+4Na2Na2CO3+C.
20、实验室制取CO2时用 _________________________ 来检验CO2,而验满的方法是_______________ 。
【答案】澄清的石灰水 用一根燃着的木条放在瓶口,看木条是否熄灭
21、如图所示是一个正在燃烧的煤炉示意图,请回答下列问题。
(1)煤炉中煤层上方的蓝色火焰是________在燃烧,其反应的化学方程式为__________________ 。
(2)煤炉的进气口在煤炉的下方,在进气口,煤的燃烧一般都很充分,其反应的化学方程式为__________________。
(3)煤炉中CO有两个来源:①是煤的不充分燃烧,反应的化学方程式为____________________;②是____________________(写化学方程式)。
【答案】(1)CO(或一氧化碳) 2CO+O22CO2
(2)C+O2CO2 (3)2C+O22CO C+CO22CO
三、实验题。
22、木炭作为还原剂用于金属冶炼已有几千年历史。教材用下图实验介绍这一知识。
(1)木炭与氧化铜反应的化学方程式是_______ 。
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是__ ;
(3)酒精灯火焰处加有铁丝网罩,其作用是_______ ;
(4)不能把石灰水变浑法作为木炭跟CuO反应的充分依据。因为试管中还可能发生的反应是____ ;(写化学方程式),也可能使石灰水变浑浊。
(5)极高温下,如果木炭不足量,氧化铜还可能部分被还原为氧化亚铜,为使该反应生成亮红色的铜,氧化铜和碳的质量比可选择:(________)
A 32:3 B 40:3 C 48:3
【答案】(1)
(2)增大反应物的接触面积,使反应更充分
(3)使火焰集中并提高温度 (4) (5)A
四、计算题。
23、高温煅烧贝壳(主要成分是碳酸钙)可以生成氧化钙和二氧化碳。现有10 t贝壳煅烧后质量减少了2.2 t,可制得氧化钙的质量是多少 (假设其他成分不参加反应)
【答案】解:设可制得氧化钙的质量为x
CaCO3CaO+ CO2↑
56 44
x 2.2 t
56:44=x:2.2 t 解得x=2.8 t
答:可制得氧化钙为2.8 t。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
