粤教版化学九年级上册同步提优训练: 3.2 制取氧气 第1课时 过氧化氢制氧气、催化剂(word版有答案)
文档属性
| 名称 | 粤教版化学九年级上册同步提优训练: 3.2 制取氧气 第1课时 过氧化氢制氧气、催化剂(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 237.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-09 00:00:00 | ||
图片预览

文档简介
3.2 制取氧气
第1课时 过氧化氢制氧气、催化剂
核心·易错
请判断下列说法的正误:(在括号内打“√”或“×”)
(1)凡是含氧的物质都可以作为实验室制氧气的原料( )
(2)催化剂只能加快其他物质的化学反应速率( )
(3)过氧化氢在不加入二氧化锰的条件下不产生氧气( )
(4)在过氧化氢中加入二氧化锰可以增加产生氧气的质量( )
(5)在过氧化氢制备氧气的实验中,反应后二氧化锰的质量减少( )
[易错点拨]
1.催化剂只能改变(加快或减慢)化学反应的速率,不能决定反应是否发生,也不能改变生成物的质量。2.没有催化剂,并不意味着反应不能发生。
1.按照所示进行实验,下列说法错误的是( )
A.甲中带火星的木条不复燃
B.乙中现象说明二氧化锰常温下不能产生氧气
C.丙中现象说明过氧化氢使二氧化锰产生氧气
D.该实验说明二氧化锰促进过氧化氢产生氧气
2.[2020·东莞改编] 实验室用过氧化氢制氧气的实验中,应加入少量二氧化锰。下列说法中正确的是( )
A.只有加入二氧化锰,过氧化氢才能分解产生氧气
B.二氧化锰只能作过氧化氢分解的催化剂
C.加入二氧化锰可以增加过氧化氢分解产生氧气的质量
D.二氧化锰能加快过氧化氢分解
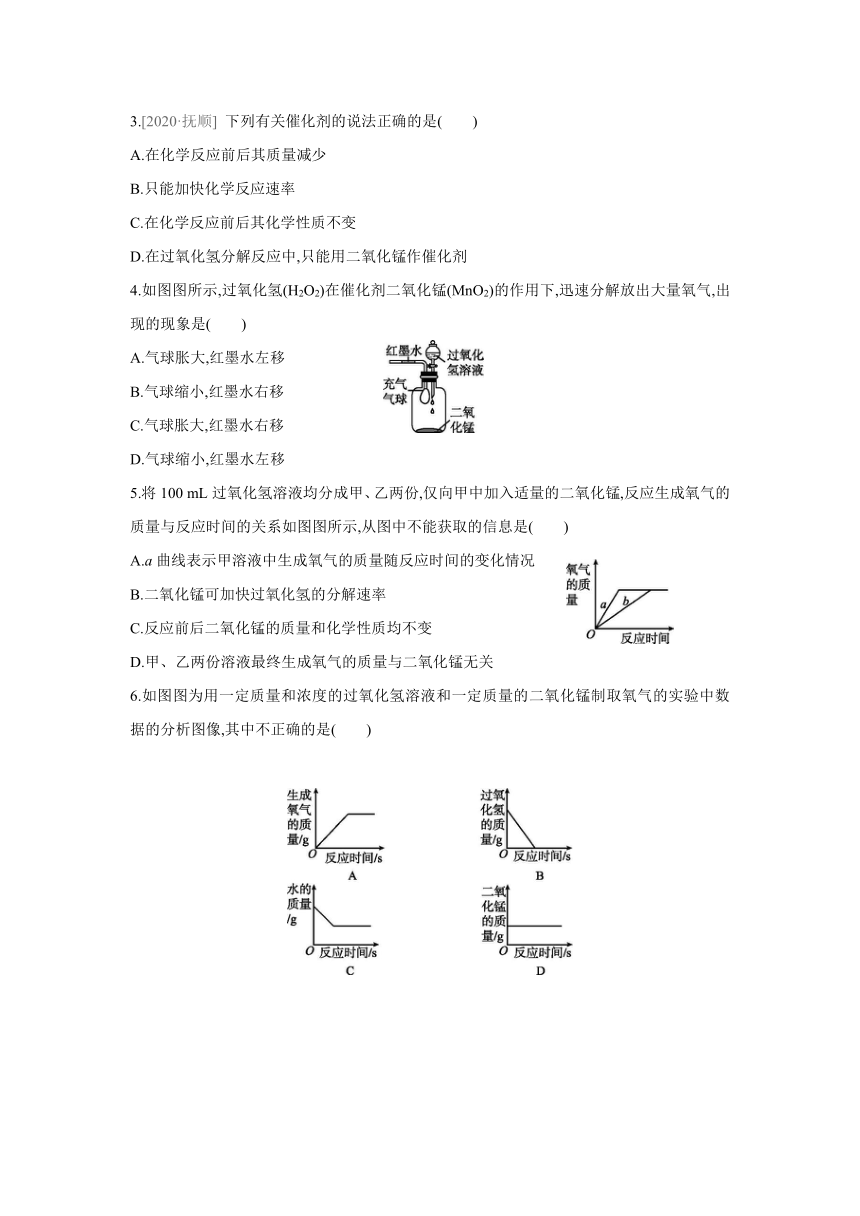
3.[2020·抚顺] 下列有关催化剂的说法正确的是( )
A.在化学反应前后其质量减少
B.只能加快化学反应速率
C.在化学反应前后其化学性质不变
D.在过氧化氢分解反应中,只能用二氧化锰作催化剂
4.如图图所示,过氧化氢(H2O2)在催化剂二氧化锰(MnO2)的作用下,迅速分解放出大量氧气,出现的现象是( )
A.气球胀大,红墨水左移
B.气球缩小,红墨水右移
C.气球胀大,红墨水右移
D.气球缩小,红墨水左移
5.将100 mL过氧化氢溶液均分成甲、乙两份,仅向甲中加入适量的二氧化锰,反应生成氧气的质量与反应时间的关系如图图所示,从图中不能获取的信息是( )
A.a曲线表示甲溶液中生成氧气的质量随反应时间的变化情况
B.二氧化锰可加快过氧化氢的分解速率
C.反应前后二氧化锰的质量和化学性质均不变
D.甲、乙两份溶液最终生成氧气的质量与二氧化锰无关
6.如图图为用一定质量和浓度的过氧化氢溶液和一定质量的二氧化锰制取氧气的实验中数据的分析图像,其中不正确的是( )
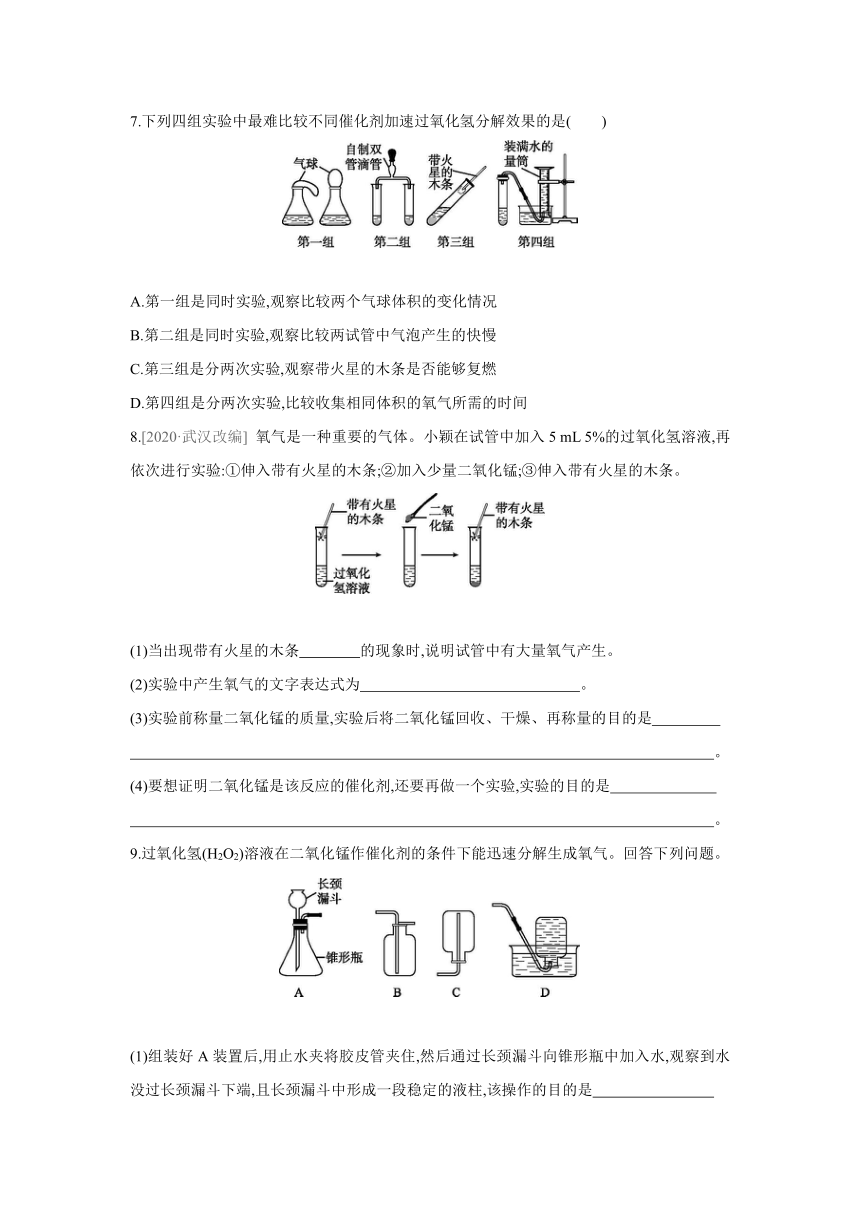
7.下列四组实验中最难比较不同催化剂加速过氧化氢分解效果的是( )
A.第一组是同时实验,观察比较两个气球体积的变化情况
B.第二组是同时实验,观察比较两试管中气泡产生的快慢
C.第三组是分两次实验,观察带火星的木条是否能够复燃
D.第四组是分两次实验,比较收集相同体积的氧气所需的时间
8.[2020·武汉改编] 氧气是一种重要的气体。小颖在试管中加入5 mL 5%的过氧化氢溶液,再依次进行实验:①伸入带有火星的木条;②加入少量二氧化锰;③伸入带有火星的木条。
(1)当出现带有火星的木条 的现象时,说明试管中有大量氧气产生。
(2)实验中产生氧气的文字表达式为 。
(3)实验前称量二氧化锰的质量,实验后将二氧化锰回收、干燥、再称量的目的是
。
(4)要想证明二氧化锰是该反应的催化剂,还要再做一个实验,实验的目的是
。
9.过氧化氢(H2O2)溶液在二氧化锰作催化剂的条件下能迅速分解生成氧气。回答下列问题。
(1)组装好A装置后,用止水夹将胶皮管夹住,然后通过长颈漏斗向锥形瓶中加入水,观察到水没过长颈漏斗下端,且长颈漏斗中形成一段稳定的液柱,该操作的目的是
。
(2)实验中通过长颈漏斗加入的物质是 ,锥形瓶中应放入的物质是 。
(3)要收集一瓶纯净的氧气,最好选择的收集装置是 (填字母);应将收集满氧气的集气瓶 放在桌面上。
(4)小红用家里的小针筒和废药瓶组装成一套微型装置(如图图所示)替代装置A,得到老师的表扬。用该装置做实验的优点是 (填序号)。
①节约药品用量
②能完全消除废液排放
③能控制液体的滴加速率
④产生的气体不含任何杂质
10.资料显示,将新制的5%的过氧化氢溶液加热到80 ℃时,才有较多氧气产生,而向相同质量5%的过氧化氢溶液中加入催化剂,常温下就会立即产生氧气,反应速率快,所需时间短。
(1)小晨按甲装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,他利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星的木条未复燃的原因是 。
(2)小柯利用催化剂使过氧化氢溶液分解制取氧气,图丙是他设计的气体发生装置,请你指出一处错误: 。
(3)采用相同质量5%的过氧化氢溶液,中虚线表示加热分解制取氧气的曲线,请你在该图中用实线画出利用催化剂制取氧气的大致曲线(假定两种方法中过氧化氢均完全分解)。
11.某同学想探究氧化铜能否作过氧化氢分解制取氧气的催化剂,下列做法中错误的是( )
A.设计对比实验探究氧化铜能否改变反应速率
B.称量反应前后氧化铜的质量是否改变
C.探究反应前后氧化铜的化学性质是否改变
D.只需要探究氧化铜能否改变反应速率即可
答案
[核心·易错]
(1)× (2)× (3)× (4)× (5)×
[应考能力提升练]
1.C
2.D 不是只有加入二氧化锰,过氧化氢才能分解产生氧气,其他的物质也可以作过氧化氢分解的催化剂,如图图硫酸铜溶液、氧化铁;二氧化锰可以作其他物质反应的催化剂,如图图氯酸钾分解制取氧气;催化剂只能改变化学反应速率,对生成物的质量无影响。
催化剂只能改变化学反应速率,不能改变生成物的质量。
3.C 催化剂在化学反应前后本身的质量不变;催化剂能改变其他物质的化学反应速率,这里的改变包括加快和减慢;一个化学反应可以用不同的催化剂。
4.D 过氧化氢在催化剂二氧化锰的作用下,迅速分解产生大量氧气,会造成瓶内压强增大,充气气球内的气体沿导管逸出,故会观察到气球缩小,红墨水左移。
5.C
6.C 过氧化氢溶液在二氧化锰作催化剂的条件下分解生成氧气和水,氧气和水的质量都增加,过氧化氢的质量减少,完全反应后,氧气和水的质量不再改变,过氧化氢质量为零;二氧化锰是催化剂,其质量在化学反应前后不变。
7.C 第一组装置相同,只有催化剂种类不同,气球胀大越快,说明催化剂加速过氧化氢分解的效果越好;第二组只有催化剂种类不同,产生气泡的速率越快,说明催化剂加速过氧化氢分解的效果越好;第三组只是比较木条是否复燃,只要物质能作催化剂,产生的氧气就能使带火星的木条复燃,不能比较出不同催化剂的催化效果;第四组只有催化剂种类不同,收集相同体积的氧气需要的时间越短,说明催化剂的催化效果越好。
8.(1)复燃
(2)过氧化氢水+氧气
(3)验证反应前后二氧化锰的质量不变
(4)验证反应前后二氧化锰的化学性质不变
探究某物质是不是某反应的催化剂,需要探究该物质能否改变反应速率,在反应前后质量和化学性质是否改变。
9.(1)检查装置气密性 (2)过氧化氢溶液 二氧化锰
(3)D 正
(4)①③
10.(1)加热过氧化氢溶液的同时,溶液中的水蒸发产生的水蒸气随氧气一起逸出,氧气中水蒸气含量过高(合理即可)
(2)长颈漏斗的下端未伸入液面以下
(3)如图图图所示(曲线要体现:①从原点开始;②斜率大于虚线;③最终产生氧气的质量相等)
[初高衔接拓展练]
11.D 能改变反应的速率,本身的质量和化学性质在反应前后没有改变的物质,才是该反应的催化剂。
第1课时 过氧化氢制氧气、催化剂
核心·易错
请判断下列说法的正误:(在括号内打“√”或“×”)
(1)凡是含氧的物质都可以作为实验室制氧气的原料( )
(2)催化剂只能加快其他物质的化学反应速率( )
(3)过氧化氢在不加入二氧化锰的条件下不产生氧气( )
(4)在过氧化氢中加入二氧化锰可以增加产生氧气的质量( )
(5)在过氧化氢制备氧气的实验中,反应后二氧化锰的质量减少( )
[易错点拨]
1.催化剂只能改变(加快或减慢)化学反应的速率,不能决定反应是否发生,也不能改变生成物的质量。2.没有催化剂,并不意味着反应不能发生。
1.按照所示进行实验,下列说法错误的是( )
A.甲中带火星的木条不复燃
B.乙中现象说明二氧化锰常温下不能产生氧气
C.丙中现象说明过氧化氢使二氧化锰产生氧气
D.该实验说明二氧化锰促进过氧化氢产生氧气
2.[2020·东莞改编] 实验室用过氧化氢制氧气的实验中,应加入少量二氧化锰。下列说法中正确的是( )
A.只有加入二氧化锰,过氧化氢才能分解产生氧气
B.二氧化锰只能作过氧化氢分解的催化剂
C.加入二氧化锰可以增加过氧化氢分解产生氧气的质量
D.二氧化锰能加快过氧化氢分解
3.[2020·抚顺] 下列有关催化剂的说法正确的是( )
A.在化学反应前后其质量减少
B.只能加快化学反应速率
C.在化学反应前后其化学性质不变
D.在过氧化氢分解反应中,只能用二氧化锰作催化剂
4.如图图所示,过氧化氢(H2O2)在催化剂二氧化锰(MnO2)的作用下,迅速分解放出大量氧气,出现的现象是( )
A.气球胀大,红墨水左移
B.气球缩小,红墨水右移
C.气球胀大,红墨水右移
D.气球缩小,红墨水左移
5.将100 mL过氧化氢溶液均分成甲、乙两份,仅向甲中加入适量的二氧化锰,反应生成氧气的质量与反应时间的关系如图图所示,从图中不能获取的信息是( )
A.a曲线表示甲溶液中生成氧气的质量随反应时间的变化情况
B.二氧化锰可加快过氧化氢的分解速率
C.反应前后二氧化锰的质量和化学性质均不变
D.甲、乙两份溶液最终生成氧气的质量与二氧化锰无关
6.如图图为用一定质量和浓度的过氧化氢溶液和一定质量的二氧化锰制取氧气的实验中数据的分析图像,其中不正确的是( )
7.下列四组实验中最难比较不同催化剂加速过氧化氢分解效果的是( )
A.第一组是同时实验,观察比较两个气球体积的变化情况
B.第二组是同时实验,观察比较两试管中气泡产生的快慢
C.第三组是分两次实验,观察带火星的木条是否能够复燃
D.第四组是分两次实验,比较收集相同体积的氧气所需的时间
8.[2020·武汉改编] 氧气是一种重要的气体。小颖在试管中加入5 mL 5%的过氧化氢溶液,再依次进行实验:①伸入带有火星的木条;②加入少量二氧化锰;③伸入带有火星的木条。
(1)当出现带有火星的木条 的现象时,说明试管中有大量氧气产生。
(2)实验中产生氧气的文字表达式为 。
(3)实验前称量二氧化锰的质量,实验后将二氧化锰回收、干燥、再称量的目的是
。
(4)要想证明二氧化锰是该反应的催化剂,还要再做一个实验,实验的目的是
。
9.过氧化氢(H2O2)溶液在二氧化锰作催化剂的条件下能迅速分解生成氧气。回答下列问题。
(1)组装好A装置后,用止水夹将胶皮管夹住,然后通过长颈漏斗向锥形瓶中加入水,观察到水没过长颈漏斗下端,且长颈漏斗中形成一段稳定的液柱,该操作的目的是
。
(2)实验中通过长颈漏斗加入的物质是 ,锥形瓶中应放入的物质是 。
(3)要收集一瓶纯净的氧气,最好选择的收集装置是 (填字母);应将收集满氧气的集气瓶 放在桌面上。
(4)小红用家里的小针筒和废药瓶组装成一套微型装置(如图图所示)替代装置A,得到老师的表扬。用该装置做实验的优点是 (填序号)。
①节约药品用量
②能完全消除废液排放
③能控制液体的滴加速率
④产生的气体不含任何杂质
10.资料显示,将新制的5%的过氧化氢溶液加热到80 ℃时,才有较多氧气产生,而向相同质量5%的过氧化氢溶液中加入催化剂,常温下就会立即产生氧气,反应速率快,所需时间短。
(1)小晨按甲装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,他利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星的木条未复燃的原因是 。
(2)小柯利用催化剂使过氧化氢溶液分解制取氧气,图丙是他设计的气体发生装置,请你指出一处错误: 。
(3)采用相同质量5%的过氧化氢溶液,中虚线表示加热分解制取氧气的曲线,请你在该图中用实线画出利用催化剂制取氧气的大致曲线(假定两种方法中过氧化氢均完全分解)。
11.某同学想探究氧化铜能否作过氧化氢分解制取氧气的催化剂,下列做法中错误的是( )
A.设计对比实验探究氧化铜能否改变反应速率
B.称量反应前后氧化铜的质量是否改变
C.探究反应前后氧化铜的化学性质是否改变
D.只需要探究氧化铜能否改变反应速率即可
答案
[核心·易错]
(1)× (2)× (3)× (4)× (5)×
[应考能力提升练]
1.C
2.D 不是只有加入二氧化锰,过氧化氢才能分解产生氧气,其他的物质也可以作过氧化氢分解的催化剂,如图图硫酸铜溶液、氧化铁;二氧化锰可以作其他物质反应的催化剂,如图图氯酸钾分解制取氧气;催化剂只能改变化学反应速率,对生成物的质量无影响。
催化剂只能改变化学反应速率,不能改变生成物的质量。
3.C 催化剂在化学反应前后本身的质量不变;催化剂能改变其他物质的化学反应速率,这里的改变包括加快和减慢;一个化学反应可以用不同的催化剂。
4.D 过氧化氢在催化剂二氧化锰的作用下,迅速分解产生大量氧气,会造成瓶内压强增大,充气气球内的气体沿导管逸出,故会观察到气球缩小,红墨水左移。
5.C
6.C 过氧化氢溶液在二氧化锰作催化剂的条件下分解生成氧气和水,氧气和水的质量都增加,过氧化氢的质量减少,完全反应后,氧气和水的质量不再改变,过氧化氢质量为零;二氧化锰是催化剂,其质量在化学反应前后不变。
7.C 第一组装置相同,只有催化剂种类不同,气球胀大越快,说明催化剂加速过氧化氢分解的效果越好;第二组只有催化剂种类不同,产生气泡的速率越快,说明催化剂加速过氧化氢分解的效果越好;第三组只是比较木条是否复燃,只要物质能作催化剂,产生的氧气就能使带火星的木条复燃,不能比较出不同催化剂的催化效果;第四组只有催化剂种类不同,收集相同体积的氧气需要的时间越短,说明催化剂的催化效果越好。
8.(1)复燃
(2)过氧化氢水+氧气
(3)验证反应前后二氧化锰的质量不变
(4)验证反应前后二氧化锰的化学性质不变
探究某物质是不是某反应的催化剂,需要探究该物质能否改变反应速率,在反应前后质量和化学性质是否改变。
9.(1)检查装置气密性 (2)过氧化氢溶液 二氧化锰
(3)D 正
(4)①③
10.(1)加热过氧化氢溶液的同时,溶液中的水蒸发产生的水蒸气随氧气一起逸出,氧气中水蒸气含量过高(合理即可)
(2)长颈漏斗的下端未伸入液面以下
(3)如图图图所示(曲线要体现:①从原点开始;②斜率大于虚线;③最终产生氧气的质量相等)
[初高衔接拓展练]
11.D 能改变反应的速率,本身的质量和化学性质在反应前后没有改变的物质,才是该反应的催化剂。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
