粤教版化学九年级上册同步提优训练: 实验四 二氧化碳实验室制取与性质(word版有答案)
文档属性
| 名称 | 粤教版化学九年级上册同步提优训练: 实验四 二氧化碳实验室制取与性质(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 252.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-09 00:00:00 | ||
图片预览


文档简介
实验四 二氧化碳实验室制取与性质
类型一 二氧化碳的实验室制取与性质
1.在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”。是他的主要实验操作,其中有误的是( )
2.[2020·滨州] 实验室制取某些气体的装置如图图所示。下列说法正确的是( )
A.装置①和③组合可以用来制取氢气
B.装置②和③组合可以用来制取氧气
C.装置②和⑤组合可以用来制取二氧化碳
D.装置②可以控制反应随时发生随时停止
3.如图图是研究二氧化碳性质的创新实验,①③为湿润的紫色石蕊试纸,②为干燥的紫色石蕊试纸。下列说法正确的是( )
A.装置A中加入的稀盐酸可用稀硫酸代替,使实验现象更明显
B.装置B中能说明二氧化碳密度比空气大的现象是③比①先变红
C.装置中①③变红,②不变红是因为生成的CO2呈酸性,能使石蕊试
纸变红
D.装置C中点燃的蜡烛自上而下熄灭,说明CO2不支持燃烧
4.[2020·眉山] 是实验室制取气体常用的发生装置和收集装置。
(1)写出仪器①的名称: 。
(2)实验室用大理石和稀盐酸反应制备二氧化碳,装入药品前的操作是 ,写出该反应的化学方程式: 。
(3)B装置中棉花的作用是 。
5.[2020·黔西南改编] 实验室利用如图图所示装置进行相关实验。
(1)实验室制取二氧化碳的化学方程式为 。
(2)C装置中实验所需二氧化碳,应选用A、B发生装置中的 装置获得。在仪器组装后、加入药品前,需要进行的操作是 。
(3)制得的二氧化碳干燥后利用C装置进行实验,b处的实验现象是 。若要证明b处二氧化碳与水发生了反应,可在a处放置 。
(4)根据烧杯中的实验现象,能得出的结论是 、 。
类型二 实验室制取气体的一般思路
6.下列关于实验室制取气体的思路和方法,说法正确的是( )
A.选择制取气体的药品,应考虑反应是否易发生、原料是否易获得、价格是否便宜等
B.设计气体发生装置和收集装置时,都应该充分考虑该气体的密度和溶解性
C.验满氧气时,应将燃着的木条伸入集气瓶中
D.检验二氧化碳时将燃着的木条置于集气瓶口,若火焰熄灭,说明制取的气体是二氧化碳
7.实验室用过氧化氢溶液制氧气和用大理石与稀盐酸反应制二氧化碳相比较,正确的是
( )
A.反应都需要催化剂
B.反应基本类型都是分解反应
C.所用药品的状态相同
D.收集的方法完全不同
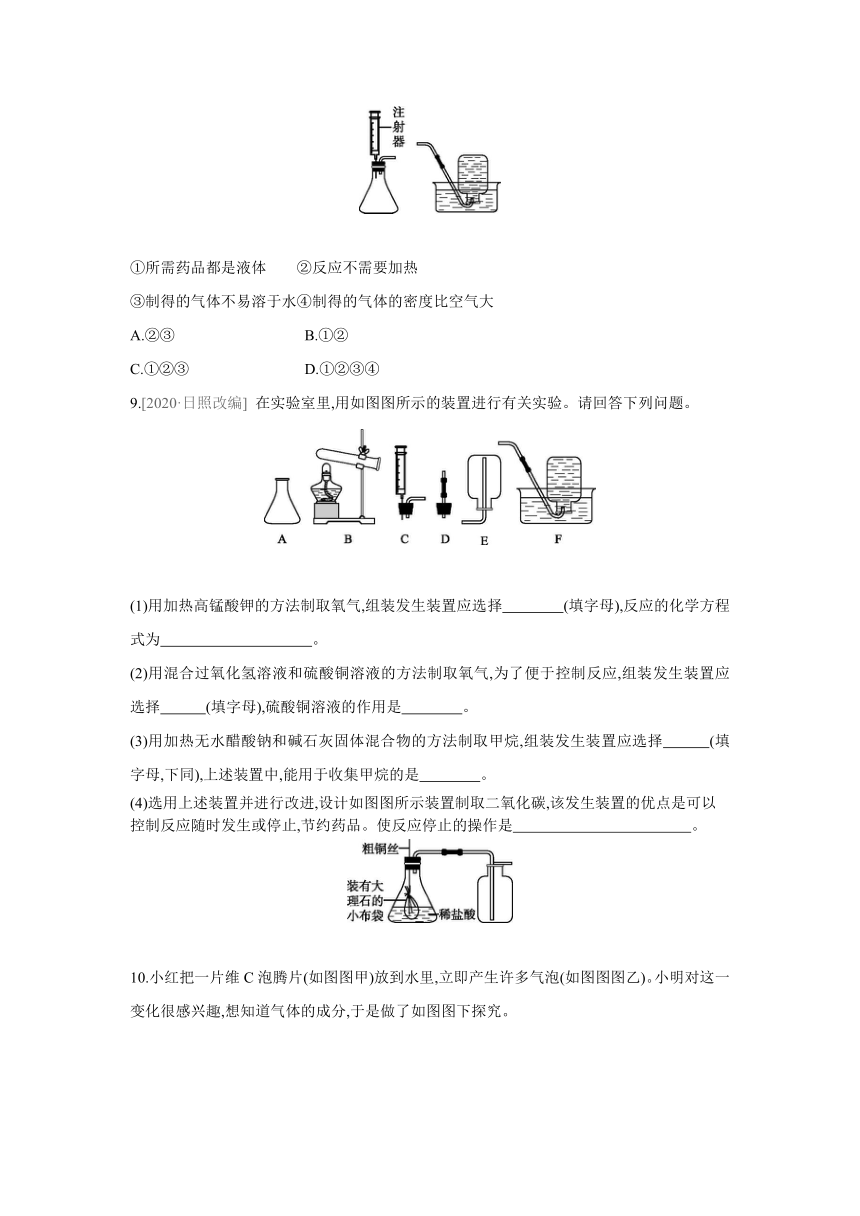
8.用如图图所示装置来制取和收集气体,需要满足的条件是( )
①所需药品都是液体 ②反应不需要加热
③制得的气体不易溶于水④制得的气体的密度比空气大
A.②③ B.①②
C.①②③ D.①②③④
9.[2020·日照改编] 在实验室里,用如图图所示的装置进行有关实验。请回答下列问题。
(1)用加热高锰酸钾的方法制取氧气,组装发生装置应选择 (填字母),反应的化学方程式为 。
(2)用混合过氧化氢溶液和硫酸铜溶液的方法制取氧气,为了便于控制反应,组装发生装置应选择 (填字母),硫酸铜溶液的作用是 。
(3)用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,组装发生装置应选择 (填字母,下同),上述装置中,能用于收集甲烷的是 。
(4)选用上述装置并进行改进,设计如图图所示装置制取二氧化碳,该发生装置的优点是可以控制反应随时发生或停止,节约药品。使反应停止的操作是 。
10.小红把一片维C泡腾片(如图图甲)放到水里,立即产生许多气泡(如图图图乙)。小明对这一变化很感兴趣,想知道气体的成分,于是做了如图图下探究。
[作出猜想] 该气体可能是CO2、O2、CO、H2、N2。
小明说:“不可能含有N2,因为
。”
小红说:“不可能含有CO和H2,因为从安全角度考虑,H2易燃易爆,CO 。”
经分析,他们认为:该气体可能含有CO2、O2中的一种或两种。
[进行实验]
实验编号 实验操作 实验现象
① 将气体通入澄清石灰水中 澄清石灰水变浑浊
② 将带火星的木条伸入该气体中 带火星的木条没有复燃
[得出结论] (1)由实验①可知,该气体中肯定含有CO2,发生反应的化学方程式是
。
(2)由实验②不能确定该气体中不含氧气,改进的方法是先 ,然后再用带火星的木条检验。经实验证实气体中确实不含氧气。
[拓展与反思] 用维C泡腾片制取二氧化碳气体。
用下列仪器组合一套制备并收集二氧化碳的装置,所用仪器组合是 (填序号)。你组装的装置的优点是 。
答案
1.B 用向上排空气法收集二氧化碳时,导管要伸到集气瓶底部。
2.B 实验室用锌和稀硫酸常温制取氢气,属于固液不加热型,发生装置选②,由于氢气密度比空气小,可以用向下排空气法收集,收集装置应选④; 实验室制取氧气可以采取过氧化氢分解法,用二氧化锰作催化剂,属于固液不加热型,发生装置选②,由于氧气密度比空气大,不易溶于水,可以选择向上排空气法或排水法收集,收集装置选③或⑤;实验室用大理石(或石灰石)与稀盐酸制取二氧化碳,属于固液不加热型,因此发生装置选②,由于二氧化碳能溶于水,因此收集装置不能选择⑤;装置②中固体与液体接触后不能进行分离,不能控制反应随时发生随时停止。
3.B 石灰石与稀硫酸反应,生成微溶于水的硫酸钙,硫酸钙覆盖在石灰石表面,阻碍反应进一步进行,装置A中加入的稀盐酸若用稀硫酸代替,实验现象更不明显;湿润的石蕊试纸变红,且③比①先变红,说明二氧化碳的密度比空气的大;①③为湿润的紫色石蕊试纸,②为干燥的紫色石蕊试纸,②不变红,说明二氧化碳不能使紫色石蕊变红,①③变红,是因为二氧化碳与水反应生成的碳酸呈酸性,能使石蕊试纸变红;装置C中点燃的蜡烛应该自下而上熄灭,说明二氧化碳的密度比空气的大,不能燃烧也不支持燃烧。
4.(1)集气瓶
(2)检查装置气密性 CaCO3+2HClCaCl2+CO2↑+H2O
(3)防止高锰酸钾粉末进入导气管
5.(1)CaCO3 + 2HClCaCl2 + H2O + CO2↑
(2)B 检查装置的气密性
(3)紫色石蕊溶液变红 用石蕊溶液染成紫色的干燥小花
(4)CO2不能燃烧也不支持燃烧 CO2密度比空气大
(1)实验室用大理石或石灰石和稀盐酸来制取二氧化碳,化学方程式是CaCO3+2HClCaCl2+H2O+CO2↑。(2)实验室制取二氧化碳不需要加热,C装置中实验所需要的二氧化碳,应选用B装置获得;在仪器组装后、加入药品前,需要进行的操作是检查装置的气密性。(3)CO2与水反应生成碳酸,碳酸能使紫色石蕊溶液变红;若要证明b处二氧化碳与水发生了反应,可在a处放置石蕊溶液染成紫色的干燥小花。(4)向小烧杯中通入二氧化碳,放在低处的蜡烛先熄灭,放在高处的蜡烛后熄灭,能得出的结论是二氧化碳的密度比空气大,既不能燃烧也不支持燃烧。
6.A 选择制取气体的药品,应考虑反应是否易发生、原料是否易获得、价格是否便宜、制得的气体要纯净等;发生装置的选择与反应物的状态和反应条件有关,无须考虑气体的密度和溶解性,设计气体的收集装置时,应该充分考虑该气体的密度和溶解性;检验氧气是否收集满时,应将带火星的木条放在集气瓶口;检验二氧化碳应使用澄清石灰水。
7.C 实验室用过氧化氢溶液制氧气和用大理石与稀盐酸反应制二氧化碳,所用药品的状态相同,都属于固液常温型。
8.A
9. (1)BD 2KMnO4K2MnO4+MnO2+O2↑
(2)AC 催化作用
(3)BD E(或F)
(4)抽拉(或提起)粗铜丝,使小布袋与液体脱离接触
(1)用加热高锰酸钾的方法制取氧气,属于固体加热型,组装发生装置应选择BD,加热高锰酸钾反应生成锰酸钾、二氧化锰和氧气,化学方程式为2KMnO4K2MnO4+MnO2+O2↑ 。(2)用混合过氧化氢溶液和硫酸铜溶液的方法制取氧气,属于液体混合不需加热型,为了便于控制反应,组装发生装置应选择AC,硫酸铜溶液的作用是作催化剂,起催化作用。(3)用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,属于固体混合加热型,组装发生装置应选择BD,甲烷难溶于水、密度比空气小,可用排水法或向下排空气法收集,图中装置中,能用于收集甲烷的是 E或F。(4)液体与固体分离可使反应停止,操作是抽拉(或提起)粗铜丝,使小布袋与液体脱离接触。
10.[作出猜想] 化学反应前后元素种类不变,泡腾片和水中都不含氮元素 有毒
[得出结论] (1)Ca(OH)2+CO2CaCO3↓+H2O
(2)将该气体通过足量的澄清石灰水
[拓展与反思] ①②⑦⑧ 可以随时添加药品并制得较多量的气体(与上空对应,合理即可)
类型一 二氧化碳的实验室制取与性质
1.在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”。是他的主要实验操作,其中有误的是( )
2.[2020·滨州] 实验室制取某些气体的装置如图图所示。下列说法正确的是( )
A.装置①和③组合可以用来制取氢气
B.装置②和③组合可以用来制取氧气
C.装置②和⑤组合可以用来制取二氧化碳
D.装置②可以控制反应随时发生随时停止
3.如图图是研究二氧化碳性质的创新实验,①③为湿润的紫色石蕊试纸,②为干燥的紫色石蕊试纸。下列说法正确的是( )
A.装置A中加入的稀盐酸可用稀硫酸代替,使实验现象更明显
B.装置B中能说明二氧化碳密度比空气大的现象是③比①先变红
C.装置中①③变红,②不变红是因为生成的CO2呈酸性,能使石蕊试
纸变红
D.装置C中点燃的蜡烛自上而下熄灭,说明CO2不支持燃烧
4.[2020·眉山] 是实验室制取气体常用的发生装置和收集装置。
(1)写出仪器①的名称: 。
(2)实验室用大理石和稀盐酸反应制备二氧化碳,装入药品前的操作是 ,写出该反应的化学方程式: 。
(3)B装置中棉花的作用是 。
5.[2020·黔西南改编] 实验室利用如图图所示装置进行相关实验。
(1)实验室制取二氧化碳的化学方程式为 。
(2)C装置中实验所需二氧化碳,应选用A、B发生装置中的 装置获得。在仪器组装后、加入药品前,需要进行的操作是 。
(3)制得的二氧化碳干燥后利用C装置进行实验,b处的实验现象是 。若要证明b处二氧化碳与水发生了反应,可在a处放置 。
(4)根据烧杯中的实验现象,能得出的结论是 、 。
类型二 实验室制取气体的一般思路
6.下列关于实验室制取气体的思路和方法,说法正确的是( )
A.选择制取气体的药品,应考虑反应是否易发生、原料是否易获得、价格是否便宜等
B.设计气体发生装置和收集装置时,都应该充分考虑该气体的密度和溶解性
C.验满氧气时,应将燃着的木条伸入集气瓶中
D.检验二氧化碳时将燃着的木条置于集气瓶口,若火焰熄灭,说明制取的气体是二氧化碳
7.实验室用过氧化氢溶液制氧气和用大理石与稀盐酸反应制二氧化碳相比较,正确的是
( )
A.反应都需要催化剂
B.反应基本类型都是分解反应
C.所用药品的状态相同
D.收集的方法完全不同
8.用如图图所示装置来制取和收集气体,需要满足的条件是( )
①所需药品都是液体 ②反应不需要加热
③制得的气体不易溶于水④制得的气体的密度比空气大
A.②③ B.①②
C.①②③ D.①②③④
9.[2020·日照改编] 在实验室里,用如图图所示的装置进行有关实验。请回答下列问题。
(1)用加热高锰酸钾的方法制取氧气,组装发生装置应选择 (填字母),反应的化学方程式为 。
(2)用混合过氧化氢溶液和硫酸铜溶液的方法制取氧气,为了便于控制反应,组装发生装置应选择 (填字母),硫酸铜溶液的作用是 。
(3)用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,组装发生装置应选择 (填字母,下同),上述装置中,能用于收集甲烷的是 。
(4)选用上述装置并进行改进,设计如图图所示装置制取二氧化碳,该发生装置的优点是可以控制反应随时发生或停止,节约药品。使反应停止的操作是 。
10.小红把一片维C泡腾片(如图图甲)放到水里,立即产生许多气泡(如图图图乙)。小明对这一变化很感兴趣,想知道气体的成分,于是做了如图图下探究。
[作出猜想] 该气体可能是CO2、O2、CO、H2、N2。
小明说:“不可能含有N2,因为
。”
小红说:“不可能含有CO和H2,因为从安全角度考虑,H2易燃易爆,CO 。”
经分析,他们认为:该气体可能含有CO2、O2中的一种或两种。
[进行实验]
实验编号 实验操作 实验现象
① 将气体通入澄清石灰水中 澄清石灰水变浑浊
② 将带火星的木条伸入该气体中 带火星的木条没有复燃
[得出结论] (1)由实验①可知,该气体中肯定含有CO2,发生反应的化学方程式是
。
(2)由实验②不能确定该气体中不含氧气,改进的方法是先 ,然后再用带火星的木条检验。经实验证实气体中确实不含氧气。
[拓展与反思] 用维C泡腾片制取二氧化碳气体。
用下列仪器组合一套制备并收集二氧化碳的装置,所用仪器组合是 (填序号)。你组装的装置的优点是 。
答案
1.B 用向上排空气法收集二氧化碳时,导管要伸到集气瓶底部。
2.B 实验室用锌和稀硫酸常温制取氢气,属于固液不加热型,发生装置选②,由于氢气密度比空气小,可以用向下排空气法收集,收集装置应选④; 实验室制取氧气可以采取过氧化氢分解法,用二氧化锰作催化剂,属于固液不加热型,发生装置选②,由于氧气密度比空气大,不易溶于水,可以选择向上排空气法或排水法收集,收集装置选③或⑤;实验室用大理石(或石灰石)与稀盐酸制取二氧化碳,属于固液不加热型,因此发生装置选②,由于二氧化碳能溶于水,因此收集装置不能选择⑤;装置②中固体与液体接触后不能进行分离,不能控制反应随时发生随时停止。
3.B 石灰石与稀硫酸反应,生成微溶于水的硫酸钙,硫酸钙覆盖在石灰石表面,阻碍反应进一步进行,装置A中加入的稀盐酸若用稀硫酸代替,实验现象更不明显;湿润的石蕊试纸变红,且③比①先变红,说明二氧化碳的密度比空气的大;①③为湿润的紫色石蕊试纸,②为干燥的紫色石蕊试纸,②不变红,说明二氧化碳不能使紫色石蕊变红,①③变红,是因为二氧化碳与水反应生成的碳酸呈酸性,能使石蕊试纸变红;装置C中点燃的蜡烛应该自下而上熄灭,说明二氧化碳的密度比空气的大,不能燃烧也不支持燃烧。
4.(1)集气瓶
(2)检查装置气密性 CaCO3+2HClCaCl2+CO2↑+H2O
(3)防止高锰酸钾粉末进入导气管
5.(1)CaCO3 + 2HClCaCl2 + H2O + CO2↑
(2)B 检查装置的气密性
(3)紫色石蕊溶液变红 用石蕊溶液染成紫色的干燥小花
(4)CO2不能燃烧也不支持燃烧 CO2密度比空气大
(1)实验室用大理石或石灰石和稀盐酸来制取二氧化碳,化学方程式是CaCO3+2HClCaCl2+H2O+CO2↑。(2)实验室制取二氧化碳不需要加热,C装置中实验所需要的二氧化碳,应选用B装置获得;在仪器组装后、加入药品前,需要进行的操作是检查装置的气密性。(3)CO2与水反应生成碳酸,碳酸能使紫色石蕊溶液变红;若要证明b处二氧化碳与水发生了反应,可在a处放置石蕊溶液染成紫色的干燥小花。(4)向小烧杯中通入二氧化碳,放在低处的蜡烛先熄灭,放在高处的蜡烛后熄灭,能得出的结论是二氧化碳的密度比空气大,既不能燃烧也不支持燃烧。
6.A 选择制取气体的药品,应考虑反应是否易发生、原料是否易获得、价格是否便宜、制得的气体要纯净等;发生装置的选择与反应物的状态和反应条件有关,无须考虑气体的密度和溶解性,设计气体的收集装置时,应该充分考虑该气体的密度和溶解性;检验氧气是否收集满时,应将带火星的木条放在集气瓶口;检验二氧化碳应使用澄清石灰水。
7.C 实验室用过氧化氢溶液制氧气和用大理石与稀盐酸反应制二氧化碳,所用药品的状态相同,都属于固液常温型。
8.A
9. (1)BD 2KMnO4K2MnO4+MnO2+O2↑
(2)AC 催化作用
(3)BD E(或F)
(4)抽拉(或提起)粗铜丝,使小布袋与液体脱离接触
(1)用加热高锰酸钾的方法制取氧气,属于固体加热型,组装发生装置应选择BD,加热高锰酸钾反应生成锰酸钾、二氧化锰和氧气,化学方程式为2KMnO4K2MnO4+MnO2+O2↑ 。(2)用混合过氧化氢溶液和硫酸铜溶液的方法制取氧气,属于液体混合不需加热型,为了便于控制反应,组装发生装置应选择AC,硫酸铜溶液的作用是作催化剂,起催化作用。(3)用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,属于固体混合加热型,组装发生装置应选择BD,甲烷难溶于水、密度比空气小,可用排水法或向下排空气法收集,图中装置中,能用于收集甲烷的是 E或F。(4)液体与固体分离可使反应停止,操作是抽拉(或提起)粗铜丝,使小布袋与液体脱离接触。
10.[作出猜想] 化学反应前后元素种类不变,泡腾片和水中都不含氮元素 有毒
[得出结论] (1)Ca(OH)2+CO2CaCO3↓+H2O
(2)将该气体通过足量的澄清石灰水
[拓展与反思] ①②⑦⑧ 可以随时添加药品并制得较多量的气体(与上空对应,合理即可)
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
