粤教版化学九年级上册同步提优训练: 第二章 空气、物质的构成 综合提升卷(word版有答案)
文档属性
| 名称 | 粤教版化学九年级上册同步提优训练: 第二章 空气、物质的构成 综合提升卷(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 359.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-09 00:00:00 | ||
图片预览



文档简介
第二章综合提升卷
[范围: 空气、物质的构成 时间:40分钟 分值:100分]
一、选择题(共45分)
1.[2020·怀化改编] 下列物质不是空气成分的是( )
A.作保护气的氮气(N2)
B.气球填充气氦气(He)
C.医疗急救用的氧气(O2)
D.火箭新型推进剂液氢(H2)
2.[2020·菏泽] “绿色发展”“低碳生活”等理念逐渐深入人心。下列做法不符合该理念的是
( )
A.为节约和环保,分类回收生活垃圾
B.能源结构向多元、清洁和低碳方向转型
C.为防止影响小区人们生活,在空旷偏僻的地方燃烧塑料垃圾
D.鼓励乘坐公交车或骑自行车出行
3.下列排序正确是( )
A.相对原子质量:碳原子>氧原子>硫原子
B.酒精灯火焰的温度:焰心>内焰>外焰
C.地壳中元素含量:Fe>Al>Si>O
D.物质在空气中的体积分数:氮气>氧气>稀有气体>二氧化碳
4.下列关于物质组成的叙述中,正确的是( )
A.纯净物的组成中只含一种元素
B.混合物的组成中肯定含有多种元素
C.不同物质可以含有相同的元素
D.含氧元素的化合物就是氧化物
5.下列关于原子核的叙述正确的是( )
①通常由中子和电子构成 ②通常由质子和中子构成 ③带正电荷
④不显电性 ⑤不能再分 ⑥跟原子比较体积很小,但却集中了原子的主要质量
A.②④⑥ B.①③⑤
C.①②⑤ D.②③⑥
6.用分子的相关知识解释下列生活中的现象,其中错误的是( )
A.热胀冷缩,说明分子的大小随温度升降而改变
B.“酒香不怕巷子深”,说明分子在不停地运动
C.10 mL酒精和10 mL水混合后,体积小于20 mL,说明分子间有间隔
D.湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快
7.下列对分子、原子、离子的认识,正确的是( )
A.原子是最小的微粒,不可再分
B.相同原子可构成不同的分子
C.离子不能直接构成物质
D.固体难压缩,说明固体分子间无间隔
8.铈是一种稀土元素,在元素周期表中铈元素的某些信息如图图所示,下列有关铈的说法正确的是( )
A.元素符号为Ce
B.属于非金属元素
C.相对原子质量为140.1 g
D.原子核内中子数为58
9.根据钠原子的结构示意图不能确定的是( )
A.质子数
B.电子层数
C.相对原子质量
D.元素种类
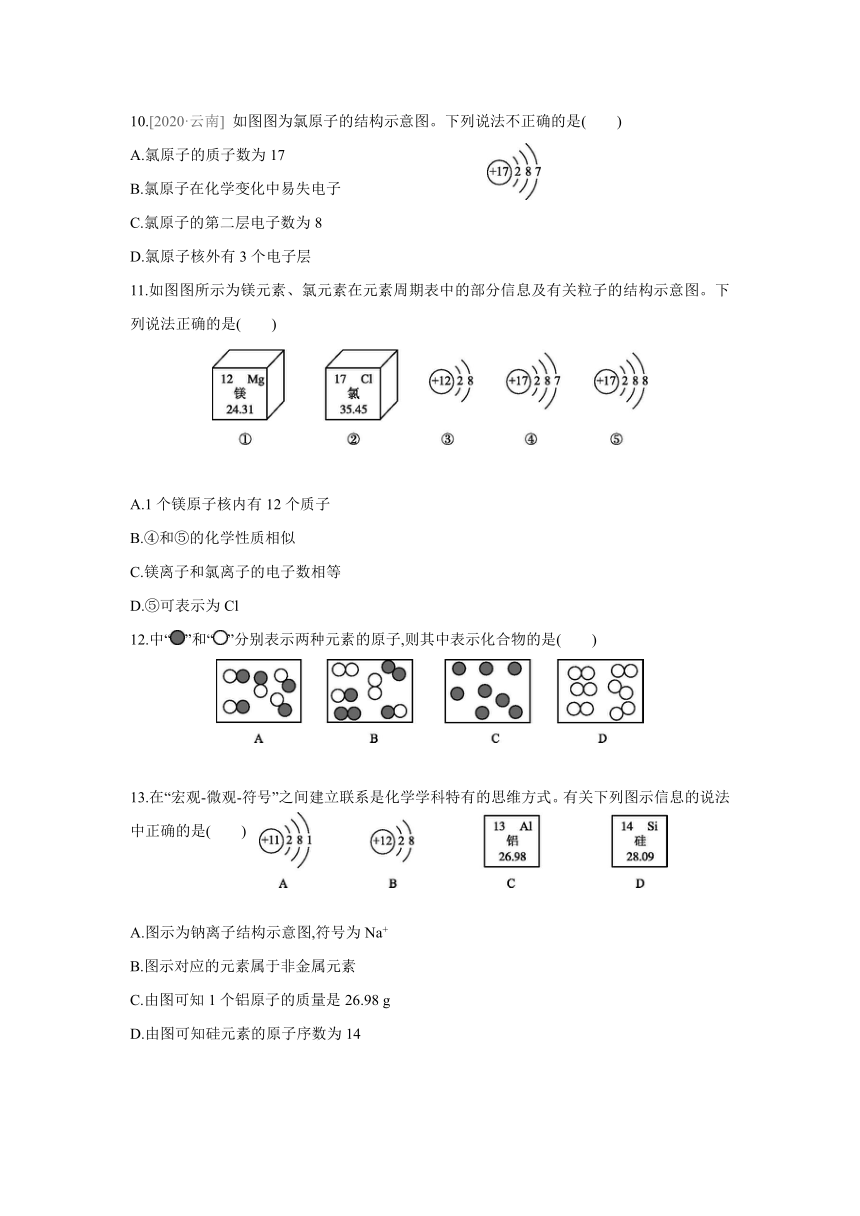
10.[2020·云南] 如图图为氯原子的结构示意图。下列说法不正确的是( )
A.氯原子的质子数为17
B.氯原子在化学变化中易失电子
C.氯原子的第二层电子数为8
D.氯原子核外有3个电子层
11.如图图所示为镁元素、氯元素在元素周期表中的部分信息及有关粒子的结构示意图。下列说法正确的是( )
A.1个镁原子核内有12个质子
B.④和⑤的化学性质相似
C.镁离子和氯离子的电子数相等
D.⑤可表示为Cl
12.中“”和“”分别表示两种元素的原子,则其中表示化合物的是( )
13.在“宏观-微观-符号”之间建立联系是化学学科特有的思维方式。有关下列图示信息的说法中正确的是( )
A.图示为钠离子结构示意图,符号为Na+
B.图示对应的元素属于非金属元素
C.由图可知1个铝原子的质量是26.98 g
D.由图可知硅元素的原子序数为14
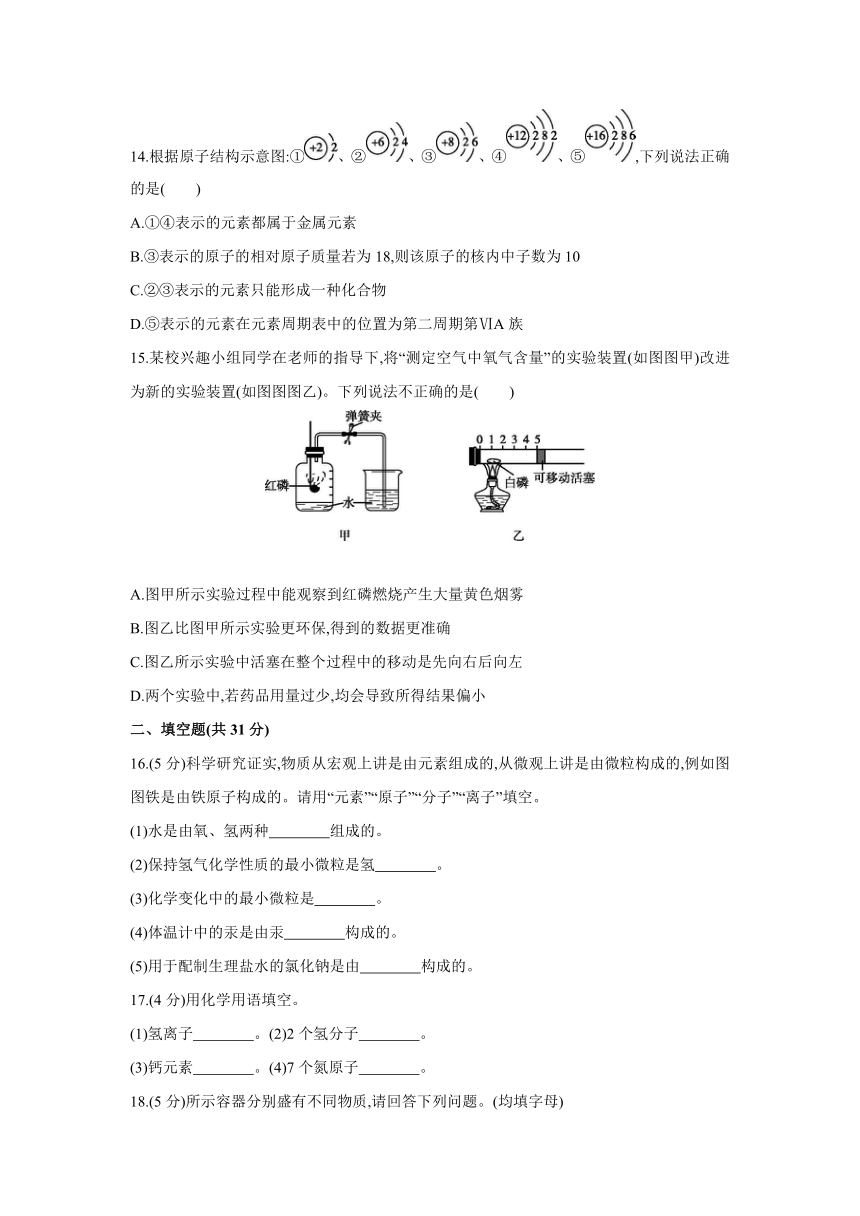
14.根据原子结构示意图:①、②、③、④、⑤,下列说法正确的是( )
A.①④表示的元素都属于金属元素
B.③表示的原子的相对原子质量若为18,则该原子的核内中子数为10
C.②③表示的元素只能形成一种化合物
D.⑤表示的元素在元素周期表中的位置为第二周期第ⅥA族
15.某校兴趣小组同学在老师的指导下,将“测定空气中氧气含量”的实验装置(如图图甲)改进为新的实验装置(如图图图乙)。下列说法不正确的是( )
A.图甲所示实验过程中能观察到红磷燃烧产生大量黄色烟雾
B.图乙比图甲所示实验更环保,得到的数据更准确
C.图乙所示实验中活塞在整个过程中的移动是先向右后向左
D.两个实验中,若药品用量过少,均会导致所得结果偏小
二、填空题(共31分)
16.(5分)科学研究证实,物质从宏观上讲是由元素组成的,从微观上讲是由微粒构成的,例如图图铁是由铁原子构成的。请用“元素”“原子”“分子”“离子”填空。
(1)水是由氧、氢两种 组成的。
(2)保持氢气化学性质的最小微粒是氢 。
(3)化学变化中的最小微粒是 。
(4)体温计中的汞是由汞 构成的。
(5)用于配制生理盐水的氯化钠是由 构成的。
17.(4分)用化学用语填空。
(1)氢离子 。(2)2个氢分子 。
(3)钙元素 。(4)7个氮原子 。
18.(5分)所示容器分别盛有不同物质,请回答下列问题。(均填字母)
(1)所盛物质属于单质的是 。
(2)所盛物质属于化合物的是 。
(3)所盛物质属于纯净物的是 。
(4)所盛物质属于混合物的是 。
(5)所盛物质属于氧化物的是 。
19.(4分)[2020·日照] 几种元素在元素周期表中的部分信息如图图Ⅰ所示,请回答下列问题。
(1)下列说法不正确的是 (填字母)。
A.氯原子的质子数为17,最外层电子数为7
B.磷的相对原子质量为30.97 g
C.X元素的原子序数为16,元素名称为硫,元素符号为S
D.X元素与磷、氯元素位于同周期,与氧元素位于同一族
(2)一种碳原子叫作碳-12,是含有6个质子和6个中子的碳原子,一个碳-12 原子的质量为a g,则一个氧原子的质量为 (用含a的代数式表示)g。
(3)图Ⅱ所示粒子共表示 种元素。X元素的化学性质与图Ⅱ中 (填字母)的化学性质相似。
20.(5分)[2020·百色改编] 元素周期表是学习化学的重要工具。下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题。
(1)位于第二周期第ⅥA族元素的名称是 ,其原子核内有
个质子,在化学反应中易 电子。
(2)为铟元素的原子结构示意图,其化学性质与铝元素的化学性质相似,原因是它们的原子 ,铟元素在元素周期表中位于第 周期。
21.(8分)请沿用科学家认识事物的方式认识空气。
(1)从分类角度:空气属于 (填“混合物”或“纯净物”)。
(2)从组成角度:①空气中稀有气体的体积分数大约为 。
②因为氮气具有 的性质,所以可充入食品包装袋内用于防腐。
(3)从微观角度:如图图所示,用“”表示氮原子,“”表示氧原子。
①“”可表示的微粒是 (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,图中可表示空气微观模型的是 (填字母,下同)。
(4)从污染角度:①下列属于空气污染物的是 ,大雾天气导致呼吸道感染病人增多是因为雾霾使空气中增加了大量的 。
A.二氧化碳 B.一氧化碳
C.可吸入颗粒物 D.二氧化硫
②请你提出一条防治空气污染的合理建议: 。
三、实验探究题(共15分)
22.(5分)某化学兴趣小组对教材中“测定空气中氧气含量”的实验(如图图中甲)进行了大胆改进,设计了如图图图乙所示(选用容积为45 mL的试管作反应容器)的实验方案进行实验,效果良好。请你对比分析图甲、图乙实验,回答下列有关问题。
(1)图甲实验中红磷燃烧的现象是 。
(2)图乙实验前,打开弹簧夹,将注射器的活塞前沿从10 mL刻度处推至5 mL 刻度处,然后松手,若活塞仍能返回至10 mL刻度处,则说明 。
(3)图乙实验的操作如图图下:①点燃酒精灯;②撤去酒精灯,待试管冷却至室温后打开弹簧夹;③将足量红磷装入试管中,将25 mL的注射器活塞置于10 mL刻度处,并按图乙中所示的连接方式固定好,再用弹簧夹夹紧橡皮管;④读取注射器活塞的数据。你认为正确的实验操作顺序是
(填序号)。
(4)图乙实验中,注射器活塞将从10 mL刻度处慢慢前移到约 mL刻度处停止。
(5)与图甲实验对比,你认为图乙实验的优点是
(写一条即可)。
23.(10分)为探究分子的运动及影响分子运动速率的因素,某同学设计了以下两种实验方案,请回答有关问题。
[实验方案一] 如图图①。
①观察到的实验现象是 。
②该方案的不足之处是 (写出一点即可)。
[实验方案二] 如图图图②、图③。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定着用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图④的操作方式分别用注射器向图②和图③的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40 ℃的热水中。
①观察到的现象是 。
②图②、图③采用对照实验的方法,变量只有一个,被控制的量有多个,请说出四个被控制的量: 。
[实验结论] 上述实验证明:分子是不断运动的,且分子的运动速率与 有关。
四、计算题(共9分)
24.科学家最近合成了核电荷数为139的原子,经测定该原子的质量为4.89946×10-25 kg(已知碳-12原子的质量为1.993×10-26 kg)。请计算:
(1)该原子的相对原子质量是多少 (结果保留整数)
(2)该原子的中子数是多少
(3)中子数与电子数之差是多少
答案
1.D
2.C 在空旷偏僻的地方燃烧塑料垃圾同样会生成有害气体和烟尘污染空气。
3.D
4.C 纯净物的组成中只含一种物质,可能只含一种元素,也可能含有多种元素;混合物的组成中不一定含有多种元素,如图图氧气和臭氧组成的混合物只含氧元素;含氧元素的化合物中,若该化合物只含两种元素就是氧化物。
5.D 原子核是由质子和中子构成的,带正电,原子核外有电子,原子核很小,但原子的质量却集中在原子核上。 6.A
7.B 原子中含有质子、中子和核外电子,不是最小的微粒,可以再分;相同原子可构成不同的分子,如图图氧分子、臭氧分子都是由氧原子构成的;离子是构成物质的一种基本微粒,可以直接构成物质;固体难压缩是由于固体分子之间的间隔小。
8.A 9.C 10.B
11.A ④和⑤最外层电子数不同,化学性质不相似; 镁离子有10个电子,氯离子有18个电子,电子数不相等;⑤是氯离子的结构示意图,表示为Cl-。
12.A B图中的物质是由不同种分子构成的,属于混合物;C图中的物质是由同种原子直接构成的,属于单质;D图中物质的分子是由同种原子构成的,属于单质。
13.D A中微粒质子数=核外电子数=11,为钠原子;由B图示可知,核内质子数为12,为镁元素,属于金属元素;根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,相对原子质量的单位是“1”,不是“g”,铝元素的相对原子质量为26.98。 14.B
15.A 图甲所示实验过程中能观察到红磷燃烧产生大量的白烟,而不是黄色烟雾。
16.(1)元素 (2)分子 (3)原子 (4)原子 (5)离子
17.(1)H+ (2)2H2 (3)Ca (4)7N
18.(1)A (2)D (3)AD (4)BCE (5)D
19.(1)B (2)a (3)3 A
(3)图Ⅱ所示粒子共表示3种元素,即氧元素、镁元素、氯元素;X元素(硫元素)的化学性质与图Ⅱ中A的化学性质相似,是因为它们最外层电子数相等。
20.(1)氧元素 8 得到 (2)最外层电子数相等 五
(1)位于第二周期第ⅥA族元素的名称是氧元素,其原子核内有8个质子,最外层电子数是6,在化学反应中易得到电子。(2)图Ⅱ为铟元素的原子结构示意图,其化学性质与铝元素的化学性质相似,原因是它们的原子最外层电子数相等。铟元素核外电子层数是5,在元素周期表中位于第五周期。
21.(1)混合物 (2)①0.94% ②常温下化学性质稳定
(3)①氮分子 ②C(4)①BCD C
②工厂废气处理达标后再排放(合理即可)
22.(1)产生大量白烟,放出热量
(2)装置气密性良好
(3)③①②④ (4)1
(5)装置始终密闭,没有气体逸出,实验结果更准确(合理答案均可)
(4)由于红磷燃烧消耗了试管内空气体积的(氧气的体积),即9 mL,所以活塞最终所处的刻度值为10 mL-9 mL=1 mL。
23.[实验方案一] ①酚酞溶液变成红色
②装置不密封,氨气逸出会污染空气(或药品用量过多等合理答案均可)
[实验方案二] ①两个塑料瓶中小纸花由下至上逐渐变成红色,且小纸花在热水中比在冷水中变红的速率快
②塑料瓶的材质、大小、形状,注入浓氨水的量(或注入浓氨水的时间,小纸花形状、大小等合理答案均可)
[实验结论] 温度
24.解:(1)该原子的相对原子质量为=295。
(2)在原子中,相对原子质量≈质子数+中子数,该原子的质子数为139,则中子数为295-139=156。
(3)在该原子中,核外电子数=质子数=139,中子数与电子数之差为156-139=17。
答:(1)该原子的相对原子质量是295;(2)该原子的中子数是156;(3)中子数与电子数之差是17。
[范围: 空气、物质的构成 时间:40分钟 分值:100分]
一、选择题(共45分)
1.[2020·怀化改编] 下列物质不是空气成分的是( )
A.作保护气的氮气(N2)
B.气球填充气氦气(He)
C.医疗急救用的氧气(O2)
D.火箭新型推进剂液氢(H2)
2.[2020·菏泽] “绿色发展”“低碳生活”等理念逐渐深入人心。下列做法不符合该理念的是
( )
A.为节约和环保,分类回收生活垃圾
B.能源结构向多元、清洁和低碳方向转型
C.为防止影响小区人们生活,在空旷偏僻的地方燃烧塑料垃圾
D.鼓励乘坐公交车或骑自行车出行
3.下列排序正确是( )
A.相对原子质量:碳原子>氧原子>硫原子
B.酒精灯火焰的温度:焰心>内焰>外焰
C.地壳中元素含量:Fe>Al>Si>O
D.物质在空气中的体积分数:氮气>氧气>稀有气体>二氧化碳
4.下列关于物质组成的叙述中,正确的是( )
A.纯净物的组成中只含一种元素
B.混合物的组成中肯定含有多种元素
C.不同物质可以含有相同的元素
D.含氧元素的化合物就是氧化物
5.下列关于原子核的叙述正确的是( )
①通常由中子和电子构成 ②通常由质子和中子构成 ③带正电荷
④不显电性 ⑤不能再分 ⑥跟原子比较体积很小,但却集中了原子的主要质量
A.②④⑥ B.①③⑤
C.①②⑤ D.②③⑥
6.用分子的相关知识解释下列生活中的现象,其中错误的是( )
A.热胀冷缩,说明分子的大小随温度升降而改变
B.“酒香不怕巷子深”,说明分子在不停地运动
C.10 mL酒精和10 mL水混合后,体积小于20 mL,说明分子间有间隔
D.湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快
7.下列对分子、原子、离子的认识,正确的是( )
A.原子是最小的微粒,不可再分
B.相同原子可构成不同的分子
C.离子不能直接构成物质
D.固体难压缩,说明固体分子间无间隔
8.铈是一种稀土元素,在元素周期表中铈元素的某些信息如图图所示,下列有关铈的说法正确的是( )
A.元素符号为Ce
B.属于非金属元素
C.相对原子质量为140.1 g
D.原子核内中子数为58
9.根据钠原子的结构示意图不能确定的是( )
A.质子数
B.电子层数
C.相对原子质量
D.元素种类
10.[2020·云南] 如图图为氯原子的结构示意图。下列说法不正确的是( )
A.氯原子的质子数为17
B.氯原子在化学变化中易失电子
C.氯原子的第二层电子数为8
D.氯原子核外有3个电子层
11.如图图所示为镁元素、氯元素在元素周期表中的部分信息及有关粒子的结构示意图。下列说法正确的是( )
A.1个镁原子核内有12个质子
B.④和⑤的化学性质相似
C.镁离子和氯离子的电子数相等
D.⑤可表示为Cl
12.中“”和“”分别表示两种元素的原子,则其中表示化合物的是( )
13.在“宏观-微观-符号”之间建立联系是化学学科特有的思维方式。有关下列图示信息的说法中正确的是( )
A.图示为钠离子结构示意图,符号为Na+
B.图示对应的元素属于非金属元素
C.由图可知1个铝原子的质量是26.98 g
D.由图可知硅元素的原子序数为14
14.根据原子结构示意图:①、②、③、④、⑤,下列说法正确的是( )
A.①④表示的元素都属于金属元素
B.③表示的原子的相对原子质量若为18,则该原子的核内中子数为10
C.②③表示的元素只能形成一种化合物
D.⑤表示的元素在元素周期表中的位置为第二周期第ⅥA族
15.某校兴趣小组同学在老师的指导下,将“测定空气中氧气含量”的实验装置(如图图甲)改进为新的实验装置(如图图图乙)。下列说法不正确的是( )
A.图甲所示实验过程中能观察到红磷燃烧产生大量黄色烟雾
B.图乙比图甲所示实验更环保,得到的数据更准确
C.图乙所示实验中活塞在整个过程中的移动是先向右后向左
D.两个实验中,若药品用量过少,均会导致所得结果偏小
二、填空题(共31分)
16.(5分)科学研究证实,物质从宏观上讲是由元素组成的,从微观上讲是由微粒构成的,例如图图铁是由铁原子构成的。请用“元素”“原子”“分子”“离子”填空。
(1)水是由氧、氢两种 组成的。
(2)保持氢气化学性质的最小微粒是氢 。
(3)化学变化中的最小微粒是 。
(4)体温计中的汞是由汞 构成的。
(5)用于配制生理盐水的氯化钠是由 构成的。
17.(4分)用化学用语填空。
(1)氢离子 。(2)2个氢分子 。
(3)钙元素 。(4)7个氮原子 。
18.(5分)所示容器分别盛有不同物质,请回答下列问题。(均填字母)
(1)所盛物质属于单质的是 。
(2)所盛物质属于化合物的是 。
(3)所盛物质属于纯净物的是 。
(4)所盛物质属于混合物的是 。
(5)所盛物质属于氧化物的是 。
19.(4分)[2020·日照] 几种元素在元素周期表中的部分信息如图图Ⅰ所示,请回答下列问题。
(1)下列说法不正确的是 (填字母)。
A.氯原子的质子数为17,最外层电子数为7
B.磷的相对原子质量为30.97 g
C.X元素的原子序数为16,元素名称为硫,元素符号为S
D.X元素与磷、氯元素位于同周期,与氧元素位于同一族
(2)一种碳原子叫作碳-12,是含有6个质子和6个中子的碳原子,一个碳-12 原子的质量为a g,则一个氧原子的质量为 (用含a的代数式表示)g。
(3)图Ⅱ所示粒子共表示 种元素。X元素的化学性质与图Ⅱ中 (填字母)的化学性质相似。
20.(5分)[2020·百色改编] 元素周期表是学习化学的重要工具。下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题。
(1)位于第二周期第ⅥA族元素的名称是 ,其原子核内有
个质子,在化学反应中易 电子。
(2)为铟元素的原子结构示意图,其化学性质与铝元素的化学性质相似,原因是它们的原子 ,铟元素在元素周期表中位于第 周期。
21.(8分)请沿用科学家认识事物的方式认识空气。
(1)从分类角度:空气属于 (填“混合物”或“纯净物”)。
(2)从组成角度:①空气中稀有气体的体积分数大约为 。
②因为氮气具有 的性质,所以可充入食品包装袋内用于防腐。
(3)从微观角度:如图图所示,用“”表示氮原子,“”表示氧原子。
①“”可表示的微粒是 (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,图中可表示空气微观模型的是 (填字母,下同)。
(4)从污染角度:①下列属于空气污染物的是 ,大雾天气导致呼吸道感染病人增多是因为雾霾使空气中增加了大量的 。
A.二氧化碳 B.一氧化碳
C.可吸入颗粒物 D.二氧化硫
②请你提出一条防治空气污染的合理建议: 。
三、实验探究题(共15分)
22.(5分)某化学兴趣小组对教材中“测定空气中氧气含量”的实验(如图图中甲)进行了大胆改进,设计了如图图图乙所示(选用容积为45 mL的试管作反应容器)的实验方案进行实验,效果良好。请你对比分析图甲、图乙实验,回答下列有关问题。
(1)图甲实验中红磷燃烧的现象是 。
(2)图乙实验前,打开弹簧夹,将注射器的活塞前沿从10 mL刻度处推至5 mL 刻度处,然后松手,若活塞仍能返回至10 mL刻度处,则说明 。
(3)图乙实验的操作如图图下:①点燃酒精灯;②撤去酒精灯,待试管冷却至室温后打开弹簧夹;③将足量红磷装入试管中,将25 mL的注射器活塞置于10 mL刻度处,并按图乙中所示的连接方式固定好,再用弹簧夹夹紧橡皮管;④读取注射器活塞的数据。你认为正确的实验操作顺序是
(填序号)。
(4)图乙实验中,注射器活塞将从10 mL刻度处慢慢前移到约 mL刻度处停止。
(5)与图甲实验对比,你认为图乙实验的优点是
(写一条即可)。
23.(10分)为探究分子的运动及影响分子运动速率的因素,某同学设计了以下两种实验方案,请回答有关问题。
[实验方案一] 如图图①。
①观察到的实验现象是 。
②该方案的不足之处是 (写出一点即可)。
[实验方案二] 如图图图②、图③。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定着用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图④的操作方式分别用注射器向图②和图③的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40 ℃的热水中。
①观察到的现象是 。
②图②、图③采用对照实验的方法,变量只有一个,被控制的量有多个,请说出四个被控制的量: 。
[实验结论] 上述实验证明:分子是不断运动的,且分子的运动速率与 有关。
四、计算题(共9分)
24.科学家最近合成了核电荷数为139的原子,经测定该原子的质量为4.89946×10-25 kg(已知碳-12原子的质量为1.993×10-26 kg)。请计算:
(1)该原子的相对原子质量是多少 (结果保留整数)
(2)该原子的中子数是多少
(3)中子数与电子数之差是多少
答案
1.D
2.C 在空旷偏僻的地方燃烧塑料垃圾同样会生成有害气体和烟尘污染空气。
3.D
4.C 纯净物的组成中只含一种物质,可能只含一种元素,也可能含有多种元素;混合物的组成中不一定含有多种元素,如图图氧气和臭氧组成的混合物只含氧元素;含氧元素的化合物中,若该化合物只含两种元素就是氧化物。
5.D 原子核是由质子和中子构成的,带正电,原子核外有电子,原子核很小,但原子的质量却集中在原子核上。 6.A
7.B 原子中含有质子、中子和核外电子,不是最小的微粒,可以再分;相同原子可构成不同的分子,如图图氧分子、臭氧分子都是由氧原子构成的;离子是构成物质的一种基本微粒,可以直接构成物质;固体难压缩是由于固体分子之间的间隔小。
8.A 9.C 10.B
11.A ④和⑤最外层电子数不同,化学性质不相似; 镁离子有10个电子,氯离子有18个电子,电子数不相等;⑤是氯离子的结构示意图,表示为Cl-。
12.A B图中的物质是由不同种分子构成的,属于混合物;C图中的物质是由同种原子直接构成的,属于单质;D图中物质的分子是由同种原子构成的,属于单质。
13.D A中微粒质子数=核外电子数=11,为钠原子;由B图示可知,核内质子数为12,为镁元素,属于金属元素;根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,相对原子质量的单位是“1”,不是“g”,铝元素的相对原子质量为26.98。 14.B
15.A 图甲所示实验过程中能观察到红磷燃烧产生大量的白烟,而不是黄色烟雾。
16.(1)元素 (2)分子 (3)原子 (4)原子 (5)离子
17.(1)H+ (2)2H2 (3)Ca (4)7N
18.(1)A (2)D (3)AD (4)BCE (5)D
19.(1)B (2)a (3)3 A
(3)图Ⅱ所示粒子共表示3种元素,即氧元素、镁元素、氯元素;X元素(硫元素)的化学性质与图Ⅱ中A的化学性质相似,是因为它们最外层电子数相等。
20.(1)氧元素 8 得到 (2)最外层电子数相等 五
(1)位于第二周期第ⅥA族元素的名称是氧元素,其原子核内有8个质子,最外层电子数是6,在化学反应中易得到电子。(2)图Ⅱ为铟元素的原子结构示意图,其化学性质与铝元素的化学性质相似,原因是它们的原子最外层电子数相等。铟元素核外电子层数是5,在元素周期表中位于第五周期。
21.(1)混合物 (2)①0.94% ②常温下化学性质稳定
(3)①氮分子 ②C(4)①BCD C
②工厂废气处理达标后再排放(合理即可)
22.(1)产生大量白烟,放出热量
(2)装置气密性良好
(3)③①②④ (4)1
(5)装置始终密闭,没有气体逸出,实验结果更准确(合理答案均可)
(4)由于红磷燃烧消耗了试管内空气体积的(氧气的体积),即9 mL,所以活塞最终所处的刻度值为10 mL-9 mL=1 mL。
23.[实验方案一] ①酚酞溶液变成红色
②装置不密封,氨气逸出会污染空气(或药品用量过多等合理答案均可)
[实验方案二] ①两个塑料瓶中小纸花由下至上逐渐变成红色,且小纸花在热水中比在冷水中变红的速率快
②塑料瓶的材质、大小、形状,注入浓氨水的量(或注入浓氨水的时间,小纸花形状、大小等合理答案均可)
[实验结论] 温度
24.解:(1)该原子的相对原子质量为=295。
(2)在原子中,相对原子质量≈质子数+中子数,该原子的质子数为139,则中子数为295-139=156。
(3)在该原子中,核外电子数=质子数=139,中子数与电子数之差为156-139=17。
答:(1)该原子的相对原子质量是295;(2)该原子的中子数是156;(3)中子数与电子数之差是17。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
