人教版化学九年级上册同步提优训练:第四单元 自然界的水 综合提升卷 全国(word版有答案)
文档属性
| 名称 | 人教版化学九年级上册同步提优训练:第四单元 自然界的水 综合提升卷 全国(word版有答案) |  | |
| 格式 | docx | ||
| 文件大小 | 294.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-09 16:02:01 | ||
图片预览



文档简介
第四单元综合提升卷
[范围:自然界的水 时间:40分钟 分值:100分]
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Cl—35.5 Zn—65
题号 1 2 3 4 5 6 7 8 9 10 11 12
选项
一、选择题(每小题3分,共36分)
1.地球表面约有71%被水覆盖,陆地淡水只占全球水储量的2.53%。下列有关水的说法错误的是( )
A.自来水煮沸后变成纯水 B.常用肥皂水鉴别硬水和软水
C.天然水是混合物 D.海水淡化能缓解水资源短缺的危机
2.过滤操作过程中用到的下列仪器不属于玻璃仪器的是 ( )
A.漏斗 B.烧杯 C.铁架台 D.玻璃棒
3.(2020黄冈)下面是萌萌同学的一次化学用语练习的部分内容,其中正确的是 ( )
A.氦气:He2
B.硝酸铵中-3价的氮元素:H4NO3
C.N2:2个氮原子
D.2Fe2+:2个铁离子
4.(2020广州)自来水厂净水过程示意图如图,下列说法正确的是 ( )
A.明矾是一种常用的絮凝剂 B.过滤可除去水中杂质离子
C.活性炭可长期使用无须更换 D.经该净水过程得到的是纯水
5.(2020山西)氮元素形成的化合物种类较多,下列化合物中氮元素化合价为+2的是 ( )
A.NO B.N2O3 C.NH3 D.N2O5
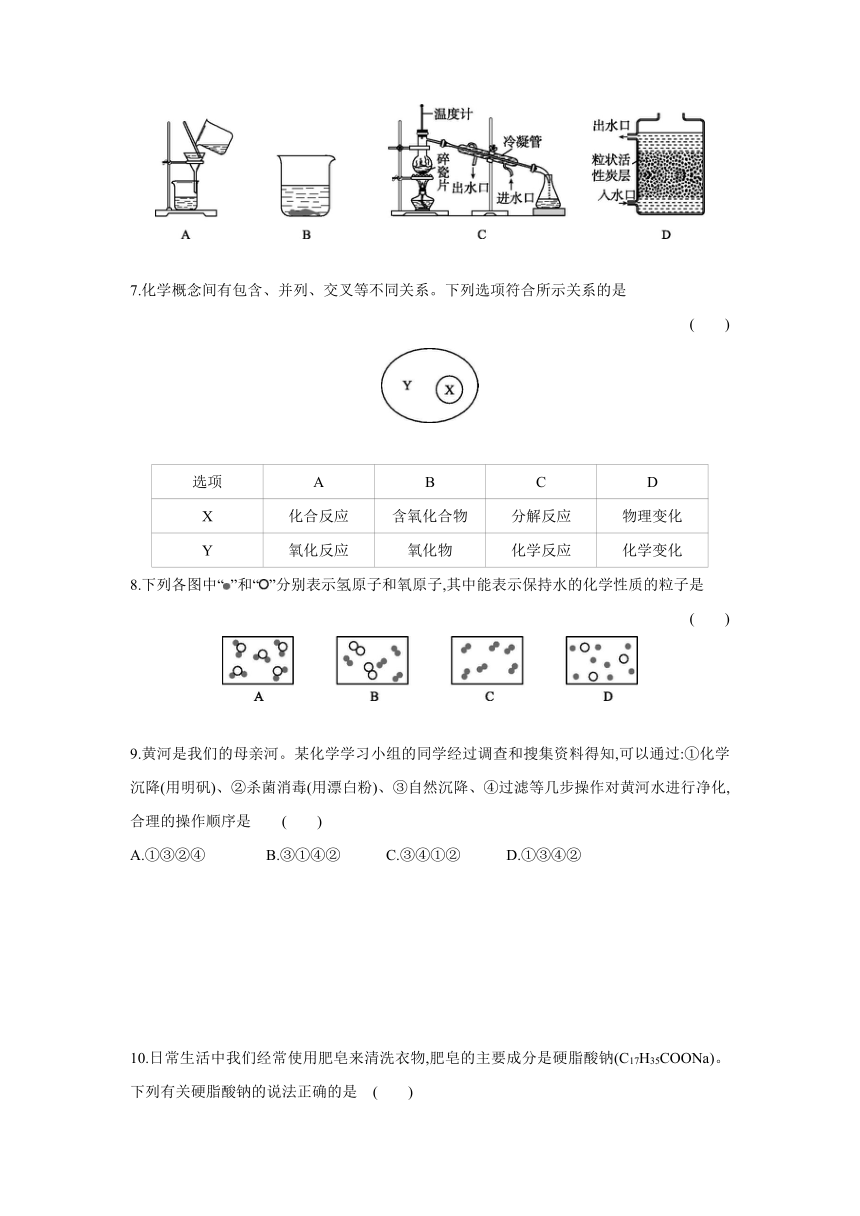
6.下列单一净化水的操作中,净化程度最高的是 ( )
7.化学概念间有包含、并列、交叉等不同关系。下列选项符合所示关系的是
( )
选项 A B C D
X 化合反应 含氧化合物 分解反应 物理变化
Y 氧化反应 氧化物 化学反应 化学变化
8.下列各图中“”和“”分别表示氢原子和氧原子,其中能表示保持水的化学性质的粒子是
( )
9.黄河是我们的母亲河。某化学学习小组的同学经过调查和搜集资料得知,可以通过:①化学沉降(用明矾)、②杀菌消毒(用漂白粉)、③自然沉降、④过滤等几步操作对黄河水进行净化,合理的操作顺序是 ( )
A.①③②④ B.③①④② C.③④①② D.①③④②
10.日常生活中我们经常使用肥皂来清洗衣物,肥皂的主要成分是硬脂酸钠(C17H35COONa)。下列有关硬脂酸钠的说法正确的是 ( )
A.从微观上看:硬脂酸钠含有18个碳原子、35个氢原子、2个氧原子和1个钠原子
B.从宏观上看:硬脂酸钠分子是由碳、氢、氧、钠四种元素组成的
C.从分类上看:硬脂酸钠属于化合物
D.从质量上看:硬脂酸钠中碳、氧元素的质量比为9∶1
11.(2020安徽)理论上电解水得到氧气和氢气的体积比为1∶2。某同学用碳棒作电极进行电解水实验,得到氧气和氢气的体积比小于1∶2,对产生此现象原因的猜想不合理的是 ( )
A.部分氧气溶于水
B.部分氧气与碳棒反应
C.部分氧气被碳棒吸附
D.部分氧气与氢气反应重新生成了水
12.(2020河南)生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是 ( )
A.双氧水消毒液(H2O2) B.“84”消毒液(NaClO)
C.酒精消毒液(C2H5OH) D.过氧乙酸消毒液(C2H4O3)
二、填空题(共22分)
13.(4分)请用相应的化学符号填空。
(1)2个氮分子: 。 (2)-2价的硫元素: 。
(3)铝离子: 。 (4)硫酸铵: 。
14.(4分)水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。为自来水厂净水过程示意图。
取水口反应沉淀池过滤池活性炭吸附池清水池配水泵用户
(1)取水后加入絮凝剂的作用是 。
(2)吸附池内的活性炭起 作用,经沉淀、过滤净化处理后所得的水 (填“是”或“不是”)纯水。
(3)有人说:“世界上最后一滴水就是人类的眼泪。”请你列举一条可行的节水措施:
。
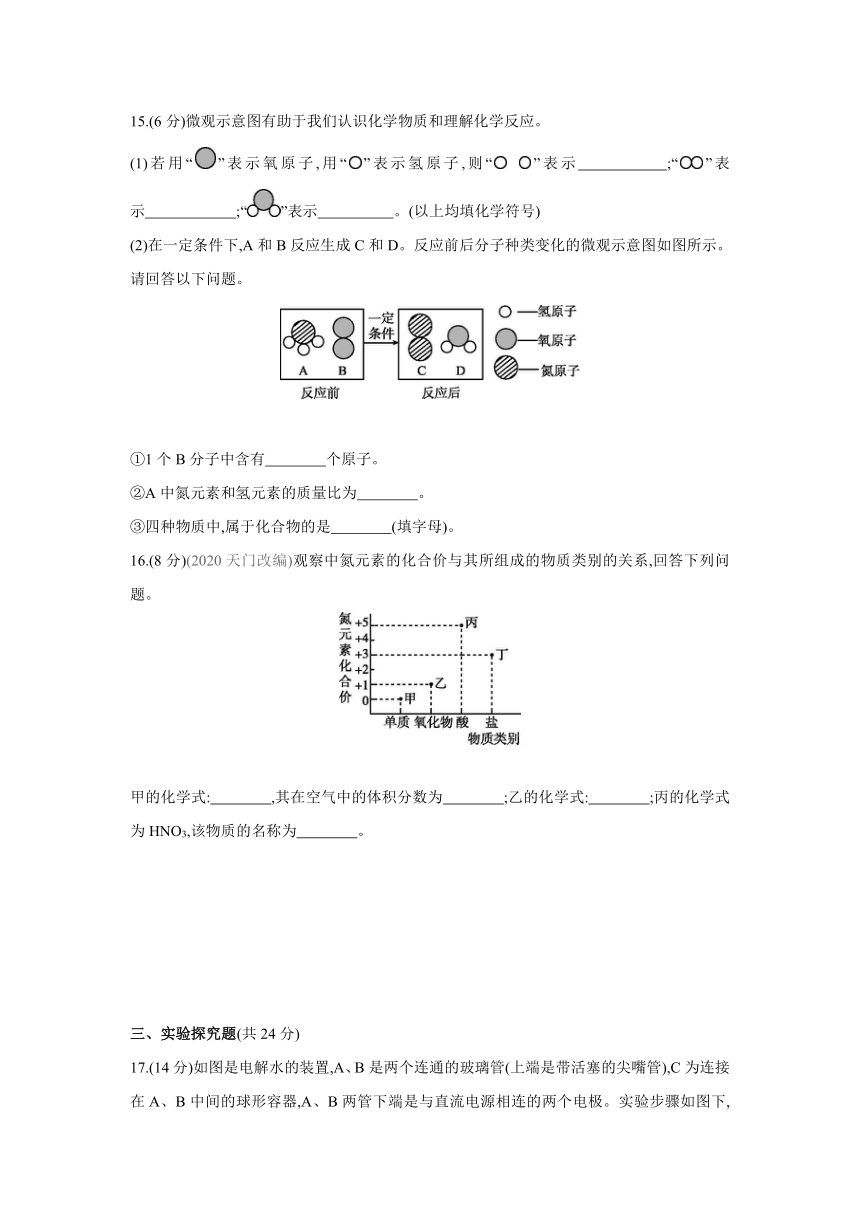
15.(6分)微观示意图有助于我们认识化学物质和理解化学反应。
(1)若用“”表示氧原子,用“”表示氢原子,则“ ”表示 ;“”表示 ;“”表示 。(以上均填化学符号)
(2)在一定条件下,A和B反应生成C和D。反应前后分子种类变化的微观示意图如图所示。请回答以下问题。
①1个B分子中含有 个原子。
②A中氮元素和氢元素的质量比为 。
③四种物质中,属于化合物的是 (填字母)。
16.(8分)(2020天门改编)观察中氮元素的化合价与其所组成的物质类别的关系,回答下列问题。
甲的化学式: ,其在空气中的体积分数为 ;乙的化学式: ;丙的化学式为HNO3,该物质的名称为 。
三、实验探究题(共24分)
17.(14分)如图是电解水的装置,A、B是两个连通的玻璃管(上端是带活塞的尖嘴管),C为连接在A、B中间的球形容器,A、B两管下端是与直流电源相连的两个电极。实验步骤如图下,根据实验填空。
①先将活塞打开,然后从C处将水倒入装置中,使A、B玻璃管中充满水,关闭活塞后再接通电源。
②打开电源开关,几分钟后在A、B玻璃管中生成气体的体积如图图所示。
(1)A、B管内生成的气体聚集在上部的原因是 。
(2)球形容器中液体的液面 (填“上升”或“下降”),产生此现象的原因是
。
(3)B管中的气体是 ,验证B管中气体的最简便的方法是
。
(4)电解一定量的水,当其中一个电极产生5 mL气体时,另一电极产生的气体体积可能是 mL或 mL。
18.(10分)纯水的导电能力很弱,电解水时常在水中加入一些氢氧化钠(NaOH)增强导电性。为研究影响电解水反应速率的因素,某课外活动小组进行了实验探究,数据记录如图下表,请回答下列问题。
实验编号 温度/℃ NaOH溶液浓度 H2体积/mL O2体积/mL 电解时间/s
A 20 2% 20 9.8 54.0
B 20 5% 20 9.8 36.2
C 30 2% 20 9.6 46.2
D 30 5% 20 9.7 x
(1)该小组研究的影响电解水反应速率的因素是 和 。
(2)本实验通过比较 来比较电解水速率的快慢。
(3)比较实验A和C,可得到的结论是 。
(4)分析实验A、B、C的数据,推测实验D的电解时间“x”可能是 (填字母)。
A.35.4 B.37.8 C.50.2 D.55.6
四、计算题(共18分)
19.(4分)(2020泰安)甲醇是一种无色、有特殊香味、易挥发的液体。已知甲醇由碳、氢、氧三种元素组成,其中氢元素的质量分数为12.5%,氧元素的质量分数为50%;1个甲醇分子中含有1个氧原子。回答下列问题。
(1)甲醇的相对分子质量是 。
(2)1个甲醇分子中含氢原子的个数是 。
20.(6分)自然界生命体的有机物组成除碳、氢、氧外还有其他元素,如图某藻类物质(化学式可表示为C106H263O110N16P)的组成中就含有氮元素和磷元素。α-丙氨酸是组成人体蛋白质的氨基酸之一,其分子结构如图所示。
(1)写出α-丙氨酸的化学式: 。
(2)α-丙氨酸中氮元素的质量分数是多少 (结果保留至0.1%)
21.(8分)儿童缺锌会引起食欲不振、发育不良等症状。为某补锌口服液说明书的部分信息,图中葡萄糖酸锌的化学式已不完整,请根据相关信息回答下列问题。
(1)葡萄糖酸锌的相对分子质量是455,则葡萄糖酸锌化学式中氢原子右下角的数字为 。
(2)若儿童每1 kg体重每日需要0.5 mg锌,每天从食物中只能摄入所需锌的一半。体重为20 kg的儿童,理论上一天还需服该口服液多少支
答案
第四单元综合提升卷
1.A 自来水煮沸后,可使钙、镁离子从水中沉淀出来,但水中还有一些可溶性物质没有除去,不能变成纯水;肥皂水可以用来鉴别硬水和软水;天然水中含有可溶性杂质和细菌等,是混合物。
2.C 铁架台由金属制成,不属于玻璃仪器。
3.B 氦气直接用元素符号表示为He;硝酸铵中-3价的氮元素是铵根中的氮元素,所以表示为H4NO3;氮气的化学式是N2,元素符号右下角的数字“2”表示1个氮分子中含有2个氮原子;2Fe2+表示2个亚铁离子。
4.A 明矾是沉降常用的絮凝剂,明矾能与水反应生成胶状物,吸附悬浮杂质,使其沉降;过滤可除去水中的难溶性物质,杂质离子是溶解在水中的,无法通过过滤除去;活性炭长期使用,吸附能力会下降,所以需要定时更换;经该净水过程得到的水中还含有部分可溶性杂质,不是纯水。
5.A 6.C
7.C 化合反应与氧化反应属于交叉关系;物理变化和化学变化是并列关系;含氧化合物与氧化物、分解反应与化学反应都属于包含关系,前者是X包含Y,后者是Y包含X。
8.A A图表示水分子,水分子能保持水的化学性质;B图表示氢分子和氧分子,C图表示氢分子,D图表示氢原子和氧原子,均不能保持水的化学性质。
9.B
10.C 从微观上看,分子是由原子构成的,1个硬脂酸钠分子中含有18个碳原子、35个氢原子、2个氧原子和1个钠原子;从宏观上看,物质是由元素组成的,硬脂酸钠是由碳、氢、氧、钠四种元素组成的;由不同种元素组成的纯净物叫作化合物,从分类上看,硬脂酸钠是由碳、氢、氧、钠四种元素组成的纯净物,属于化合物;从质量上看,硬脂酸钠中碳、氧元素的质量比为(12×18)∶(16×2)=27∶4。
11.D 在室温下,1 L水中能溶解约30 mL氧气,而氢气难溶于水,故得到氧气和氢气的体积比小于1∶2;碳能与氧气在一定条件下反应生成二氧化碳,故可能是部分氧气与碳棒发生了反应;碳棒具有疏松多孔的结构,可能会吸附一部分氧气;电解水时,生成的氢气和氧气一般无法接触,且若氧气与氢气反应重新生成了水,每2体积的氢气与1体积的氧气反应,对生成的氧气与氢气的体积比没有影响。
12.A H2O2中氧元素的质量分数为×100%=94.1%;NaClO中氧元素的质量分数为×100%=21.5%;C2H5OH中氧元素的质量分数为×100%=34.8%;C2H4O3中氧元素的质量分数为×100%=63.2%。
13.(1)2N2 (2) (3)Al3+ (4)(NH4)2SO4
本题主要考查常用的化学用语。化学符号前面的数字表示粒子的个数;化合价标注在元素符号(或原子团)的正上方,正负号在前,数字在后;离子所带电荷标注在元素符号的右上角,数字在前,正负号在后;书写化学式要遵循正负化合价的代数和为零的原则。
14.(1)使水中的悬浮杂质沉降 (2)吸附 不是 (3)用淘米水浇花(合理即可)
(1)絮凝剂的主要成分是明矾,明矾溶于水后形成的胶状物对悬浮杂质有吸附作用,能使其沉降而达到净水的目的。(2)活性炭具有疏松多孔的结构,在自来水生产中起到吸附水中色素和异味的作用;经沉淀、过滤的水只是除去了水中不溶性固体杂质,水中仍含有许多可溶性物质,所以得到的不是纯水。(3)节约用水应从每个人做起,可结合生活中的具体事例来说明如图何节约用水,如图及时关闭水龙头、用淘米水浇花、农业上改大水漫灌为喷灌等。
15.(1)2H H2 H2O (2)①2 ②14∶3 ③AD
(1)原子没有结合在一起,表示几个单独的原子;原子结合在一起,表示分子;化合物的分子由不同种原子构成。(2)②1个A分子由1个氮原子和3个氢原子构成,化学式为NH3,其中氮、氢两种元素的质量比为(14×1)∶(1×3)=14∶3。
16.N2 78% N2O 硝酸
从图中可以看出甲是由氮元素组成的单质,所以甲是氮气,化学式为N2,乙是显+1价的氮元素的氧化物,化学式为N2O。
17.(1)气体的密度比水小,且氧气不易溶于水,氢气难溶于水
(2)上升 A、B管内有气体生成,气压变大,将液体压入C中
(3)氧气 将带火星的木条置于B管上方尖嘴处,慢慢打开活塞,木条复燃,证明该气体为氧气
(4)2.5 10
(1)水在通电的条件下生成氢气和氧气,由于气体的密度比水小,且氧气不易溶于水,氢气难溶于水,所以A、B管内生成的气体聚集在上部。(2)由于A、B管内有气体生成,气压变大,将液体压入C中,所以球形容器中液面上升。(3)水在通电时,正极产生氧气,负极产生氢气,所以B管中的气体是氧气,验证B管中气体的最简便方法是将带火星的木条置于B管上方尖嘴处,慢慢打开活塞,木条复燃,证明该气体为氧气。(4)电解一定量的水,当其中一个电极产生5 mL气体时,该气体可能是氢气,也可能是氧气,所以另一电极产生的气体体积可能是2.5 mL或10 mL。
18.(1)温度 氢氧化钠溶液浓度 (2)得到相同体积氢气所用的时间
(3)氢氧化钠溶液浓度相同时,温度越高,电解水的速率越快 (4)A
(1)分析表中数据,A和B、C和D是温度相同,氢氧化钠溶液浓度不同,得到相同体积氢气所需电解时间不同;A和C、B和D是温度不同,氢氧化钠溶液浓度相同,得到相同体积氢气所需电解时间不同,由此可知小组研究的影响电解水反应速率的因素是温度和氢氧化钠溶液浓度。(2)表中收集的氢气的体积相同,故本实验是通过比较得到相同体积的氢气所用的时间来比较电解水速率的快慢。(3)比较实验A和C,氢氧化钠溶液浓度相同,温度越高,得到相同体积的氢气所用时间越少,故得到的结论是氢氧化钠溶液浓度相同时,温度越高,电解水的速率越快。(4)分析实验B,温度为20 ℃,产生20 mL氢气,需要电解5%的氢氧化钠溶液36.2 s,而实验D温度为30 ℃,则电解时间应小于36.2 s。
19.(1)32 (2)4
(1)根据题意,氧元素的相对原子质量为16,1个甲醇分子中含有1个氧原子,甲醇中氧元素的质量分数为50%,因此甲醇分子的相对分子质量为32。(2)氢元素的质量分数为12.5%,则1个甲醇分子中氢原子的相对质量为32×12.5%=4,因此氢原子的个数是4。
20.(1)C3H7O2N
(2)解:α-丙氨酸中氮元素的质量分数为
×100%=15.7%。
答:α-丙氨酸中氮元素的质量分数为15.7%。
21.(1)22
(2)解:体重为20 kg的儿童每天需要的锌的质量为20 kg×0.5 mg/kg=10 mg,食物提供5 mg,需要服该口服液补充5 mg,故理论上一天需要口服1支口服液。
答:理论上一天还需服该口服液1支。
(1)设氢原子的个数为x,根据相对分子质量的计算方法列出以下方程:12×12+1×x+16×14+65=455,解得x=22。
[范围:自然界的水 时间:40分钟 分值:100分]
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Cl—35.5 Zn—65
题号 1 2 3 4 5 6 7 8 9 10 11 12
选项
一、选择题(每小题3分,共36分)
1.地球表面约有71%被水覆盖,陆地淡水只占全球水储量的2.53%。下列有关水的说法错误的是( )
A.自来水煮沸后变成纯水 B.常用肥皂水鉴别硬水和软水
C.天然水是混合物 D.海水淡化能缓解水资源短缺的危机
2.过滤操作过程中用到的下列仪器不属于玻璃仪器的是 ( )
A.漏斗 B.烧杯 C.铁架台 D.玻璃棒
3.(2020黄冈)下面是萌萌同学的一次化学用语练习的部分内容,其中正确的是 ( )
A.氦气:He2
B.硝酸铵中-3价的氮元素:H4NO3
C.N2:2个氮原子
D.2Fe2+:2个铁离子
4.(2020广州)自来水厂净水过程示意图如图,下列说法正确的是 ( )
A.明矾是一种常用的絮凝剂 B.过滤可除去水中杂质离子
C.活性炭可长期使用无须更换 D.经该净水过程得到的是纯水
5.(2020山西)氮元素形成的化合物种类较多,下列化合物中氮元素化合价为+2的是 ( )
A.NO B.N2O3 C.NH3 D.N2O5
6.下列单一净化水的操作中,净化程度最高的是 ( )
7.化学概念间有包含、并列、交叉等不同关系。下列选项符合所示关系的是
( )
选项 A B C D
X 化合反应 含氧化合物 分解反应 物理变化
Y 氧化反应 氧化物 化学反应 化学变化
8.下列各图中“”和“”分别表示氢原子和氧原子,其中能表示保持水的化学性质的粒子是
( )
9.黄河是我们的母亲河。某化学学习小组的同学经过调查和搜集资料得知,可以通过:①化学沉降(用明矾)、②杀菌消毒(用漂白粉)、③自然沉降、④过滤等几步操作对黄河水进行净化,合理的操作顺序是 ( )
A.①③②④ B.③①④② C.③④①② D.①③④②
10.日常生活中我们经常使用肥皂来清洗衣物,肥皂的主要成分是硬脂酸钠(C17H35COONa)。下列有关硬脂酸钠的说法正确的是 ( )
A.从微观上看:硬脂酸钠含有18个碳原子、35个氢原子、2个氧原子和1个钠原子
B.从宏观上看:硬脂酸钠分子是由碳、氢、氧、钠四种元素组成的
C.从分类上看:硬脂酸钠属于化合物
D.从质量上看:硬脂酸钠中碳、氧元素的质量比为9∶1
11.(2020安徽)理论上电解水得到氧气和氢气的体积比为1∶2。某同学用碳棒作电极进行电解水实验,得到氧气和氢气的体积比小于1∶2,对产生此现象原因的猜想不合理的是 ( )
A.部分氧气溶于水
B.部分氧气与碳棒反应
C.部分氧气被碳棒吸附
D.部分氧气与氢气反应重新生成了水
12.(2020河南)生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是 ( )
A.双氧水消毒液(H2O2) B.“84”消毒液(NaClO)
C.酒精消毒液(C2H5OH) D.过氧乙酸消毒液(C2H4O3)
二、填空题(共22分)
13.(4分)请用相应的化学符号填空。
(1)2个氮分子: 。 (2)-2价的硫元素: 。
(3)铝离子: 。 (4)硫酸铵: 。
14.(4分)水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。为自来水厂净水过程示意图。
取水口反应沉淀池过滤池活性炭吸附池清水池配水泵用户
(1)取水后加入絮凝剂的作用是 。
(2)吸附池内的活性炭起 作用,经沉淀、过滤净化处理后所得的水 (填“是”或“不是”)纯水。
(3)有人说:“世界上最后一滴水就是人类的眼泪。”请你列举一条可行的节水措施:
。
15.(6分)微观示意图有助于我们认识化学物质和理解化学反应。
(1)若用“”表示氧原子,用“”表示氢原子,则“ ”表示 ;“”表示 ;“”表示 。(以上均填化学符号)
(2)在一定条件下,A和B反应生成C和D。反应前后分子种类变化的微观示意图如图所示。请回答以下问题。
①1个B分子中含有 个原子。
②A中氮元素和氢元素的质量比为 。
③四种物质中,属于化合物的是 (填字母)。
16.(8分)(2020天门改编)观察中氮元素的化合价与其所组成的物质类别的关系,回答下列问题。
甲的化学式: ,其在空气中的体积分数为 ;乙的化学式: ;丙的化学式为HNO3,该物质的名称为 。
三、实验探究题(共24分)
17.(14分)如图是电解水的装置,A、B是两个连通的玻璃管(上端是带活塞的尖嘴管),C为连接在A、B中间的球形容器,A、B两管下端是与直流电源相连的两个电极。实验步骤如图下,根据实验填空。
①先将活塞打开,然后从C处将水倒入装置中,使A、B玻璃管中充满水,关闭活塞后再接通电源。
②打开电源开关,几分钟后在A、B玻璃管中生成气体的体积如图图所示。
(1)A、B管内生成的气体聚集在上部的原因是 。
(2)球形容器中液体的液面 (填“上升”或“下降”),产生此现象的原因是
。
(3)B管中的气体是 ,验证B管中气体的最简便的方法是
。
(4)电解一定量的水,当其中一个电极产生5 mL气体时,另一电极产生的气体体积可能是 mL或 mL。
18.(10分)纯水的导电能力很弱,电解水时常在水中加入一些氢氧化钠(NaOH)增强导电性。为研究影响电解水反应速率的因素,某课外活动小组进行了实验探究,数据记录如图下表,请回答下列问题。
实验编号 温度/℃ NaOH溶液浓度 H2体积/mL O2体积/mL 电解时间/s
A 20 2% 20 9.8 54.0
B 20 5% 20 9.8 36.2
C 30 2% 20 9.6 46.2
D 30 5% 20 9.7 x
(1)该小组研究的影响电解水反应速率的因素是 和 。
(2)本实验通过比较 来比较电解水速率的快慢。
(3)比较实验A和C,可得到的结论是 。
(4)分析实验A、B、C的数据,推测实验D的电解时间“x”可能是 (填字母)。
A.35.4 B.37.8 C.50.2 D.55.6
四、计算题(共18分)
19.(4分)(2020泰安)甲醇是一种无色、有特殊香味、易挥发的液体。已知甲醇由碳、氢、氧三种元素组成,其中氢元素的质量分数为12.5%,氧元素的质量分数为50%;1个甲醇分子中含有1个氧原子。回答下列问题。
(1)甲醇的相对分子质量是 。
(2)1个甲醇分子中含氢原子的个数是 。
20.(6分)自然界生命体的有机物组成除碳、氢、氧外还有其他元素,如图某藻类物质(化学式可表示为C106H263O110N16P)的组成中就含有氮元素和磷元素。α-丙氨酸是组成人体蛋白质的氨基酸之一,其分子结构如图所示。
(1)写出α-丙氨酸的化学式: 。
(2)α-丙氨酸中氮元素的质量分数是多少 (结果保留至0.1%)
21.(8分)儿童缺锌会引起食欲不振、发育不良等症状。为某补锌口服液说明书的部分信息,图中葡萄糖酸锌的化学式已不完整,请根据相关信息回答下列问题。
(1)葡萄糖酸锌的相对分子质量是455,则葡萄糖酸锌化学式中氢原子右下角的数字为 。
(2)若儿童每1 kg体重每日需要0.5 mg锌,每天从食物中只能摄入所需锌的一半。体重为20 kg的儿童,理论上一天还需服该口服液多少支
答案
第四单元综合提升卷
1.A 自来水煮沸后,可使钙、镁离子从水中沉淀出来,但水中还有一些可溶性物质没有除去,不能变成纯水;肥皂水可以用来鉴别硬水和软水;天然水中含有可溶性杂质和细菌等,是混合物。
2.C 铁架台由金属制成,不属于玻璃仪器。
3.B 氦气直接用元素符号表示为He;硝酸铵中-3价的氮元素是铵根中的氮元素,所以表示为H4NO3;氮气的化学式是N2,元素符号右下角的数字“2”表示1个氮分子中含有2个氮原子;2Fe2+表示2个亚铁离子。
4.A 明矾是沉降常用的絮凝剂,明矾能与水反应生成胶状物,吸附悬浮杂质,使其沉降;过滤可除去水中的难溶性物质,杂质离子是溶解在水中的,无法通过过滤除去;活性炭长期使用,吸附能力会下降,所以需要定时更换;经该净水过程得到的水中还含有部分可溶性杂质,不是纯水。
5.A 6.C
7.C 化合反应与氧化反应属于交叉关系;物理变化和化学变化是并列关系;含氧化合物与氧化物、分解反应与化学反应都属于包含关系,前者是X包含Y,后者是Y包含X。
8.A A图表示水分子,水分子能保持水的化学性质;B图表示氢分子和氧分子,C图表示氢分子,D图表示氢原子和氧原子,均不能保持水的化学性质。
9.B
10.C 从微观上看,分子是由原子构成的,1个硬脂酸钠分子中含有18个碳原子、35个氢原子、2个氧原子和1个钠原子;从宏观上看,物质是由元素组成的,硬脂酸钠是由碳、氢、氧、钠四种元素组成的;由不同种元素组成的纯净物叫作化合物,从分类上看,硬脂酸钠是由碳、氢、氧、钠四种元素组成的纯净物,属于化合物;从质量上看,硬脂酸钠中碳、氧元素的质量比为(12×18)∶(16×2)=27∶4。
11.D 在室温下,1 L水中能溶解约30 mL氧气,而氢气难溶于水,故得到氧气和氢气的体积比小于1∶2;碳能与氧气在一定条件下反应生成二氧化碳,故可能是部分氧气与碳棒发生了反应;碳棒具有疏松多孔的结构,可能会吸附一部分氧气;电解水时,生成的氢气和氧气一般无法接触,且若氧气与氢气反应重新生成了水,每2体积的氢气与1体积的氧气反应,对生成的氧气与氢气的体积比没有影响。
12.A H2O2中氧元素的质量分数为×100%=94.1%;NaClO中氧元素的质量分数为×100%=21.5%;C2H5OH中氧元素的质量分数为×100%=34.8%;C2H4O3中氧元素的质量分数为×100%=63.2%。
13.(1)2N2 (2) (3)Al3+ (4)(NH4)2SO4
本题主要考查常用的化学用语。化学符号前面的数字表示粒子的个数;化合价标注在元素符号(或原子团)的正上方,正负号在前,数字在后;离子所带电荷标注在元素符号的右上角,数字在前,正负号在后;书写化学式要遵循正负化合价的代数和为零的原则。
14.(1)使水中的悬浮杂质沉降 (2)吸附 不是 (3)用淘米水浇花(合理即可)
(1)絮凝剂的主要成分是明矾,明矾溶于水后形成的胶状物对悬浮杂质有吸附作用,能使其沉降而达到净水的目的。(2)活性炭具有疏松多孔的结构,在自来水生产中起到吸附水中色素和异味的作用;经沉淀、过滤的水只是除去了水中不溶性固体杂质,水中仍含有许多可溶性物质,所以得到的不是纯水。(3)节约用水应从每个人做起,可结合生活中的具体事例来说明如图何节约用水,如图及时关闭水龙头、用淘米水浇花、农业上改大水漫灌为喷灌等。
15.(1)2H H2 H2O (2)①2 ②14∶3 ③AD
(1)原子没有结合在一起,表示几个单独的原子;原子结合在一起,表示分子;化合物的分子由不同种原子构成。(2)②1个A分子由1个氮原子和3个氢原子构成,化学式为NH3,其中氮、氢两种元素的质量比为(14×1)∶(1×3)=14∶3。
16.N2 78% N2O 硝酸
从图中可以看出甲是由氮元素组成的单质,所以甲是氮气,化学式为N2,乙是显+1价的氮元素的氧化物,化学式为N2O。
17.(1)气体的密度比水小,且氧气不易溶于水,氢气难溶于水
(2)上升 A、B管内有气体生成,气压变大,将液体压入C中
(3)氧气 将带火星的木条置于B管上方尖嘴处,慢慢打开活塞,木条复燃,证明该气体为氧气
(4)2.5 10
(1)水在通电的条件下生成氢气和氧气,由于气体的密度比水小,且氧气不易溶于水,氢气难溶于水,所以A、B管内生成的气体聚集在上部。(2)由于A、B管内有气体生成,气压变大,将液体压入C中,所以球形容器中液面上升。(3)水在通电时,正极产生氧气,负极产生氢气,所以B管中的气体是氧气,验证B管中气体的最简便方法是将带火星的木条置于B管上方尖嘴处,慢慢打开活塞,木条复燃,证明该气体为氧气。(4)电解一定量的水,当其中一个电极产生5 mL气体时,该气体可能是氢气,也可能是氧气,所以另一电极产生的气体体积可能是2.5 mL或10 mL。
18.(1)温度 氢氧化钠溶液浓度 (2)得到相同体积氢气所用的时间
(3)氢氧化钠溶液浓度相同时,温度越高,电解水的速率越快 (4)A
(1)分析表中数据,A和B、C和D是温度相同,氢氧化钠溶液浓度不同,得到相同体积氢气所需电解时间不同;A和C、B和D是温度不同,氢氧化钠溶液浓度相同,得到相同体积氢气所需电解时间不同,由此可知小组研究的影响电解水反应速率的因素是温度和氢氧化钠溶液浓度。(2)表中收集的氢气的体积相同,故本实验是通过比较得到相同体积的氢气所用的时间来比较电解水速率的快慢。(3)比较实验A和C,氢氧化钠溶液浓度相同,温度越高,得到相同体积的氢气所用时间越少,故得到的结论是氢氧化钠溶液浓度相同时,温度越高,电解水的速率越快。(4)分析实验B,温度为20 ℃,产生20 mL氢气,需要电解5%的氢氧化钠溶液36.2 s,而实验D温度为30 ℃,则电解时间应小于36.2 s。
19.(1)32 (2)4
(1)根据题意,氧元素的相对原子质量为16,1个甲醇分子中含有1个氧原子,甲醇中氧元素的质量分数为50%,因此甲醇分子的相对分子质量为32。(2)氢元素的质量分数为12.5%,则1个甲醇分子中氢原子的相对质量为32×12.5%=4,因此氢原子的个数是4。
20.(1)C3H7O2N
(2)解:α-丙氨酸中氮元素的质量分数为
×100%=15.7%。
答:α-丙氨酸中氮元素的质量分数为15.7%。
21.(1)22
(2)解:体重为20 kg的儿童每天需要的锌的质量为20 kg×0.5 mg/kg=10 mg,食物提供5 mg,需要服该口服液补充5 mg,故理论上一天需要口服1支口服液。
答:理论上一天还需服该口服液1支。
(1)设氢原子的个数为x,根据相对分子质量的计算方法列出以下方程:12×12+1×x+16×14+65=455,解得x=22。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
