人教版化学九年级上册同步提优训练:第6单元 碳和碳的氧化物 专题训练 常见气体的实验室制备(word版有答案)
文档属性
| 名称 | 人教版化学九年级上册同步提优训练:第6单元 碳和碳的氧化物 专题训练 常见气体的实验室制备(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 307.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-09 00:00:00 | ||
图片预览

文档简介
专题训练 常见气体的实验室制备
题型一 氧气与二氧化碳的制取
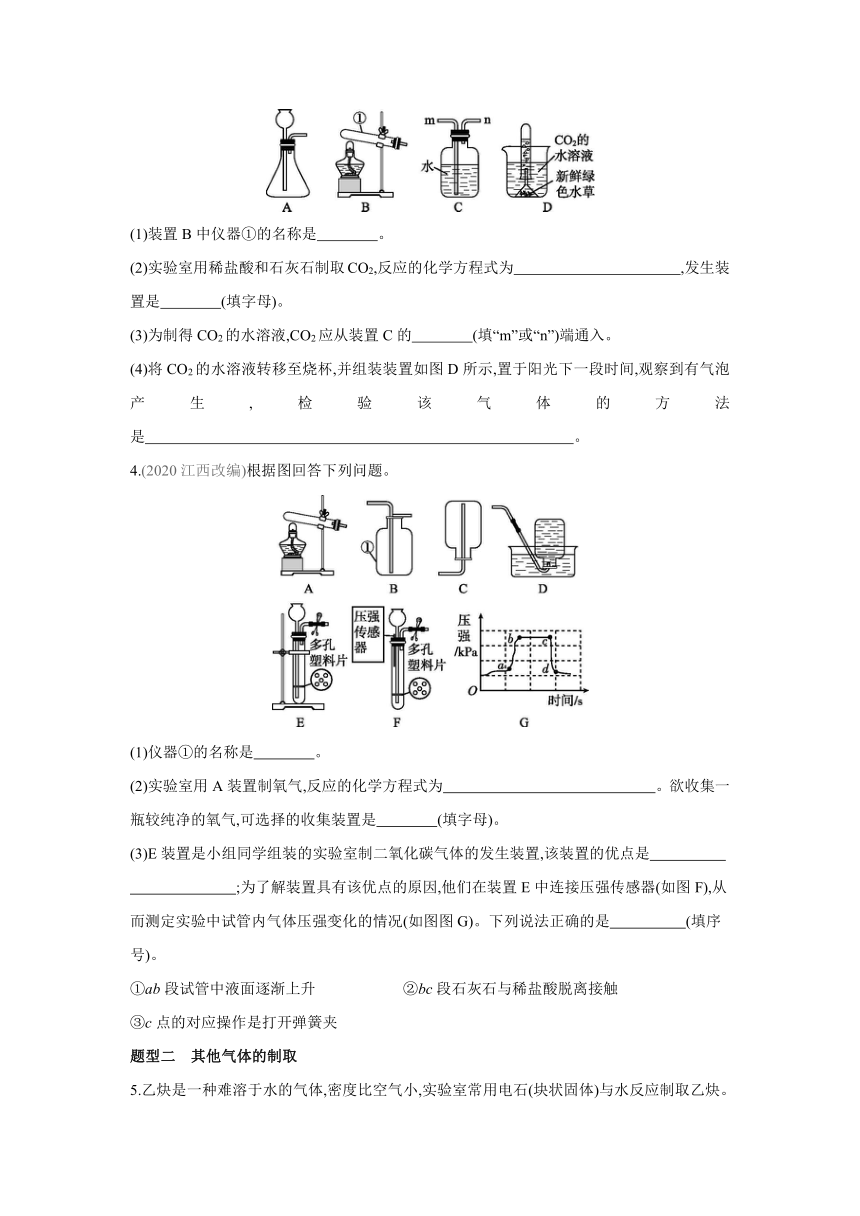
1.(2020上海)如图图所示实验设计,能制取二氧化碳并可控制反应发生或停止的是
( )
2.(2020沈阳改编)图是实验室制取气体的常用装置,请回答下列问题。
(1)写出标号仪器的名称:① ,② 。
(2)实验室用C、D装置制取二氧化碳时,选用的固体药品名称是 ,加入的液体药品液面高度应该在 (填C装置中的“a”或“b”)处,该反应的化学方程式为 。
(3)实验室用高锰酸钾制取氧气,该反应的化学方程式为 ,应选用的发生装置是 (填字母)。若用F装置收集氧气,集满后应将导管从集气瓶中移出, ,将集气瓶移出水面,正放在桌面上。
3.(2021安徽)某小组利用如图下装置制备CO2,并模拟自然界中CO2的循环。回答下列问题。
(1)装置B中仪器①的名称是 。
(2)实验室用稀盐酸和石灰石制取CO2,反应的化学方程式为 ,发生装置是 (填字母)。
(3)为制得CO2的水溶液,CO2应从装置C的 (填“m”或“n”)端通入。
(4)将CO2的水溶液转移至烧杯,并组装装置如图D所示,置于阳光下一段时间,观察到有气泡产生,检验该气体的方法是 。
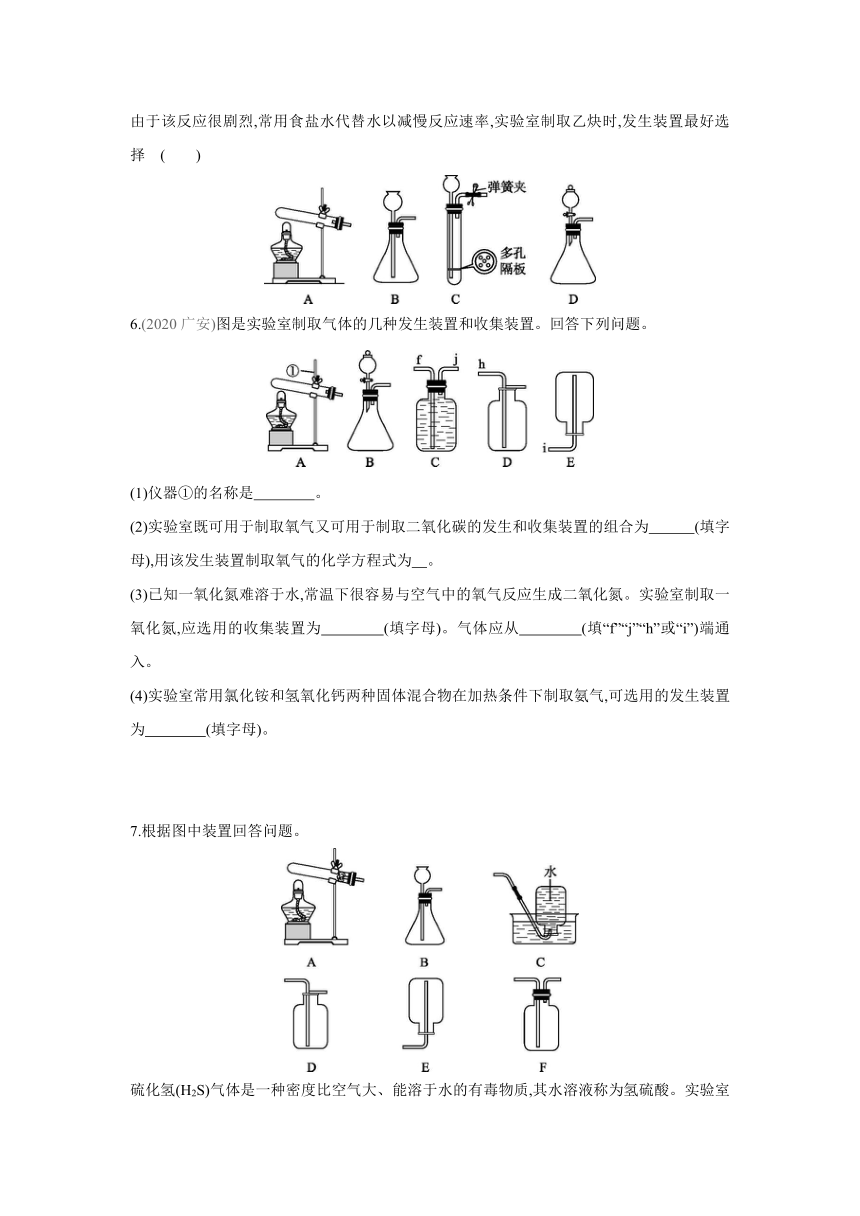
4.(2020江西改编)根据图回答下列问题。
(1)仪器①的名称是 。
(2)实验室用A装置制氧气,反应的化学方程式为 。欲收集一瓶较纯净的氧气,可选择的收集装置是 (填字母)。
(3)E装置是小组同学组装的实验室制二氧化碳气体的发生装置,该装置的优点是
;为了解装置具有该优点的原因,他们在装置E中连接压强传感器(如图F),从而测定实验中试管内气体压强变化的情况(如图图G)。下列说法正确的是 (填序号)。
①ab段试管中液面逐渐上升 ②bc段石灰石与稀盐酸脱离接触
③c点的对应操作是打开弹簧夹
题型二 其他气体的制取
5.乙炔是一种难溶于水的气体,密度比空气小,实验室常用电石(块状固体)与水反应制取乙炔。由于该反应很剧烈,常用食盐水代替水以减慢反应速率,实验室制取乙炔时,发生装置最好选择 ( )
6.(2020广安)图是实验室制取气体的几种发生装置和收集装置。回答下列问题。
(1)仪器①的名称是 。
(2)实验室既可用于制取氧气又可用于制取二氧化碳的发生和收集装置的组合为 (填字母),用该发生装置制取氧气的化学方程式为 。
(3)已知一氧化氮难溶于水,常温下很容易与空气中的氧气反应生成二氧化氮。实验室制取一氧化氮,应选用的收集装置为 (填字母)。气体应从 (填“f”“j”“h”或“i”)端通入。
(4)实验室常用氯化铵和氢氧化钙两种固体混合物在加热条件下制取氨气,可选用的发生装置为 (填字母)。
7.根据图中装置回答问题。
硫化氢(H2S)气体是一种密度比空气大、能溶于水的有毒物质,其水溶液称为氢硫酸。实验室常用硫化亚铁(FeS)固体和稀硫酸在常温下反应制取硫化氢气体,应选择的发生装置是 。小虹同学认为收集硫化氢气体可用D装置,但小娟有不同的意见,小娟的理由是 。写出你改进后的收集方法:
。
答案
常见气体的实验室制备
1.B
固液常温型气体发生装置的比较:
气体发生装置 优点
装置简单
能制取较多量气体,便于向反应容器中添加液体
连续制取且可以控制反应的速率,得到平稳的气流
能控制反应的发生和停止
2.(1)铁架台 水槽
(2)大理石(或石灰石) b
CaCO3+2HClCaCl2+CO2↑+H2O
(3)2KMnO4K2MnO4+MnO2+O2↑ A 用玻璃片的磨砂面盖住集气瓶口
(2)实验室制取二氧化碳选用的药品是大理石(或石灰石)与稀盐酸。加入的液体药品应使长颈漏斗下端管口形成液封。(3)实验室用高锰酸钾制取氧气,其化学方程式为2KMnO4K2MnO4+MnO2+O2↑;该反应需要加热,故应选用的气体发生装置为A;用排水法收集气体,气体集满后,将导管从集气瓶中移出,用玻璃片的磨砂面盖住集气瓶口,将集气瓶移出水面,正放在桌面上。
3.(1)试管
(2)2HCl+CaCO3CaCl2+H2O+CO2↑ A
(3)m
(4)将带火星的木条伸入收集到的气体中,观察木条是否复燃
(4)水草进行光合作用生成氧气,要检验氧气,一般是将带火星的木条伸入收集到的气体中,观察木条是否复燃。
4.(1)集气瓶
(2)2KClO32KCl+3O2↑ D
(3)可以控制反应的发生和停止 ②③
(2)A装置适用于加热固体制取氧气,试管口没有放一团棉花,故适用于加热氯酸钾和二氧化锰制取氧气;氧气不易溶于水,密度比空气的大,可用排水法或向上排空气法收集,排水法收集的氧气比较纯净。(3)E装置可以控制反应的发生和停止,将石灰石置于多孔塑料片上,通过长颈漏斗添加稀盐酸,夹紧弹簧夹,反应产生的气体无法逸出,装置内压强增大;稀盐酸被压入长颈漏斗中,固液分离,反应停止,压强不再变化;打开弹簧夹气体排出,压强减小。
5.D 制取乙炔的反应很剧烈,实验时需控制反应速率,而B、C无法控制反应速率,D可利用分液漏斗控制加入食盐水的速率,从而控制反应的速率。
抓住关键词“反应很剧烈”,所以所用发生装置应该可以控制反应速率。
6.(1)铁架台 (2)BD 2H2O22H2O+O2↑ (3)C j (4)A
(3)NO常温下很容易与空气中的O2反应生成NO2,因此不能用排空气法收集;NO难溶于水,因此可以用排水法收集,应选用的收集装置为C,排水集气时,气体要从短导管进,将水从长导管排出,因此,气体应从j端通入。(4)实验室制取NH3的发生装置为固体加热型,因此可选用的发生装置为A。
选择“陌生”气体的制取装置,需根据实验室中制取气体的一般思路和方法进行知识的迁移。首先要熟悉固体加热型和固液不加热型两种气体发生装置,知道根据气体的密度和溶解性来选择收集装置。
7.B H2S气体有毒会污染空气 用F装置收集,排出的气体用塑料袋收集(或用水吸收,合理即可)
实验室用硫化亚铁固体和稀硫酸常温下反应制取硫化氢气体,故应该选择B装置作为反应的发生装置。硫化氢的密度比空气的大,可以用向上排空气法收集,但是硫化氢气体有毒,不能用普通的向上排空气法收集,应用密封型气体收集装置即F装置来收集,最后注意将排出的气体用塑料袋收集(或用水吸收)。
若气体的密度与空气接近或气体与空气中的成分反应,则不适合用排空气法收集;若收集有毒气体,则需用密封型气体收集装置,且需要处理尾气。
题型一 氧气与二氧化碳的制取
1.(2020上海)如图图所示实验设计,能制取二氧化碳并可控制反应发生或停止的是
( )
2.(2020沈阳改编)图是实验室制取气体的常用装置,请回答下列问题。
(1)写出标号仪器的名称:① ,② 。
(2)实验室用C、D装置制取二氧化碳时,选用的固体药品名称是 ,加入的液体药品液面高度应该在 (填C装置中的“a”或“b”)处,该反应的化学方程式为 。
(3)实验室用高锰酸钾制取氧气,该反应的化学方程式为 ,应选用的发生装置是 (填字母)。若用F装置收集氧气,集满后应将导管从集气瓶中移出, ,将集气瓶移出水面,正放在桌面上。
3.(2021安徽)某小组利用如图下装置制备CO2,并模拟自然界中CO2的循环。回答下列问题。
(1)装置B中仪器①的名称是 。
(2)实验室用稀盐酸和石灰石制取CO2,反应的化学方程式为 ,发生装置是 (填字母)。
(3)为制得CO2的水溶液,CO2应从装置C的 (填“m”或“n”)端通入。
(4)将CO2的水溶液转移至烧杯,并组装装置如图D所示,置于阳光下一段时间,观察到有气泡产生,检验该气体的方法是 。
4.(2020江西改编)根据图回答下列问题。
(1)仪器①的名称是 。
(2)实验室用A装置制氧气,反应的化学方程式为 。欲收集一瓶较纯净的氧气,可选择的收集装置是 (填字母)。
(3)E装置是小组同学组装的实验室制二氧化碳气体的发生装置,该装置的优点是
;为了解装置具有该优点的原因,他们在装置E中连接压强传感器(如图F),从而测定实验中试管内气体压强变化的情况(如图图G)。下列说法正确的是 (填序号)。
①ab段试管中液面逐渐上升 ②bc段石灰石与稀盐酸脱离接触
③c点的对应操作是打开弹簧夹
题型二 其他气体的制取
5.乙炔是一种难溶于水的气体,密度比空气小,实验室常用电石(块状固体)与水反应制取乙炔。由于该反应很剧烈,常用食盐水代替水以减慢反应速率,实验室制取乙炔时,发生装置最好选择 ( )
6.(2020广安)图是实验室制取气体的几种发生装置和收集装置。回答下列问题。
(1)仪器①的名称是 。
(2)实验室既可用于制取氧气又可用于制取二氧化碳的发生和收集装置的组合为 (填字母),用该发生装置制取氧气的化学方程式为 。
(3)已知一氧化氮难溶于水,常温下很容易与空气中的氧气反应生成二氧化氮。实验室制取一氧化氮,应选用的收集装置为 (填字母)。气体应从 (填“f”“j”“h”或“i”)端通入。
(4)实验室常用氯化铵和氢氧化钙两种固体混合物在加热条件下制取氨气,可选用的发生装置为 (填字母)。
7.根据图中装置回答问题。
硫化氢(H2S)气体是一种密度比空气大、能溶于水的有毒物质,其水溶液称为氢硫酸。实验室常用硫化亚铁(FeS)固体和稀硫酸在常温下反应制取硫化氢气体,应选择的发生装置是 。小虹同学认为收集硫化氢气体可用D装置,但小娟有不同的意见,小娟的理由是 。写出你改进后的收集方法:
。
答案
常见气体的实验室制备
1.B
固液常温型气体发生装置的比较:
气体发生装置 优点
装置简单
能制取较多量气体,便于向反应容器中添加液体
连续制取且可以控制反应的速率,得到平稳的气流
能控制反应的发生和停止
2.(1)铁架台 水槽
(2)大理石(或石灰石) b
CaCO3+2HClCaCl2+CO2↑+H2O
(3)2KMnO4K2MnO4+MnO2+O2↑ A 用玻璃片的磨砂面盖住集气瓶口
(2)实验室制取二氧化碳选用的药品是大理石(或石灰石)与稀盐酸。加入的液体药品应使长颈漏斗下端管口形成液封。(3)实验室用高锰酸钾制取氧气,其化学方程式为2KMnO4K2MnO4+MnO2+O2↑;该反应需要加热,故应选用的气体发生装置为A;用排水法收集气体,气体集满后,将导管从集气瓶中移出,用玻璃片的磨砂面盖住集气瓶口,将集气瓶移出水面,正放在桌面上。
3.(1)试管
(2)2HCl+CaCO3CaCl2+H2O+CO2↑ A
(3)m
(4)将带火星的木条伸入收集到的气体中,观察木条是否复燃
(4)水草进行光合作用生成氧气,要检验氧气,一般是将带火星的木条伸入收集到的气体中,观察木条是否复燃。
4.(1)集气瓶
(2)2KClO32KCl+3O2↑ D
(3)可以控制反应的发生和停止 ②③
(2)A装置适用于加热固体制取氧气,试管口没有放一团棉花,故适用于加热氯酸钾和二氧化锰制取氧气;氧气不易溶于水,密度比空气的大,可用排水法或向上排空气法收集,排水法收集的氧气比较纯净。(3)E装置可以控制反应的发生和停止,将石灰石置于多孔塑料片上,通过长颈漏斗添加稀盐酸,夹紧弹簧夹,反应产生的气体无法逸出,装置内压强增大;稀盐酸被压入长颈漏斗中,固液分离,反应停止,压强不再变化;打开弹簧夹气体排出,压强减小。
5.D 制取乙炔的反应很剧烈,实验时需控制反应速率,而B、C无法控制反应速率,D可利用分液漏斗控制加入食盐水的速率,从而控制反应的速率。
抓住关键词“反应很剧烈”,所以所用发生装置应该可以控制反应速率。
6.(1)铁架台 (2)BD 2H2O22H2O+O2↑ (3)C j (4)A
(3)NO常温下很容易与空气中的O2反应生成NO2,因此不能用排空气法收集;NO难溶于水,因此可以用排水法收集,应选用的收集装置为C,排水集气时,气体要从短导管进,将水从长导管排出,因此,气体应从j端通入。(4)实验室制取NH3的发生装置为固体加热型,因此可选用的发生装置为A。
选择“陌生”气体的制取装置,需根据实验室中制取气体的一般思路和方法进行知识的迁移。首先要熟悉固体加热型和固液不加热型两种气体发生装置,知道根据气体的密度和溶解性来选择收集装置。
7.B H2S气体有毒会污染空气 用F装置收集,排出的气体用塑料袋收集(或用水吸收,合理即可)
实验室用硫化亚铁固体和稀硫酸常温下反应制取硫化氢气体,故应该选择B装置作为反应的发生装置。硫化氢的密度比空气的大,可以用向上排空气法收集,但是硫化氢气体有毒,不能用普通的向上排空气法收集,应用密封型气体收集装置即F装置来收集,最后注意将排出的气体用塑料袋收集(或用水吸收)。
若气体的密度与空气接近或气体与空气中的成分反应,则不适合用排空气法收集;若收集有毒气体,则需用密封型气体收集装置,且需要处理尾气。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
