沪教版九上化学 3.4 整理与复习 课件(共29张PPT)
文档属性
| 名称 | 沪教版九上化学 3.4 整理与复习 课件(共29张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 487.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-12 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
第 3 章
(分子原子复习课)
物质构成的奥秘
本章主要分四部分复习:
1.构成物质的微粒
2.组成物质的元素
3.物质的分类
4.有关化学式的计算
心中有数:
分子
原子
离子
分
解
构
成
得
失
电
子
失
得
电
子
微粒的性质
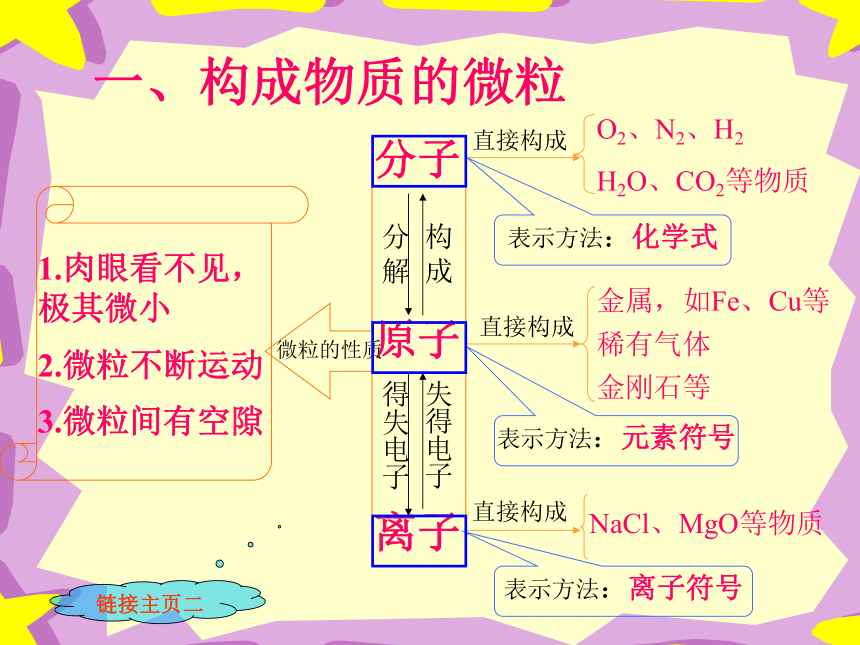
1.肉眼看不见,极其微小
2.微粒不断运动
3.微粒间有空隙
直接构成
O2、N2、H2
直接构成
金属,如Fe、Cu等
直接构成
NaCl、MgO等物质
一、构成物质的微粒
表示方法:化学式
表示方法:元素符号
表示方法:离子符号
H2O、CO2等物质
稀有气体
金刚石等
链接主页二
原子核
电子
质子
中子
决定
元素种类
最外层电子数决定元素化学性质
决定
原子质量
(+)
(-)
(+)
(不带电)
核电荷数=质子数=电子数
相对原子质量=质子数+中子数
返主页
一
分子原子 的区别:
在化学变化中,分子可分,原子不可分!
原子是化学变化中的最小微粒!
原子结构
二、组成物质的元素
元素
自然界中分布
与人体健康→
表示方法→
组成化学式
元素符号
含义
地壳中→
海洋中→
人体中→
O、Si、Al、Fe
O
O
Ca、Fe、Zn、I、F 等对人体的影响
表示一种元素
表示一个原子
1.写法
单质→
化合物→
化合价
2.含义
表示一种物质
表示组成物质的元素
表示一个分子
表示一个分子中原子个数
链接主页三
O2、N2、H2 等
物质
按物质
种类分
按元素
种类分
混合物
(不同种物质组成)
纯净物
(同种物质组成)
单质
(同种元素组成)
化合物
(不同种元素组成)
按性质分
金属(如Fe、Cu等)
非金属(如C、P、O2等)
稀有气体(如He、Ne等)
按组成和
性质分
氧化物
(如H2O、MgO等)
酸(如H2CO3等)
碱(如Ca(OH)2等)
盐(如NaCl、CaCO3等)
(如空气、海水、澄清石灰水、石灰石等)
三、物质分类
链接主页四
四、有关化学式的计算
掌握
三种
基本
题型
1.求相对分子质量
2.求化合物中各元素的质量比
3.求化合物中某元素的质量分数
点击练习
1.用微粒的观点解释:
⑴2500L液化气能压缩在40L钢瓶中,说明
⑵丁香花开的季节可以闻到浓郁的香气,说明
⑶一滴水水中含有1.7×1021个水分子,说明
微粒间有空隙
微粒不断运动
微粒体积小
2.下列现象中不能用分子运动论解释的是( )
A.把两块表面平滑干净的铅压紧,就不容易将
它们拉开
B.在室内,同样表面积的热水比冷水蒸发得快
C.氧化汞受热分解生成汞和氧气
D.医院里充满了酒精味和药味
C
用微粒的观点解释
3.用原子和分子的观点解释:水通电生成氢气和氧气以及水蒸发形成水蒸气这两个变化的实质。
水是由水分子构成。水通电时,水分子分解成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子,许多氢分子构成氢气,许多氧分子构成氧气。
水蒸发时,水分子本身没有变,只是水分子间的空隙变大,所以水变成水蒸气。
4.把充满红棕色NO2气体和无色H2的集气瓶中间的玻璃片抽走,使两瓶口密合在一起(不要振荡),可观察到左边的两瓶气体的颜色很快趋于一致(两瓶气体不反应),右边两瓶气体需要很长时间才能达到同样的效果。
NO2
NO2
H2
H2
观察、对比实验现象,你能得出的结论有:
(1)
(2)
NO2的密度比H2大
分子在不断运动
(或分子间有空隙)
汞原子
二氧化碳分子
钠离子、氯离子
用化学符号表示:
2个氮原子 2个氮分子
2个铁离子 2个亚铁离子
2个铁原子 n个水分子
1个铵根离子 2个氢氧根离子
2N
2N2
2Fe 3+
2Fe 2+
2Fe
n H2O
NH4 +
2OH -
科学研究证实,物质是由微粒构成的,例如铁是由铁原子构成的。请你填写构成下列物质的具体微粒的名称。
⑴体温计中的汞是由 构成的;
⑵人工降雨用的干冰是由 构成的;
⑶食盐中的氯化钠是由 构成的。
物质由微粒构成
相对原子质量:
m m 12m 12n
n 12n n m
2.1991年,我国化学家张青莲教授与别人合作,重新测定了铟元素的相对原子质量。铟元素的核电荷数为49,相对原子质量为115,则铟原子核外电子数 ,核内质子数为 ,中子数为 。
1.若碳——12原子的质量为n g,A原子的质量为m g,则A原子的相对原子质量为( )
A. B. C. D.
以一种碳原子质量的1/12作为标准,其他原子的质量与
这一基准的比值,称为这种原子的相对原子质量。
相对原子质量只是个比值,不是原子的实际质量。
C
49
49
66
对于Fe、Fe2+、Fe3+三种微粒的判断,正确的是( )
①核电荷数相同
②核外电子数相等
③电子层结构完全相同
④质量几乎相等
⑤等质量的三种微粒所含的质子数相等
A.①④⑤ B.①③⑤
C.②③④ D.①②③④⑤
A
分子、原子、离子说法
1.下列关于分子、原子、离子说法不正确的是( ) A.分子是保持物质化学性质的一种微粒 B.原子是不能再分的最小微粒 C.分子、原子、离子都是构成物质的微粒 D.分子、原子、离子都是在不停运动
B
2.已知R2+核外电子数为N,仍不能确定的是原子的
A.质子数 B. 中子数 ( )
C.核电荷数 D. 电子层数
B
在空格中填写适当的元素符号。
地壳中含量最多的非金属元素是 ,其次是 ;地壳中含量最多的金属元素是 ,其次是 ;地球大气里含量最多的元素是 ;人体里含量最多的元素是 ;海洋里含量最多的元素是 ;太阳中含量最多的元素是 ;地核中含量最多的元素是 ;人体缺少 元素,容易得贫血症;小儿体内缺少 元素,容易得佝偻病;缺 会导致儿童发育迟缓,智力低下;人体缺 元素会引起龋齿,但它含量过高,又会使牙齿釉质受损。
O
Si
Al
Fe
N
O
O
Fe
Fe
Ca
Zn
F
H
元素分布
化合价:
根据化合价书写化合物的化学式:
1.通常正价元素写在前,负价元素写在后。
2.根据正负元素化合价代数和为零的原则确定
原子个数。
2.下列物质的名称与化学式相符的是( )
A.硫酸亚铁(FeSO4) B.氧化铁(FeO)
C.硫酸钠(NaSO4) D.氯化铜(CuCl)
1. 地壳中含量最多的金属元素与地壳中含量最多的非金属元素组成的化合物的化学式为 。
Al2O3
A
1.干燥多风的季节里,夜晚人们走在荒野中,有时会看到“鬼火”现象,其实它是一种类似于氨气组成的气体(PH3)在空气中自燃的现象。PH3中P的化合价是 ( )
A.+3 B.-3 C.+1 D.+5
2. 下列的物质按照一定的规律排列,则空格内的物质应是( )
Na2SO4 H2SO3 H2S
A.H2SO4 B .Na2S C.SO2 D.S
B
D
根据正负元素化合价代数和为零的原则确定化
学式中某元素的化合价。
+6 +4 -2
1.下列符号中,既能表示宏观含义,也能表示微观含义的是( )
A.2H2O B. 5O C. S D. Fe 2+
B
C
2.下列符号既能表示一种元素又能表示一个原子,还能表示一种单质的是 ( )
A.O2 B.Mg C.H D.N
3.保持氢气化学性质的最小微粒是( )
A.H2 B.H C.H+ D.H2O
A
4. 2003年,齐齐哈尔市发生了重大中毒事件,该事件的“肇事者”是侵华日军遗留下来的,被称为“毒气之王”的“芥子气”。芥子气,学名二氯二乙硫醚,化学式为(C2H4Cl)2S。下列有关二氯二乙硫醚的说法中错误的是( )
A.是有机物
B.由C、H、Cl、S四种元素组成
C.一个分子中含有15个原子
D.分子中C、H、Cl、S的原子个数比为2:4:2:1
D
5.我们日常生活中出现了加碘食盐、高钙牛奶、富硒大米等物质。这里的碘、钙、硒应理解为( )
A.单质 B.分子 C.元素 D.离子
6.一种元素与另一种元素的本质区别是( )
A.相对原子质量不同 B.质子数不同
C.中子数不同 D.电子数不同
7.关于水的描述,下列说法不正确的是( )
A.水是由氢元素和氧元素组成的
B.水分子是由氢原子和氧原子构成的
C.水是由许许多多的水分子构成的
D.水是由两个氢原子和一个氧原子构成的
C
B
D
物质分类
1.家庭日常生活中经常用到的下列物质中,属于纯净物的是( )
A.餐饮用的可口可乐 B.调味用的加碘食盐
C.炒菜用的铁锅 D.降温用的冰水共存物
2.有下列两组物质,每组中均有一种与其他物质所属类别不同,请在下面的横线上填写出这种物质的名称:
(1)食醋、牛奶、加碘盐、蔗糖
(2)氧化镁、水、碳酸钙、五氧化二磷
(1) (2)
D
蔗糖
碳酸钙
4.一瓶气体经化验只由一种元素组成,则该气体是( )
A.一种单质 B.一种化合物
C.一种纯净物
D.可能是一种单质,也可能是几种单质组成的
混合物
D
3.下列各组物质中,前者是单质,后者是氧化物的是( )
A.石灰石 冰 B.金刚石 干冰
C.液氧 高锰酸钾 D.水银 碘酒
B
1.求出下列各物质的相对分子质量:
Mr(CO2) =
Mr(2H2O)=
Mr[Ca(OH)2]=
Mr(CuSO4·5H2O)
=
12+16×2=44
64+32+16×4 + 5×(2+16)=250
40+2×(16+1)=74
2×(16+1×2)=36
2、求化合物中各元素的质量比
CO2中, C、O元素的质量比为
Ca(OH)2中,Ca、O、H元素的质量比
NH4NO3中,N、H、O元素的质量比
= 12 : 2×16 = 3 :8
=40 :16×2 :1×2 = 20 :6 :1
=14×2 : 1×4 : 16×3 =7 :1 :12
3、求化合物中某元素的质量分数
CO2中碳元素的质量分数
=
=
Ar(C) 12×1
Mr(CO2) 12+16×2
×100%
×100%
=35%
=
×100%
27.3%
NH4NO3中氮元素的质量分数
=
=
14×2
14×2+1×4+16×3
Ar(N)×2
Mr( NH4NO3 )
×100%
1.食物在煎炸的过程中会产生一种强致癌物质——丙烯醛,化学式为C2H3CHO,所以油炸食品不宜多吃。请回答:
(1)丙烯醛的相对分子质量是 。
(2)丙烯醛中C、H、O元素的质量比是 。
(3)丙烯醛中氧元素的质量分数为 (结果保留一位小数) 。
56
28.6%
9:1:4
2.市售的“脑黄金”(DHA)是从深海鱼油中提取的,主要成分为一种不饱和脂肪酸,其化学式为C25H50COOH,它是由 种元素组成的,每个分子中有 个原子。
3.下图是小明使用的修正液包装标签上的部分文字,这种修正液中甲基环已烷的相对分子质量是 ,假若其中甲基环已烷的质量分数是75%,则含甲基环已烷的质量为 g。
××修正液
主要成分:甲基环已烷(C6H11CH3)、钛白粉、
合成树脂
净含量:18g
通过ISO9001国际质量体系认证
3
79
98
13.5
点击综合练习
第 3 章
(分子原子复习课)
物质构成的奥秘
本章主要分四部分复习:
1.构成物质的微粒
2.组成物质的元素
3.物质的分类
4.有关化学式的计算
心中有数:
分子
原子
离子
分
解
构
成
得
失
电
子
失
得
电
子
微粒的性质
1.肉眼看不见,极其微小
2.微粒不断运动
3.微粒间有空隙
直接构成
O2、N2、H2
直接构成
金属,如Fe、Cu等
直接构成
NaCl、MgO等物质
一、构成物质的微粒
表示方法:化学式
表示方法:元素符号
表示方法:离子符号
H2O、CO2等物质
稀有气体
金刚石等
链接主页二
原子核
电子
质子
中子
决定
元素种类
最外层电子数决定元素化学性质
决定
原子质量
(+)
(-)
(+)
(不带电)
核电荷数=质子数=电子数
相对原子质量=质子数+中子数
返主页
一
分子原子 的区别:
在化学变化中,分子可分,原子不可分!
原子是化学变化中的最小微粒!
原子结构
二、组成物质的元素
元素
自然界中分布
与人体健康→
表示方法→
组成化学式
元素符号
含义
地壳中→
海洋中→
人体中→
O、Si、Al、Fe
O
O
Ca、Fe、Zn、I、F 等对人体的影响
表示一种元素
表示一个原子
1.写法
单质→
化合物→
化合价
2.含义
表示一种物质
表示组成物质的元素
表示一个分子
表示一个分子中原子个数
链接主页三
O2、N2、H2 等
物质
按物质
种类分
按元素
种类分
混合物
(不同种物质组成)
纯净物
(同种物质组成)
单质
(同种元素组成)
化合物
(不同种元素组成)
按性质分
金属(如Fe、Cu等)
非金属(如C、P、O2等)
稀有气体(如He、Ne等)
按组成和
性质分
氧化物
(如H2O、MgO等)
酸(如H2CO3等)
碱(如Ca(OH)2等)
盐(如NaCl、CaCO3等)
(如空气、海水、澄清石灰水、石灰石等)
三、物质分类
链接主页四
四、有关化学式的计算
掌握
三种
基本
题型
1.求相对分子质量
2.求化合物中各元素的质量比
3.求化合物中某元素的质量分数
点击练习
1.用微粒的观点解释:
⑴2500L液化气能压缩在40L钢瓶中,说明
⑵丁香花开的季节可以闻到浓郁的香气,说明
⑶一滴水水中含有1.7×1021个水分子,说明
微粒间有空隙
微粒不断运动
微粒体积小
2.下列现象中不能用分子运动论解释的是( )
A.把两块表面平滑干净的铅压紧,就不容易将
它们拉开
B.在室内,同样表面积的热水比冷水蒸发得快
C.氧化汞受热分解生成汞和氧气
D.医院里充满了酒精味和药味
C
用微粒的观点解释
3.用原子和分子的观点解释:水通电生成氢气和氧气以及水蒸发形成水蒸气这两个变化的实质。
水是由水分子构成。水通电时,水分子分解成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子,许多氢分子构成氢气,许多氧分子构成氧气。
水蒸发时,水分子本身没有变,只是水分子间的空隙变大,所以水变成水蒸气。
4.把充满红棕色NO2气体和无色H2的集气瓶中间的玻璃片抽走,使两瓶口密合在一起(不要振荡),可观察到左边的两瓶气体的颜色很快趋于一致(两瓶气体不反应),右边两瓶气体需要很长时间才能达到同样的效果。
NO2
NO2
H2
H2
观察、对比实验现象,你能得出的结论有:
(1)
(2)
NO2的密度比H2大
分子在不断运动
(或分子间有空隙)
汞原子
二氧化碳分子
钠离子、氯离子
用化学符号表示:
2个氮原子 2个氮分子
2个铁离子 2个亚铁离子
2个铁原子 n个水分子
1个铵根离子 2个氢氧根离子
2N
2N2
2Fe 3+
2Fe 2+
2Fe
n H2O
NH4 +
2OH -
科学研究证实,物质是由微粒构成的,例如铁是由铁原子构成的。请你填写构成下列物质的具体微粒的名称。
⑴体温计中的汞是由 构成的;
⑵人工降雨用的干冰是由 构成的;
⑶食盐中的氯化钠是由 构成的。
物质由微粒构成
相对原子质量:
m m 12m 12n
n 12n n m
2.1991年,我国化学家张青莲教授与别人合作,重新测定了铟元素的相对原子质量。铟元素的核电荷数为49,相对原子质量为115,则铟原子核外电子数 ,核内质子数为 ,中子数为 。
1.若碳——12原子的质量为n g,A原子的质量为m g,则A原子的相对原子质量为( )
A. B. C. D.
以一种碳原子质量的1/12作为标准,其他原子的质量与
这一基准的比值,称为这种原子的相对原子质量。
相对原子质量只是个比值,不是原子的实际质量。
C
49
49
66
对于Fe、Fe2+、Fe3+三种微粒的判断,正确的是( )
①核电荷数相同
②核外电子数相等
③电子层结构完全相同
④质量几乎相等
⑤等质量的三种微粒所含的质子数相等
A.①④⑤ B.①③⑤
C.②③④ D.①②③④⑤
A
分子、原子、离子说法
1.下列关于分子、原子、离子说法不正确的是( ) A.分子是保持物质化学性质的一种微粒 B.原子是不能再分的最小微粒 C.分子、原子、离子都是构成物质的微粒 D.分子、原子、离子都是在不停运动
B
2.已知R2+核外电子数为N,仍不能确定的是原子的
A.质子数 B. 中子数 ( )
C.核电荷数 D. 电子层数
B
在空格中填写适当的元素符号。
地壳中含量最多的非金属元素是 ,其次是 ;地壳中含量最多的金属元素是 ,其次是 ;地球大气里含量最多的元素是 ;人体里含量最多的元素是 ;海洋里含量最多的元素是 ;太阳中含量最多的元素是 ;地核中含量最多的元素是 ;人体缺少 元素,容易得贫血症;小儿体内缺少 元素,容易得佝偻病;缺 会导致儿童发育迟缓,智力低下;人体缺 元素会引起龋齿,但它含量过高,又会使牙齿釉质受损。
O
Si
Al
Fe
N
O
O
Fe
Fe
Ca
Zn
F
H
元素分布
化合价:
根据化合价书写化合物的化学式:
1.通常正价元素写在前,负价元素写在后。
2.根据正负元素化合价代数和为零的原则确定
原子个数。
2.下列物质的名称与化学式相符的是( )
A.硫酸亚铁(FeSO4) B.氧化铁(FeO)
C.硫酸钠(NaSO4) D.氯化铜(CuCl)
1. 地壳中含量最多的金属元素与地壳中含量最多的非金属元素组成的化合物的化学式为 。
Al2O3
A
1.干燥多风的季节里,夜晚人们走在荒野中,有时会看到“鬼火”现象,其实它是一种类似于氨气组成的气体(PH3)在空气中自燃的现象。PH3中P的化合价是 ( )
A.+3 B.-3 C.+1 D.+5
2. 下列的物质按照一定的规律排列,则空格内的物质应是( )
Na2SO4 H2SO3 H2S
A.H2SO4 B .Na2S C.SO2 D.S
B
D
根据正负元素化合价代数和为零的原则确定化
学式中某元素的化合价。
+6 +4 -2
1.下列符号中,既能表示宏观含义,也能表示微观含义的是( )
A.2H2O B. 5O C. S D. Fe 2+
B
C
2.下列符号既能表示一种元素又能表示一个原子,还能表示一种单质的是 ( )
A.O2 B.Mg C.H D.N
3.保持氢气化学性质的最小微粒是( )
A.H2 B.H C.H+ D.H2O
A
4. 2003年,齐齐哈尔市发生了重大中毒事件,该事件的“肇事者”是侵华日军遗留下来的,被称为“毒气之王”的“芥子气”。芥子气,学名二氯二乙硫醚,化学式为(C2H4Cl)2S。下列有关二氯二乙硫醚的说法中错误的是( )
A.是有机物
B.由C、H、Cl、S四种元素组成
C.一个分子中含有15个原子
D.分子中C、H、Cl、S的原子个数比为2:4:2:1
D
5.我们日常生活中出现了加碘食盐、高钙牛奶、富硒大米等物质。这里的碘、钙、硒应理解为( )
A.单质 B.分子 C.元素 D.离子
6.一种元素与另一种元素的本质区别是( )
A.相对原子质量不同 B.质子数不同
C.中子数不同 D.电子数不同
7.关于水的描述,下列说法不正确的是( )
A.水是由氢元素和氧元素组成的
B.水分子是由氢原子和氧原子构成的
C.水是由许许多多的水分子构成的
D.水是由两个氢原子和一个氧原子构成的
C
B
D
物质分类
1.家庭日常生活中经常用到的下列物质中,属于纯净物的是( )
A.餐饮用的可口可乐 B.调味用的加碘食盐
C.炒菜用的铁锅 D.降温用的冰水共存物
2.有下列两组物质,每组中均有一种与其他物质所属类别不同,请在下面的横线上填写出这种物质的名称:
(1)食醋、牛奶、加碘盐、蔗糖
(2)氧化镁、水、碳酸钙、五氧化二磷
(1) (2)
D
蔗糖
碳酸钙
4.一瓶气体经化验只由一种元素组成,则该气体是( )
A.一种单质 B.一种化合物
C.一种纯净物
D.可能是一种单质,也可能是几种单质组成的
混合物
D
3.下列各组物质中,前者是单质,后者是氧化物的是( )
A.石灰石 冰 B.金刚石 干冰
C.液氧 高锰酸钾 D.水银 碘酒
B
1.求出下列各物质的相对分子质量:
Mr(CO2) =
Mr(2H2O)=
Mr[Ca(OH)2]=
Mr(CuSO4·5H2O)
=
12+16×2=44
64+32+16×4 + 5×(2+16)=250
40+2×(16+1)=74
2×(16+1×2)=36
2、求化合物中各元素的质量比
CO2中, C、O元素的质量比为
Ca(OH)2中,Ca、O、H元素的质量比
NH4NO3中,N、H、O元素的质量比
= 12 : 2×16 = 3 :8
=40 :16×2 :1×2 = 20 :6 :1
=14×2 : 1×4 : 16×3 =7 :1 :12
3、求化合物中某元素的质量分数
CO2中碳元素的质量分数
=
=
Ar(C) 12×1
Mr(CO2) 12+16×2
×100%
×100%
=35%
=
×100%
27.3%
NH4NO3中氮元素的质量分数
=
=
14×2
14×2+1×4+16×3
Ar(N)×2
Mr( NH4NO3 )
×100%
1.食物在煎炸的过程中会产生一种强致癌物质——丙烯醛,化学式为C2H3CHO,所以油炸食品不宜多吃。请回答:
(1)丙烯醛的相对分子质量是 。
(2)丙烯醛中C、H、O元素的质量比是 。
(3)丙烯醛中氧元素的质量分数为 (结果保留一位小数) 。
56
28.6%
9:1:4
2.市售的“脑黄金”(DHA)是从深海鱼油中提取的,主要成分为一种不饱和脂肪酸,其化学式为C25H50COOH,它是由 种元素组成的,每个分子中有 个原子。
3.下图是小明使用的修正液包装标签上的部分文字,这种修正液中甲基环已烷的相对分子质量是 ,假若其中甲基环已烷的质量分数是75%,则含甲基环已烷的质量为 g。
××修正液
主要成分:甲基环已烷(C6H11CH3)、钛白粉、
合成树脂
净含量:18g
通过ISO9001国际质量体系认证
3
79
98
13.5
点击综合练习
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
