化学人教版(2019)选择性必修3 3.1卤代烃(共35张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.1卤代烃(共35张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 107.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-14 00:00:00 | ||
图片预览









文档简介
第一节 卤代烃
学习目标
1. 认识溴乙烷的结构特点和主要化学性质。
2. 理解水解反应和消去反应的概念和原理。
3. 理解卤代烃的结构特点、物理性质、化学性质以及卤代烃在有机合成中的桥梁作用。
情景引入
液态的氯乙烷汽化时大量吸热(沸点12.27℃),具有冷冻麻醉作用,可在身体局部产生快速镇痛效果。因此常用氯乙烷与其他药物制成“复方氯乙烷喷雾剂”,用于运动中的急性损伤,如肌肉拉伤,关节扭伤等的阵痛。
情景引入
生活中的卤代烃
有些品牌的涂改液中的溶剂含有三氯乙烯
聚氯乙烯(PVC)
雨衣
七氟丙烷
灭火器
干洗剂
四氯乙烯
CCl2
CCl2
四氯乙烯干洗机
思考交流
1、通过观察得出卤代烃的结构特点
四氯乙烯
氯乙烷
氯乙烯
四氟乙烯
CH CH2
Cl
CF2
CF2
CH3CH2Cl
CCl2
CCl2
任务一:卤代烃
一、卤代烃的组成与结构
碳卤键
官能团:
X
C
1、定义
烃分子中的氢原子被卤素原子取代后所生成的化合物。
2、结构
3、烃的衍生物:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物
常见的烃的衍生物:卤代烃、醇、酚、醛、羧酸和酯
氟代烃
氯代烃
溴代烃
碘代烃
任务一:卤代烃
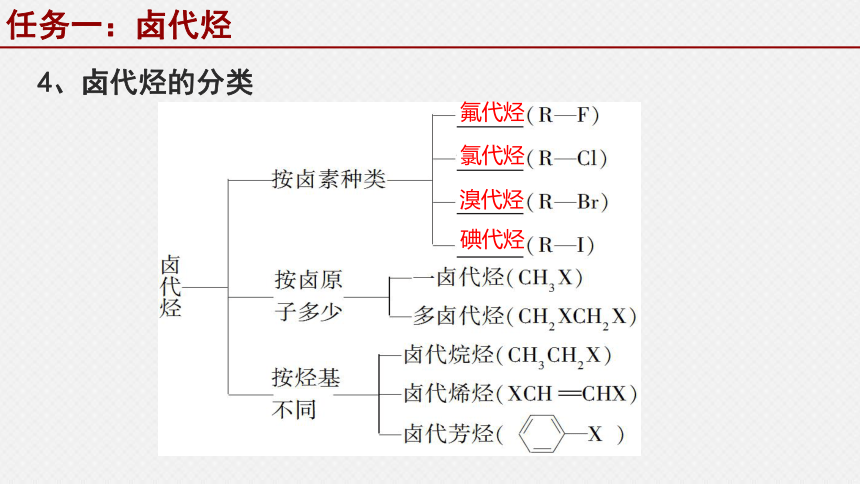
4、卤代烃的分类
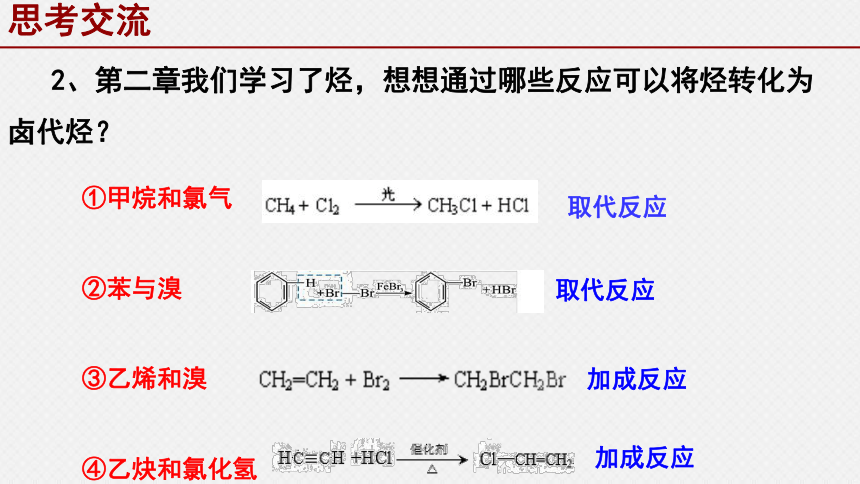
2、第二章我们学习了烃,想想通过哪些反应可以将烃转化为卤代烃?
①甲烷和氯气
②苯与溴
③乙烯和溴
④乙炔和氯化氢
取代反应
取代反应
加成反应
加成反应
思考交流
3、卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出卤代烃的命名原则。
选主链
定编号
写名称
选择含官能团的最长碳链
将卤素原子看做取代基,编号时从距简单取代基近的一端编号,
有碳碳双键时从距离碳碳双键近的一端开始编号
从简入繁
思考交流
几种氯代烃的密度和沸点
{16D9F66E-5EB9-4882-86FB-DCBF35E3C3E4}名称
结构简式
液态时密度/(g·cm-3)
沸点/℃
一氯甲烷
CH3Cl
0.916
-24
一氯乙烷
CH3CH2Cl
0.898
12
1-氯丙烷
CH3CH2CH2Cl
0.890
46
1-氯丁烷
CH3CH2CH2CH2Cl
0.886
78
1-氯戊烷
CH3CH2CH2CH2CH2Cl
0.882
108
思考交流
4、阅读教材,以氯代烃的密度和沸点为例,同时结合烷烃的物理性质的变化规律,总结卤代烃的物理性质。
(1)状态:常温下,卤代烃中除一氯甲烷、一溴甲烷、氯乙烯、氯乙烷为气体外,其余均为液体或固体。
(2)溶解性:卤代烃都不溶于水,可溶于有机溶剂,某些卤代烃本身就是很好的有机溶剂,如CCl4、氯仿(CHCl3)等。
(3)密度与沸点:
①卤代烃的密度和沸点都高于相应的烃;
二、卤代烃的物理性质
任务一:卤代烃
③沸点: 一般随碳原子数增多,沸点依次升高(碳原子数相同时,支链越多沸点越低)。如沸点CH3Cl<CH3CH2Cl。
②密度:除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。卤代烃的密度一般随烃基中碳原子数目的增加而减小,如ρ(CH3Cl)>ρ(CH3CH2Cl);
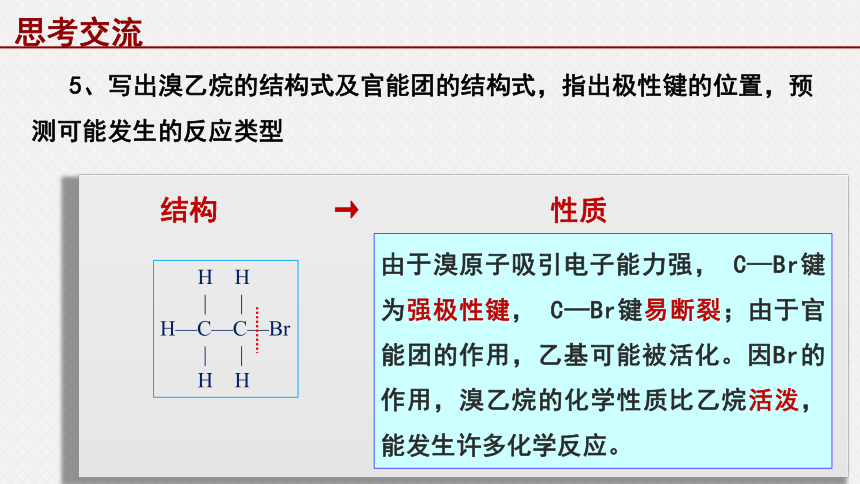
5、写出溴乙烷的结构式及官能团的结构式,指出极性键的位置,预测可能发生的反应类型
结构 → 性质
由于溴原子吸引电子能力强, C—Br键为强极性键, C—Br键易断裂;由于官能团的作用,乙基可能被活化。因Br的作用,溴乙烷的化学性质比乙烷活泼,能发生许多化学反应。
H H
| |
H—C—C—Br
| |
H H
思考交流
一、溴乙烷的结构与物理性质
1.溴乙烷的物理性质
2.溴乙烷的分子结构
有2种化学环境的H原子,则核磁共振有2组峰,强度比为3:2
核磁共振氢谱图
纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如乙醇、苯、汽油等)。
任务二、认识卤代烃的性质(以溴乙烷为例)
6、复习乙烷、乙醇的结构和性质,对比乙烷、乙烯、溴乙烷的结构,讨论他们结构上的差异,推测溴乙烷的性质。
{5940675A-B579-460E-94D1-54222C63F5DA}
乙烷
乙醇
溴乙烷
结构简式
C2H6
C2H5OH
C2H5Br
结构特点(官能团)
无
—OH
—Br
结构中相同部分
都有C2H5—
结构中相同点
都是饱和的
化学性质
取代
√
√
√
加成
×
×
×
消去
×
√
√
其他
被氧化,与Na反应
思考交流
取一支试管,滴入10~15滴溴乙烷;再加入1 mL 5% NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1 mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察实验现象。
实验探究
实验
现象
溴乙烷中加入NaOH溶液,振荡后加热,静置后,液体分层,取上层清液滴入过量稀硝酸中,再向其中滴加AgNO3溶液,试管中有浅黄色沉淀生成
有关的化学方程式
C2H5Br+NaOH C2H5OH+NaBr,
NaBr+AgNO3===AgBr↓+NaNO3
原理
在卤代烃分子中,卤素原子的电负性比碳原子大,使C—X的电子向卤素原子偏移,进而使碳原子带部分正电荷(δ+),卤素原子带部分负电荷(δ-),这样就形成一个极性较强的共价键:Cδ+—Xδ。因此,卤代烃在化学反应中,C—X较易断裂,使卤素原子被其他原子或原子团所取代,生成负离子而离去。
(1)为什么要加入稀硝酸酸化溶液?
中和过量的NaOH溶液,防止生成Ag2O棕褐色沉淀,影响Br-检验。
(2)如何判断CH3CH2Br是否完全水解?
看反应后的溶液是否出现分层,如分层,则没有完全水解。
(3)如何判断CH3CH2Br已发生水解?
R-X
? NaOH水溶液
△
?稀HNO3
? AgNO3溶液
淡黄色沉淀(AgBr)
取上层清液
黄色沉淀(AgI)
白色沉淀(AgCl)
思考交流
1、取代反应——又称水解反应
①条件:NaOH水溶液、加热。
②反应方程式:
由于卤素原子的引入使卤代烃的反应活性增强。
二、溴乙烷的化学性质
任务二、认识卤代烃的性质(以溴乙烷为例)
2、消去反应——又称为消除反应。
①条件:NaOH的乙醇溶液、加热
③反应方程式:(以溴乙烷为例)
②反应原理:
CH2=CH2 ↑ + NaBr+H2O
△
乙醇
CH2-CH2
Br
H
+ NaOH
④实质:相邻的两个C上脱去HX形成不饱和键!
二、溴乙烷的化学性质
消去反应(消除反应)
反应条件
强碱(如NaOH或KOH)的乙醇溶液、加热
断键方式
断裂C—Br和邻位碳原子上的C—H
化学方程式
C2H5Br+NaOH CH2=CH2↑+NaBr+H2O
①定义
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键的化合物的反应。
②溴乙烷的消去反应
a. 没有邻位碳原子的卤代烃不能发生消去反应,例如CH3Br。
d. 二卤代烃发生消去反应后可能在有机化合物中引入碳碳三键或两个碳碳双键。例如,
c. 有两个邻位碳原子,且碳原子上均有氢原子时,发生消去反应可能生成不同的产物。例如,
发生消去反应的产物为CH3—CH=CH—CH3、CH2 =CH—CH2—CH3。
b. 有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不能发生消去反应。例如
③卤代烃的消去反应规律
消去反应(消除反应)
思考交流
7、试判断下列物质能否发生消去反应或下列反应是否为消去反应。
CH3Cl
CH3CHCHBrCH3
CH3
H3C—C—CH2Cl
CH3
CH3
√
×
√
×
×
CH2—(CH2)4—CH2
—
—
H
Br
催化剂
CH ≡ CH↑+ 2HCl
醇、NaOH
CH2—CH2?
? ?????
Cl
Cl
|
|
归纳小结
比较溴乙烷的取代反应和消去反应,体会反应条件对化学反应的影响。
取代反应
消去反应
反应物
反应条件
生成物
断键位置
应用
结论
CH3CH2Br
CH3CH2Br
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2OH、NaBr
CH2=CH2、NaBr、H2O
溴乙烷在不同的条件下发生不同类型的反应
C—Br
C—Br、邻碳的C—H
引入羟基
引入不饱和键
无醇则有醇,有醇则无醇
3、加成和加聚反应
①氯乙烯加聚反应生成聚氯乙烯:
②四氟乙烯加聚反应生成聚四氟乙烯:
含有不饱和键(如 )的卤代烃也可以发生加成和加聚反应。
二、溴乙烷的化学性质
能力提升
实验探究1-溴丁烷的化学性质
【问题】卤代烷在不同溶剂中发生反应的情况不同。根据所学知识,设计实验验证取代反应与消去反应的产物?试剂,仪器自选。
【实验装置】
【讨论与实验】
(1)用哪种分析手段可以检验出1-溴丁烷取代反应生成物中的丁醇?
(2)如图所示,向圆底烧瓶中加入2.0gNaOH和15mL无水乙醇,搅拌。再向其中加入5mL1-溴丁烷和几片碎瓷片,微热。将产生的气体通入盛水的试管中,再用酸性高锰酸钾溶液进行检验。
8、为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试管?除了酸性高锰酸钾溶液,还可以用什么方法检验丁烯?此时还有必要将气体先通入水中吗?
9、预测2?-溴丁烷发生消去反应的可能产物有几种?写出结构简式。
除去挥发出的乙醇,消除乙醇对酸性KMnO4的影响。
用溴水,不用将气体通入水中
2种。CH3CH2CH==CH2,CH3CH==CHCH3
思考交流
三、卤代烃的用途与危害
用途: 制冷剂、灭火剂、溶剂、清洗剂
危害:氟氯烃——造成臭氧空洞的“罪魁祸首”
卤代烃破坏臭氧层原理(了解):氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为
知识拓展
二氟一氯一溴甲烷
三氟一溴甲烷
C
Cl
Br
F
F
C
F
Br
F
F
1211灭火器
1301灭火器
1.卤代烷灭火器
知识拓展
三、卤代烃的用途与危害
[CF2 CF2]
2.聚四氟乙烯(特氟龙)
n
四氟乙烯
特氟龙
不粘锅
n CF2 CF2
一定条件
知识拓展
三、卤代烃的用途与危害
用途: 制冷剂、灭火剂、溶剂、清洗剂
危害: 氟氯烃——造成臭氧空洞的“罪魁祸首”
臭氧层的保护
卤代烃破坏臭氧层原理:
氟氯烃可在强烈的紫外线作用下分解,产生的氯自由基会对平流层中的臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为:
CCl3F CCl2F·+Cl·
紫外线
课堂小结
1、下列关于卤代烃的叙述中正确的是 ( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低
D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
C
课堂检测
2、为了检验2?溴丁烷中含有溴元素,有以下操作,顺序合理的是( )
①加AgNO3溶液 ②加NaOH水溶液 ③加热 ④加蒸馏水
⑤加稀硝酸至溶液显酸性
A.②①③⑤ B.②④⑤③
C.②③⑤① D.②①⑤③
C
课堂检测
学习目标
1. 认识溴乙烷的结构特点和主要化学性质。
2. 理解水解反应和消去反应的概念和原理。
3. 理解卤代烃的结构特点、物理性质、化学性质以及卤代烃在有机合成中的桥梁作用。
情景引入
液态的氯乙烷汽化时大量吸热(沸点12.27℃),具有冷冻麻醉作用,可在身体局部产生快速镇痛效果。因此常用氯乙烷与其他药物制成“复方氯乙烷喷雾剂”,用于运动中的急性损伤,如肌肉拉伤,关节扭伤等的阵痛。
情景引入
生活中的卤代烃
有些品牌的涂改液中的溶剂含有三氯乙烯
聚氯乙烯(PVC)
雨衣
七氟丙烷
灭火器
干洗剂
四氯乙烯
CCl2
CCl2
四氯乙烯干洗机
思考交流
1、通过观察得出卤代烃的结构特点
四氯乙烯
氯乙烷
氯乙烯
四氟乙烯
CH CH2
Cl
CF2
CF2
CH3CH2Cl
CCl2
CCl2
任务一:卤代烃
一、卤代烃的组成与结构
碳卤键
官能团:
X
C
1、定义
烃分子中的氢原子被卤素原子取代后所生成的化合物。
2、结构
3、烃的衍生物:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物
常见的烃的衍生物:卤代烃、醇、酚、醛、羧酸和酯
氟代烃
氯代烃
溴代烃
碘代烃
任务一:卤代烃
4、卤代烃的分类
2、第二章我们学习了烃,想想通过哪些反应可以将烃转化为卤代烃?
①甲烷和氯气
②苯与溴
③乙烯和溴
④乙炔和氯化氢
取代反应
取代反应
加成反应
加成反应
思考交流
3、卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出卤代烃的命名原则。
选主链
定编号
写名称
选择含官能团的最长碳链
将卤素原子看做取代基,编号时从距简单取代基近的一端编号,
有碳碳双键时从距离碳碳双键近的一端开始编号
从简入繁
思考交流
几种氯代烃的密度和沸点
{16D9F66E-5EB9-4882-86FB-DCBF35E3C3E4}名称
结构简式
液态时密度/(g·cm-3)
沸点/℃
一氯甲烷
CH3Cl
0.916
-24
一氯乙烷
CH3CH2Cl
0.898
12
1-氯丙烷
CH3CH2CH2Cl
0.890
46
1-氯丁烷
CH3CH2CH2CH2Cl
0.886
78
1-氯戊烷
CH3CH2CH2CH2CH2Cl
0.882
108
思考交流
4、阅读教材,以氯代烃的密度和沸点为例,同时结合烷烃的物理性质的变化规律,总结卤代烃的物理性质。
(1)状态:常温下,卤代烃中除一氯甲烷、一溴甲烷、氯乙烯、氯乙烷为气体外,其余均为液体或固体。
(2)溶解性:卤代烃都不溶于水,可溶于有机溶剂,某些卤代烃本身就是很好的有机溶剂,如CCl4、氯仿(CHCl3)等。
(3)密度与沸点:
①卤代烃的密度和沸点都高于相应的烃;
二、卤代烃的物理性质
任务一:卤代烃
③沸点: 一般随碳原子数增多,沸点依次升高(碳原子数相同时,支链越多沸点越低)。如沸点CH3Cl<CH3CH2Cl。
②密度:除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。卤代烃的密度一般随烃基中碳原子数目的增加而减小,如ρ(CH3Cl)>ρ(CH3CH2Cl);
5、写出溴乙烷的结构式及官能团的结构式,指出极性键的位置,预测可能发生的反应类型
结构 → 性质
由于溴原子吸引电子能力强, C—Br键为强极性键, C—Br键易断裂;由于官能团的作用,乙基可能被活化。因Br的作用,溴乙烷的化学性质比乙烷活泼,能发生许多化学反应。
H H
| |
H—C—C—Br
| |
H H
思考交流
一、溴乙烷的结构与物理性质
1.溴乙烷的物理性质
2.溴乙烷的分子结构
有2种化学环境的H原子,则核磁共振有2组峰,强度比为3:2
核磁共振氢谱图
纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如乙醇、苯、汽油等)。
任务二、认识卤代烃的性质(以溴乙烷为例)
6、复习乙烷、乙醇的结构和性质,对比乙烷、乙烯、溴乙烷的结构,讨论他们结构上的差异,推测溴乙烷的性质。
{5940675A-B579-460E-94D1-54222C63F5DA}
乙烷
乙醇
溴乙烷
结构简式
C2H6
C2H5OH
C2H5Br
结构特点(官能团)
无
—OH
—Br
结构中相同部分
都有C2H5—
结构中相同点
都是饱和的
化学性质
取代
√
√
√
加成
×
×
×
消去
×
√
√
其他
被氧化,与Na反应
思考交流
取一支试管,滴入10~15滴溴乙烷;再加入1 mL 5% NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1 mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察实验现象。
实验探究
实验
现象
溴乙烷中加入NaOH溶液,振荡后加热,静置后,液体分层,取上层清液滴入过量稀硝酸中,再向其中滴加AgNO3溶液,试管中有浅黄色沉淀生成
有关的化学方程式
C2H5Br+NaOH C2H5OH+NaBr,
NaBr+AgNO3===AgBr↓+NaNO3
原理
在卤代烃分子中,卤素原子的电负性比碳原子大,使C—X的电子向卤素原子偏移,进而使碳原子带部分正电荷(δ+),卤素原子带部分负电荷(δ-),这样就形成一个极性较强的共价键:Cδ+—Xδ。因此,卤代烃在化学反应中,C—X较易断裂,使卤素原子被其他原子或原子团所取代,生成负离子而离去。
(1)为什么要加入稀硝酸酸化溶液?
中和过量的NaOH溶液,防止生成Ag2O棕褐色沉淀,影响Br-检验。
(2)如何判断CH3CH2Br是否完全水解?
看反应后的溶液是否出现分层,如分层,则没有完全水解。
(3)如何判断CH3CH2Br已发生水解?
R-X
? NaOH水溶液
△
?稀HNO3
? AgNO3溶液
淡黄色沉淀(AgBr)
取上层清液
黄色沉淀(AgI)
白色沉淀(AgCl)
思考交流
1、取代反应——又称水解反应
①条件:NaOH水溶液、加热。
②反应方程式:
由于卤素原子的引入使卤代烃的反应活性增强。
二、溴乙烷的化学性质
任务二、认识卤代烃的性质(以溴乙烷为例)
2、消去反应——又称为消除反应。
①条件:NaOH的乙醇溶液、加热
③反应方程式:(以溴乙烷为例)
②反应原理:
CH2=CH2 ↑ + NaBr+H2O
△
乙醇
CH2-CH2
Br
H
+ NaOH
④实质:相邻的两个C上脱去HX形成不饱和键!
二、溴乙烷的化学性质
消去反应(消除反应)
反应条件
强碱(如NaOH或KOH)的乙醇溶液、加热
断键方式
断裂C—Br和邻位碳原子上的C—H
化学方程式
C2H5Br+NaOH CH2=CH2↑+NaBr+H2O
①定义
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键的化合物的反应。
②溴乙烷的消去反应
a. 没有邻位碳原子的卤代烃不能发生消去反应,例如CH3Br。
d. 二卤代烃发生消去反应后可能在有机化合物中引入碳碳三键或两个碳碳双键。例如,
c. 有两个邻位碳原子,且碳原子上均有氢原子时,发生消去反应可能生成不同的产物。例如,
发生消去反应的产物为CH3—CH=CH—CH3、CH2 =CH—CH2—CH3。
b. 有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不能发生消去反应。例如
③卤代烃的消去反应规律
消去反应(消除反应)
思考交流
7、试判断下列物质能否发生消去反应或下列反应是否为消去反应。
CH3Cl
CH3CHCHBrCH3
CH3
H3C—C—CH2Cl
CH3
CH3
√
×
√
×
×
CH2—(CH2)4—CH2
—
—
H
Br
催化剂
CH ≡ CH↑+ 2HCl
醇、NaOH
CH2—CH2?
? ?????
Cl
Cl
|
|
归纳小结
比较溴乙烷的取代反应和消去反应,体会反应条件对化学反应的影响。
取代反应
消去反应
反应物
反应条件
生成物
断键位置
应用
结论
CH3CH2Br
CH3CH2Br
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2OH、NaBr
CH2=CH2、NaBr、H2O
溴乙烷在不同的条件下发生不同类型的反应
C—Br
C—Br、邻碳的C—H
引入羟基
引入不饱和键
无醇则有醇,有醇则无醇
3、加成和加聚反应
①氯乙烯加聚反应生成聚氯乙烯:
②四氟乙烯加聚反应生成聚四氟乙烯:
含有不饱和键(如 )的卤代烃也可以发生加成和加聚反应。
二、溴乙烷的化学性质
能力提升
实验探究1-溴丁烷的化学性质
【问题】卤代烷在不同溶剂中发生反应的情况不同。根据所学知识,设计实验验证取代反应与消去反应的产物?试剂,仪器自选。
【实验装置】
【讨论与实验】
(1)用哪种分析手段可以检验出1-溴丁烷取代反应生成物中的丁醇?
(2)如图所示,向圆底烧瓶中加入2.0gNaOH和15mL无水乙醇,搅拌。再向其中加入5mL1-溴丁烷和几片碎瓷片,微热。将产生的气体通入盛水的试管中,再用酸性高锰酸钾溶液进行检验。
8、为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试管?除了酸性高锰酸钾溶液,还可以用什么方法检验丁烯?此时还有必要将气体先通入水中吗?
9、预测2?-溴丁烷发生消去反应的可能产物有几种?写出结构简式。
除去挥发出的乙醇,消除乙醇对酸性KMnO4的影响。
用溴水,不用将气体通入水中
2种。CH3CH2CH==CH2,CH3CH==CHCH3
思考交流
三、卤代烃的用途与危害
用途: 制冷剂、灭火剂、溶剂、清洗剂
危害:氟氯烃——造成臭氧空洞的“罪魁祸首”
卤代烃破坏臭氧层原理(了解):氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为
知识拓展
二氟一氯一溴甲烷
三氟一溴甲烷
C
Cl
Br
F
F
C
F
Br
F
F
1211灭火器
1301灭火器
1.卤代烷灭火器
知识拓展
三、卤代烃的用途与危害
[CF2 CF2]
2.聚四氟乙烯(特氟龙)
n
四氟乙烯
特氟龙
不粘锅
n CF2 CF2
一定条件
知识拓展
三、卤代烃的用途与危害
用途: 制冷剂、灭火剂、溶剂、清洗剂
危害: 氟氯烃——造成臭氧空洞的“罪魁祸首”
臭氧层的保护
卤代烃破坏臭氧层原理:
氟氯烃可在强烈的紫外线作用下分解,产生的氯自由基会对平流层中的臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为:
CCl3F CCl2F·+Cl·
紫外线
课堂小结
1、下列关于卤代烃的叙述中正确的是 ( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低
D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
C
课堂检测
2、为了检验2?溴丁烷中含有溴元素,有以下操作,顺序合理的是( )
①加AgNO3溶液 ②加NaOH水溶液 ③加热 ④加蒸馏水
⑤加稀硝酸至溶液显酸性
A.②①③⑤ B.②④⑤③
C.②③⑤① D.②①⑤③
C
课堂检测
