化学人教版(2019)必修第二册7.3.1 乙醇(共24张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.1 乙醇(共24张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-14 13:52:01 | ||
图片预览




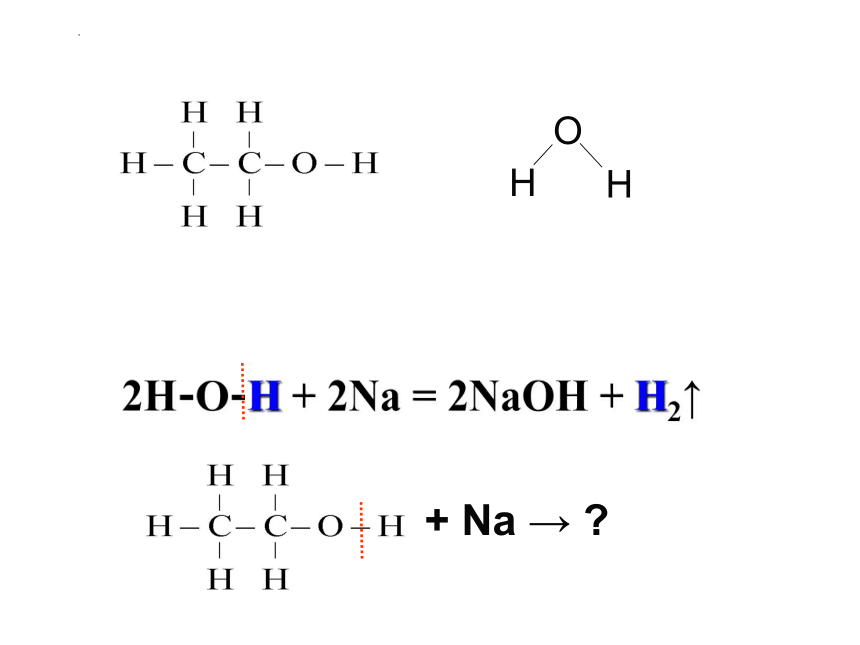
文档简介
(共24张PPT)
化学课堂
第三节 生活中两种常见的有机物
第1课时 乙醇
含酒精:3% - 5%
含酒精:6% - 20%
含酒精:38% - 65%
75%
95%
含酒精:8% - 15%
让我
看一看?
想一想?
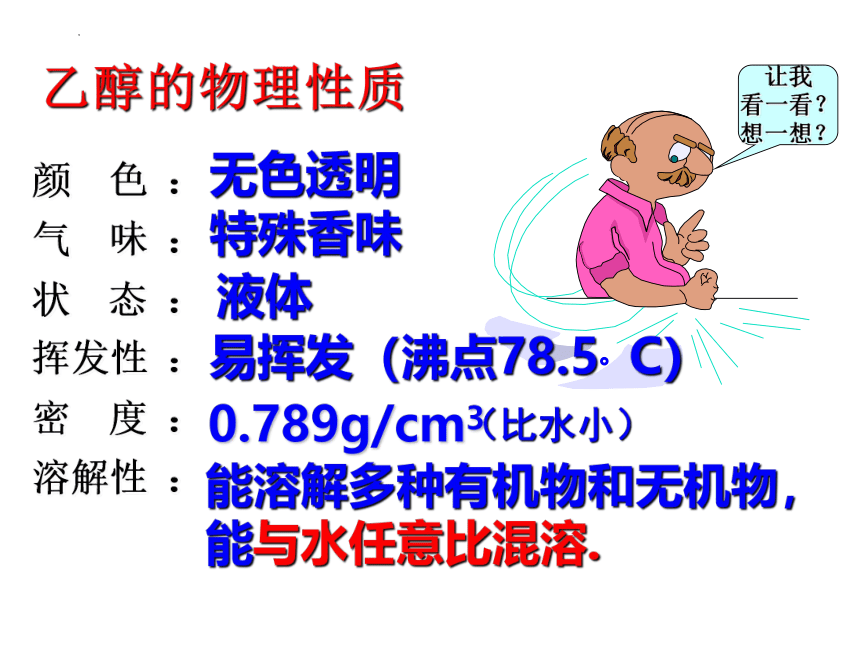
颜 色 :
气 味 :
状 态 :
挥发性 :
密 度 :
溶解性 :
无色透明
特殊香味
液体
易挥发(沸点78.5。C)
乙醇的物理性质
能溶解多种有机物和无机物,
能与水任意比混溶.
0.789g/cm3
(比水小)
1、如何分离水和酒精?
2、工业上如何制取无水的乙醇?
参考:由于水和酒精是互溶的,所以通常用蒸馏的方法分离水和酒精。
参考:先加生石灰,生石灰与水反应生成氢氧化钙,然后加热蒸馏分离乙醇。
思 考 题
3、怎样检验工业酒精中的少量水
答案:往工业酒精中加入无水硫酸铜,若变蓝色,证明有水。
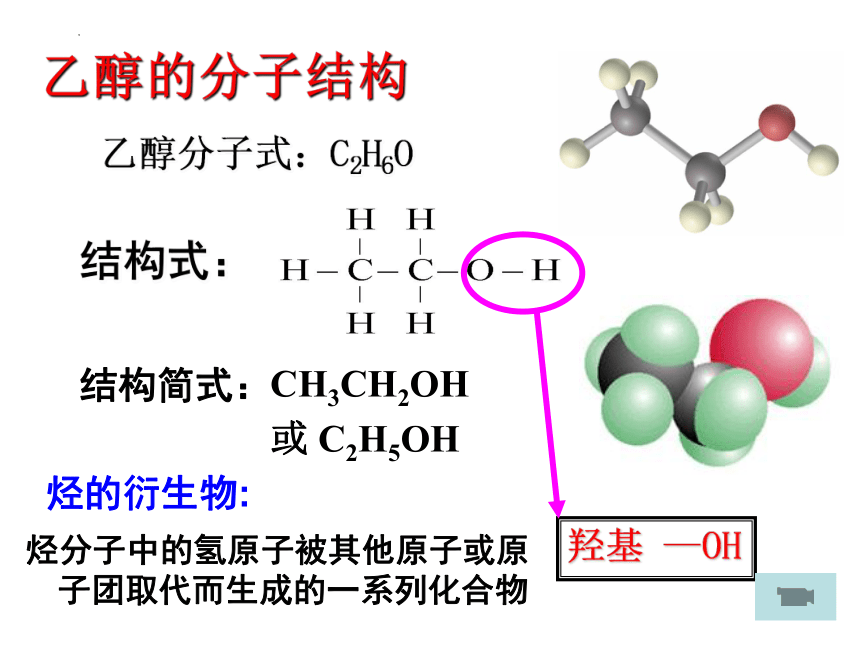
乙醇的分子结构
乙醇分子式:C2H6O
结构式:
CH3CH2OH
或 C2H5OH
结构简式:
羟基 —OH
烃的衍生物:
烃分子中的氢原子被其他原子或原子团取代而生成的一系列化合物
官能团:
决定有机化合物化学特性的原子或原子团。
常见的官能团:
卤原子(—X)、羟基(—OH)、硝基(—NO2)
醛基(—CHO)、羧基(—COOH)等;
烯烃中的碳碳双键也是官能团 。
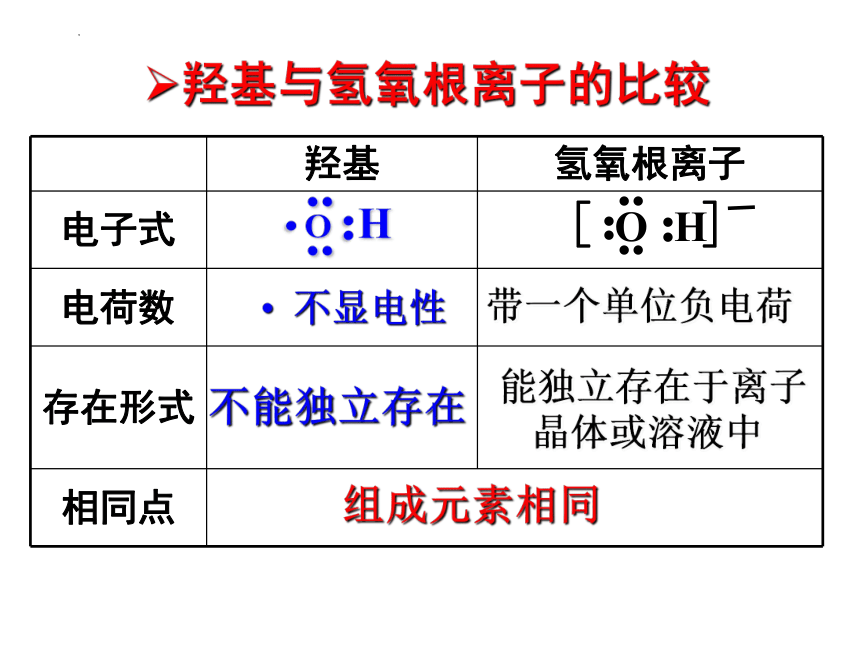
羟基 氢氧根离子
电子式
电荷数
存在形式
相同点
O
..
.
..
..
H
..
..
..
..
H
O
[ ]
不显电性
带一个单位负电荷
不能独立存在
能独立存在于离子晶体或溶液中
组成元素相同
羟基与氢氧根离子的比较
H
H
O
2H-O-H + 2Na = 2NaOH + H2↑
+ Na →
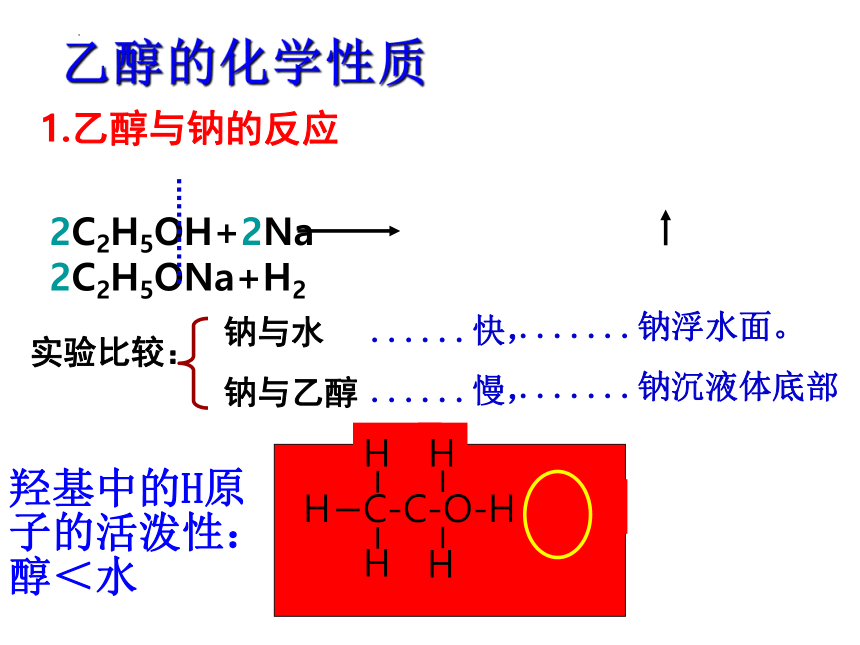
2C2H5OH+2Na 2C2H5ONa+H2
1.乙醇与钠的反应
实验比较:
钠与水
钠与乙醇
......快,
......慢,
.......钠浮水面。
.......钠沉液体底部
C-C-O-H
H
H
H
H
H
乙醇的化学性质
羟基中的H原子的活泼性:醇<水
2、乙醇的氧化反应
2CO2 +3H2O
C2H5OH + 3 O2
点燃
(1)燃烧
(2)催化氧化
思考:焊接银器、铜器时,表面会生成发黑的氧化膜,银匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!这是何原理?在实验室中模拟以上实验?
实验现象:红热的铜丝,移离火焰变黑,迅速伸入乙醇中,铜丝由黑变红,同时产生刺激性气味。
2Cu + O2 2CuO
△
Δ
C2H5OH+CuO +Cu
CH3CHO
+H2O
总反应方程式:
2CH3CH2OH + O2 2CH3CHO + 2H2O
Cu
乙醇的催化氧化
乙醛(-CHO 醛基 )
2CH3CH2OH + O2 2CH3—C—H+ 2H2O
Cu或Ag
O
-OH中的H和相邻碳上的H脱去,与O结合成水。脱去H的碳被氧化
断键方式
C—C—O—H
H
H
H
H
H
醇催化氧化的条件是:
羟基所连碳上必须有氢原子
乙醇被催化氧化的机理:
① ③断键
+ O2
2
生成醛
+ 2H2 O
—C=O
H
CH3
2
Cu
△
CH3—C—O—H
H
H
①
③
②
这个反应在人体内由酶催化完成,乙醛具有让毛细血管扩张的功能从而脸发红,还能引起神经中枢系统功能由兴奋到抑制,进而产生一系列的症状,对人体多个器官产生损害,尤其是肝脏和大脑。
思考:C(CH3)3OH 能否发生催化氧化?能就写出结果,不能请说明原因。
醇催化氧化的条件是:
羟基所连碳上必须有氢原子
不能,原因如下:
CH3CH2OH CH3COOH
酸性高锰酸钾溶液或
酸性重铬酸钾溶液
乙酸
紫色的酸性高锰酸钾溶液褪色,
酸性重铬酸钾溶液由橙色变为绿色,
判定司机饮酒超标。
2、乙醇的氧化反应
(3) 乙醇被强氧化剂氧化
乙醇
K2Cr2O7
Cr2(SO4)3
(橙色)
(绿色)
四、乙醇的用途
作燃料、有机溶剂、消毒剂(体积分数75%)制造饮料和香精 、乙酸、乙醚。
练习:
C—C—O—H
H
H
H
H
H
①
②
④
③
1、与钠反应时在何处断键。
A: ①
2、发生催化氧化反应时在何处断键。
A: ① ④
B: ②
B: ① ③
C: ③
C: ② ④
D: ④
D: ② ④
A
B
3.下列物质,都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )
①C2H5OH ②H2CO3溶液 ③H2O
A.①>②>③ B.②>①>③
C.③>①>② D.②>③>①
D
【课堂练习】
3. 可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A、1mol乙醇燃烧生成3mol 水
B、1mol乙醇可以生成1mol乙醛
C、1mol乙醇跟足量的钠作用放出0.5molH2
C
【应用1】
1、下列关于乙醇的叙述正确的是( )
A. 乙醇能萃取碘水中的碘
B. 乙醇能与钠反应生成H2,主要是因为乙
醇分子结构中含有官能团-OH
C. 乙醇与钠反应时断开-OH中的氢氧键
D.1mol乙醇与足量的钠反应可以得1mol H2
BC
【课堂练习】
1.比较乙烷和乙醇的分子结构,下列说法错误的是
A、两个碳原子以单键相连
B、分子里都含有6个相同的氢原子
C、乙基与一个氢原子相连就是乙烷分子
D、乙基与一个羟基相连就是乙醇分子
B
2.可用于检验乙醇中是否含有水的试剂是( )
A、无水硫酸铜 B、生石灰
C、金属钠 D、胆矾
A
典 例精 析
下列醇不能在铜的催化下发生氧化反应的是( )
D
4. 青岛国际啤酒节在青岛国际啤酒城盛装开幕。已知啤酒是酒精(乙醇)含量最低的酒精饮品。下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多的有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可勾兑各种浓度的酒
D.乙醇容易挥发且有香味,所以有“酒香不怕巷子深”的说法
A
化学课堂
第三节 生活中两种常见的有机物
第1课时 乙醇
含酒精:3% - 5%
含酒精:6% - 20%
含酒精:38% - 65%
75%
95%
含酒精:8% - 15%
让我
看一看?
想一想?
颜 色 :
气 味 :
状 态 :
挥发性 :
密 度 :
溶解性 :
无色透明
特殊香味
液体
易挥发(沸点78.5。C)
乙醇的物理性质
能溶解多种有机物和无机物,
能与水任意比混溶.
0.789g/cm3
(比水小)
1、如何分离水和酒精?
2、工业上如何制取无水的乙醇?
参考:由于水和酒精是互溶的,所以通常用蒸馏的方法分离水和酒精。
参考:先加生石灰,生石灰与水反应生成氢氧化钙,然后加热蒸馏分离乙醇。
思 考 题
3、怎样检验工业酒精中的少量水
答案:往工业酒精中加入无水硫酸铜,若变蓝色,证明有水。
乙醇的分子结构
乙醇分子式:C2H6O
结构式:
CH3CH2OH
或 C2H5OH
结构简式:
羟基 —OH
烃的衍生物:
烃分子中的氢原子被其他原子或原子团取代而生成的一系列化合物
官能团:
决定有机化合物化学特性的原子或原子团。
常见的官能团:
卤原子(—X)、羟基(—OH)、硝基(—NO2)
醛基(—CHO)、羧基(—COOH)等;
烯烃中的碳碳双键也是官能团 。
羟基 氢氧根离子
电子式
电荷数
存在形式
相同点
O
..
.
..
..
H
..
..
..
..
H
O
[ ]
不显电性
带一个单位负电荷
不能独立存在
能独立存在于离子晶体或溶液中
组成元素相同
羟基与氢氧根离子的比较
H
H
O
2H-O-H + 2Na = 2NaOH + H2↑
+ Na →
2C2H5OH+2Na 2C2H5ONa+H2
1.乙醇与钠的反应
实验比较:
钠与水
钠与乙醇
......快,
......慢,
.......钠浮水面。
.......钠沉液体底部
C-C-O-H
H
H
H
H
H
乙醇的化学性质
羟基中的H原子的活泼性:醇<水
2、乙醇的氧化反应
2CO2 +3H2O
C2H5OH + 3 O2
点燃
(1)燃烧
(2)催化氧化
思考:焊接银器、铜器时,表面会生成发黑的氧化膜,银匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初!这是何原理?在实验室中模拟以上实验?
实验现象:红热的铜丝,移离火焰变黑,迅速伸入乙醇中,铜丝由黑变红,同时产生刺激性气味。
2Cu + O2 2CuO
△
Δ
C2H5OH+CuO +Cu
CH3CHO
+H2O
总反应方程式:
2CH3CH2OH + O2 2CH3CHO + 2H2O
Cu
乙醇的催化氧化
乙醛(-CHO 醛基 )
2CH3CH2OH + O2 2CH3—C—H+ 2H2O
Cu或Ag
O
-OH中的H和相邻碳上的H脱去,与O结合成水。脱去H的碳被氧化
断键方式
C—C—O—H
H
H
H
H
H
醇催化氧化的条件是:
羟基所连碳上必须有氢原子
乙醇被催化氧化的机理:
① ③断键
+ O2
2
生成醛
+ 2H2 O
—C=O
H
CH3
2
Cu
△
CH3—C—O—H
H
H
①
③
②
这个反应在人体内由酶催化完成,乙醛具有让毛细血管扩张的功能从而脸发红,还能引起神经中枢系统功能由兴奋到抑制,进而产生一系列的症状,对人体多个器官产生损害,尤其是肝脏和大脑。
思考:C(CH3)3OH 能否发生催化氧化?能就写出结果,不能请说明原因。
醇催化氧化的条件是:
羟基所连碳上必须有氢原子
不能,原因如下:
CH3CH2OH CH3COOH
酸性高锰酸钾溶液或
酸性重铬酸钾溶液
乙酸
紫色的酸性高锰酸钾溶液褪色,
酸性重铬酸钾溶液由橙色变为绿色,
判定司机饮酒超标。
2、乙醇的氧化反应
(3) 乙醇被强氧化剂氧化
乙醇
K2Cr2O7
Cr2(SO4)3
(橙色)
(绿色)
四、乙醇的用途
作燃料、有机溶剂、消毒剂(体积分数75%)制造饮料和香精 、乙酸、乙醚。
练习:
C—C—O—H
H
H
H
H
H
①
②
④
③
1、与钠反应时在何处断键。
A: ①
2、发生催化氧化反应时在何处断键。
A: ① ④
B: ②
B: ① ③
C: ③
C: ② ④
D: ④
D: ② ④
A
B
3.下列物质,都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )
①C2H5OH ②H2CO3溶液 ③H2O
A.①>②>③ B.②>①>③
C.③>①>② D.②>③>①
D
【课堂练习】
3. 可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A、1mol乙醇燃烧生成3mol 水
B、1mol乙醇可以生成1mol乙醛
C、1mol乙醇跟足量的钠作用放出0.5molH2
C
【应用1】
1、下列关于乙醇的叙述正确的是( )
A. 乙醇能萃取碘水中的碘
B. 乙醇能与钠反应生成H2,主要是因为乙
醇分子结构中含有官能团-OH
C. 乙醇与钠反应时断开-OH中的氢氧键
D.1mol乙醇与足量的钠反应可以得1mol H2
BC
【课堂练习】
1.比较乙烷和乙醇的分子结构,下列说法错误的是
A、两个碳原子以单键相连
B、分子里都含有6个相同的氢原子
C、乙基与一个氢原子相连就是乙烷分子
D、乙基与一个羟基相连就是乙醇分子
B
2.可用于检验乙醇中是否含有水的试剂是( )
A、无水硫酸铜 B、生石灰
C、金属钠 D、胆矾
A
典 例精 析
下列醇不能在铜的催化下发生氧化反应的是( )
D
4. 青岛国际啤酒节在青岛国际啤酒城盛装开幕。已知啤酒是酒精(乙醇)含量最低的酒精饮品。下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多的有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可勾兑各种浓度的酒
D.乙醇容易挥发且有香味,所以有“酒香不怕巷子深”的说法
A
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
