2013年高考真题解析——江苏卷(化学)纯word版
文档属性
| 名称 | 2013年高考真题解析——江苏卷(化学)纯word版 |  | |
| 格式 | zip | ||
| 文件大小 | 808.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-07-18 13:38:58 | ||
图片预览



文档简介
2013·江苏卷
1. 燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇 B.天然气
C.液化石油气 D.氢气
1.D [解析] 甲醇、天然气、液化石油气燃烧后都能产生温室气体CO2,而H2燃烧生成的水对环境无污染,D项正确。
2. 下列有关化学用语表示正确的是( )
A.丙烯的结构简式:C3H6
B.氢氧根离子的电子式:[∶O?,? ∶H]-
C.氯原子的结构示意图:
D.中子数为146、质子数为92的铀(U)原子:U
2.B [解析] 烯烃的结构简式应写出碳碳双键,A项错误;氢氧根离子是带一个单位负电荷的阴离子,氢、氧原子共用一对电子对,最外层都达到稳定结构,B项正确;氯原子最外层有7个电子,C项错误; U原子的质量数为146+92=238,故原子符号为U,D项错误。
3. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使甲基橙变红色的溶液:Mg2+、K+、SO、NO
B.使酚酞变红色的溶液:Na+、Cu2+、HCO、NO
C.0.1 mol·L-1AgNO3溶液:H+、K+、SO、I-
D.0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO
3.A [解析] 使甲基橙变红色的溶液显酸性,该组四种离子能大量共存,A项正确;使酚酞变红的溶液显碱性,HCO、Cu2+与OH-反应,不能大量存在,B项错误; SO、I-与Ag+生成Ag2SO4、AgI沉淀而不能大量共存,C项错误; AlO与H+能生成沉淀而不能大量共存,D项错误。
4.
下列有关物质性质的应用正确的是( )
A.液氨汽化时要吸收大量的热,可用作制冷剂
B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
C.生石灰能与水反应,可用来干燥氯气
D.氯化铝是一种电解质,可用于电解法制铝
4.A [解析] NH3易液化,汽化时吸收大量的热,可作制冷剂,A项正确;二氧化硅能与氢氟酸反应生成SiF4和H2O,B项错误;生石灰吸水后生成Ca(OH)2,能吸收氯气,C项错误;氯化铝是共价化合物,工业上用电解熔融的Al2O3制铝,D项错误。
5. 用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )
图0
5.B [解析] 称量固体时,应遵循“左物右码”的原则,A项错误;用玻璃棒搅拌可以加快溶解速率,B项正确;向容量瓶中转移溶液时用玻璃棒引流,C项错误;定容时胶头滴管不能插入到容量瓶中,D项错误。
6.
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲乙丙。下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
6.C [解析] C在O2中不完全燃烧生成CO,CO继续与O2燃烧后生成CO2,CO2与C在高温条件下能生成CO,A项正确;根据反应SO2+NH3·H2O===NH4HSO3、NH4HSO3+NH3·H2O===(NH4)2SO3+H2O、(NH4)2SO3+SO2+H2O===2NH4HSO3,B项正确;铁与盐酸反应只能生成FeCl2,无法实现上述转化关系,C项错误;根据反应CO2+2NaOH===Na2CO3+H2O、Na2CO3+H2O+CO2===2NaHCO3、NaHCO3+NaOH===Na2CO3+H2O,D项正确。
7. 设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.78 g苯含有C=C双键的数目为3NA
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
7.C [解析] 在溶液中,ClO-水解,故ClO-数目小于NA,A项错误;苯分子中没有碳碳双键,B项错误; N2和CO的相对分子质量都是28,且每个分子中都含有两个原子,C项正确;NO2与水反应的方程式为3NO2+H2O===2HNO3+NO,故标准状况下6.72 L NO2与水反应时转移0.2NA电子,D项错误。
8. 下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HClMn2++2Cl-+Cl2↑+2H2O
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O===Al(OH)3↓+3H+
C.Na2O2溶于水产生O2:Na2O2+H2O===2Na++2OH-+O2↑
D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO+Ca2++OH-===CaCO3↓+H2O
8.D [解析] HCl是强电解质,在离子方程式中应写离子形式,A项错误;明矾溶于水产生的 Al(OH)3胶体不能写成沉淀,B项错误;Na2O2+H2O===2Na++2OH-+O2↑中氧原子数不守恒,得失电子数不守恒,C项错误; Ca(HCO3)2溶液中加入少量NaOH溶液后生成CaCO3的同时生成NaHCO3,D项正确。
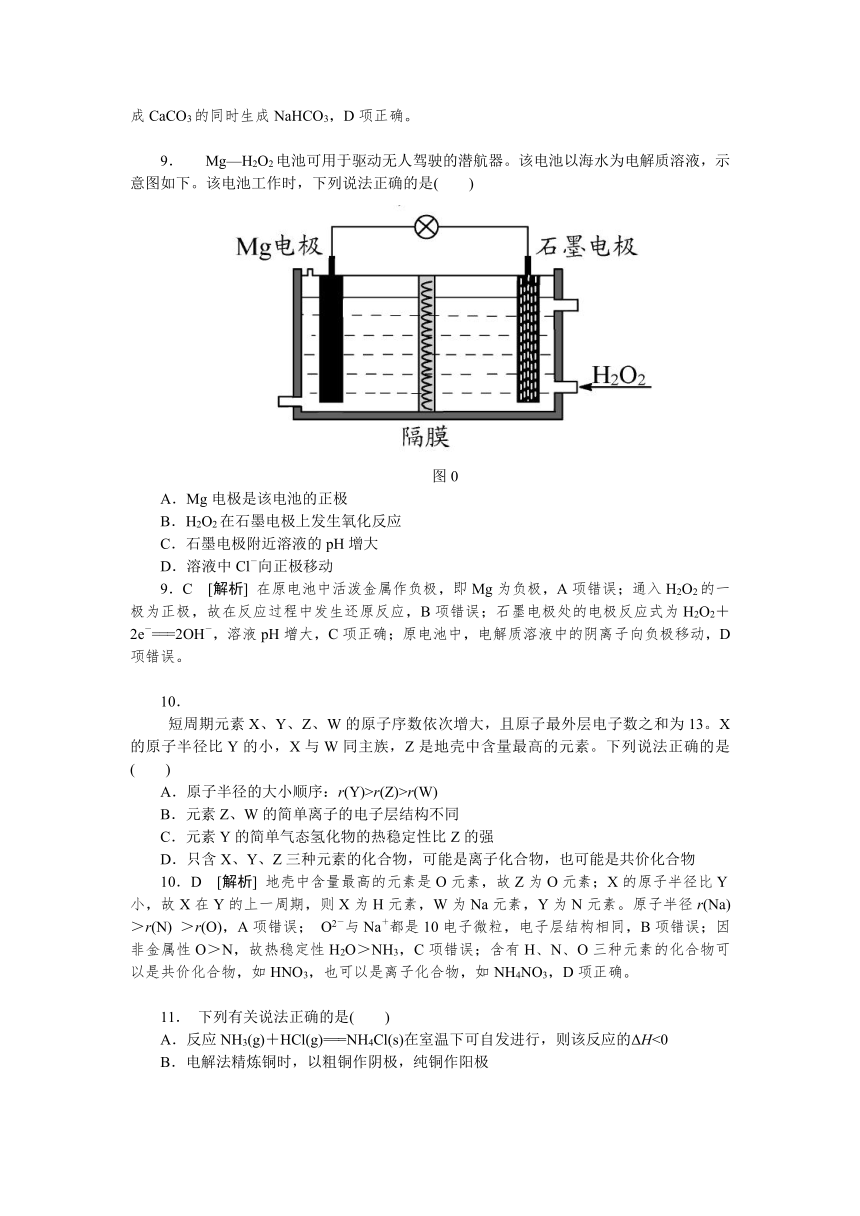
9. Mg—H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
图0
A.Mg电极是该电池的正极
B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH增大
D.溶液中Cl-向正极移动
9.C [解析] 在原电池中活泼金属作负极,即Mg为负极,A项错误;通入H2O2的一极为正极,故在反应过程中发生还原反应,B项错误;石墨电极处的电极反应式为H2O2+2e-===2OH-,溶液pH增大,C项正确;原电池中,电解质溶液中的阴离子向负极移动,D项错误。
10.
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
10.D [解析] 地壳中含量最高的元素是O元素,故Z为O元素;X的原子半径比Y小,故X在Y的上一周期,则X为H元素,W为Na元素,Y为N元素。原子半径r(Na)>r(N) >r(O),A项错误; O2-与Na+都是10电子微粒,电子层结构相同,B项错误;因非金属性O>N,故热稳定性H2O>NH3,C项错误;含有H、N、O三种元素的化合物可以是共价化合物,如HNO3,也可以是离子化合物,如NH4NO3,D项正确。
11. 下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)===NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH溶液加水稀释后,溶液中的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO水解程度减小,溶液的pH减小
11.AC [解析] 根据该反应中各物质的聚集状态可知,该反应的ΔS<0,因反应能自发进行,则该反应一定为放热反应,A项正确;在电解精炼铜中,粗铜作阳极,纯铜作阴极,B项错误;醋酸加水稀释过程中,c(H+)减小,但电离常数不变,故C项中式子的比值将减小,C项正确;向Na2CO3溶液中加入Ca(OH)2后生成CaCO3沉淀,溶液中c(CO)减小,c(OH-)增大,pH增大,D项错误。
12. 药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
下列有关叙述正确的是( )
A.贝诺酯分子中有三种含氧官能团
B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D.贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
12.B [解析] 贝诺酯中含有两种含氧官能团,酯基和肽键,A项错误;乙酰水杨酸中无酚羟基,而对乙酰氨基酚中含有酚羟基,故可以用FeCl3溶液区别两者,B项正确;对乙酰氨基酚中的酚羟基不能与NaHCO3反应,C项错误;乙酰水杨酸中酯基在NaOH中会水解,D项错误。
13. 下列依据相关实验得出的结论正确的是( )
A.向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液
B.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
C.将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯
D.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+
13.D [解析] 所述溶液中含有HCO也会有类似现象,A项错误;焰色反应是元素的性质,故原溶液也可能是NaOH溶液,B项错误; SO2、甲醛、乙烯、丙烯等气体都能使溴水褪色,C项错误;向某溶液中加入KSCN溶液不变色,证明溶液中无Fe3+,滴加氯水后显红色则证明溶液中有Fe2+被氧化成Fe3+,D项正确。
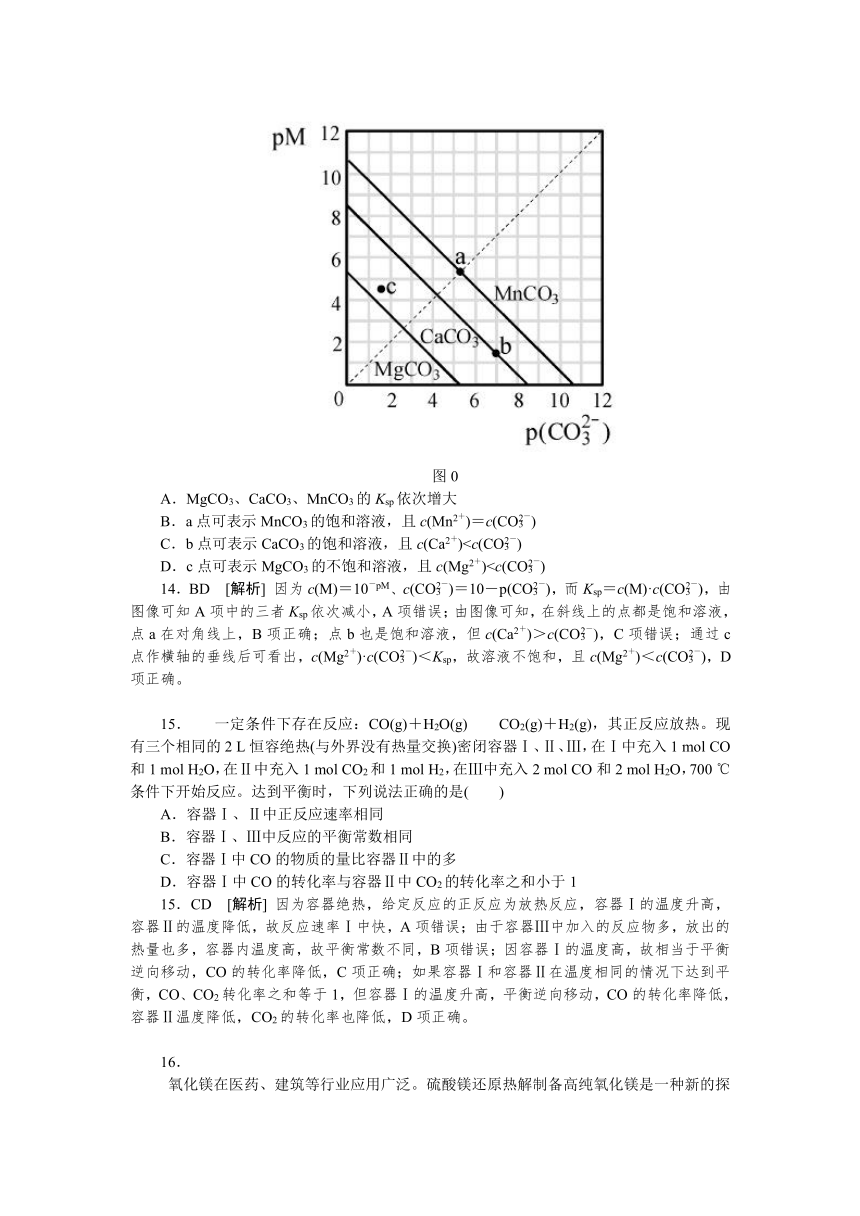
14. 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图0所示。已知:pM=-lgc(M),p(CO)=-lgc(CO)。下列说法正确的是( )
图0
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)14.BD [解析] 因为c(M)=10-pM、c(CO)=10-p(CO),而Ksp=c(M)·c(CO),由图像可知A项中的三者Ksp依次减小,A项错误;由图像可知,在斜线上的点都是饱和溶液,点a在对角线上,B项正确;点b也是饱和溶液,但c(Ca2+)>c(CO),C项错误;通过c点作横轴的垂线后可看出,c(Mg2+)·c(CO)<Ksp,故溶液不饱和,且c(Mg2+)<c(CO),D项正确。
15. 一定条件下存在反应:CO(g)+H2O(g)??CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中CO的物质的量比容器Ⅱ中的多
D.容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1
15.CD [解析] 因为容器绝热,给定反应的正反应为放热反应,容器Ⅰ的温度升高,容器Ⅱ的温度降低,故反应速率Ⅰ中快,A项错误;由于容器Ⅲ中加入的反应物多,放出的热量也多,容器内温度高,故平衡常数不同,B项错误;因容器Ⅰ的温度高,故相当于平衡逆向移动,CO的转化率降低,C项正确;如果容器Ⅰ和容器Ⅱ在温度相同的情况下达到平衡,CO、CO2转化率之和等于1,但容器Ⅰ的温度升高,平衡逆向移动,CO的转化率降低,容器Ⅱ温度降低,CO2的转化率也降低,D项正确。
16.
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
图0
(1)MgCO3与稀硫酸反应的离子方程式为______________________________________。
(2)加入H2O2氧化时,发生反应的化学方程式为____________________________。
(3)滤渣2的成分是________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C2MgO+2SO2↑+CO2↑;
MgSO4+CMgO+SO2↑+CO↑;
MgSO4+3CMgO+S↑+3CO↑。
利用如图0装置对煅烧产生的气体进行分步吸收或收集。
图0
①D中收集的气体是________(填化学式)。
②B中盛放的溶液可以是________(填字母)。
a.NaOH溶液 b.Na2CO3溶液
c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:________________________________________。
16.[答案] (1)MgCO3+2H+===Mg2++CO2↑+H2O
(2)2FeSO4+H2O2+H2SO4===Fe2(SO4)3+2H2O
(3)Fe(OH)3
(4)①CO
②d
③3S+6OH-2S2-+SO+3H2O
[解析] (1)MgCO3为难溶性物质,写离子方程式不能拆分成离子。(2)根据菱镁矿的成分,可知滤液中含有Fe2+,H2O2的作用是将Fe2+氧化成Fe3+。加入稀硫酸则溶液显酸性,所以离子方程式为2FeSO4+H2SO4+H2O2===Fe2(SO4)3+2H2O。(3)要提取镁元素,必须除去不溶性杂质和铁元素。根据流程图可知滤渣1是不溶性杂质,滤渣2中含的是铁元素。结合加入一水合氨和H2O2,可知滤渣2是Fe(OH)3。(4)根据反应原理,可知气体中含有SO2、CO2、CO和硫蒸气。①D采用排水集气法,气体必然不溶于水,所以是CO。②SO2和CO2均属于酸性氧化物,均能与NaOH、Na2CO3溶液反应,达不到分离的目的,a、b错误。SO2与稀HNO3反应同时得到NO,产生新杂质,干扰后续操作,c错误。SO2能被酸性KMnO4溶液氧化,而且没有新气体生成,d正确。③根据“淡黄色固体”,可知A中是硫单质。产物中有+4价硫,说明是Na2SO3,进而可知发生氧化还原反应,必然有部分硫化合价降低转化成Na2S。根据化合价升降总数相等,所以有3S+6OH-SO+2S2-+3H2O。
17. 化合物A(分子式为C6H6O)是一种有机化工原料,在空气中易被氧化。A的有关转化反应如下(部分反应条件略去):
图0
已知:
①R—BrR—MgBrCR′RR″OH
②CRROCRRCH2
(R表示烃基,R′和R″表示烃基或氢)
(1)写出A的结构简式:________。
(2)G是常用指示剂酚酞。写出G中含氧官能团的名称:________和________。
(3)某化合物是E的同分异构体,且分子中只有两种不同化学环境的氢。写出该化合物的结构简式:________(任写一种)。
(4)F和D互为同分异构体。写出反应E→F的化学方程式:________________________________________________________________________。
(5)根据已有知识并结合相关信息,写出以A和HCHO为原料制备的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C===CH2CH3CH2BrCH3CH2OH
17.[答案] (1)OH
(2)(酚)羟基 酯基
(3)CHH3CCH3COCHCH3CH3或
(4)CH3OHCH3+H2O
(5)OHOHBrMgBrCH2OHCHO
[解析] 根据反应条件和提示,可知A、B、C、D依次是OH、OH、O、CH2。(1)根据A的分子组成,可知A中含有苯环和—OH,所以A是苯酚。(2)从G的结构简式知,其中含有酚羟基和酯基。(3)只有两种不同的氢,说明分子高度对称,而且有一个双键或环。如果含有双键,根据对称性要求,应该是C=O键,左右各有3个饱和碳原子、两种氢原子,即为异丙基(CHCH3CH3),所以结构简式为CHH3CCH3COCHCH3CH3。如果含有环,O原子必然在环上,而且对称性要求支链必须是偶数,位于O的对位或两侧,所以只能是。(4)D中含有一个环和碳碳双键,D和F为同分异构体,故E中的羟基应在环上发生消去反应。条件为浓硫酸,加热。(5)本题采用逆推合成法,要制得目标产物,即可合成CH2OH,它可由MgBr与HCHO利用已知①的信息合成。而MgBr可由Br与Mg反应获得。对比Br与苯酚的结构,可知应先将苯环加成、再与HBr取代。
18.
硫酸镍铵[(NH4)xNiy(SO4)m·nH2O]可用于电镀、印刷等领域。某同学为测定硫酸镍铵的组成,进行如下实验:
①准确称取2.335 0 g样品,配制成100.00 mL溶液A;
②准确量取25.00 mL溶液A,用0.040 00 mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-===NiY2-+2H+),消耗EDTA标准溶液31.25 mL;
③另取25.00 mL溶液A,加足量的NaOH溶液并充分加热,生成NH3 56.00 mL(标准状况)。
(1)若滴定管在使用前未用EDTA标准溶液润洗,测得的Ni2+含量将________(填“偏高”“偏低”或“不变”)。
(2)氨气常用_____________________________检验,现象是______________________。
(3)通过计算确定硫酸镍铵的化学式(写出计算过程)。
18.[答案] (1)偏高
(2)湿润的红色石蕊试纸 试纸颜色由红变蓝
(3)n(Ni2+)=0.040 00 mol·L-1×31.25 mL×10-3 L·mL-1=1.250×10-3 mol
n(NH)==2.500×10-3 mol
n(SO)==
=
2.500×10-3 mol
m(Ni2+)=59 g·mol-1×1.250×10-3 mol=0.073 75 g
m(NH)=18 g·mol-1×2.500×10-3 mol=0.045 00 g
m(SO)=96 g·mol-1×2.500×10-3 mol=0.240 0 g
n(H2O)=
=1.250×10-2 mol
x∶y∶m∶n=n(NH)∶n(Ni2+)∶n(SO)∶n(H2O)=2∶1∶2∶10
硫酸镍铵的化学式为(NH4)2Ni(SO4)2·10H2O
[解析] (1)滴定管未润洗,则标准溶液EDTA的物质的量将增多,故测得的Ni2+含量偏高。(2)NH3为碱性气体,遇湿润的红色石蕊试纸变蓝。(3)根据滴定反应计算出Ni2+的量,根据生成NH3的量计算出NH的量。根据电荷守恒计算出SO的量,最后由质量守恒计算出H2O的量,由四者的物质的量比值,可确定出硫酸镍铵的化学式。
19.
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3===FeCO3↓+Na2SO4
FeCO3+C6H8O7===FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子
开始沉淀的pH
沉淀完全的pH
Fe3+
1.1
3.2
Al3+
3.0
5.0
Fe2+
5.8
8.8
(1)制备FeCO3时,选用的加料方式是________(填字母),原因是____________。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是________________________________________________________________________
________________________________________________________________________。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。
①铁粉的作用是________________。
②反应结束后,无需过滤,除去过量铁粉的方法是________________________________________________________________________
________________________________________________________________________。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是____________________________________。
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合图0的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应,____________,得到FeSO4溶液,__________,得到FeSO4·7H2O晶体。
图0
19.[答案] (1)c 避免生成Fe(OH)2沉淀
(2)取最后一次的洗涤滤液1~2 mL于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净
(3)①防止+2价的铁元素被氧化 ②加入适量柠檬酸让铁粉反应完全
(4)降低柠檬酸亚铁在水中的溶解量,有利于晶体析出
(5)过滤,向反应液中加入足量的铁粉,充分搅拌后,滴加NaOH溶液调节反应液的pH约为5,过滤(或过滤,向滤液中滴加过量的NaOH溶液,过滤,充分洗涤固体,向固体中加入足量稀硫酸至固体完全溶解,再加入足量的铁粉,充分搅拌后,过滤) (滴加稀硫酸酸化,)加热浓缩得到60 ℃饱和溶液,冷却至0 ℃结晶,过滤,少量冰水洗涤,低温干燥
[解析] (1)Na2CO3溶液显碱性,若将Fe2+加入时,会生成Fe(OH)2沉淀。所以应将Na2CO3溶液加入FeSO4溶液中。(2)由制备FeCO3的方程式知,沉淀表面会附有Na2SO4,故只要检验洗涤液中是否含有SO,即可证明沉淀是否洗净。(3)①Fe2+在溶解过程中,易被氧化成Fe3+,加入铁粉可以使Fe3+还原为Fe2+。②过量的铁粉用柠檬酸溶解,可得更多产物柠檬酸亚铁。(4)柠檬酸亚铁晶体在乙醇中的溶解量比在水中的小,故有利于其析出。(5)硫铁矿烧渣中加入稀硫酸,SiO2不溶,先过滤除去。含有的Fe2O3和Al2O3被溶解成Fe3+和Al3+,加入铁粉,可以将Fe3+还原为Fe2+,以增加FeSO4的产量。然后调节pH为5,除去Al3+,此时溶液仅为FeSO4。从溶解度曲线知,在60 ℃时FeSO4的溶解度最大,故将温度控制在60 ℃时,可获得含量最多的FeSO4,降低温度到0 ℃,可析出FeSO4·7H2O晶体。
20.
磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)===6CaO(s)+P4(s)+10CO(g) ΔH1=+3359.26 kJ·mol-1
CaO(s)+SiO2(s)===CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)===6CaSiO3(s)+P4(s)+10CO(g) ΔH3
则ΔH3=______________kJ·mol-1。
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:
11P4+60CuSO4+96H2O===20Cu3P+24H3PO4+60H2SO4
60 mol CuSO4能氧化白磷的物质的量是__________。
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如下图所示。
图0
①为获得尽可能纯的NaH2PO4,pH应控制在________;pH=8时,溶液中主要含磷物种浓度大小关系为____________。
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是________________________________________________________________________
________________________________________________________________________(用离子方程式表示)。
(4)磷的化合物三氯氧磷(PClOClCl)与季戊四醇(CHOH2CHOH2CCH2OHCH2OH)以物质的量之比2∶1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢谱如下图所示。
图0
①酸性气体是____________(填化学式)。
②X的结构简式为________________。
20.[答案] (1)2821.6
(2)3 mol
(3)①4~5.5(介于此区间内的任意值或区间均可)
c(HPO)>c(H2PO)
②3Ca2++2HPO===Ca3(PO4)2↓+2H+
(4)①HCl
②POClOOCH2CCH2CH2OPOClOCH2
[解析] (1)依据盖斯定律,将“上式+下式×6”,即得所求反应的ΔH=+3359.26 kJ·mol-1+(-89.61 kJ·mol-1)×6=2821.6 kJ·mol-1。(2)P的化合价有升有降,Cu的化合价只降低。P从0价升到+5价,1 mol P4共失去20 mol 电子,根据得失电子守恒有:n(P4)×20=n(CuSO4)×1,所以60 mol CuSO4可以氧化3 mol P4。(3)①从图中不难看出,pH在4~5.5之间时,H2PO的含量最高。在pH=8时,溶液中含有HPO和H2PO两种离子,且前者大于后者。②足量的Ca2+与HPO部分电离出的PO结合,生成难溶的Ca3(PO4)2沉淀,促进了HPO的电离,故溶液显酸性。(4)三氯氧磷与季戊四醇以2∶1反应,核磁共振氢谱中的峰由2组变成1组,显然应为四个羟基上的H原子被取代了,生成了HCl及POClOOCH2CCH2CH2OPOClOCH2。
21.
A.[物质结构与性质]元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如下图所示。
图0
①在1个晶胞中,X离子的数目为__________。
②该化合物的化学式为__________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是____________。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_______________________________________。
(4)Y与Z可形成YZ。
①YZ的空间构型为______________________________(用文字描述)。
②写出一种与YZ互为等电子体的分子的化学式:____________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
B.[实验化学]3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
HOOHOH+2CH3OHH3COOHOCH3+2H2O
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质
沸点/℃
熔点/℃
密度(20 ℃)/
g·cm-3
溶解性
甲醇
64.7
0.791 5
易溶于水
乙醚
34.5
0.713 8
微溶于水
3,5-二甲氧基
苯酚
33~36
易溶于甲醇、
乙醚,微溶于水
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是____________。②萃取用到的分液漏斗使用前需__________并洗净,分液时有机层在分液漏斗的__________(填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是________________;用饱和食盐水洗涤的目的是________________________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是__________(填字母)。
a.蒸馏除去乙醚 b.重结晶
c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先________________,再________________。
21.[答案] A.[物质结构与性质]
(1)①4 ②ZnS (2)sp3
(3)水分子与乙醇分子之间形成氢键
(4)①正四面体
②CCl4或SiCl4等
(5)16 mol或16×6.02×1023个
B.[实验化学]
(1)①蒸馏 ②检查是否漏水 上
(2)除去HCl 除去少量NaHCO3且减少产物损失
(3)dcab
(4)拆去连接抽气泵和吸滤瓶的橡皮管 关闭抽气泵
[解析] A.X为第四周期元素,且内层轨道电子数全满,最外层电子数为2,则其基态电子排布式应为[Ar]3d104s2,所以为Zn。Y的3p轨道上有4个电子,则应为S。Z的最外层电子数是内层的3倍,故为O。(1)从晶胞图分析,含有X离子为8×+6×=4。Y为4个,所以化合物中X与Y原子个数之比为1∶1,则化学式为ZnS。(2)H2S分子中,S有两对孤对电子,价层电子对数为2+2=4,所以S为sp3杂化。(3)H2O与乙醇分子间形成氢键,增大了H2O在乙醇中的溶解度。(4)SO中S无孤对电子,S的价层电子对数为4,则S为sp3杂化,所以SO为正四面体结构。等电子体的原子数相等,价电子数相等,SO的原子数为5,价电子数为32。(5)NH3分子中的σ键数为3,它与Zn形成的配位键也属于σ键,故1 mol[Zn(NH3)4]Cl2中的σ键为16 mol。
B.(1)甲醇和乙醚是互溶的有机物,但沸点相差较大,因此可用蒸馏法分离。分液漏斗使用前需要检查是否漏水,乙醚作萃取剂,其密度小于水,故有机层在上层。(2)反应在HCl的甲醇溶液中进行,所以有机层中会溶有HCl,故用NaHCO3溶液可除去。用饱和食盐水可以降低有机物的溶解度。(3)先加无水CaCl2,吸收水分,然后过滤除去CaCl2,再蒸馏除去乙醚杂质,最后重结晶获得产物。(4)为防倒吸,应将吸滤瓶与抽气泵先断开,再关闭抽气泵。
1. 燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇 B.天然气
C.液化石油气 D.氢气
1.D [解析] 甲醇、天然气、液化石油气燃烧后都能产生温室气体CO2,而H2燃烧生成的水对环境无污染,D项正确。
2. 下列有关化学用语表示正确的是( )
A.丙烯的结构简式:C3H6
B.氢氧根离子的电子式:[∶O?,? ∶H]-
C.氯原子的结构示意图:
D.中子数为146、质子数为92的铀(U)原子:U
2.B [解析] 烯烃的结构简式应写出碳碳双键,A项错误;氢氧根离子是带一个单位负电荷的阴离子,氢、氧原子共用一对电子对,最外层都达到稳定结构,B项正确;氯原子最外层有7个电子,C项错误; U原子的质量数为146+92=238,故原子符号为U,D项错误。
3. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使甲基橙变红色的溶液:Mg2+、K+、SO、NO
B.使酚酞变红色的溶液:Na+、Cu2+、HCO、NO
C.0.1 mol·L-1AgNO3溶液:H+、K+、SO、I-
D.0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO
3.A [解析] 使甲基橙变红色的溶液显酸性,该组四种离子能大量共存,A项正确;使酚酞变红的溶液显碱性,HCO、Cu2+与OH-反应,不能大量存在,B项错误; SO、I-与Ag+生成Ag2SO4、AgI沉淀而不能大量共存,C项错误; AlO与H+能生成沉淀而不能大量共存,D项错误。
4.
下列有关物质性质的应用正确的是( )
A.液氨汽化时要吸收大量的热,可用作制冷剂
B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
C.生石灰能与水反应,可用来干燥氯气
D.氯化铝是一种电解质,可用于电解法制铝
4.A [解析] NH3易液化,汽化时吸收大量的热,可作制冷剂,A项正确;二氧化硅能与氢氟酸反应生成SiF4和H2O,B项错误;生石灰吸水后生成Ca(OH)2,能吸收氯气,C项错误;氯化铝是共价化合物,工业上用电解熔融的Al2O3制铝,D项错误。
5. 用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )
图0
5.B [解析] 称量固体时,应遵循“左物右码”的原则,A项错误;用玻璃棒搅拌可以加快溶解速率,B项正确;向容量瓶中转移溶液时用玻璃棒引流,C项错误;定容时胶头滴管不能插入到容量瓶中,D项错误。
6.
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲乙丙。下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
6.C [解析] C在O2中不完全燃烧生成CO,CO继续与O2燃烧后生成CO2,CO2与C在高温条件下能生成CO,A项正确;根据反应SO2+NH3·H2O===NH4HSO3、NH4HSO3+NH3·H2O===(NH4)2SO3+H2O、(NH4)2SO3+SO2+H2O===2NH4HSO3,B项正确;铁与盐酸反应只能生成FeCl2,无法实现上述转化关系,C项错误;根据反应CO2+2NaOH===Na2CO3+H2O、Na2CO3+H2O+CO2===2NaHCO3、NaHCO3+NaOH===Na2CO3+H2O,D项正确。
7. 设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.78 g苯含有C=C双键的数目为3NA
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
7.C [解析] 在溶液中,ClO-水解,故ClO-数目小于NA,A项错误;苯分子中没有碳碳双键,B项错误; N2和CO的相对分子质量都是28,且每个分子中都含有两个原子,C项正确;NO2与水反应的方程式为3NO2+H2O===2HNO3+NO,故标准状况下6.72 L NO2与水反应时转移0.2NA电子,D项错误。
8. 下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HClMn2++2Cl-+Cl2↑+2H2O
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O===Al(OH)3↓+3H+
C.Na2O2溶于水产生O2:Na2O2+H2O===2Na++2OH-+O2↑
D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO+Ca2++OH-===CaCO3↓+H2O
8.D [解析] HCl是强电解质,在离子方程式中应写离子形式,A项错误;明矾溶于水产生的 Al(OH)3胶体不能写成沉淀,B项错误;Na2O2+H2O===2Na++2OH-+O2↑中氧原子数不守恒,得失电子数不守恒,C项错误; Ca(HCO3)2溶液中加入少量NaOH溶液后生成CaCO3的同时生成NaHCO3,D项正确。
9. Mg—H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
图0
A.Mg电极是该电池的正极
B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH增大
D.溶液中Cl-向正极移动
9.C [解析] 在原电池中活泼金属作负极,即Mg为负极,A项错误;通入H2O2的一极为正极,故在反应过程中发生还原反应,B项错误;石墨电极处的电极反应式为H2O2+2e-===2OH-,溶液pH增大,C项正确;原电池中,电解质溶液中的阴离子向负极移动,D项错误。
10.
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
10.D [解析] 地壳中含量最高的元素是O元素,故Z为O元素;X的原子半径比Y小,故X在Y的上一周期,则X为H元素,W为Na元素,Y为N元素。原子半径r(Na)>r(N) >r(O),A项错误; O2-与Na+都是10电子微粒,电子层结构相同,B项错误;因非金属性O>N,故热稳定性H2O>NH3,C项错误;含有H、N、O三种元素的化合物可以是共价化合物,如HNO3,也可以是离子化合物,如NH4NO3,D项正确。
11. 下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)===NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH溶液加水稀释后,溶液中的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO水解程度减小,溶液的pH减小
11.AC [解析] 根据该反应中各物质的聚集状态可知,该反应的ΔS<0,因反应能自发进行,则该反应一定为放热反应,A项正确;在电解精炼铜中,粗铜作阳极,纯铜作阴极,B项错误;醋酸加水稀释过程中,c(H+)减小,但电离常数不变,故C项中式子的比值将减小,C项正确;向Na2CO3溶液中加入Ca(OH)2后生成CaCO3沉淀,溶液中c(CO)减小,c(OH-)增大,pH增大,D项错误。
12. 药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
下列有关叙述正确的是( )
A.贝诺酯分子中有三种含氧官能团
B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D.贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
12.B [解析] 贝诺酯中含有两种含氧官能团,酯基和肽键,A项错误;乙酰水杨酸中无酚羟基,而对乙酰氨基酚中含有酚羟基,故可以用FeCl3溶液区别两者,B项正确;对乙酰氨基酚中的酚羟基不能与NaHCO3反应,C项错误;乙酰水杨酸中酯基在NaOH中会水解,D项错误。
13. 下列依据相关实验得出的结论正确的是( )
A.向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液
B.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
C.将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯
D.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+
13.D [解析] 所述溶液中含有HCO也会有类似现象,A项错误;焰色反应是元素的性质,故原溶液也可能是NaOH溶液,B项错误; SO2、甲醛、乙烯、丙烯等气体都能使溴水褪色,C项错误;向某溶液中加入KSCN溶液不变色,证明溶液中无Fe3+,滴加氯水后显红色则证明溶液中有Fe2+被氧化成Fe3+,D项正确。
14. 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图0所示。已知:pM=-lgc(M),p(CO)=-lgc(CO)。下列说法正确的是( )
图0
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)
15. 一定条件下存在反应:CO(g)+H2O(g)??CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中CO的物质的量比容器Ⅱ中的多
D.容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1
15.CD [解析] 因为容器绝热,给定反应的正反应为放热反应,容器Ⅰ的温度升高,容器Ⅱ的温度降低,故反应速率Ⅰ中快,A项错误;由于容器Ⅲ中加入的反应物多,放出的热量也多,容器内温度高,故平衡常数不同,B项错误;因容器Ⅰ的温度高,故相当于平衡逆向移动,CO的转化率降低,C项正确;如果容器Ⅰ和容器Ⅱ在温度相同的情况下达到平衡,CO、CO2转化率之和等于1,但容器Ⅰ的温度升高,平衡逆向移动,CO的转化率降低,容器Ⅱ温度降低,CO2的转化率也降低,D项正确。
16.
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
图0
(1)MgCO3与稀硫酸反应的离子方程式为______________________________________。
(2)加入H2O2氧化时,发生反应的化学方程式为____________________________。
(3)滤渣2的成分是________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C2MgO+2SO2↑+CO2↑;
MgSO4+CMgO+SO2↑+CO↑;
MgSO4+3CMgO+S↑+3CO↑。
利用如图0装置对煅烧产生的气体进行分步吸收或收集。
图0
①D中收集的气体是________(填化学式)。
②B中盛放的溶液可以是________(填字母)。
a.NaOH溶液 b.Na2CO3溶液
c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:________________________________________。
16.[答案] (1)MgCO3+2H+===Mg2++CO2↑+H2O
(2)2FeSO4+H2O2+H2SO4===Fe2(SO4)3+2H2O
(3)Fe(OH)3
(4)①CO
②d
③3S+6OH-2S2-+SO+3H2O
[解析] (1)MgCO3为难溶性物质,写离子方程式不能拆分成离子。(2)根据菱镁矿的成分,可知滤液中含有Fe2+,H2O2的作用是将Fe2+氧化成Fe3+。加入稀硫酸则溶液显酸性,所以离子方程式为2FeSO4+H2SO4+H2O2===Fe2(SO4)3+2H2O。(3)要提取镁元素,必须除去不溶性杂质和铁元素。根据流程图可知滤渣1是不溶性杂质,滤渣2中含的是铁元素。结合加入一水合氨和H2O2,可知滤渣2是Fe(OH)3。(4)根据反应原理,可知气体中含有SO2、CO2、CO和硫蒸气。①D采用排水集气法,气体必然不溶于水,所以是CO。②SO2和CO2均属于酸性氧化物,均能与NaOH、Na2CO3溶液反应,达不到分离的目的,a、b错误。SO2与稀HNO3反应同时得到NO,产生新杂质,干扰后续操作,c错误。SO2能被酸性KMnO4溶液氧化,而且没有新气体生成,d正确。③根据“淡黄色固体”,可知A中是硫单质。产物中有+4价硫,说明是Na2SO3,进而可知发生氧化还原反应,必然有部分硫化合价降低转化成Na2S。根据化合价升降总数相等,所以有3S+6OH-SO+2S2-+3H2O。
17. 化合物A(分子式为C6H6O)是一种有机化工原料,在空气中易被氧化。A的有关转化反应如下(部分反应条件略去):
图0
已知:
①R—BrR—MgBrCR′RR″OH
②CRROCRRCH2
(R表示烃基,R′和R″表示烃基或氢)
(1)写出A的结构简式:________。
(2)G是常用指示剂酚酞。写出G中含氧官能团的名称:________和________。
(3)某化合物是E的同分异构体,且分子中只有两种不同化学环境的氢。写出该化合物的结构简式:________(任写一种)。
(4)F和D互为同分异构体。写出反应E→F的化学方程式:________________________________________________________________________。
(5)根据已有知识并结合相关信息,写出以A和HCHO为原料制备的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C===CH2CH3CH2BrCH3CH2OH
17.[答案] (1)OH
(2)(酚)羟基 酯基
(3)CHH3CCH3COCHCH3CH3或
(4)CH3OHCH3+H2O
(5)OHOHBrMgBrCH2OHCHO
[解析] 根据反应条件和提示,可知A、B、C、D依次是OH、OH、O、CH2。(1)根据A的分子组成,可知A中含有苯环和—OH,所以A是苯酚。(2)从G的结构简式知,其中含有酚羟基和酯基。(3)只有两种不同的氢,说明分子高度对称,而且有一个双键或环。如果含有双键,根据对称性要求,应该是C=O键,左右各有3个饱和碳原子、两种氢原子,即为异丙基(CHCH3CH3),所以结构简式为CHH3CCH3COCHCH3CH3。如果含有环,O原子必然在环上,而且对称性要求支链必须是偶数,位于O的对位或两侧,所以只能是。(4)D中含有一个环和碳碳双键,D和F为同分异构体,故E中的羟基应在环上发生消去反应。条件为浓硫酸,加热。(5)本题采用逆推合成法,要制得目标产物,即可合成CH2OH,它可由MgBr与HCHO利用已知①的信息合成。而MgBr可由Br与Mg反应获得。对比Br与苯酚的结构,可知应先将苯环加成、再与HBr取代。
18.
硫酸镍铵[(NH4)xNiy(SO4)m·nH2O]可用于电镀、印刷等领域。某同学为测定硫酸镍铵的组成,进行如下实验:
①准确称取2.335 0 g样品,配制成100.00 mL溶液A;
②准确量取25.00 mL溶液A,用0.040 00 mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-===NiY2-+2H+),消耗EDTA标准溶液31.25 mL;
③另取25.00 mL溶液A,加足量的NaOH溶液并充分加热,生成NH3 56.00 mL(标准状况)。
(1)若滴定管在使用前未用EDTA标准溶液润洗,测得的Ni2+含量将________(填“偏高”“偏低”或“不变”)。
(2)氨气常用_____________________________检验,现象是______________________。
(3)通过计算确定硫酸镍铵的化学式(写出计算过程)。
18.[答案] (1)偏高
(2)湿润的红色石蕊试纸 试纸颜色由红变蓝
(3)n(Ni2+)=0.040 00 mol·L-1×31.25 mL×10-3 L·mL-1=1.250×10-3 mol
n(NH)==2.500×10-3 mol
n(SO)==
=
2.500×10-3 mol
m(Ni2+)=59 g·mol-1×1.250×10-3 mol=0.073 75 g
m(NH)=18 g·mol-1×2.500×10-3 mol=0.045 00 g
m(SO)=96 g·mol-1×2.500×10-3 mol=0.240 0 g
n(H2O)=
=1.250×10-2 mol
x∶y∶m∶n=n(NH)∶n(Ni2+)∶n(SO)∶n(H2O)=2∶1∶2∶10
硫酸镍铵的化学式为(NH4)2Ni(SO4)2·10H2O
[解析] (1)滴定管未润洗,则标准溶液EDTA的物质的量将增多,故测得的Ni2+含量偏高。(2)NH3为碱性气体,遇湿润的红色石蕊试纸变蓝。(3)根据滴定反应计算出Ni2+的量,根据生成NH3的量计算出NH的量。根据电荷守恒计算出SO的量,最后由质量守恒计算出H2O的量,由四者的物质的量比值,可确定出硫酸镍铵的化学式。
19.
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3===FeCO3↓+Na2SO4
FeCO3+C6H8O7===FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子
开始沉淀的pH
沉淀完全的pH
Fe3+
1.1
3.2
Al3+
3.0
5.0
Fe2+
5.8
8.8
(1)制备FeCO3时,选用的加料方式是________(填字母),原因是____________。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是________________________________________________________________________
________________________________________________________________________。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。
①铁粉的作用是________________。
②反应结束后,无需过滤,除去过量铁粉的方法是________________________________________________________________________
________________________________________________________________________。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是____________________________________。
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合图0的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应,____________,得到FeSO4溶液,__________,得到FeSO4·7H2O晶体。
图0
19.[答案] (1)c 避免生成Fe(OH)2沉淀
(2)取最后一次的洗涤滤液1~2 mL于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净
(3)①防止+2价的铁元素被氧化 ②加入适量柠檬酸让铁粉反应完全
(4)降低柠檬酸亚铁在水中的溶解量,有利于晶体析出
(5)过滤,向反应液中加入足量的铁粉,充分搅拌后,滴加NaOH溶液调节反应液的pH约为5,过滤(或过滤,向滤液中滴加过量的NaOH溶液,过滤,充分洗涤固体,向固体中加入足量稀硫酸至固体完全溶解,再加入足量的铁粉,充分搅拌后,过滤) (滴加稀硫酸酸化,)加热浓缩得到60 ℃饱和溶液,冷却至0 ℃结晶,过滤,少量冰水洗涤,低温干燥
[解析] (1)Na2CO3溶液显碱性,若将Fe2+加入时,会生成Fe(OH)2沉淀。所以应将Na2CO3溶液加入FeSO4溶液中。(2)由制备FeCO3的方程式知,沉淀表面会附有Na2SO4,故只要检验洗涤液中是否含有SO,即可证明沉淀是否洗净。(3)①Fe2+在溶解过程中,易被氧化成Fe3+,加入铁粉可以使Fe3+还原为Fe2+。②过量的铁粉用柠檬酸溶解,可得更多产物柠檬酸亚铁。(4)柠檬酸亚铁晶体在乙醇中的溶解量比在水中的小,故有利于其析出。(5)硫铁矿烧渣中加入稀硫酸,SiO2不溶,先过滤除去。含有的Fe2O3和Al2O3被溶解成Fe3+和Al3+,加入铁粉,可以将Fe3+还原为Fe2+,以增加FeSO4的产量。然后调节pH为5,除去Al3+,此时溶液仅为FeSO4。从溶解度曲线知,在60 ℃时FeSO4的溶解度最大,故将温度控制在60 ℃时,可获得含量最多的FeSO4,降低温度到0 ℃,可析出FeSO4·7H2O晶体。
20.
磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)===6CaO(s)+P4(s)+10CO(g) ΔH1=+3359.26 kJ·mol-1
CaO(s)+SiO2(s)===CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)===6CaSiO3(s)+P4(s)+10CO(g) ΔH3
则ΔH3=______________kJ·mol-1。
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:
11P4+60CuSO4+96H2O===20Cu3P+24H3PO4+60H2SO4
60 mol CuSO4能氧化白磷的物质的量是__________。
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如下图所示。
图0
①为获得尽可能纯的NaH2PO4,pH应控制在________;pH=8时,溶液中主要含磷物种浓度大小关系为____________。
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是________________________________________________________________________
________________________________________________________________________(用离子方程式表示)。
(4)磷的化合物三氯氧磷(PClOClCl)与季戊四醇(CHOH2CHOH2CCH2OHCH2OH)以物质的量之比2∶1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢谱如下图所示。
图0
①酸性气体是____________(填化学式)。
②X的结构简式为________________。
20.[答案] (1)2821.6
(2)3 mol
(3)①4~5.5(介于此区间内的任意值或区间均可)
c(HPO)>c(H2PO)
②3Ca2++2HPO===Ca3(PO4)2↓+2H+
(4)①HCl
②POClOOCH2CCH2CH2OPOClOCH2
[解析] (1)依据盖斯定律,将“上式+下式×6”,即得所求反应的ΔH=+3359.26 kJ·mol-1+(-89.61 kJ·mol-1)×6=2821.6 kJ·mol-1。(2)P的化合价有升有降,Cu的化合价只降低。P从0价升到+5价,1 mol P4共失去20 mol 电子,根据得失电子守恒有:n(P4)×20=n(CuSO4)×1,所以60 mol CuSO4可以氧化3 mol P4。(3)①从图中不难看出,pH在4~5.5之间时,H2PO的含量最高。在pH=8时,溶液中含有HPO和H2PO两种离子,且前者大于后者。②足量的Ca2+与HPO部分电离出的PO结合,生成难溶的Ca3(PO4)2沉淀,促进了HPO的电离,故溶液显酸性。(4)三氯氧磷与季戊四醇以2∶1反应,核磁共振氢谱中的峰由2组变成1组,显然应为四个羟基上的H原子被取代了,生成了HCl及POClOOCH2CCH2CH2OPOClOCH2。
21.
A.[物质结构与性质]元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如下图所示。
图0
①在1个晶胞中,X离子的数目为__________。
②该化合物的化学式为__________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是____________。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_______________________________________。
(4)Y与Z可形成YZ。
①YZ的空间构型为______________________________(用文字描述)。
②写出一种与YZ互为等电子体的分子的化学式:____________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
B.[实验化学]3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
HOOHOH+2CH3OHH3COOHOCH3+2H2O
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质
沸点/℃
熔点/℃
密度(20 ℃)/
g·cm-3
溶解性
甲醇
64.7
0.791 5
易溶于水
乙醚
34.5
0.713 8
微溶于水
3,5-二甲氧基
苯酚
33~36
易溶于甲醇、
乙醚,微溶于水
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是____________。②萃取用到的分液漏斗使用前需__________并洗净,分液时有机层在分液漏斗的__________(填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是________________;用饱和食盐水洗涤的目的是________________________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是__________(填字母)。
a.蒸馏除去乙醚 b.重结晶
c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先________________,再________________。
21.[答案] A.[物质结构与性质]
(1)①4 ②ZnS (2)sp3
(3)水分子与乙醇分子之间形成氢键
(4)①正四面体
②CCl4或SiCl4等
(5)16 mol或16×6.02×1023个
B.[实验化学]
(1)①蒸馏 ②检查是否漏水 上
(2)除去HCl 除去少量NaHCO3且减少产物损失
(3)dcab
(4)拆去连接抽气泵和吸滤瓶的橡皮管 关闭抽气泵
[解析] A.X为第四周期元素,且内层轨道电子数全满,最外层电子数为2,则其基态电子排布式应为[Ar]3d104s2,所以为Zn。Y的3p轨道上有4个电子,则应为S。Z的最外层电子数是内层的3倍,故为O。(1)从晶胞图分析,含有X离子为8×+6×=4。Y为4个,所以化合物中X与Y原子个数之比为1∶1,则化学式为ZnS。(2)H2S分子中,S有两对孤对电子,价层电子对数为2+2=4,所以S为sp3杂化。(3)H2O与乙醇分子间形成氢键,增大了H2O在乙醇中的溶解度。(4)SO中S无孤对电子,S的价层电子对数为4,则S为sp3杂化,所以SO为正四面体结构。等电子体的原子数相等,价电子数相等,SO的原子数为5,价电子数为32。(5)NH3分子中的σ键数为3,它与Zn形成的配位键也属于σ键,故1 mol[Zn(NH3)4]Cl2中的σ键为16 mol。
B.(1)甲醇和乙醚是互溶的有机物,但沸点相差较大,因此可用蒸馏法分离。分液漏斗使用前需要检查是否漏水,乙醚作萃取剂,其密度小于水,故有机层在上层。(2)反应在HCl的甲醇溶液中进行,所以有机层中会溶有HCl,故用NaHCO3溶液可除去。用饱和食盐水可以降低有机物的溶解度。(3)先加无水CaCl2,吸收水分,然后过滤除去CaCl2,再蒸馏除去乙醚杂质,最后重结晶获得产物。(4)为防倒吸,应将吸滤瓶与抽气泵先断开,再关闭抽气泵。
同课章节目录
