2022-2023学年高一上学期化学人教版(2019)必修第一册第三章 实验活动2:铁及其化合物的性质 课件(共19张PPT)
文档属性
| 名称 | 2022-2023学年高一上学期化学人教版(2019)必修第一册第三章 实验活动2:铁及其化合物的性质 课件(共19张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 282.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-16 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
实验活动2:铁及其化合物的性质
高一—人教版—化学—第三章
【实验目的】
1.认识铁及其化合物的重要化学性质。
2.学会铁离子的检验方法。
3.认识可通过氧化还原反应实现含有不同价态同种元素的物质间的相互转化。
铁及其化合物的性质
【实验内容】
1.铁及其化合物的性质
2.铁离子的检验
铁及其化合物的性质
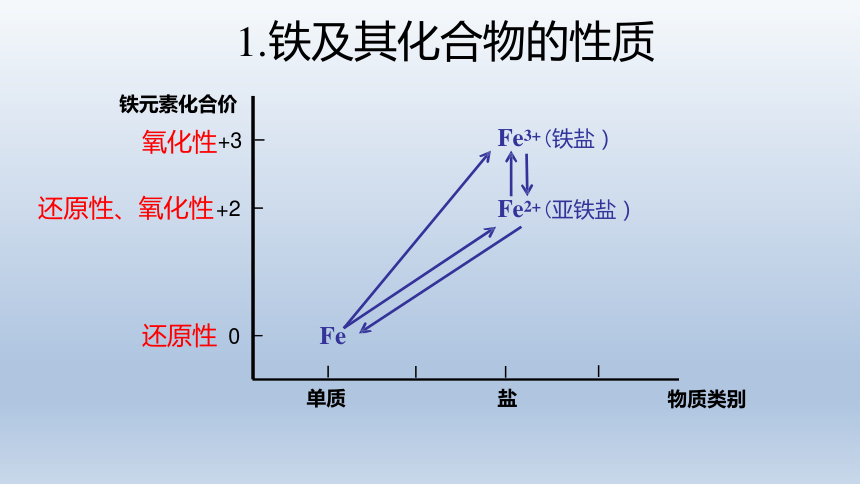
铁元素化合价
I
I
I
单质
盐
物质类别
Fe
I
Fe2+(亚铁盐)
Fe3+(铁盐)
还原性 0 -
氧化性+3 -
还原性、氧化性+2 -
1.铁及其化合物的性质
1.铁及其化合物的性质
(1)铁单质的还原性
实验用品:铁丝、CuSO4溶液、试管
实验步骤:在一支试管中加入2mLCuSO4溶液,再将一段铁丝放入
CuSO4溶液中,过一会儿,取出铁丝,观察现象。
1.铁及其化合物的性质
(1)铁单质的还原性
实验现象:铁丝上附有红色的铜,蓝色溶液变成浅绿色。
0
Fe + CuSO4
+2
FeSO4 + Cu
1.铁及其化合物的性质
(2)铁盐的氧化性
实验用品:铜片、FeCl3稀溶液、KI溶液、淀粉溶液、蒸馏水、试管、胶头滴管、镊子
实验步骤:
①取3mLFeCl3稀溶液加入试管中,加入几小块铜片,振荡,过一会儿,观察现象。
②在一支盛有3mL水的试管中滴加几滴FeCl3稀溶液,再滴加3滴KI溶
液,振荡,观察现象。然后向溶液中滴加少量淀粉溶液,观察现象。
(2)铁盐的氧化性
实验现象①:黄色溶液变蓝绿色,铜片质量减少。
实验现象②:溶液黄色加深,加入淀粉溶液后,溶液变蓝紫色。
1.铁及其化合物的性质
+3
2FeCl3 + Cu
+2
2FeCl2 + CuCl2
+3
2FeCl3 + 2KI
+2
2FeCl2 + 2KCl + I2
1.铁及其化合物的性质
(3)亚铁盐的氧化性和还原性
实验用品:锌片、KMnO4酸性溶液、FeSO4溶液、KSCN溶液、试管、胶头滴管、镊子
实验步骤:
①取3mL FeSO4溶液加入试管中,加入几小块锌片,振荡,过一会儿,观察现象。
②在一支试管中加入少量KMnO4酸性溶液,然后向试管中加入少量
FeSO4溶液,观察溶液的颜色变化。当溶液的紫色褪去时,再滴加2滴
KSCN溶液,观察现象。
1.铁及其化合物的性质
(3)亚铁盐的氧化性和还原性
实验现象①:锌片失去光泽变黑,溶液由浅绿色变无色。
实验现象②:溶液紫红色褪去变黄色,滴入KSCN后,溶液变血红色。
5Fe2+ + MnO4- + 8H+ 5Fe3+ + Mn2+ + 4H2O
+2
FeCl2 + Zn
0
Fe + ZnCl2
2.铁离子的检验
实验用品:铁粉、FeCl3稀溶液、KSCN溶液、蒸馏水、试管、胶头滴管
实验步骤:
(1)在一支试管中加入2mL蒸馏水,再滴加几滴FeCl3稀溶液,然后滴加几滴KSCN溶液,观察现象。
(2)在一支试管中加入少量FeCl3稀溶液,然后加入适量铁粉,轻轻振荡片刻,再滴加几滴KSCN溶液,观察现象。
2.铁离子的检验
实验现象(1):滴入KSCN溶液后,溶液变血红色。
Fe3+能与SCN-反应,Th成红色物质。
实验现象(2):黄色溶液褪至无色,滴入KSCN后,无明显变化。
2FeCl3 + Fe 3FeCl2
【结论】可用KSCN试剂检验Fe3+是否存在。
铁元素化合价
I
I
I
单质
盐
物质类别
【总结】
Fe
I
Fe2+(亚铁盐)
Fe3+(铁盐)
CuSO4
Fe、Cu、KI
Zn
KMnO4/H+
KSCN检验
还原性 0 -
氧化性+3 -
还原性、氧化性+2 -
血红色溶液
【问题和讨论1】
以铁屑为原料,如何制备硫酸亚铁晶体?
思考:铁屑的主要成分有什么?
Fe 和Fe2O3(少量)
【问题和讨论1】
Fe2O3
H2SO4
H SO
2 4
Fe3+
Fe、Cu、KI Fe2+
+3 -
+2 -
0 -
铁元素化合价
Fe
I
I
I
I
单质
盐
物质类别
【问题和讨论1】
铁屑
酸浸
稀硫酸
结晶
过滤
硫酸亚铁晶体
以铁屑为原料,如何制备硫酸亚铁晶体?
Fe + H2SO4
FeSO4 + H2↑
Fe2(SO4)3 + 3H2O
Fe2O3 + 3H2SO4 Fe + Fe2(SO4)3
3FeSO4
你能设计实验证明补血剂中含有亚铁离子吗
(已知:这种补血剂的主要成分为硫酸亚铁、叶酸等)
【问题和讨论2】
Fe2+(亚铁盐)
KSCN检验
Fe3+(铁盐)氯水或H2氧O化2溶剂液
+3 -
+2 -
0 -
铁元素化合价
Fe
I
I
I
I
单质
盐
物质类别
血红色溶液
设计实验证明补血剂中含有Fe2+离子。
补血剂药片
过滤
碾碎,用水溶解 滤液
(Fe2+)
KSCN溶液
【问题和讨论2】
血红色溶液
(Fe3+)
溶液 氯水或H2O2溶液不变
红色 氧化剂
实验活动2:铁及其化合物的性质
高一—人教版—化学—第三章
【实验目的】
1.认识铁及其化合物的重要化学性质。
2.学会铁离子的检验方法。
3.认识可通过氧化还原反应实现含有不同价态同种元素的物质间的相互转化。
铁及其化合物的性质
【实验内容】
1.铁及其化合物的性质
2.铁离子的检验
铁及其化合物的性质
铁元素化合价
I
I
I
单质
盐
物质类别
Fe
I
Fe2+(亚铁盐)
Fe3+(铁盐)
还原性 0 -
氧化性+3 -
还原性、氧化性+2 -
1.铁及其化合物的性质
1.铁及其化合物的性质
(1)铁单质的还原性
实验用品:铁丝、CuSO4溶液、试管
实验步骤:在一支试管中加入2mLCuSO4溶液,再将一段铁丝放入
CuSO4溶液中,过一会儿,取出铁丝,观察现象。
1.铁及其化合物的性质
(1)铁单质的还原性
实验现象:铁丝上附有红色的铜,蓝色溶液变成浅绿色。
0
Fe + CuSO4
+2
FeSO4 + Cu
1.铁及其化合物的性质
(2)铁盐的氧化性
实验用品:铜片、FeCl3稀溶液、KI溶液、淀粉溶液、蒸馏水、试管、胶头滴管、镊子
实验步骤:
①取3mLFeCl3稀溶液加入试管中,加入几小块铜片,振荡,过一会儿,观察现象。
②在一支盛有3mL水的试管中滴加几滴FeCl3稀溶液,再滴加3滴KI溶
液,振荡,观察现象。然后向溶液中滴加少量淀粉溶液,观察现象。
(2)铁盐的氧化性
实验现象①:黄色溶液变蓝绿色,铜片质量减少。
实验现象②:溶液黄色加深,加入淀粉溶液后,溶液变蓝紫色。
1.铁及其化合物的性质
+3
2FeCl3 + Cu
+2
2FeCl2 + CuCl2
+3
2FeCl3 + 2KI
+2
2FeCl2 + 2KCl + I2
1.铁及其化合物的性质
(3)亚铁盐的氧化性和还原性
实验用品:锌片、KMnO4酸性溶液、FeSO4溶液、KSCN溶液、试管、胶头滴管、镊子
实验步骤:
①取3mL FeSO4溶液加入试管中,加入几小块锌片,振荡,过一会儿,观察现象。
②在一支试管中加入少量KMnO4酸性溶液,然后向试管中加入少量
FeSO4溶液,观察溶液的颜色变化。当溶液的紫色褪去时,再滴加2滴
KSCN溶液,观察现象。
1.铁及其化合物的性质
(3)亚铁盐的氧化性和还原性
实验现象①:锌片失去光泽变黑,溶液由浅绿色变无色。
实验现象②:溶液紫红色褪去变黄色,滴入KSCN后,溶液变血红色。
5Fe2+ + MnO4- + 8H+ 5Fe3+ + Mn2+ + 4H2O
+2
FeCl2 + Zn
0
Fe + ZnCl2
2.铁离子的检验
实验用品:铁粉、FeCl3稀溶液、KSCN溶液、蒸馏水、试管、胶头滴管
实验步骤:
(1)在一支试管中加入2mL蒸馏水,再滴加几滴FeCl3稀溶液,然后滴加几滴KSCN溶液,观察现象。
(2)在一支试管中加入少量FeCl3稀溶液,然后加入适量铁粉,轻轻振荡片刻,再滴加几滴KSCN溶液,观察现象。
2.铁离子的检验
实验现象(1):滴入KSCN溶液后,溶液变血红色。
Fe3+能与SCN-反应,Th成红色物质。
实验现象(2):黄色溶液褪至无色,滴入KSCN后,无明显变化。
2FeCl3 + Fe 3FeCl2
【结论】可用KSCN试剂检验Fe3+是否存在。
铁元素化合价
I
I
I
单质
盐
物质类别
【总结】
Fe
I
Fe2+(亚铁盐)
Fe3+(铁盐)
CuSO4
Fe、Cu、KI
Zn
KMnO4/H+
KSCN检验
还原性 0 -
氧化性+3 -
还原性、氧化性+2 -
血红色溶液
【问题和讨论1】
以铁屑为原料,如何制备硫酸亚铁晶体?
思考:铁屑的主要成分有什么?
Fe 和Fe2O3(少量)
【问题和讨论1】
Fe2O3
H2SO4
H SO
2 4
Fe3+
Fe、Cu、KI Fe2+
+3 -
+2 -
0 -
铁元素化合价
Fe
I
I
I
I
单质
盐
物质类别
【问题和讨论1】
铁屑
酸浸
稀硫酸
结晶
过滤
硫酸亚铁晶体
以铁屑为原料,如何制备硫酸亚铁晶体?
Fe + H2SO4
FeSO4 + H2↑
Fe2(SO4)3 + 3H2O
Fe2O3 + 3H2SO4 Fe + Fe2(SO4)3
3FeSO4
你能设计实验证明补血剂中含有亚铁离子吗
(已知:这种补血剂的主要成分为硫酸亚铁、叶酸等)
【问题和讨论2】
Fe2+(亚铁盐)
KSCN检验
Fe3+(铁盐)氯水或H2氧O化2溶剂液
+3 -
+2 -
0 -
铁元素化合价
Fe
I
I
I
I
单质
盐
物质类别
血红色溶液
设计实验证明补血剂中含有Fe2+离子。
补血剂药片
过滤
碾碎,用水溶解 滤液
(Fe2+)
KSCN溶液
【问题和讨论2】
血红色溶液
(Fe3+)
溶液 氯水或H2O2溶液不变
红色 氧化剂
