2022秋沪教版(全国)九年级上册第4章:认识化学变化习题选(word版有答案)
文档属性
| 名称 | 2022秋沪教版(全国)九年级上册第4章:认识化学变化习题选(word版有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 338.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-16 00:00:00 | ||
图片预览



文档简介
2022秋沪教版(全国)九年级上册第4章:认识化学变化习题选含答案
沪教版(全国)九上第4章 认识化学变化
一、选择题。
1、关于如图所示探究燃烧条件的实验中,说法不正确的是( )
A.气球的作用是收集磷燃烧产生的白烟,防止污染空气。
B.观察到的现象:试管和烧杯中的白磷能燃烧,红磷不能燃烧。
C.热水的作用是:升高温度,隔绝空气
D.由此实验得出燃烧的条件是:可燃物与氧气(或空气)接触,温度达到着火点
2、下列化学反应中,元素的化合价没有发生变化的是( )
①CO2+H2O═H2CO3 ②NH4HCO3===H2O+CO2↑+NH3↑
③2H2S+O2===2S+2H2O ④2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
A.①②③ B.①②④ C.②③④ D.①③④
3、化学反应前后,下列各项中,肯定没有变化的是( )
①原子数目 ②原子的种类 ③分子数目 ④分子的种类
⑤元素的种类 ⑥物质的总质量 ⑦物质的种类
A.①②⑤⑥ B.①②③⑤ C.①②⑤⑦ D.③④⑥⑦
4、控制变量法是实验探究的重要方法.下列设计方案不能实现探究目的是( )
A. 甲实验可探究可燃物的燃烧需要与氧气接触且温度达到着火点
B. 甲实验中a、b对比可探究可燃物的燃烧是否需要达到一定温度
C. 乙中①②对比可探究铁的锈蚀条件是否与氧气有关
D. 乙中①②③对比可探究铁的锈蚀条件是否与氧气和水等物质有关
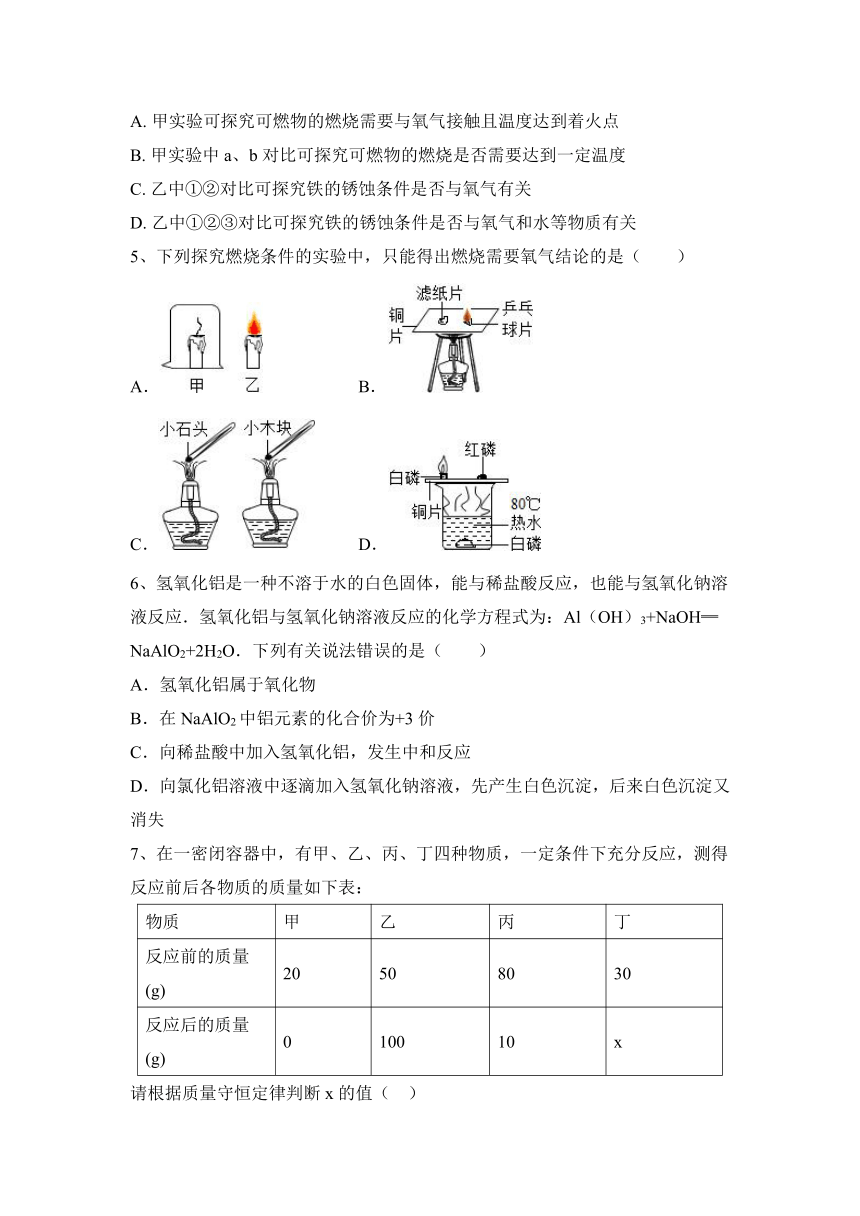
5、下列探究燃烧条件的实验中,只能得出燃烧需要氧气结论的是( )
A. B.
C. D.
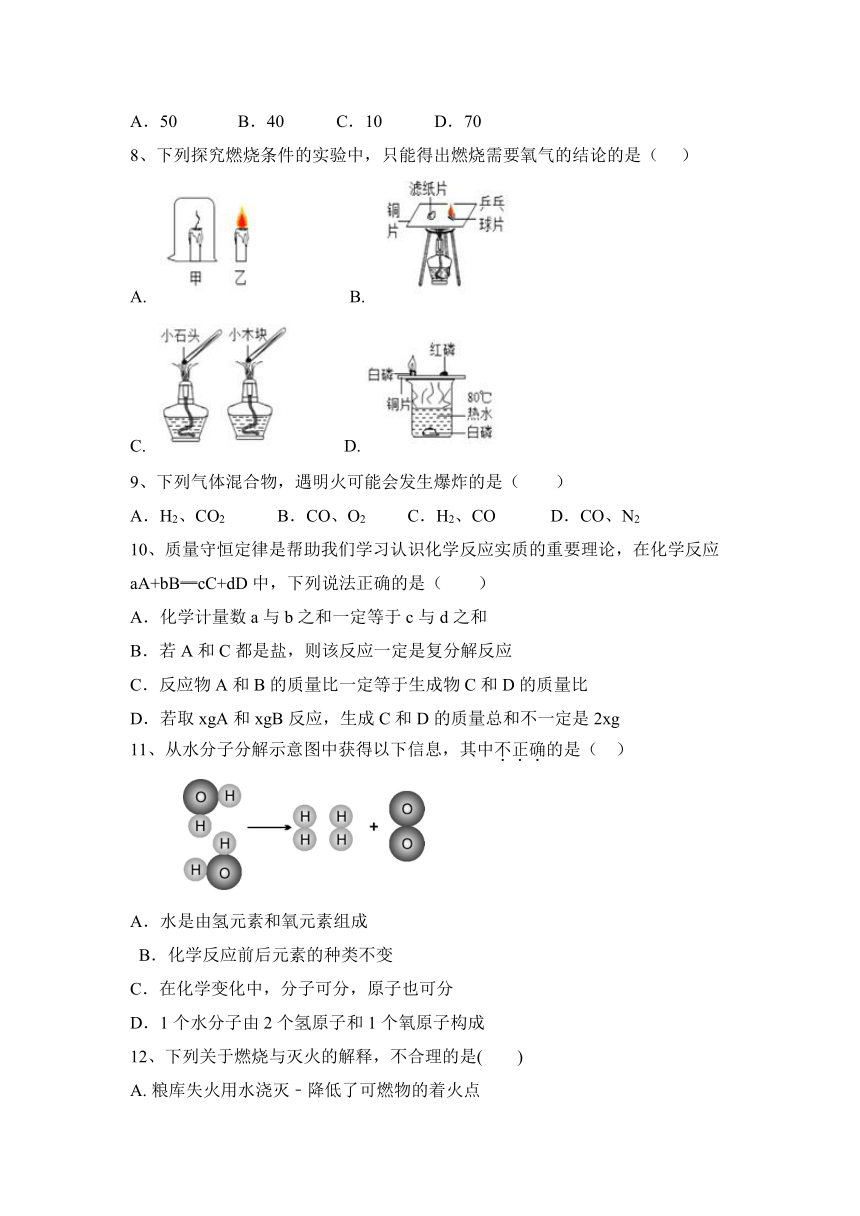
6、氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
A.氢氧化铝属于氧化物
B.在NaAlO2中铝元素的化合价为+3价
C.向稀盐酸中加入氢氧化铝,发生中和反应
D.向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失
7、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前的质量(g) 20 50 80 30
反应后的质量(g) 0 100 10 x
请根据质量守恒定律判断x的值( )
A.50 B.40 C.10 D.70
8、下列探究燃烧条件的实验中,只能得出燃烧需要氧气的结论的是( )
A. B.
C. D.
9、下列气体混合物,遇明火可能会发生爆炸的是( )
A.H2、CO2 B.CO、O2 C.H2、CO D.CO、N2
10、质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反应
aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
11、从水分子分解示意图中获得以下信息,其中不正确的是( )
A.水是由氢元素和氧元素组成
B.化学反应前后元素的种类不变
C.在化学变化中,分子可分,原子也可分
D.1个水分子由2个氢原子和1个氧原子构成
12、下列关于燃烧与灭火的解释,不合理的是( )
A. 粮库失火用水浇灭﹣降低了可燃物的着火点
B. 扑灭森林火灾时开辟隔离带﹣清除和隔离了可燃物
C. 用扇子扇煤炉,炉火越扇越旺﹣提供充足的气气
D. 图书档案起火,用液态二氧化碳扑灭﹣既隔绝氧气又降低温度
13、下列关于爆炸的说法正确的是( )
A.一定是物理变化 B.可能是物理变化,也可能是化学变化
C.一定是化学变化 D.既不是物理变化,也不是化学变化
14、在反应2A+3B=2C+4D中,A与B的相对分子质量之比为1:1,用一定质量的A与12克B恰好完全反应,生产11克C,则下列说法中错误的是( )
A.若A的相对分子质量是32,则C的相对分子质量是88
B.B与D的相对分子质量之比是16:9
C.同时生成D的质量是9克
D.反应中,A与C的质量之比是8:11
15、书写只有一种生成物的化学方程式时,肯定用到的符号是( )
A.“==” B.“↑” C.“↓” D.“△”
二、填空题。
16、下面是一些灭火的实例,请说出灭火的原理。
(1)做实验时不慎碰到酒精灯,酒精在桌面燃烧,立即用湿抹布盖灭。______
(2)扑灭森林火灾时,常是将大火蔓延路线前的片树木砍掉,形成隔离带。______
(3)用嘴吹灭蜡烛。_____
17、质量守恒定律的发现对化学的发展做出了重要贡献。
(1)化学反应前后肯定没有变化的是_________(填字母序号)
①原子数目 ②分子数目 ③元素种类 ④物质种类
⑤原子种类 ⑥物质的总质量
A①④⑥ B①③⑤⑥ C①②⑥ D②③⑤
(2)某纯净物X在空气中完全燃烧,反应的化学方程式为:(反应条件已略去),则X的化学式为_______________。
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。
①从燃烧条件分析,固体质量在前没有发生变化的原因是____________________。
②该反应的化学方程式为_____________ 。
③参加反应的氧气质量为__________g。
18、4NH3+5O24X+6H2O反应中,则X的化学式为______。
19、节约能源、保护环境、低碳生活是全社会应该倡导的生活方式。
(1)在炉灶中引燃细枯枝后,如果迅速往灶里塞满枯枝,反而燃烧不旺,并产生很多浓烟,说明可燃物充分燃烧需要的条件是_____________。
(2)自然界吸收二氧化碳的主要途径是________。
(3)硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化,发生氧化反应后得到SO3;②SO3 与水化合形成硫酸。其中反应①的化学方程式为___________。
(4)“低碳生活”是倡导减少___________的排放。
(5)氢气能作为燃料的原因是______________(用化学方程式表示)。
20、观察“白磷燃烧前后质量的测定”实验,观察到的现象是________.文字表达式为________.实验中应观察和思考的是:①反应物和生成物的状态及________.②实验中的________变化情况.
21、从微观的角度认识物质及其变化,请根据图示回答下列问题。
(1)从宏观上看,图1所示变化属于_________变化(填“物理”或“化学”),从微观角度解释图1、图2所示的两个变化的本质区别是______________________________。
(2)写出符合图2所示变化的化学方程式________________________,该反应的基本反应类型是_______。
(3)图3中,B、C、D三种物质属于氧化物的是______________(填化学式);若一定质量的A和6.4g的B恰好完全反应,可生成4.4gC和3.6gD,则组成A的元素是__________。
三、实验题。
22、如图1、2所示的一组实验可用于研究燃烧的条件.查阅资料可知白磷的着火点是40℃,红磷的着火点是240℃.
(1)此组实验烧杯中的热水除提高温度外,主要还起到________ 的作用.
(2)若将图2中的白磷换成红磷,不能观察到燃烧现象,从而再次说明,可燃物燃烧的条件之一是________ .
(3)如果白磷和红磷靠近些,白磷先起火,红磷会随后着火,这是因为________ .
(4)如图3,用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,实验初始阶段发现________ , 由此可以说明燃烧的条件之一是:________ .
四、计算题。
23、工业上用电解水的方法制取氢气(化学方程式为2H2O2H2↑+O2↑)
试计算:电解7.2t的水,能制得氢气的质量是多少?
2022秋沪教版(全国)九年级上册第4章:认识化学变化习题选含答案
沪教版(全国)九上第4章 认识化学变化
一、选择题。
1、关于如图所示探究燃烧条件的实验中,说法不正确的是( )
A.气球的作用是收集磷燃烧产生的白烟,防止污染空气。
B.观察到的现象:试管和烧杯中的白磷能燃烧,红磷不能燃烧。
C.热水的作用是:升高温度,隔绝空气
D.由此实验得出燃烧的条件是:可燃物与氧气(或空气)接触,温度达到着火点
【答案】C
2、下列化学反应中,元素的化合价没有发生变化的是( )
①CO2+H2O═H2CO3 ②NH4HCO3===H2O+CO2↑+NH3↑
③2H2S+O2===2S+2H2O ④2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
A.①②③ B.①②④ C.②③④ D.①③④
【答案】 B
3、化学反应前后,下列各项中,肯定没有变化的是( )
①原子数目 ②原子的种类 ③分子数目 ④分子的种类
⑤元素的种类 ⑥物质的总质量 ⑦物质的种类
A.①②⑤⑥ B.①②③⑤
C.①②⑤⑦ D.③④⑥⑦
【答案】A
4、控制变量法是实验探究的重要方法.下列设计方案不能实现探究目的是( )
A. 甲实验可探究可燃物的燃烧需要与氧气接触且温度达到着火点
B. 甲实验中a、b对比可探究可燃物的燃烧是否需要达到一定温度
C. 乙中①②对比可探究铁的锈蚀条件是否与氧气有关
D. 乙中①②③对比可探究铁的锈蚀条件是否与氧气和水等物质有关
【答案】 B
5、下列探究燃烧条件的实验中,只能得出燃烧需要氧气结论的是( )
A. B.
C. D.
【答案】A
6、氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
A.氢氧化铝属于氧化物
B.在NaAlO2中铝元素的化合价为+3价
C.向稀盐酸中加入氢氧化铝,发生中和反应
D.向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失
【答案】A
7、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前的质量(g) 20 50 80 30
反应后的质量(g) 0 100 10 x
请根据质量守恒定律判断x的值( )
A.50 B.40 C.10 D.70
【答案】D
8、下列探究燃烧条件的实验中,只能得出燃烧需要氧气的结论的是( )
A. B.
C. D.
【答案】 A
9、下列气体混合物,遇明火可能会发生爆炸的是( )
A.H2、CO2 B.CO、O2 C.H2、CO D.CO、N2
【答案】B
10、质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反应
aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
【答案】D
11、从水分子分解示意图中获得以下信息,其中不正确的是( )
A.水是由氢元素和氧元素组成
B.化学反应前后元素的种类不变
C.在化学变化中,分子可分,原子也可分
D.1个水分子由2个氢原子和1个氧原子构成
【答案】C
12、下列关于燃烧与灭火的解释,不合理的是( )
A. 粮库失火用水浇灭﹣降低了可燃物的着火点
B. 扑灭森林火灾时开辟隔离带﹣清除和隔离了可燃物
C. 用扇子扇煤炉,炉火越扇越旺﹣提供充足的气气
D. 图书档案起火,用液态二氧化碳扑灭﹣既隔绝氧气又降低温度
【答案】 A
13、下列关于爆炸的说法正确的是( )
A.一定是物理变化 B.可能是物理变化,也可能是化学变化
C.一定是化学变化 D.既不是物理变化,也不是化学变化
【答案】B
14、在反应2A+3B=2C+4D中,A与B的相对分子质量之比为1:1,用一定质量的A与12克B恰好完全反应,生产11克C,则下列说法中错误的是( )
A.若A的相对分子质量是32,则C的相对分子质量是88
B.B与D的相对分子质量之比是16:9
C.同时生成D的质量是9克
D.反应中,A与C的质量之比是8:11
【答案】A
15、书写只有一种生成物的化学方程式时,肯定用到的符号是( )
A.“==” B.“↑” C.“↓” D.“△”
【答案】A
二、填空题。
16、下面是一些灭火的实例,请说出灭火的原理。
(1)做实验时不慎碰到酒精灯,酒精在桌面燃烧,立即用湿抹布盖灭。______
(2)扑灭森林火灾时,常是将大火蔓延路线前的片树木砍掉,形成隔离带。______
(3)用嘴吹灭蜡烛。_____
【答案】(1)隔绝空气,降低可燃物的温度
(2)撤离可燃物 (3)降低温度至着火点以下
17、质量守恒定律的发现对化学的发展做出了重要贡献。
(1)化学反应前后肯定没有变化的是_________(填字母序号)
①原子数目 ②分子数目 ③元素种类 ④物质种类
⑤原子种类 ⑥物质的总质量
A①④⑥ B①③⑤⑥ C①②⑥ D②③⑤
(2)某纯净物X在空气中完全燃烧,反应的化学方程式为:(反应条件已略去),则X的化学式为_______________。
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。
①从燃烧条件分析,固体质量在前没有发生变化的原因是____________________。
②该反应的化学方程式为_____________。
③参加反应的氧气质量为__________g。
【答案】B (或者) 温度没达到红磷的着火点 8g
18、4NH3+5O24X+6H2O反应中,则X的化学式为______。
【答案】NO
19、节约能源、保护环境、低碳生活是全社会应该倡导的生活方式。
(1)在炉灶中引燃细枯枝后,如果迅速往灶里塞满枯枝,反而燃烧不旺,并产生很多浓烟,说明可燃物充分燃烧需要的条件是_____________。
(2)自然界吸收二氧化碳的主要途径是________。
(3)硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化,发生氧化反应后得到SO3;②SO3 与水化合形成硫酸。其中反应①的化学方程式为___________。
(4)“低碳生活”是倡导减少___________的排放。
(5)氢气能作为燃料的原因是______________(用化学方程式表示)。
【答案】充足的氧气或空气 光合作用 O2+2SO22SO3
二氧化碳 2H2+O22H2O
20、观察“白磷燃烧前后质量的测定”实验,观察到的现象是________.文字表达式为________.实验中应观察和思考的是:①反应物和生成物的状态及________.②实验中的________变化情况.
【答案】白磷燃烧,产生白烟,发出黄光,小球开始膨胀,后又变瘪,天平仍平衡 白磷+氧气五氧化二磷 其他变化 质量
21、从微观的角度认识物质及其变化,请根据图示回答下列问题。
(1)从宏观上看,图1所示变化属于_________变化(填“物理”或“化学”),从微观角度解释图1、图2所示的两个变化的本质区别是______________________________。
(2)写出符合图2所示变化的化学方程式________________________,该反应的基本反应类型是_______。
(3)图3中,B、C、D三种物质属于氧化物的是______________(填化学式);若一定质量的A和6.4g的B恰好完全反应,可生成4.4gC和3.6gD,则组成A的元素是__________。
【答案】物理 图1中分子种类没有变,分子间的间隙发生改变,而图2中分子种类发生了改变,变成其它分子 2H2O2H2↑+O2↑ 分解反应 CO2、H2O 碳元素和氢元素
三、实验题。
22、如图1、2所示的一组实验可用于研究燃烧的条件.查阅资料可知白磷的着火点是40℃,红磷的着火点是240℃.
(1)此组实验烧杯中的热水除提高温度外,主要还起到________ 的作用.
(2)若将图2中的白磷换成红磷,不能观察到燃烧现象,从而再次说明,可燃物燃烧的条件之一是________ .
(3)如果白磷和红磷靠近些,白磷先起火,红磷会随后着火,这是因为________ .
(4)如图3,用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,实验初始阶段发现________ , 由此可以说明燃烧的条件之一是:________ .
【答案】(1)隔绝氧气;
(2)温度达到着火点;
(3)白磷燃烧放出热量,使红磷的温度达到其着火点;
(4)蘸酒精的棉花燃烧、蘸水的棉花不燃烧;可燃物;
【解析】(1)此组实验烧杯中的热水可以为白磷的燃烧提供热量,还可以为水中的白磷隔绝氧气.
(2)红磷的着火点高,热水不能使红磷达到着火点,如果图2中的是红磷,就不会看到燃烧现象,从而再次说明,可燃物燃烧的条件是温度达到着火点.
(3)如果白磷和红磷靠近些,白磷先起火燃烧放出热量,使红磷的温度达到其着火点所以红磷会随后着火.
(4)小棉花球蘸水后,因水不可燃,反而会蒸发吸收热量,所以温度达不到棉花的着火点,不会燃烧;而小棉花球蘸酒精后,酒精是可燃物,在酒精灯上被点燃后会燃烧放出大量的热,使温度达到棉花的着火点,引发棉花球燃烧,因此实验的结论是燃烧的物质必须是可燃物;如果在酒精灯火焰上加热时间较长,棉花球上的水分蒸发,当温度达到棉花的着火点,蘸水的棉花球也燃烧了。
四、计算题。
23、工业上用电解水的方法制取氢气(化学方程式为2H2O2H2↑+O2↑)
试计算:电解7.2t的水,能制得氢气的质量是多少?
【答案】设制的氢气的质量为x t
2H2O2H2↑+O2↑
36 4
7.2t X
36:4=7.2t:X
X=0.8t
答:制的氢气的质量为0.8t。
沪教版(全国)九上第4章 认识化学变化
一、选择题。
1、关于如图所示探究燃烧条件的实验中,说法不正确的是( )
A.气球的作用是收集磷燃烧产生的白烟,防止污染空气。
B.观察到的现象:试管和烧杯中的白磷能燃烧,红磷不能燃烧。
C.热水的作用是:升高温度,隔绝空气
D.由此实验得出燃烧的条件是:可燃物与氧气(或空气)接触,温度达到着火点
2、下列化学反应中,元素的化合价没有发生变化的是( )
①CO2+H2O═H2CO3 ②NH4HCO3===H2O+CO2↑+NH3↑
③2H2S+O2===2S+2H2O ④2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
A.①②③ B.①②④ C.②③④ D.①③④
3、化学反应前后,下列各项中,肯定没有变化的是( )
①原子数目 ②原子的种类 ③分子数目 ④分子的种类
⑤元素的种类 ⑥物质的总质量 ⑦物质的种类
A.①②⑤⑥ B.①②③⑤ C.①②⑤⑦ D.③④⑥⑦
4、控制变量法是实验探究的重要方法.下列设计方案不能实现探究目的是( )
A. 甲实验可探究可燃物的燃烧需要与氧气接触且温度达到着火点
B. 甲实验中a、b对比可探究可燃物的燃烧是否需要达到一定温度
C. 乙中①②对比可探究铁的锈蚀条件是否与氧气有关
D. 乙中①②③对比可探究铁的锈蚀条件是否与氧气和水等物质有关
5、下列探究燃烧条件的实验中,只能得出燃烧需要氧气结论的是( )
A. B.
C. D.
6、氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
A.氢氧化铝属于氧化物
B.在NaAlO2中铝元素的化合价为+3价
C.向稀盐酸中加入氢氧化铝,发生中和反应
D.向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失
7、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前的质量(g) 20 50 80 30
反应后的质量(g) 0 100 10 x
请根据质量守恒定律判断x的值( )
A.50 B.40 C.10 D.70
8、下列探究燃烧条件的实验中,只能得出燃烧需要氧气的结论的是( )
A. B.
C. D.
9、下列气体混合物,遇明火可能会发生爆炸的是( )
A.H2、CO2 B.CO、O2 C.H2、CO D.CO、N2
10、质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反应
aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
11、从水分子分解示意图中获得以下信息,其中不正确的是( )
A.水是由氢元素和氧元素组成
B.化学反应前后元素的种类不变
C.在化学变化中,分子可分,原子也可分
D.1个水分子由2个氢原子和1个氧原子构成
12、下列关于燃烧与灭火的解释,不合理的是( )
A. 粮库失火用水浇灭﹣降低了可燃物的着火点
B. 扑灭森林火灾时开辟隔离带﹣清除和隔离了可燃物
C. 用扇子扇煤炉,炉火越扇越旺﹣提供充足的气气
D. 图书档案起火,用液态二氧化碳扑灭﹣既隔绝氧气又降低温度
13、下列关于爆炸的说法正确的是( )
A.一定是物理变化 B.可能是物理变化,也可能是化学变化
C.一定是化学变化 D.既不是物理变化,也不是化学变化
14、在反应2A+3B=2C+4D中,A与B的相对分子质量之比为1:1,用一定质量的A与12克B恰好完全反应,生产11克C,则下列说法中错误的是( )
A.若A的相对分子质量是32,则C的相对分子质量是88
B.B与D的相对分子质量之比是16:9
C.同时生成D的质量是9克
D.反应中,A与C的质量之比是8:11
15、书写只有一种生成物的化学方程式时,肯定用到的符号是( )
A.“==” B.“↑” C.“↓” D.“△”
二、填空题。
16、下面是一些灭火的实例,请说出灭火的原理。
(1)做实验时不慎碰到酒精灯,酒精在桌面燃烧,立即用湿抹布盖灭。______
(2)扑灭森林火灾时,常是将大火蔓延路线前的片树木砍掉,形成隔离带。______
(3)用嘴吹灭蜡烛。_____
17、质量守恒定律的发现对化学的发展做出了重要贡献。
(1)化学反应前后肯定没有变化的是_________(填字母序号)
①原子数目 ②分子数目 ③元素种类 ④物质种类
⑤原子种类 ⑥物质的总质量
A①④⑥ B①③⑤⑥ C①②⑥ D②③⑤
(2)某纯净物X在空气中完全燃烧,反应的化学方程式为:(反应条件已略去),则X的化学式为_______________。
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。
①从燃烧条件分析,固体质量在前没有发生变化的原因是____________________。
②该反应的化学方程式为_____________ 。
③参加反应的氧气质量为__________g。
18、4NH3+5O24X+6H2O反应中,则X的化学式为______。
19、节约能源、保护环境、低碳生活是全社会应该倡导的生活方式。
(1)在炉灶中引燃细枯枝后,如果迅速往灶里塞满枯枝,反而燃烧不旺,并产生很多浓烟,说明可燃物充分燃烧需要的条件是_____________。
(2)自然界吸收二氧化碳的主要途径是________。
(3)硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化,发生氧化反应后得到SO3;②SO3 与水化合形成硫酸。其中反应①的化学方程式为___________。
(4)“低碳生活”是倡导减少___________的排放。
(5)氢气能作为燃料的原因是______________(用化学方程式表示)。
20、观察“白磷燃烧前后质量的测定”实验,观察到的现象是________.文字表达式为________.实验中应观察和思考的是:①反应物和生成物的状态及________.②实验中的________变化情况.
21、从微观的角度认识物质及其变化,请根据图示回答下列问题。
(1)从宏观上看,图1所示变化属于_________变化(填“物理”或“化学”),从微观角度解释图1、图2所示的两个变化的本质区别是______________________________。
(2)写出符合图2所示变化的化学方程式________________________,该反应的基本反应类型是_______。
(3)图3中,B、C、D三种物质属于氧化物的是______________(填化学式);若一定质量的A和6.4g的B恰好完全反应,可生成4.4gC和3.6gD,则组成A的元素是__________。
三、实验题。
22、如图1、2所示的一组实验可用于研究燃烧的条件.查阅资料可知白磷的着火点是40℃,红磷的着火点是240℃.
(1)此组实验烧杯中的热水除提高温度外,主要还起到________ 的作用.
(2)若将图2中的白磷换成红磷,不能观察到燃烧现象,从而再次说明,可燃物燃烧的条件之一是________ .
(3)如果白磷和红磷靠近些,白磷先起火,红磷会随后着火,这是因为________ .
(4)如图3,用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,实验初始阶段发现________ , 由此可以说明燃烧的条件之一是:________ .
四、计算题。
23、工业上用电解水的方法制取氢气(化学方程式为2H2O2H2↑+O2↑)
试计算:电解7.2t的水,能制得氢气的质量是多少?
2022秋沪教版(全国)九年级上册第4章:认识化学变化习题选含答案
沪教版(全国)九上第4章 认识化学变化
一、选择题。
1、关于如图所示探究燃烧条件的实验中,说法不正确的是( )
A.气球的作用是收集磷燃烧产生的白烟,防止污染空气。
B.观察到的现象:试管和烧杯中的白磷能燃烧,红磷不能燃烧。
C.热水的作用是:升高温度,隔绝空气
D.由此实验得出燃烧的条件是:可燃物与氧气(或空气)接触,温度达到着火点
【答案】C
2、下列化学反应中,元素的化合价没有发生变化的是( )
①CO2+H2O═H2CO3 ②NH4HCO3===H2O+CO2↑+NH3↑
③2H2S+O2===2S+2H2O ④2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
A.①②③ B.①②④ C.②③④ D.①③④
【答案】 B
3、化学反应前后,下列各项中,肯定没有变化的是( )
①原子数目 ②原子的种类 ③分子数目 ④分子的种类
⑤元素的种类 ⑥物质的总质量 ⑦物质的种类
A.①②⑤⑥ B.①②③⑤
C.①②⑤⑦ D.③④⑥⑦
【答案】A
4、控制变量法是实验探究的重要方法.下列设计方案不能实现探究目的是( )
A. 甲实验可探究可燃物的燃烧需要与氧气接触且温度达到着火点
B. 甲实验中a、b对比可探究可燃物的燃烧是否需要达到一定温度
C. 乙中①②对比可探究铁的锈蚀条件是否与氧气有关
D. 乙中①②③对比可探究铁的锈蚀条件是否与氧气和水等物质有关
【答案】 B
5、下列探究燃烧条件的实验中,只能得出燃烧需要氧气结论的是( )
A. B.
C. D.
【答案】A
6、氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
A.氢氧化铝属于氧化物
B.在NaAlO2中铝元素的化合价为+3价
C.向稀盐酸中加入氢氧化铝,发生中和反应
D.向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失
【答案】A
7、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前的质量(g) 20 50 80 30
反应后的质量(g) 0 100 10 x
请根据质量守恒定律判断x的值( )
A.50 B.40 C.10 D.70
【答案】D
8、下列探究燃烧条件的实验中,只能得出燃烧需要氧气的结论的是( )
A. B.
C. D.
【答案】 A
9、下列气体混合物,遇明火可能会发生爆炸的是( )
A.H2、CO2 B.CO、O2 C.H2、CO D.CO、N2
【答案】B
10、质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反应
aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
【答案】D
11、从水分子分解示意图中获得以下信息,其中不正确的是( )
A.水是由氢元素和氧元素组成
B.化学反应前后元素的种类不变
C.在化学变化中,分子可分,原子也可分
D.1个水分子由2个氢原子和1个氧原子构成
【答案】C
12、下列关于燃烧与灭火的解释,不合理的是( )
A. 粮库失火用水浇灭﹣降低了可燃物的着火点
B. 扑灭森林火灾时开辟隔离带﹣清除和隔离了可燃物
C. 用扇子扇煤炉,炉火越扇越旺﹣提供充足的气气
D. 图书档案起火,用液态二氧化碳扑灭﹣既隔绝氧气又降低温度
【答案】 A
13、下列关于爆炸的说法正确的是( )
A.一定是物理变化 B.可能是物理变化,也可能是化学变化
C.一定是化学变化 D.既不是物理变化,也不是化学变化
【答案】B
14、在反应2A+3B=2C+4D中,A与B的相对分子质量之比为1:1,用一定质量的A与12克B恰好完全反应,生产11克C,则下列说法中错误的是( )
A.若A的相对分子质量是32,则C的相对分子质量是88
B.B与D的相对分子质量之比是16:9
C.同时生成D的质量是9克
D.反应中,A与C的质量之比是8:11
【答案】A
15、书写只有一种生成物的化学方程式时,肯定用到的符号是( )
A.“==” B.“↑” C.“↓” D.“△”
【答案】A
二、填空题。
16、下面是一些灭火的实例,请说出灭火的原理。
(1)做实验时不慎碰到酒精灯,酒精在桌面燃烧,立即用湿抹布盖灭。______
(2)扑灭森林火灾时,常是将大火蔓延路线前的片树木砍掉,形成隔离带。______
(3)用嘴吹灭蜡烛。_____
【答案】(1)隔绝空气,降低可燃物的温度
(2)撤离可燃物 (3)降低温度至着火点以下
17、质量守恒定律的发现对化学的发展做出了重要贡献。
(1)化学反应前后肯定没有变化的是_________(填字母序号)
①原子数目 ②分子数目 ③元素种类 ④物质种类
⑤原子种类 ⑥物质的总质量
A①④⑥ B①③⑤⑥ C①②⑥ D②③⑤
(2)某纯净物X在空气中完全燃烧,反应的化学方程式为:(反应条件已略去),则X的化学式为_______________。
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。
①从燃烧条件分析,固体质量在前没有发生变化的原因是____________________。
②该反应的化学方程式为_____________。
③参加反应的氧气质量为__________g。
【答案】B (或者) 温度没达到红磷的着火点 8g
18、4NH3+5O24X+6H2O反应中,则X的化学式为______。
【答案】NO
19、节约能源、保护环境、低碳生活是全社会应该倡导的生活方式。
(1)在炉灶中引燃细枯枝后,如果迅速往灶里塞满枯枝,反而燃烧不旺,并产生很多浓烟,说明可燃物充分燃烧需要的条件是_____________。
(2)自然界吸收二氧化碳的主要途径是________。
(3)硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化,发生氧化反应后得到SO3;②SO3 与水化合形成硫酸。其中反应①的化学方程式为___________。
(4)“低碳生活”是倡导减少___________的排放。
(5)氢气能作为燃料的原因是______________(用化学方程式表示)。
【答案】充足的氧气或空气 光合作用 O2+2SO22SO3
二氧化碳 2H2+O22H2O
20、观察“白磷燃烧前后质量的测定”实验,观察到的现象是________.文字表达式为________.实验中应观察和思考的是:①反应物和生成物的状态及________.②实验中的________变化情况.
【答案】白磷燃烧,产生白烟,发出黄光,小球开始膨胀,后又变瘪,天平仍平衡 白磷+氧气五氧化二磷 其他变化 质量
21、从微观的角度认识物质及其变化,请根据图示回答下列问题。
(1)从宏观上看,图1所示变化属于_________变化(填“物理”或“化学”),从微观角度解释图1、图2所示的两个变化的本质区别是______________________________。
(2)写出符合图2所示变化的化学方程式________________________,该反应的基本反应类型是_______。
(3)图3中,B、C、D三种物质属于氧化物的是______________(填化学式);若一定质量的A和6.4g的B恰好完全反应,可生成4.4gC和3.6gD,则组成A的元素是__________。
【答案】物理 图1中分子种类没有变,分子间的间隙发生改变,而图2中分子种类发生了改变,变成其它分子 2H2O2H2↑+O2↑ 分解反应 CO2、H2O 碳元素和氢元素
三、实验题。
22、如图1、2所示的一组实验可用于研究燃烧的条件.查阅资料可知白磷的着火点是40℃,红磷的着火点是240℃.
(1)此组实验烧杯中的热水除提高温度外,主要还起到________ 的作用.
(2)若将图2中的白磷换成红磷,不能观察到燃烧现象,从而再次说明,可燃物燃烧的条件之一是________ .
(3)如果白磷和红磷靠近些,白磷先起火,红磷会随后着火,这是因为________ .
(4)如图3,用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,实验初始阶段发现________ , 由此可以说明燃烧的条件之一是:________ .
【答案】(1)隔绝氧气;
(2)温度达到着火点;
(3)白磷燃烧放出热量,使红磷的温度达到其着火点;
(4)蘸酒精的棉花燃烧、蘸水的棉花不燃烧;可燃物;
【解析】(1)此组实验烧杯中的热水可以为白磷的燃烧提供热量,还可以为水中的白磷隔绝氧气.
(2)红磷的着火点高,热水不能使红磷达到着火点,如果图2中的是红磷,就不会看到燃烧现象,从而再次说明,可燃物燃烧的条件是温度达到着火点.
(3)如果白磷和红磷靠近些,白磷先起火燃烧放出热量,使红磷的温度达到其着火点所以红磷会随后着火.
(4)小棉花球蘸水后,因水不可燃,反而会蒸发吸收热量,所以温度达不到棉花的着火点,不会燃烧;而小棉花球蘸酒精后,酒精是可燃物,在酒精灯上被点燃后会燃烧放出大量的热,使温度达到棉花的着火点,引发棉花球燃烧,因此实验的结论是燃烧的物质必须是可燃物;如果在酒精灯火焰上加热时间较长,棉花球上的水分蒸发,当温度达到棉花的着火点,蘸水的棉花球也燃烧了。
四、计算题。
23、工业上用电解水的方法制取氢气(化学方程式为2H2O2H2↑+O2↑)
试计算:电解7.2t的水,能制得氢气的质量是多少?
【答案】设制的氢气的质量为x t
2H2O2H2↑+O2↑
36 4
7.2t X
36:4=7.2t:X
X=0.8t
答:制的氢气的质量为0.8t。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
