江西省抚州市2021-2022学年高一下学期期末考化学试题(Word版含答案)
文档属性
| 名称 | 江西省抚州市2021-2022学年高一下学期期末考化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 583.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-17 00:00:00 | ||
图片预览



文档简介
抚州市2021-2022学年高一下学期期末考
化学试题卷
说明:
1.本卷分为第I卷和第Ⅱ卷,共18小题,全卷满分100分,考试时间为80分钟。
2.请同学们将答案直接填在答题卷上,收卷时只收答题卷。
本卷可能用到的相对原子质量:
第I卷(选择题,共46分)
一、选择题(本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.化学与社会、生产、生活密切相关,下列说法错误的是( )
A.《格物粗谈》记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”文中的“气”是指乙烯
B.采取静电除尘、燃煤固硫、汽车尾气催化净化等方法,可提高空气质量
C.新冠疫苗需要冷藏运输主要是防止蛋白质升温变性
D.“天和”核心舱舷窗使用的耐辐射石英玻璃的主要成分是
2.设为阿伏加德罗常数的值,下列说法正确的是( )
A.中含有个极性键
B.含有的电子数为
C.常温下,与足量的浓硝酸反应,转移的电子数为
D.高温高压条件下,和充分反应,生成的为
3.下图表示部分含硫物质的类别与化合价的关系。下列说法不正确的是( )
A.a与c之间能发生氧化还原反应
B.c能使溴水褪色,说明c有漂白性
C.将c的水溶液滴到蓝色石蕊试纸上,试纸变红不褪色
D.d溶液久置于空气中会生成e,溶液的导电性增强
4,废水中的氨氮()采用微生物脱氮法、化学沉淀法均可除去,具体原理如下:
①微生物脱氮法:
②化学沉淀法:向废水中加入含的溶液,生成沉淀从而去除氨氮。
下列有关说法正确的是( )
A.步骤a发生反应:
B.含氨氮的废水直接大量排放,对水体的影响不大
C.化学沉淀法脱氯时,溶液的碱性过强,氨氮的去除率将下降
D.微生物脱氮可在高温条件下进行,以加快脱氮的速率
5.粗(含少量杂质)制备纯的流程如图所示,下列说法错误的是( )
A.X可用作木材防火剂
B.步骤II中的稀硫酸可用代替
C.步骤II中的主要反应是
D.若在实验室中完成步骤III,一般在坩埚中进行
6.现有等体积混合而成的4组气体:①、②、③、④,现将其分别通入体积相同的试管中并立即倒立在足量水中,试管内水面上升的高度分别为,则高度关系是( )
A. B. C. D.
7.下列实验能达到实验目的且符合操作要求的是( )
A.喷泉实验 B.制备并收集 C.比较的非金属性 D.制备乙酸乙酯
8.以为催化剂的光热化学循环分解反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示,下列说法正确的是( )
A.过程①钛氧键发生了断裂释放了能量
B.反应过程中,同时有极性键、非极性键的断裂和形成
C.该反应中,光能和热能转化为化学能,且可以加快化学反应速率
D.二氧化碳完全分解成一氧化碳和氧气需要吸热
9.已知分解放出热量,在含少量的溶液中,分解的机理为( )
慢
快
下列有关该反应的说法正确的是( )
A.该反应速率的快慢主要取决于反应历程Ⅱ B.反应速率与的浓度有关
C.反应物的总能量小于生成物的总能量 D.
10.我国科学家首次在实验室中实现从二氧化碳到淀粉的全合成,合成路径如下图所示。下列说法正确的是( )
A.的电子式: B.与是同系物
C.转化为为氧化反应 D.能与反应产生
二、选择题(本题共4小题,每小题4分,共16分,在每小题给出的四个选项中,有一个或两个选项符合题目要求。全部选对得4分,选对但不全的得2分,有选错的得0分)
11.下列说法正确的是( )
A.反应符合最理想的“原子经济性”
B.北京冬奥会吉祥物“冰墩墩”外壳材料是PVC(聚氯乙烯),它能使溴水褪色
C.植物秸杆的主要成分是纤维素,纤维素在催化剂作用下经水解可得葡萄糖,葡萄糖在酒化酶的作用下能转化为酒精
D.向淀粉水解液中直接加入银氨溶液,并水浴加热,观察是否有银镜生成,可用来检验淀粉是否发生水解
12.锌—空气电池是一种适宜用作城市电动车的动力电源。锌—空气电池原理如图,放电时转化为。下列说法正确的是( )
A.空气中的氧气在石墨电极上发生氧化反应
B.该电池的负极反应为
C.该电池放电时溶液中的向石墨电极移动
D.该电池放电时电子由电极经电解质溶液流向石墨电极
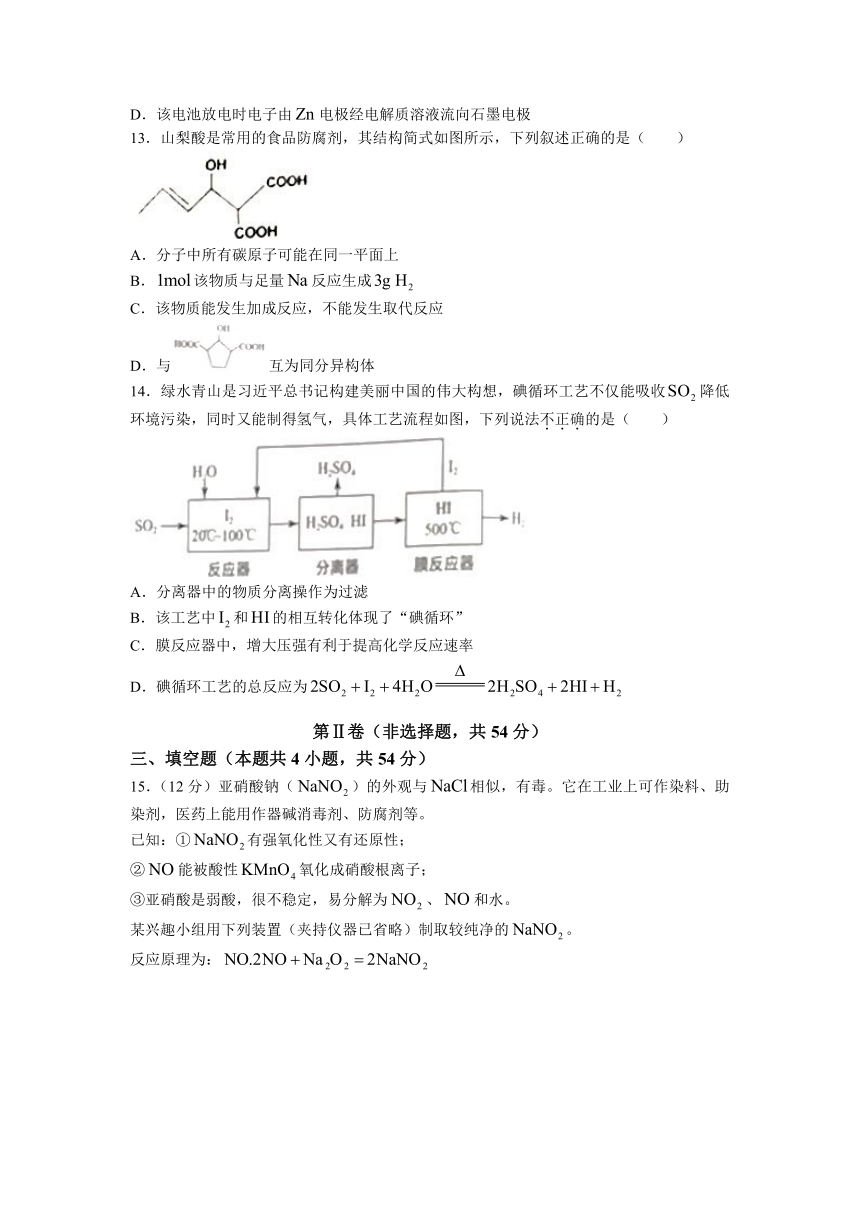
13.山梨酸是常用的食品防腐剂,其结构简式如图所示,下列叙述正确的是( )
A.分子中所有碳原子可能在同一平面上
B.该物质与足量反应生成
C.该物质能发生加成反应,不能发生取代反应
D.与互为同分异构体
14.绿水青山是习近平总书记构建美丽中国的伟大构想,碘循环工艺不仅能吸收降低环境污染,同时又能制得氢气,具体工艺流程如图,下列说法不正确的是( )
A.分离器中的物质分离操作为过滤
B.该工艺中和的相互转化体现了“碘循环”
C.膜反应器中,增大压强有利于提高化学反应速率
D.碘循环工艺的总反应为
第Ⅱ卷(非选择题,共54分)
三、填空题(本题共4小题,共54分)
15.(12分)亚硝酸钠()的外观与相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
已知:①有强氧化性又有还原性;
②能被酸性氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为、和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的。
反应原理为:
回答下列问题:
(1)乙装置的仪器名称是_____________,装置乙的作用是_____________。
(2)甲中滴入稀硝酸前需先通入,原因是__________________________。
(3)甲装置中发生反应的离子方程式为_______________________________________。
(4)反应过程中观察到丙中的现象为_______________________________________。
(5)丁中酸性的作用是_______________________________________。
(6)设计实验证明丙装置有生成_____________(写出操作、试剂和现象)。
16.(14分)燃煤的烟气中含有,为治理雾霾天气,工厂采用多种方法实现烟气脱硫。
I.“湿式吸收法”利用吸收剂与发生反应从而脱硫,下列试剂中适合用作该法吸收剂的是_____________(填字母序号)。
A.石灰乳 B.溶液 C.溶液 D.溶液
Ⅱ.某工厂利用工业废碱渣(主要成分为)来吸收燃煤烟气中含有的,还可以得到亚硫酸钠粗品。其流程如图:
(1)过程①进行的操作是__________________________。
(2)要提高吸收效率的可行措施有_____________(填数字序号)
①加快烟气的通入速率 ②将吸收液溶液进行雾化
③在高温条件下吸收 ④适当增加的浓度
(3)上述流程中,加入后,发生的化学方程式是__________________________。
(4)亚硫酸钠粗品中含有少量,原因是__________________________,设计实验证明亚硫酸钠粗品含有少量的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,__________________________,出现白色沉淀,则证明含有。
(5)己知有(已换算成标准状况)烟气(),通入足量吸收,再加足量溶液充分反应后(不考虑气中其他成分的反应),过滤、洗涤、干燥、称量得到沉淀。烟气中的含量(体积分数)的计算式是__________________________。
17.(14分)某温度下在密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图:
(1)①该反应的化学方程式是__________________________;
②用Y表示在内的平均反应速率为_____________,在该条件达到反应的限度时反应物X的转化率为_____________;
③反应初始与平衡时容器内气体压强之比为_____________。
(2)在一定温度下,在恒容的容器中充和发生反应:
。一段时何后,该反应达到化学平衡,下列能说明达到化学平衡状态的是_____________(填数字序号)。
① ② ③混合气体的压强不再改变
④混合气体的密度不再改变 ⑤混合气体的平均相对分子质量不再改变
(3)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质,溶于混合有机溶剂中,通过电解质迁移入晶格中,生成。回答下列问题:
①电子移动的方向是由_____________极流向_____________极(填字母);
②电池正极反应式为__________________________。
18.(14分)用石油裂化和裂解过程得到的两种烯烃来合成丙烯酸乙酯的路线如下:
(1)A的结构简式为_____________,E中含有的官能团为_____________,F为高分子化合物,F的结构简式为_____________。
(2)①的反应类型为_____________,②的化学方程式为__________________________。
(3)⑥的化学方程式为__________________________。
(4)工业生产中,试剂I最可能是下列试剂中的_____________(填字母序号)
a. b.酸性溶液 c.新制的悬浊液(含) d.银氨溶液
(5)与丙烯酸乙酯互为同分异构体且满足下列条件:
①含碳碳双键;②所有碳原子一定共面;③与碳酸氢钠溶液反应能产生气体。
请写出满足条件的任一种结构简式__________________________。
抚州市2021-2022学年高一下学期期末考化学试题参考答案
第Ⅰ卷(选择题,共46分)
一、选择题(本题共10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1 2 3 4 5 6 7 8 9 10
D A B C B D D C B C
二、选择题(本题共4小题,每小题4分,共16分。每小题有一至二个选项符合题意)
11 12 13 14
AC B BD AD
第Ⅱ卷(非选择题,共54分)
三、填空题(本题共4小题,共54分)
15.(12分,除标注外,每空2分)
(1)球形干燥管(1分) 吸收NO中的水蒸气(1分)
(2)赶尽装置内的O2,防止干扰NO的生成
(3)3Cu+8H++2NO3-=3Cu2+ + 2NO↑ + 4H2O
(4)淡黄色固体逐渐变为白色粉末
(5)吸收NO,防止污染环境
(6)取少量丙装置中的固体于试管中,加入稀硫酸,在试管中观察到有红棕色气体产生,证明有NaNO2 生成
16.(14分,每空2分)
I.A B C(漏选得1分,错选不得分)
II.(1)溶解、过滤
(2)②④ (漏选得1分,错选不得分)
(3)NaOH + NaHSO3 = Na2SO3 + H2O
(4)Na2SO3被氧化 加入过量盐酸,再加入BaCl2溶液
(5)
17.(14分,除标注外,每空2分)
(1) ① 3X(g) + Y(g) 2Z(g)
② 0.025mol·L-1·min-1 60%
③ 21:17
(2)①③⑤ (漏选得1分,错选不得分)
(3)①a b(每空1分) ② MnO2 + e- + Li+ = LiMnO2
18.(14分,除标注外,每空2分)
(1)CH2=CH2 (1分) 碳碳双键、羧基
(2)加成反应 (1分)
(3)
(4)a
(5)(CH3)2C=CHCOOH或CH3CH=C(CH3)COOH
化学试题卷
说明:
1.本卷分为第I卷和第Ⅱ卷,共18小题,全卷满分100分,考试时间为80分钟。
2.请同学们将答案直接填在答题卷上,收卷时只收答题卷。
本卷可能用到的相对原子质量:
第I卷(选择题,共46分)
一、选择题(本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.化学与社会、生产、生活密切相关,下列说法错误的是( )
A.《格物粗谈》记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”文中的“气”是指乙烯
B.采取静电除尘、燃煤固硫、汽车尾气催化净化等方法,可提高空气质量
C.新冠疫苗需要冷藏运输主要是防止蛋白质升温变性
D.“天和”核心舱舷窗使用的耐辐射石英玻璃的主要成分是
2.设为阿伏加德罗常数的值,下列说法正确的是( )
A.中含有个极性键
B.含有的电子数为
C.常温下,与足量的浓硝酸反应,转移的电子数为
D.高温高压条件下,和充分反应,生成的为
3.下图表示部分含硫物质的类别与化合价的关系。下列说法不正确的是( )
A.a与c之间能发生氧化还原反应
B.c能使溴水褪色,说明c有漂白性
C.将c的水溶液滴到蓝色石蕊试纸上,试纸变红不褪色
D.d溶液久置于空气中会生成e,溶液的导电性增强
4,废水中的氨氮()采用微生物脱氮法、化学沉淀法均可除去,具体原理如下:
①微生物脱氮法:
②化学沉淀法:向废水中加入含的溶液,生成沉淀从而去除氨氮。
下列有关说法正确的是( )
A.步骤a发生反应:
B.含氨氮的废水直接大量排放,对水体的影响不大
C.化学沉淀法脱氯时,溶液的碱性过强,氨氮的去除率将下降
D.微生物脱氮可在高温条件下进行,以加快脱氮的速率
5.粗(含少量杂质)制备纯的流程如图所示,下列说法错误的是( )
A.X可用作木材防火剂
B.步骤II中的稀硫酸可用代替
C.步骤II中的主要反应是
D.若在实验室中完成步骤III,一般在坩埚中进行
6.现有等体积混合而成的4组气体:①、②、③、④,现将其分别通入体积相同的试管中并立即倒立在足量水中,试管内水面上升的高度分别为,则高度关系是( )
A. B. C. D.
7.下列实验能达到实验目的且符合操作要求的是( )
A.喷泉实验 B.制备并收集 C.比较的非金属性 D.制备乙酸乙酯
8.以为催化剂的光热化学循环分解反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示,下列说法正确的是( )
A.过程①钛氧键发生了断裂释放了能量
B.反应过程中,同时有极性键、非极性键的断裂和形成
C.该反应中,光能和热能转化为化学能,且可以加快化学反应速率
D.二氧化碳完全分解成一氧化碳和氧气需要吸热
9.已知分解放出热量,在含少量的溶液中,分解的机理为( )
慢
快
下列有关该反应的说法正确的是( )
A.该反应速率的快慢主要取决于反应历程Ⅱ B.反应速率与的浓度有关
C.反应物的总能量小于生成物的总能量 D.
10.我国科学家首次在实验室中实现从二氧化碳到淀粉的全合成,合成路径如下图所示。下列说法正确的是( )
A.的电子式: B.与是同系物
C.转化为为氧化反应 D.能与反应产生
二、选择题(本题共4小题,每小题4分,共16分,在每小题给出的四个选项中,有一个或两个选项符合题目要求。全部选对得4分,选对但不全的得2分,有选错的得0分)
11.下列说法正确的是( )
A.反应符合最理想的“原子经济性”
B.北京冬奥会吉祥物“冰墩墩”外壳材料是PVC(聚氯乙烯),它能使溴水褪色
C.植物秸杆的主要成分是纤维素,纤维素在催化剂作用下经水解可得葡萄糖,葡萄糖在酒化酶的作用下能转化为酒精
D.向淀粉水解液中直接加入银氨溶液,并水浴加热,观察是否有银镜生成,可用来检验淀粉是否发生水解
12.锌—空气电池是一种适宜用作城市电动车的动力电源。锌—空气电池原理如图,放电时转化为。下列说法正确的是( )
A.空气中的氧气在石墨电极上发生氧化反应
B.该电池的负极反应为
C.该电池放电时溶液中的向石墨电极移动
D.该电池放电时电子由电极经电解质溶液流向石墨电极
13.山梨酸是常用的食品防腐剂,其结构简式如图所示,下列叙述正确的是( )
A.分子中所有碳原子可能在同一平面上
B.该物质与足量反应生成
C.该物质能发生加成反应,不能发生取代反应
D.与互为同分异构体
14.绿水青山是习近平总书记构建美丽中国的伟大构想,碘循环工艺不仅能吸收降低环境污染,同时又能制得氢气,具体工艺流程如图,下列说法不正确的是( )
A.分离器中的物质分离操作为过滤
B.该工艺中和的相互转化体现了“碘循环”
C.膜反应器中,增大压强有利于提高化学反应速率
D.碘循环工艺的总反应为
第Ⅱ卷(非选择题,共54分)
三、填空题(本题共4小题,共54分)
15.(12分)亚硝酸钠()的外观与相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
已知:①有强氧化性又有还原性;
②能被酸性氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为、和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的。
反应原理为:
回答下列问题:
(1)乙装置的仪器名称是_____________,装置乙的作用是_____________。
(2)甲中滴入稀硝酸前需先通入,原因是__________________________。
(3)甲装置中发生反应的离子方程式为_______________________________________。
(4)反应过程中观察到丙中的现象为_______________________________________。
(5)丁中酸性的作用是_______________________________________。
(6)设计实验证明丙装置有生成_____________(写出操作、试剂和现象)。
16.(14分)燃煤的烟气中含有,为治理雾霾天气,工厂采用多种方法实现烟气脱硫。
I.“湿式吸收法”利用吸收剂与发生反应从而脱硫,下列试剂中适合用作该法吸收剂的是_____________(填字母序号)。
A.石灰乳 B.溶液 C.溶液 D.溶液
Ⅱ.某工厂利用工业废碱渣(主要成分为)来吸收燃煤烟气中含有的,还可以得到亚硫酸钠粗品。其流程如图:
(1)过程①进行的操作是__________________________。
(2)要提高吸收效率的可行措施有_____________(填数字序号)
①加快烟气的通入速率 ②将吸收液溶液进行雾化
③在高温条件下吸收 ④适当增加的浓度
(3)上述流程中,加入后,发生的化学方程式是__________________________。
(4)亚硫酸钠粗品中含有少量,原因是__________________________,设计实验证明亚硫酸钠粗品含有少量的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,__________________________,出现白色沉淀,则证明含有。
(5)己知有(已换算成标准状况)烟气(),通入足量吸收,再加足量溶液充分反应后(不考虑气中其他成分的反应),过滤、洗涤、干燥、称量得到沉淀。烟气中的含量(体积分数)的计算式是__________________________。
17.(14分)某温度下在密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图:
(1)①该反应的化学方程式是__________________________;
②用Y表示在内的平均反应速率为_____________,在该条件达到反应的限度时反应物X的转化率为_____________;
③反应初始与平衡时容器内气体压强之比为_____________。
(2)在一定温度下,在恒容的容器中充和发生反应:
。一段时何后,该反应达到化学平衡,下列能说明达到化学平衡状态的是_____________(填数字序号)。
① ② ③混合气体的压强不再改变
④混合气体的密度不再改变 ⑤混合气体的平均相对分子质量不再改变
(3)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质,溶于混合有机溶剂中,通过电解质迁移入晶格中,生成。回答下列问题:
①电子移动的方向是由_____________极流向_____________极(填字母);
②电池正极反应式为__________________________。
18.(14分)用石油裂化和裂解过程得到的两种烯烃来合成丙烯酸乙酯的路线如下:
(1)A的结构简式为_____________,E中含有的官能团为_____________,F为高分子化合物,F的结构简式为_____________。
(2)①的反应类型为_____________,②的化学方程式为__________________________。
(3)⑥的化学方程式为__________________________。
(4)工业生产中,试剂I最可能是下列试剂中的_____________(填字母序号)
a. b.酸性溶液 c.新制的悬浊液(含) d.银氨溶液
(5)与丙烯酸乙酯互为同分异构体且满足下列条件:
①含碳碳双键;②所有碳原子一定共面;③与碳酸氢钠溶液反应能产生气体。
请写出满足条件的任一种结构简式__________________________。
抚州市2021-2022学年高一下学期期末考化学试题参考答案
第Ⅰ卷(选择题,共46分)
一、选择题(本题共10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1 2 3 4 5 6 7 8 9 10
D A B C B D D C B C
二、选择题(本题共4小题,每小题4分,共16分。每小题有一至二个选项符合题意)
11 12 13 14
AC B BD AD
第Ⅱ卷(非选择题,共54分)
三、填空题(本题共4小题,共54分)
15.(12分,除标注外,每空2分)
(1)球形干燥管(1分) 吸收NO中的水蒸气(1分)
(2)赶尽装置内的O2,防止干扰NO的生成
(3)3Cu+8H++2NO3-=3Cu2+ + 2NO↑ + 4H2O
(4)淡黄色固体逐渐变为白色粉末
(5)吸收NO,防止污染环境
(6)取少量丙装置中的固体于试管中,加入稀硫酸,在试管中观察到有红棕色气体产生,证明有NaNO2 生成
16.(14分,每空2分)
I.A B C(漏选得1分,错选不得分)
II.(1)溶解、过滤
(2)②④ (漏选得1分,错选不得分)
(3)NaOH + NaHSO3 = Na2SO3 + H2O
(4)Na2SO3被氧化 加入过量盐酸,再加入BaCl2溶液
(5)
17.(14分,除标注外,每空2分)
(1) ① 3X(g) + Y(g) 2Z(g)
② 0.025mol·L-1·min-1 60%
③ 21:17
(2)①③⑤ (漏选得1分,错选不得分)
(3)①a b(每空1分) ② MnO2 + e- + Li+ = LiMnO2
18.(14分,除标注外,每空2分)
(1)CH2=CH2 (1分) 碳碳双键、羧基
(2)加成反应 (1分)
(3)
(4)a
(5)(CH3)2C=CHCOOH或CH3CH=C(CH3)COOH
同课章节目录
