浙江省舟山市岱山中学2021-2022年初升高分班考试化学试题卷(word版含答案)
文档属性
| 名称 | 浙江省舟山市岱山中学2021-2022年初升高分班考试化学试题卷(word版含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 434.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-18 00:00:00 | ||
图片预览


文档简介
浙江省舟山市岱山中学2021-2022年初升高分班考试化学试题卷
考生须知:
1.本卷满分100分,考试时间90分钟;
2.答题前,在答题卷指定区域填写班级、姓名、考场、座位号及准考证号并核对条形码信息;
3.所有答案必须写在答题卷上,写在试卷上无效,考试结束后,只需上交答题卷。
4.可能用到的相对原子质量:H-1 C-12 N-14 0-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Ca-40 Fe-56 Cu-64 Ag-108 I-127 Ba-137
第I卷(选择题60分)
一、选择题I(本大题共15小题,每小题2分,共30分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.化学反应前后肯定没有变化的是
①原子数目②分子数目③元素种类④物质的总质量⑤物质的种类
A.①②③ B.①③④ C.①③⑤ D.③④⑤
2.配制250mL1.00mol/LNaCl溶液无需用到的仪器是
A. B. C. D.
3.下列不属于分散系的是
A.冰 B.豆浆 C.云、雾 D.有色玻璃
4.下列说法:①只含一种元素的物质一定是纯净物②BaSO4是一种难溶于水的强电解质③磷酸、烧碱、小苏打分别属于酸、碱、盐。其中正确的表述是
A.①②③ B.①③ C.②③ D.①②
5.下列物质属于电解质的是
A.稀盐酸 B.铜 C.硫酸钡 D.氨气
6.“84”消毒液在日常生活中广泛使用,该消毒液无色,溶液呈碱性,有漂白作用。它的有效成分是下列物质中的一种,这种物质是
A.NaOH B.NaClO C. D.
7.油画上使用的白色颜料经一段时间后会变为黑色的PbS(硫化铅),使颜料恢复白色的方法是蘸涂双氧水,发生反应的化学方程式为:PbS+4H2O2=PbSO4+4H2O,此反应中Pb元素、H元素的化合价不变,O元素的化合价变化为:-l→-2,则S元素的化合价变化为
A.+2→+4 B.+2→+6 C.-2→+4 D.-2→+6
8.二氧化碳资源化利用是解决温室效应的重要途径。下列利用CO2生产燃料或化学品的过程中未涉及氧化还原反应的是
A.光催化CO2制CH3OH B.CO2-CH4重整制合成气CO、H2
C.电催化CO2制取HCOOH、CO D.利用NaCl、NH3及CO2生产Na2CO3
9.下列各溶液中,浓度最大的是
A. B.
C. D.
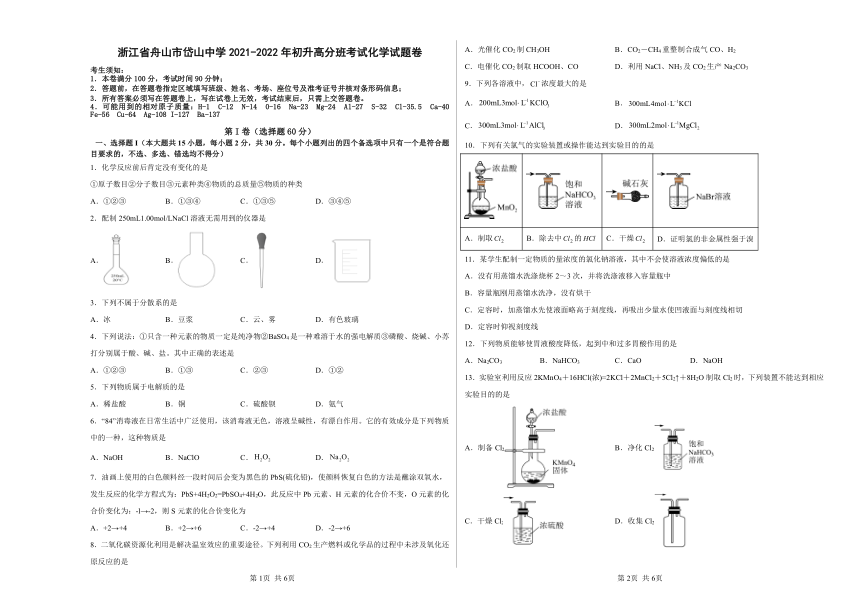
10.下列有关氯气的实验装置或操作能达到实验目的的是
A.制取 B.除去中的 C.干燥 D.证明氯的非金属性强于溴
11.某学生配制一定物质的量浓度的氯化钠溶液,其中不会使溶液浓度偏低的是
A.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
B.容量瓶刚用蒸馏水洗净,没有烘干
C.定容时,加蒸馏水先使液面略高于刻度线,再吸出少量水使凹液面与刻度线相切
D.定容时仰视刻度线
12.下列物质能够使胃液酸度降低,起到中和过多胃酸作用的是
A.Na2CO3 B.NaHCO3 C.CaO D.NaOH
13.实验室利用反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O制取Cl2时,下列装置不能达到相应实验目的的是
A.制备Cl2 B.净化Cl2
C.干燥Cl2 D.收集Cl2
14.除去Na2CO3粉末中少量NaHCO3的方法是
A.加热 B.加入KOH溶液 C.加入适量硫酸 D.加入适量BaCl2溶液
15.如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是
①碳酸钠和盐酸 ②稀硫酸和锌 ③水和过氧化钠 ④水和硝酸铵
A.①②③④ B.①②③ C.①③④ D.②③
二、选择题II(本大题共10小题,每小题3分,共30分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
16.下列物质对应的化学式不正确的是
A.熟石膏: B.红宝石主要成分:
C.尿素: D.孔雀石主要成分:
17.分类是学习和研究化学的一种重要方法,下列物质的分类错误的是
A.CaO和Na2O2都属于碱性氧化物 B.HNO3和H2SO3都属于酸
C.Fe(OH)3和NH3.·H2O都属于碱 D.NaHSO4 和NH4Cl都属于盐
18.下列物质的分类正确的是
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱
B
C 氨水
D 明矾
19.将一定量溶质的质量分数为6%的Na2CO3溶液加热蒸发掉15g水后,还剩溶质的质量分数为14%的溶液10mL,此时溶液的浓度为
A.1.49mol·L-1 B.1.52mol·L-1 C.2mol·L-1 D.2.5mol·L-1
20.下列有关反应的离子方程式书写正确的是
A.FeO与稀硝酸反应:2H++ FeO = Fe2+ +H2O
B.向碳酸氢铵溶液中滴加少量的氢氧化钠溶液:NH+ HCO + 2OH- = CO+NH3·H2O + H2O
C.向AlCl3溶液中加入过量浓氨水: Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH
D.HNO3与氨水反应:H+ +OH- = H2O
21.某实验小组设计以氮气为主要原料制备硝酸的转化过程如图所示,其中氮元素既被氧化又被还原的一步是
A.① B.② C.③ D.④
22.我国著名化工实业家侯德榜提出了“联合制碱法”,该生产工艺流程如图所示。下列说法不正确的是
A.沉淀池发生反应:
B.吸收可使母液中的转化为,以提高纯度
C.该过程充分利用了合成氨工业提供的和
D.向饱和食盐水中先通,再通,更有利于析出
23.设为阿伏加德罗常数的值。火箭推进时发生反应,下列说法正确的是
A.火箭推进时,每生成1mol 转移的电子数目为4
B.常温常压下,46g 和的混合物中含有质子数为23
C.1mol 与4mol 在一定条件下反应生成的分子数为2
D.3.2g 中含有共价键数目为0.6
24.有一包白色粉末,由、、、NaOH、中的一种或几种组成,为了探究它的成分,进行了如下实验。下列判断正确的是
A.白色滤渣A中一定有,可能有 B.、一定存在,NaOH可能存在
C.NaOH一定存在,一定不存在 D.、NaOH、一定存在
25.为检验溶液里的某种离子,分别取少量待测液进行下列实验,其中结论正确的是
A.先加适量的盐酸将溶液酸化,再加入AgNO3溶液,产生了白色沉淀,则原溶液中一定含有大量的Cl- 离子
B.用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色,则溶液有Na+,无K+
C.溶液中加入稀盐酸酸化,无明显现象,再加入BaCl2溶液,产生了白色沉淀,则原溶液中一定含有大量的SO离子
D.溶液中加入盐酸,有能使澄清石灰水变浑浊的无色气体放出,则溶液中一定含有CO 离子
第II卷(非选择题40分)
26.(6分)按要求回答下列问题
(1)漂白液有效成分的化学式___________。
(2)氯气与水反应的离子方程式___________________________________。
(3)小苏打受热分解的化学方程式___________________________________;
27.现有中学化学中常见的八种物质:①固体氢氧化钡 ②石墨棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥熔融氯化钠 ⑦蔗糖 ⑧碳酸钠粉末。请用序号填空:
(1)上述状态下可导电的是___________,属于非电解质的是___________。
(2)属于酸的是___________,属于碱的是___________,属于盐的是___________。
28.回答下列问题
(1)高铁酸钾是一种新型、高效、多功能绿色水处理剂,且无二次污染。中为_______价,盐酸中加入少量固体,产生,被还原成,该反应的化学方程式是___________
________________________________。
(2)是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验是否泄漏,有关反应的化学方程式为。用双线桥标出电子转移的方向和数目:__________。
(3)已知常温下在溶液中可发生如下反应:,。由此可以确定、、三种离子的氧化性由强到弱的顺序是___________。
29.下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。
可供选用的仪器有:①胶头滴管 ②烧瓶 ③烧杯 ④玻璃棒 ⑤药匙 ⑥量筒 ⑦托盘天平。请回答下列问题:
(1)该硫酸的物质的量浓度为_______mol·L-1。
(2)配制稀硫酸时,还缺少的仪器有 _______ (写仪器名称)。
(3)经计算,配制480mL1mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为_______mL。
(4)对所配制的稀硫酸进行测定,发现其浓度小于1 mol·L-1,配制过程中下列各项操作可能引起该误差的原因有_______。(填字母)
A.定容时,俯视容量瓶刻度线进行定容
B.将稀释后的硫酸未经冷却直接转移至容量瓶中
C.移溶液时,不慎将少量溶液洒到容量瓶外面
D.所用容量瓶经蒸馏水洗涤后未干燥,有少量残留蒸馏水
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,再滴水至刻度线处
(5)在5 L 硫酸和盐酸的混合溶液中,H+的浓度为0.4mol·L-1,和足量BaCl2溶液反应可得沉淀0.5mol,则原溶液中盐酸的物质的量浓度是_______mol·L-1。
30.取1.43g Na2CO3 xH2O溶于水,配成10mL溶液。然后向其中逐滴滴入稀盐酸直至没有气体放出,共用去盐酸20mL,并收集到112mLCO2(标准状况下)。请回答下列问题:
(1)稀盐酸的物质的量浓度为_____________;
(2)Na2CO3 xH2O的摩尔质量为___________;
(3)x的值为___________。
第1页 共4页 第2页 共4页
第1页 共4页 第2页 共4页
参考答案
一、单选题Ⅰ(本大题共有25个小题,1-15每小题每题2分,每小题均只有一个正确选项,共计30分)。
1 2 3 4 5 6 7 8 9 10
B B A C C B D D C D
11 12 13 14 15
B B B A B
二、选择题II(本大题共10小题,每小题3分,共30分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
16 17 18 19 20 21 22 23 24 25
A A D A C D D B C C
三、非选择题
26.(1)NaClO
(2)Cl2+H2O=H++Cl-+HClO
(3)2NaHCO3Na2CO3+CO2↑+H2O
27.(1) ②⑥ ⑦ (2) ③④ ① ⑤⑥⑧
28.(1)
(2)
(3)
29.(1)18.4
(2)500mL容量瓶
(3)27.2
(4)CE
(5)0.2
30. 0.5mol/L 286g/mol 10
答案第1页,共2页
答案第1页,共2页
考生须知:
1.本卷满分100分,考试时间90分钟;
2.答题前,在答题卷指定区域填写班级、姓名、考场、座位号及准考证号并核对条形码信息;
3.所有答案必须写在答题卷上,写在试卷上无效,考试结束后,只需上交答题卷。
4.可能用到的相对原子质量:H-1 C-12 N-14 0-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Ca-40 Fe-56 Cu-64 Ag-108 I-127 Ba-137
第I卷(选择题60分)
一、选择题I(本大题共15小题,每小题2分,共30分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.化学反应前后肯定没有变化的是
①原子数目②分子数目③元素种类④物质的总质量⑤物质的种类
A.①②③ B.①③④ C.①③⑤ D.③④⑤
2.配制250mL1.00mol/LNaCl溶液无需用到的仪器是
A. B. C. D.
3.下列不属于分散系的是
A.冰 B.豆浆 C.云、雾 D.有色玻璃
4.下列说法:①只含一种元素的物质一定是纯净物②BaSO4是一种难溶于水的强电解质③磷酸、烧碱、小苏打分别属于酸、碱、盐。其中正确的表述是
A.①②③ B.①③ C.②③ D.①②
5.下列物质属于电解质的是
A.稀盐酸 B.铜 C.硫酸钡 D.氨气
6.“84”消毒液在日常生活中广泛使用,该消毒液无色,溶液呈碱性,有漂白作用。它的有效成分是下列物质中的一种,这种物质是
A.NaOH B.NaClO C. D.
7.油画上使用的白色颜料经一段时间后会变为黑色的PbS(硫化铅),使颜料恢复白色的方法是蘸涂双氧水,发生反应的化学方程式为:PbS+4H2O2=PbSO4+4H2O,此反应中Pb元素、H元素的化合价不变,O元素的化合价变化为:-l→-2,则S元素的化合价变化为
A.+2→+4 B.+2→+6 C.-2→+4 D.-2→+6
8.二氧化碳资源化利用是解决温室效应的重要途径。下列利用CO2生产燃料或化学品的过程中未涉及氧化还原反应的是
A.光催化CO2制CH3OH B.CO2-CH4重整制合成气CO、H2
C.电催化CO2制取HCOOH、CO D.利用NaCl、NH3及CO2生产Na2CO3
9.下列各溶液中,浓度最大的是
A. B.
C. D.
10.下列有关氯气的实验装置或操作能达到实验目的的是
A.制取 B.除去中的 C.干燥 D.证明氯的非金属性强于溴
11.某学生配制一定物质的量浓度的氯化钠溶液,其中不会使溶液浓度偏低的是
A.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
B.容量瓶刚用蒸馏水洗净,没有烘干
C.定容时,加蒸馏水先使液面略高于刻度线,再吸出少量水使凹液面与刻度线相切
D.定容时仰视刻度线
12.下列物质能够使胃液酸度降低,起到中和过多胃酸作用的是
A.Na2CO3 B.NaHCO3 C.CaO D.NaOH
13.实验室利用反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O制取Cl2时,下列装置不能达到相应实验目的的是
A.制备Cl2 B.净化Cl2
C.干燥Cl2 D.收集Cl2
14.除去Na2CO3粉末中少量NaHCO3的方法是
A.加热 B.加入KOH溶液 C.加入适量硫酸 D.加入适量BaCl2溶液
15.如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是
①碳酸钠和盐酸 ②稀硫酸和锌 ③水和过氧化钠 ④水和硝酸铵
A.①②③④ B.①②③ C.①③④ D.②③
二、选择题II(本大题共10小题,每小题3分,共30分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
16.下列物质对应的化学式不正确的是
A.熟石膏: B.红宝石主要成分:
C.尿素: D.孔雀石主要成分:
17.分类是学习和研究化学的一种重要方法,下列物质的分类错误的是
A.CaO和Na2O2都属于碱性氧化物 B.HNO3和H2SO3都属于酸
C.Fe(OH)3和NH3.·H2O都属于碱 D.NaHSO4 和NH4Cl都属于盐
18.下列物质的分类正确的是
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱
B
C 氨水
D 明矾
19.将一定量溶质的质量分数为6%的Na2CO3溶液加热蒸发掉15g水后,还剩溶质的质量分数为14%的溶液10mL,此时溶液的浓度为
A.1.49mol·L-1 B.1.52mol·L-1 C.2mol·L-1 D.2.5mol·L-1
20.下列有关反应的离子方程式书写正确的是
A.FeO与稀硝酸反应:2H++ FeO = Fe2+ +H2O
B.向碳酸氢铵溶液中滴加少量的氢氧化钠溶液:NH+ HCO + 2OH- = CO+NH3·H2O + H2O
C.向AlCl3溶液中加入过量浓氨水: Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH
D.HNO3与氨水反应:H+ +OH- = H2O
21.某实验小组设计以氮气为主要原料制备硝酸的转化过程如图所示,其中氮元素既被氧化又被还原的一步是
A.① B.② C.③ D.④
22.我国著名化工实业家侯德榜提出了“联合制碱法”,该生产工艺流程如图所示。下列说法不正确的是
A.沉淀池发生反应:
B.吸收可使母液中的转化为,以提高纯度
C.该过程充分利用了合成氨工业提供的和
D.向饱和食盐水中先通,再通,更有利于析出
23.设为阿伏加德罗常数的值。火箭推进时发生反应,下列说法正确的是
A.火箭推进时,每生成1mol 转移的电子数目为4
B.常温常压下,46g 和的混合物中含有质子数为23
C.1mol 与4mol 在一定条件下反应生成的分子数为2
D.3.2g 中含有共价键数目为0.6
24.有一包白色粉末,由、、、NaOH、中的一种或几种组成,为了探究它的成分,进行了如下实验。下列判断正确的是
A.白色滤渣A中一定有,可能有 B.、一定存在,NaOH可能存在
C.NaOH一定存在,一定不存在 D.、NaOH、一定存在
25.为检验溶液里的某种离子,分别取少量待测液进行下列实验,其中结论正确的是
A.先加适量的盐酸将溶液酸化,再加入AgNO3溶液,产生了白色沉淀,则原溶液中一定含有大量的Cl- 离子
B.用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色,则溶液有Na+,无K+
C.溶液中加入稀盐酸酸化,无明显现象,再加入BaCl2溶液,产生了白色沉淀,则原溶液中一定含有大量的SO离子
D.溶液中加入盐酸,有能使澄清石灰水变浑浊的无色气体放出,则溶液中一定含有CO 离子
第II卷(非选择题40分)
26.(6分)按要求回答下列问题
(1)漂白液有效成分的化学式___________。
(2)氯气与水反应的离子方程式___________________________________。
(3)小苏打受热分解的化学方程式___________________________________;
27.现有中学化学中常见的八种物质:①固体氢氧化钡 ②石墨棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥熔融氯化钠 ⑦蔗糖 ⑧碳酸钠粉末。请用序号填空:
(1)上述状态下可导电的是___________,属于非电解质的是___________。
(2)属于酸的是___________,属于碱的是___________,属于盐的是___________。
28.回答下列问题
(1)高铁酸钾是一种新型、高效、多功能绿色水处理剂,且无二次污染。中为_______价,盐酸中加入少量固体,产生,被还原成,该反应的化学方程式是___________
________________________________。
(2)是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验是否泄漏,有关反应的化学方程式为。用双线桥标出电子转移的方向和数目:__________。
(3)已知常温下在溶液中可发生如下反应:,。由此可以确定、、三种离子的氧化性由强到弱的顺序是___________。
29.下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。
可供选用的仪器有:①胶头滴管 ②烧瓶 ③烧杯 ④玻璃棒 ⑤药匙 ⑥量筒 ⑦托盘天平。请回答下列问题:
(1)该硫酸的物质的量浓度为_______mol·L-1。
(2)配制稀硫酸时,还缺少的仪器有 _______ (写仪器名称)。
(3)经计算,配制480mL1mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为_______mL。
(4)对所配制的稀硫酸进行测定,发现其浓度小于1 mol·L-1,配制过程中下列各项操作可能引起该误差的原因有_______。(填字母)
A.定容时,俯视容量瓶刻度线进行定容
B.将稀释后的硫酸未经冷却直接转移至容量瓶中
C.移溶液时,不慎将少量溶液洒到容量瓶外面
D.所用容量瓶经蒸馏水洗涤后未干燥,有少量残留蒸馏水
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,再滴水至刻度线处
(5)在5 L 硫酸和盐酸的混合溶液中,H+的浓度为0.4mol·L-1,和足量BaCl2溶液反应可得沉淀0.5mol,则原溶液中盐酸的物质的量浓度是_______mol·L-1。
30.取1.43g Na2CO3 xH2O溶于水,配成10mL溶液。然后向其中逐滴滴入稀盐酸直至没有气体放出,共用去盐酸20mL,并收集到112mLCO2(标准状况下)。请回答下列问题:
(1)稀盐酸的物质的量浓度为_____________;
(2)Na2CO3 xH2O的摩尔质量为___________;
(3)x的值为___________。
第1页 共4页 第2页 共4页
第1页 共4页 第2页 共4页
参考答案
一、单选题Ⅰ(本大题共有25个小题,1-15每小题每题2分,每小题均只有一个正确选项,共计30分)。
1 2 3 4 5 6 7 8 9 10
B B A C C B D D C D
11 12 13 14 15
B B B A B
二、选择题II(本大题共10小题,每小题3分,共30分。每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
16 17 18 19 20 21 22 23 24 25
A A D A C D D B C C
三、非选择题
26.(1)NaClO
(2)Cl2+H2O=H++Cl-+HClO
(3)2NaHCO3Na2CO3+CO2↑+H2O
27.(1) ②⑥ ⑦ (2) ③④ ① ⑤⑥⑧
28.(1)
(2)
(3)
29.(1)18.4
(2)500mL容量瓶
(3)27.2
(4)CE
(5)0.2
30. 0.5mol/L 286g/mol 10
答案第1页,共2页
答案第1页,共2页
同课章节目录
