第一章 认识化学科学 复习
图片预览






文档简介
课件25张PPT。第一章复习普通高中课程标准实验教科书 化学1(必修)第一节 走进化学科学相关知识回顾:
化学研究的对象:物质组成、结构、性质、变化、制备和应用。
物理变化:没有生成其他物质的变化。
化学变化:生成了其他物质的变化,也叫化学反应。
物理性质:不需要发生化学反应就表现出来的性质,如颜色、状态、气味、熔点、沸点、硬度、密度等
化学性质:物质在化学变化中表现出来的性质。
分子:保持物质化学性质的最小粒子。
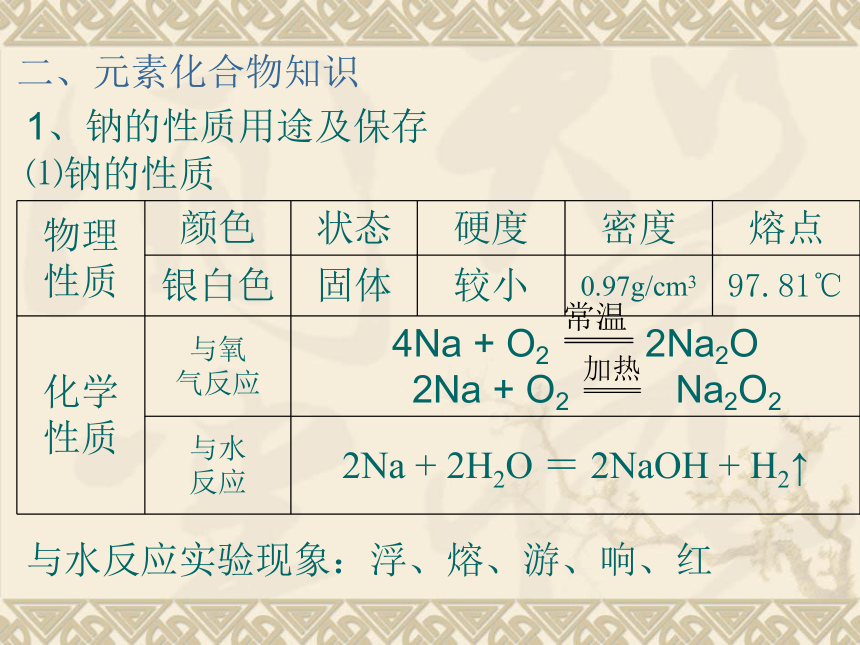
原子:化学变化中的最小粒子。知识点一、化学科学的创造性和实用性化学的特征:认识分子制造分子。知识点二、化学科学的形成和发展1661年,英国科学家波义耳提出了化学元素的概念,标志着近代化学的诞生。1771年,法国科学家拉瓦锡,建立燃烧氧化学说,使近代化学取得了革命性的进展。1803年,英国科学家道尔顿提出原子学说,为近代化学的发展奠定了坚实的基础。1869年,俄国科学家门捷列夫发现元素周期律,把化学元素及化合物纳入一个统一的理论系统。第二节 研究物质性质的方法和程序1、研究物质性质的基本方法:2、研究物质性质的程序:观察、实验、分类、比较。观察外观、预测性质、实验观察、解释现象、结论并归纳整合。一、理论知识二、元素化合物知识1、钠的性质用途及保存⑴钠的性质与水反应实验现象:浮、熔、游、响、红(2)钠的用途制Na2O2 制原子反应堆的导热剂k-Na合
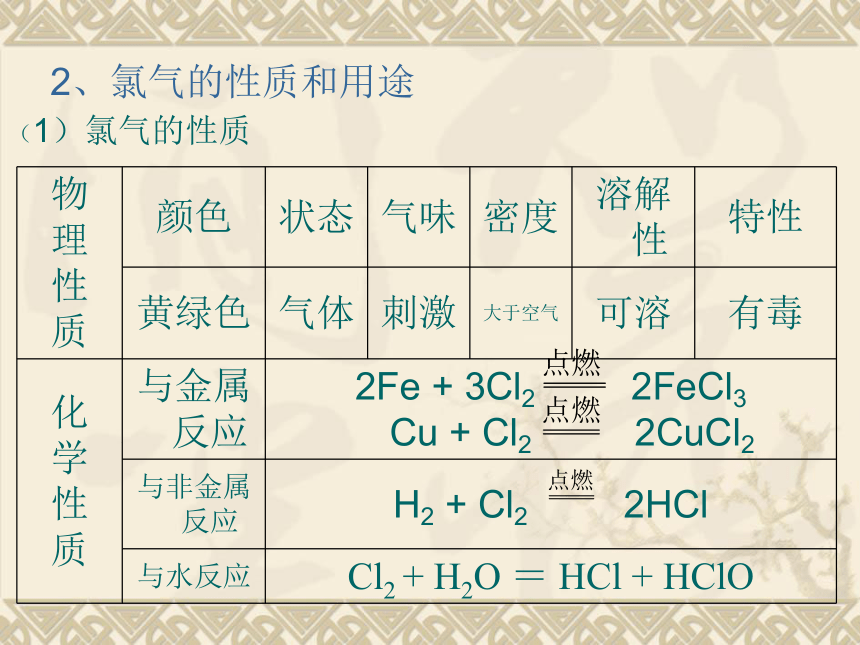
制造钛、锆、铌等稀有金属 做光源(3)钠的保存少量的钠保存于煤油中2、氯气的性质和用途(1)氯气的性质氯水的成分:Cl2、H2O、HCl、HClO氯气和碱反应
Cl2 + NaOH = NaCl + NaClO + H2O
(制84消毒液)
2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
(制漂白粉)HClO的性质:
不稳定性:2HClO = 2HCl+O2↑
弱酸性、漂白性光照(2)氯气的用途:消毒 农药 盐酸 漂白剂第三节 物质的量1、基本概念
(1)摩尔:摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒。
(2)摩尔质量:1mol物质的质量叫摩尔质量,摩尔质量在数值上等于该物质的式量。
(3)标准状况下的气体摩尔体积:在标准状况(0℃、101.3kPa)下,1mol的任何气体的体积都大约是22.4L。
(4)物质的量浓度:以1L溶液中所含溶质物质的量来表示的溶液浓度叫物质的量浓度。2、各物理量之间的关系n =N/NA=m/Mn=V / Vm
=N/NA
=m / Mn=CB V n
=V / Vm
=N/NA
=m / M3、配制一定物质的量浓度溶液 操作细则以及实验仪器的选择主要是围绕减小实验误差来考虑。 关键在于:溶质的计量和转移、溶液体积的计量 其操作步骤为:计算、称量、溶解、转移、洗涤、定容、摇匀、装瓶。4、物质的量与化学反应
2H2 + O2 2H2O
从质量角度: 4g 32g 36g
从分子数角度: 2分子 1分子 2分子
从物质的量角度: 2mol 1mol 2mol
从标况下气体体积角度: 44.8L 22.4L
从任意相同条件气体体积角度: 2体积 1体积练习1.为中国近代化学发展做出突出贡献的科学家是
A.李四光 B.华罗更 C.候德榜 D.钱学森答案:B。 研析:题述四个选项中的科学家均为我国科学事业的发展做出了突出的贡献。其中,李四光是我国当代著名的地质学家;华罗更是著名的数学家;钱学森是著名的物理学家;候德榜被称为中国近代化学史上的第一颗明星,为中国化学工业发展做出卓越贡献,是中国近代化工工业的奠基人,他发明的联合制碱法为中华民族争得了荣誉。2.0.5mol Na2SO4中所含的Na+离子数为
A.3.01×1023 B.6.02×1023 C.0.5 D.1答案:B。 研析:
N(Na+)=n(Na2SO4)×2×NA
=0.5mol×2×6.02×1023mol-1
=6.02×1023。
3、下列各种物理性质中,对氯气来说不正确的是
A.黄绿色的气体 B.密度比空气小
C.能溶于水 D.有刺激性气味答案:B。 研析:氯气是一种黄绿色、有刺激性气味、能溶于水(1∶2)、易液化、密度比空气大的有毒气体。B选项不正确。 4.在配制物质的量浓度溶液的实验中,最后用胶头滴管定容后,液面正确的是
A. B. C. D.答案:B。 研析:在配制物质的量浓度溶液的实验中,定容后,溶液凹液面最低点应该与刻度线平齐。 5.下列叙述正确的是
A.1molO2的质量为32g·mol-1
B.1mol物质的质量等于该物质的相对分子质量或相对原子质量
C.SO42-的摩尔质量为96 g·mol-1
D.CO2的摩尔质量为44g答案:C。 研析:质量的单位是“g”、摩尔质量的单位是“g·mol-1”、式量的单位是“1”,A、B、D选项单位使用不正确。正确的说法为:1molO2的质量为32g;1mol物质的质量如果以“g”为单位,则在数值上等于该物质的式量;CO2的摩尔质量为44 g·mol-1。C无论数值,还是单位均正确。 6.下列物质属于纯净物的是
A.液氯 B.氯水 C.盐酸 D.漂粉精答案:A 研析:纯净物指只有一种成分组成的物质,液氯的成分为Cl2;氯水中含HCl、HClO、Cl2、H2O;盐酸为HCl的水溶液;漂粉精的成分为CaCl2和Ca(ClO)2 6、用Zn与实验室中的盐酸反应制取4.48L H2(标准状况)。
(1)如果选用所贴标签为2.0mol·L-1的盐酸,至少需该盐酸多少毫升?
(2)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升?研析:Zn + 2HCl = ZnCl2 + H2↑(1) 2 mol 22.4L n(HCl) 4.48L n(HCl)= 4.48L÷22.4L×2 mol =0.4 molV(HCl)= n(HCl)÷c(HCl)
= 0.4 mol÷2.0mol·L-1
= 0.2L
= 200mL(2)Zn + 2HCl = ZnCl2 + H2↑73g 22.4L m(HCl) 4.48L m(HCl)= 4.48L÷22.4L×73 g =14.6 g V(HCl) = m(HCl)÷W(HCl)÷ρ(HCl) = 14.6 g÷7% ÷1.043g·mL-1 = 200mL 谢谢!
化学研究的对象:物质组成、结构、性质、变化、制备和应用。
物理变化:没有生成其他物质的变化。
化学变化:生成了其他物质的变化,也叫化学反应。
物理性质:不需要发生化学反应就表现出来的性质,如颜色、状态、气味、熔点、沸点、硬度、密度等
化学性质:物质在化学变化中表现出来的性质。
分子:保持物质化学性质的最小粒子。
原子:化学变化中的最小粒子。知识点一、化学科学的创造性和实用性化学的特征:认识分子制造分子。知识点二、化学科学的形成和发展1661年,英国科学家波义耳提出了化学元素的概念,标志着近代化学的诞生。1771年,法国科学家拉瓦锡,建立燃烧氧化学说,使近代化学取得了革命性的进展。1803年,英国科学家道尔顿提出原子学说,为近代化学的发展奠定了坚实的基础。1869年,俄国科学家门捷列夫发现元素周期律,把化学元素及化合物纳入一个统一的理论系统。第二节 研究物质性质的方法和程序1、研究物质性质的基本方法:2、研究物质性质的程序:观察、实验、分类、比较。观察外观、预测性质、实验观察、解释现象、结论并归纳整合。一、理论知识二、元素化合物知识1、钠的性质用途及保存⑴钠的性质与水反应实验现象:浮、熔、游、响、红(2)钠的用途制Na2O2 制原子反应堆的导热剂k-Na合
制造钛、锆、铌等稀有金属 做光源(3)钠的保存少量的钠保存于煤油中2、氯气的性质和用途(1)氯气的性质氯水的成分:Cl2、H2O、HCl、HClO氯气和碱反应
Cl2 + NaOH = NaCl + NaClO + H2O
(制84消毒液)
2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
(制漂白粉)HClO的性质:
不稳定性:2HClO = 2HCl+O2↑
弱酸性、漂白性光照(2)氯气的用途:消毒 农药 盐酸 漂白剂第三节 物质的量1、基本概念
(1)摩尔:摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒。
(2)摩尔质量:1mol物质的质量叫摩尔质量,摩尔质量在数值上等于该物质的式量。
(3)标准状况下的气体摩尔体积:在标准状况(0℃、101.3kPa)下,1mol的任何气体的体积都大约是22.4L。
(4)物质的量浓度:以1L溶液中所含溶质物质的量来表示的溶液浓度叫物质的量浓度。2、各物理量之间的关系n =N/NA=m/Mn=V / Vm
=N/NA
=m / Mn=CB V n
=V / Vm
=N/NA
=m / M3、配制一定物质的量浓度溶液 操作细则以及实验仪器的选择主要是围绕减小实验误差来考虑。 关键在于:溶质的计量和转移、溶液体积的计量 其操作步骤为:计算、称量、溶解、转移、洗涤、定容、摇匀、装瓶。4、物质的量与化学反应
2H2 + O2 2H2O
从质量角度: 4g 32g 36g
从分子数角度: 2分子 1分子 2分子
从物质的量角度: 2mol 1mol 2mol
从标况下气体体积角度: 44.8L 22.4L
从任意相同条件气体体积角度: 2体积 1体积练习1.为中国近代化学发展做出突出贡献的科学家是
A.李四光 B.华罗更 C.候德榜 D.钱学森答案:B。 研析:题述四个选项中的科学家均为我国科学事业的发展做出了突出的贡献。其中,李四光是我国当代著名的地质学家;华罗更是著名的数学家;钱学森是著名的物理学家;候德榜被称为中国近代化学史上的第一颗明星,为中国化学工业发展做出卓越贡献,是中国近代化工工业的奠基人,他发明的联合制碱法为中华民族争得了荣誉。2.0.5mol Na2SO4中所含的Na+离子数为
A.3.01×1023 B.6.02×1023 C.0.5 D.1答案:B。 研析:
N(Na+)=n(Na2SO4)×2×NA
=0.5mol×2×6.02×1023mol-1
=6.02×1023。
3、下列各种物理性质中,对氯气来说不正确的是
A.黄绿色的气体 B.密度比空气小
C.能溶于水 D.有刺激性气味答案:B。 研析:氯气是一种黄绿色、有刺激性气味、能溶于水(1∶2)、易液化、密度比空气大的有毒气体。B选项不正确。 4.在配制物质的量浓度溶液的实验中,最后用胶头滴管定容后,液面正确的是
A. B. C. D.答案:B。 研析:在配制物质的量浓度溶液的实验中,定容后,溶液凹液面最低点应该与刻度线平齐。 5.下列叙述正确的是
A.1molO2的质量为32g·mol-1
B.1mol物质的质量等于该物质的相对分子质量或相对原子质量
C.SO42-的摩尔质量为96 g·mol-1
D.CO2的摩尔质量为44g答案:C。 研析:质量的单位是“g”、摩尔质量的单位是“g·mol-1”、式量的单位是“1”,A、B、D选项单位使用不正确。正确的说法为:1molO2的质量为32g;1mol物质的质量如果以“g”为单位,则在数值上等于该物质的式量;CO2的摩尔质量为44 g·mol-1。C无论数值,还是单位均正确。 6.下列物质属于纯净物的是
A.液氯 B.氯水 C.盐酸 D.漂粉精答案:A 研析:纯净物指只有一种成分组成的物质,液氯的成分为Cl2;氯水中含HCl、HClO、Cl2、H2O;盐酸为HCl的水溶液;漂粉精的成分为CaCl2和Ca(ClO)2 6、用Zn与实验室中的盐酸反应制取4.48L H2(标准状况)。
(1)如果选用所贴标签为2.0mol·L-1的盐酸,至少需该盐酸多少毫升?
(2)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升?研析:Zn + 2HCl = ZnCl2 + H2↑(1) 2 mol 22.4L n(HCl) 4.48L n(HCl)= 4.48L÷22.4L×2 mol =0.4 molV(HCl)= n(HCl)÷c(HCl)
= 0.4 mol÷2.0mol·L-1
= 0.2L
= 200mL(2)Zn + 2HCl = ZnCl2 + H2↑73g 22.4L m(HCl) 4.48L m(HCl)= 4.48L÷22.4L×73 g =14.6 g V(HCl) = m(HCl)÷W(HCl)÷ρ(HCl) = 14.6 g÷7% ÷1.043g·mL-1 = 200mL 谢谢!
