4.2电解池【人教版(2019)】高中化学选修1 同步练习(含答案解析)
文档属性
| 名称 | 4.2电解池【人教版(2019)】高中化学选修1 同步练习(含答案解析) |  | |
| 格式 | docx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-22 17:09:39 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
4.2电解池人教版(2019)高中化学选择性必修一同步练习
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
3.考试结束后,本试卷和答题卡一并交回。
第I卷(选择题)
一、单选题(本大题共7小题,共21.0分)
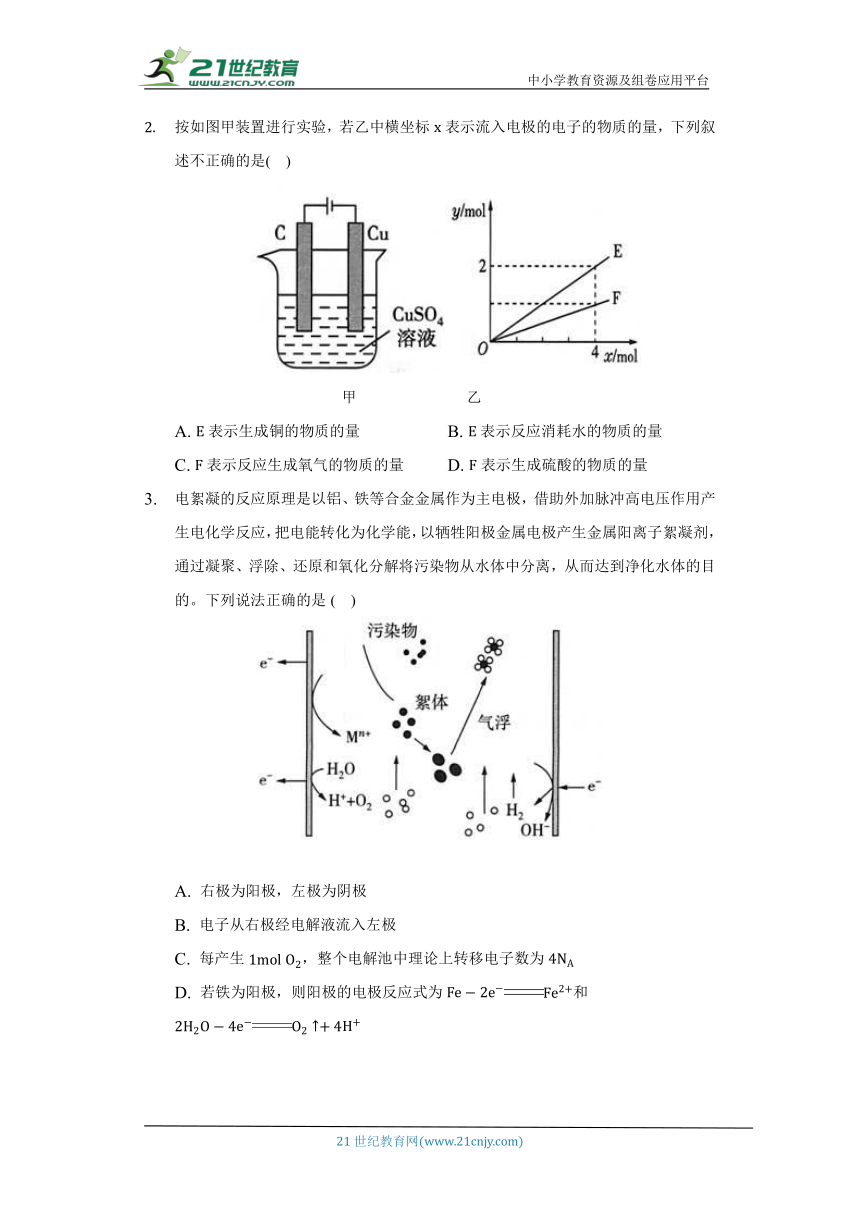
如图是工业电解饱和食盐水的装置示意图,下列有关说法不正确的是( )
A. 装置中的离子交换膜只能让阳离子通过,不能让阴离子通过
B. 装置中出口处的物质是氢气,出口处的物质是氯气
C. 除去杂质后的氢氧化钠溶液从出口处导出
D. 转移电子时产生氢气标准状况
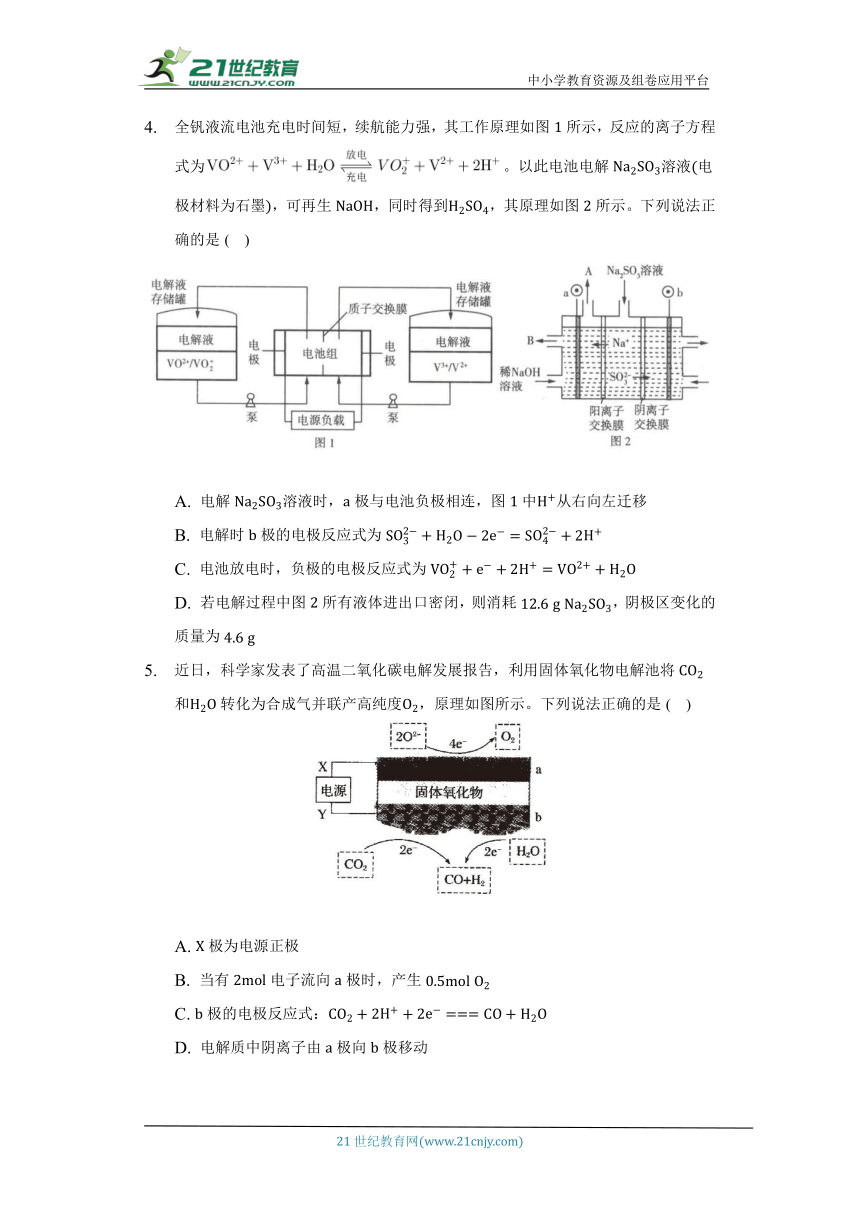
按如图甲装置进行实验,若乙中横坐标表示流入电极的电子的物质的量,下列叙述不正确的是( )
甲 乙
A. 表示生成铜的物质的量 B. 表示反应消耗水的物质的量
C. 表示反应生成氧气的物质的量 D. 表示生成硫酸的物质的量
电絮凝的反应原理是以铝、铁等合金金属作为主电极,借助外加脉冲高电压作用产生电化学反应,把电能转化为化学能,以牺牲阳极金属电极产生金属阳离子絮凝剂,通过凝聚、浮除、还原和氧化分解将污染物从水体中分离,从而达到净化水体的目的。下列说法正确的是( )
A. 右极为阳极,左极为阴极
B. 电子从右极经电解液流入左极
C. 每产生,整个电解池中理论上转移电子数为
D. 若铁为阳极,则阳极的电极反应式为和
全钒液流电池充电时间短,续航能力强,其工作原理如图所示,反应的离子方程式为。以此电池电解溶液电极材料为石墨,可再生,同时得到,其原理如图所示。下列说法正确的是( )
A. 电解溶液时,极与电池负极相连,图中从右向左迁移
B. 电解时极的电极反应式为
C. 电池放电时,负极的电极反应式为
D. 若电解过程中图所有液体进出口密闭,则消耗,阴极区变化的质量为
近日,科学家发表了高温二氧化碳电解发展报告,利用固体氧化物电解池将和转化为合成气并联产高纯度,原理如图所示。下列说法正确的是( )
A. 极为电源正极
B. 当有电子流向极时,产生
C. 极的电极反应式:
D. 电解质中阴离子由极向极移动
三室式电渗析法处理含废水的原理如图所示,采用惰性电极,、均为离子交换膜,在直流电场的作用下,两膜中间的和可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是( )
A. 通电后中间隔室的向正极迁移,正极区溶液增大
B. 该法在处理含废水时可以得到和产品
C. 负极反应为,负极区溶液降低
D. 当电路中通过电子的电荷量时,会有的生成
电解饱和食盐水为饱和食盐水,若生成,则下列说法正确的是。( )
A. 在极生成
B. 在极生成
C. 在极生成
D. 在极生成
第II卷(非选择题)
二、流程题(本大题共1小题,共8.0分)
某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如图所示:
步骤的作用是清洗废铁屑表面的油污,其中加热的目的是 。
写出步骤中生成的离子方程式: 。写一个即可
步骤中“氯气”不引入杂质但有毒,可以用 代替填化学式。
溶液中只含有而不含,可证明该事实的实验操作是 。
步骤产生金属铜的化学方程式为 。
三、实验题(本大题共1小题,共10.0分)
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,、、、、、都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在极附近显红色。试回答下列问题:
电源极的名称是________。
甲装置中电解反应的总化学方程式是_____________________________。
如果收集乙装置中产生的气体,两种气体的体积比是________。
欲用丙装置精炼铜,应该是____填“纯铜”或“粗铜”,电解液的成分是____。
接通电源后装置丁中的现象是_____________________________。
在实验室电解的溶液,通电一段时间后溶液中设电解时溶液的体积变化忽略不计,阴极产生________标况气体,溶液中的浓度为__________。
四、简答题(本大题共2小题,共16.0分)
电解原理在物质制备、污水处理等领域应用广泛。以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图所示。
电源负极为________填“”或“”,写出阳极的电极反应式:________________。
若参加反应的为标准状况,制得的碳酸二甲酯的质量为________。
高剂量的亚硝酸盐有很大毒性,电化学降解的原理如图所示。
阴极的电极反应式为_____________________________。
若电解过程中转移了电子,则质子交换膜两侧电解液的质量变化差为________。
和都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
阴极上的反应式为 。
若生成的乙烯和乙烷的体积比为,则消耗的和体积比为 。
用如图所示装置除去含、废水中的时,控制溶液为,阳极产生的将氧化为两种无污染的气体。阳极的电极反应式是 ,阴极的电极反应式是 ,除去的反应为 。
电解制备,其工作原理如图所示。为使电解产物全部转化为,需补充物质。是 ,说明理由: 。
可由与次氯酸钠溶液反应制得,反应的离子方程式为 ;也可以通过石墨为电极,和的混合溶液为电解液电解制取。阳极发生的电极反应式为 ,阴极上观察到的现象是 ;若电解液中不加入,阴极发生的电极反应式为 ,这样做的主要缺点是 。
五、推断题(本大题共1小题,共10.0分)
、、、、是原子序数依次增大的短周期主族元素。的最外层电子数是内层电子数的两倍,可用于呼吸面具,的主族序数与周期数相等,的氢化物的分子式为。
在周期表中的位置是 , 的原子结构示意图是 。
的结构式是 ,的电子式是
溶液呈 性填“酸”“碱”或“中”,原因是用离子方程式表示 。
某传感器可以检测空气中的含量,工作原理如图所示。则其阴极电极反应式 。
答案和解析
1.【答案】
【解析】离子交换膜有选择性,根据题图可知,该离子交换膜只能让阳离子通过,不能让阴离子通过,故A正确;
根据题图知,左边电极上氯离子放电生成氯气,右边电极上氢离子放电生成氢气,所以装置中出口处的物质是氯气,出口处的物质是氢气,故B错误;
根据题图知,左边电极上氯离子放电生成氯气,右边电极上氢离子放电生成氢气,右边氢氧根离子浓度增加,碱性增强,所以除去杂质后的氢氧化钠溶液从出口处导出,故C正确;
电解总反应式为,转移电子时产生氢气,转移电子时产生氢气,标准状况下的体积是,故D正确。
2.【答案】
【解析】由甲图可知,为阳极,电极反应式为;为阴极,电极反应式为;总反应式为。结合乙图可知,转移电子生成和。
对,由电子与生成物的物质的量的关系可知,表示生成铜的物质的量。
对,由总反应结合电子与生成物的物质的量的关系可知,表示反应消耗水的物质的量。
对,由电子与生成物的物质的量的关系可知,表示反应生成氧气的物质的量。
错,由总反应结合电子与反应物的物质的量的关系可知,不能表示生成硫酸的物质的量。
3.【答案】
【解析】错,该装置是把电能转化为化学能的电解池,电子流入的电极为阴极,电子流出的电极为阳极,所以左极为阳极,右极为阴极;
错,电子不能通过电解质溶液,电解质溶液中通过离子的定向移动,在两极得失电子形成电流;
错,每产生,根据电极反应,代表金属和知,转移电子的物质的量大于,转移电子数大于;
对,根据题意,若铁为阳极,则阳极电极反应式为和。
故选:。
4.【答案】
【解析】A.由题图可知,电解溶液时向左迁移,电解池中阳离子向阴极迁移,则极为阴极,应与电池负极相连;由得,放电时,,化合价升高,所以题图中左侧电极为负极,右侧电极为正极,原电池中阳离子由负极向正极迁移,即题图中从左向右迁移,A错误。
B.电解时移向极阳极,失电子生成,B正确。
C.电池放电时,负极上发生失电子的氧化反应,电极反应式为,C错误。
D.消耗时,转移,有移入阴极区,同时在阴极得电子生成氢气,即阴极区变化的质量为,D错误。
5.【答案】
【解析】略
6.【答案】
【解析】电解池中,阴离子向阳极迁移,因此向阳极正极迁移,根据离子放电顺序,溶液中水电离出的在阳极正极失去电子发生氧化反应生成氧气,由于两端隔室中离子被阻挡不能进入中间隔室,因此水电离出的保留在正极区,最终导致该极区浓度增大,减小,项错误。
由于两端隔室中离子被阻挡不能进入中间隔室,因此在阳极正极区浓度增大,同时中间隔室的将迁移到正极区,最终会生成;在阴极负极,溶液中水电离出的得到电子发生还原反应生成氢气,水电离出的保留在该极区,最终导致该极区浓度增大,同时中间隔室的将迁移到负极区,最终会生成,项正确。
阴极负极电极反应式为,项错误。
每生成要转移电子,因此当电路中通过电子的电荷量时,生成的应为,项错误。
7.【答案】
【解析】由装置图可知为电解池的阳极,电极反应式为,为阴极,电极反应式为。电极为阴极,生成的是,项错误;生成,同时生成,项正确;电极为电解池阳极,生成,同时生成,项错误;阴极附近放电促进水电离,溶液中浓度增大,在极生成,项错误。
8.【答案】促进碳酸钠的水解,提高清洗效率
或
取少量溶液于试管中,先加溶液,不显红色,再而氯水后显红色
【解析】
溶液因水解呈碱性,加热能促进水解,使溶液碱性增强,从而提高油污的清洗效率。
与溶液或与盐酸反应均能生成。
步骤通入是为了将溶液中的氧化成,可用绿色氧化剂代替有毒的。
向溶液中加入溶液无明显现象,滴入氯水后出现红色,则可证明溶液中仅含而无。
步骤电解时,阳极和阴极分别为和放电,相当于电解溶液生成和。
9.【答案】正极;
;
:;
粗铜; 硫酸铜溶液;
极附近红褐色变深;
;。
【解析】
【分析】
本题考查电解原理的应用,侧重考查电解和电镀,掌握电极反应式以及化学方程式为解题关键,难度不大。
【解答】
向乙中滴入酚酞试液,在极附近显红色,说明该极上氢离子放电,则该电极是阴极,故E电极是阳极,电极是阴极,电极是阳极,电极是阳极,电极是阴极,电极是阳极,是阴极,是电源的正极,是原电池的负极,
故答案为:正极;
电解氯化铜溶液时的阳极是氯离子放电,阴极是铜离子放电,所以电解反应为:,
故答案为:;
电解饱和食盐水的电解原理是:,产生的氢气和氯气体积比为:,
故答案为::;
电解精炼铜时,粗铜作阳极,纯铜作阴极,含有铜离子的盐作电解质即可,
故答案为:粗铜;硫酸铜溶液;
根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的粒子会向阴极即极移动,所以极附近红褐色变深,
故答案为:极附近红褐色变深;
电解饱和食盐水时,阳极上是氯离子失电子,电极反应为:,阴极上是氢离子得电子,,通电一段时间后溶液中为,阴极产生,,
标况下的体积是:,
反应的氯离子的物质的量,
的溶液剩余的物质的量为:,
浓度,
故答案为:;。
10.【答案】
【解析】由题图知,右侧得电子被还原,则右侧为阴极室,为电源负极,为电源正极。左侧阳极室中的由价升高为价,则阳极反应式为。
阴极反应式主,总反应式为,则。
由题图知,右侧氮元素的化合价由降低到,发生还原反应,据此判断右侧为阴极区,则阴极反应式为。
转移电子时,有由左侧穿过质子交换膜进入右侧,。
左侧阳极区放氧生酸:
转移电子时,有由左侧穿过质子交换膜进入右侧,。。
11.【答案】;
;;
;根据反应,电解产生的多
;;石墨上包上红色镀层;;不能有效利用
【解析】结合题图可知在阴极发生还原反应生成,即阴极上的反应式为。设生成和的物质的量分别为和,则反应中转移电子的物质的量为,根据碳原子守恒,可知反应的为,,转移电子,需消耗,则反应中消耗和的体积比为。
在阳极被氧化为,阳极的电极反应式为 ;阴极为水得电子生成氢气,阴极的电极反应式为;根据题目信息提示,除去的反应为。
由题图知,阴极的被还原为,阳极的被氧化为,总反应方程式为:,补充适量可以使电解产生的转化为。由题意知,作还原剂,作氧化剂,反应的离子方程式为;根据阳极发生氧化反应知,阳极反应式为,阴极发生还原反应,放电生成,现象为石墨上包上红色镀层;若电解液中不加入,则溶液中的放电,这样就不能很好地转化为,导致的利用率降低。
12.【答案】第三周期第Ⅵ族
碱
【解析】
【分析】
本题考查物质结构与性质及电化学知识,考查的学科素养是化学观念、思维方法,难度一般,解题的关键是对元素的正确推断和对基础知识的灵活运用。
【解答】
的最外层电子数为内层电子数的两倍,则为能与水和二氧化碳反应生成氧气,常用于呼吸面具作氧气的来源,则为,为、、、、是原子序数依次增大的短周期主族元素,的主族序数与周期数相等,则为的氢化物的分子式为,则为。
为号元素,在周期表中位于第三周期第Ⅵ族为号元素,其原子结构示意图。
和的结构相似,均为直线形,其结构式为 为离子化合物,其电子式与相似,可表示为。
为强碱弱酸盐,其溶液因水解显碱性,其水解方程式为:。
电解池中阴极发生还原反应,由电解装置图可知电极为阴极,
其电极反应式为:。
第14页,共15页
21世纪教育网(www.21cnjy.com)
4.2电解池人教版(2019)高中化学选择性必修一同步练习
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
3.考试结束后,本试卷和答题卡一并交回。
第I卷(选择题)
一、单选题(本大题共7小题,共21.0分)
如图是工业电解饱和食盐水的装置示意图,下列有关说法不正确的是( )
A. 装置中的离子交换膜只能让阳离子通过,不能让阴离子通过
B. 装置中出口处的物质是氢气,出口处的物质是氯气
C. 除去杂质后的氢氧化钠溶液从出口处导出
D. 转移电子时产生氢气标准状况
按如图甲装置进行实验,若乙中横坐标表示流入电极的电子的物质的量,下列叙述不正确的是( )
甲 乙
A. 表示生成铜的物质的量 B. 表示反应消耗水的物质的量
C. 表示反应生成氧气的物质的量 D. 表示生成硫酸的物质的量
电絮凝的反应原理是以铝、铁等合金金属作为主电极,借助外加脉冲高电压作用产生电化学反应,把电能转化为化学能,以牺牲阳极金属电极产生金属阳离子絮凝剂,通过凝聚、浮除、还原和氧化分解将污染物从水体中分离,从而达到净化水体的目的。下列说法正确的是( )
A. 右极为阳极,左极为阴极
B. 电子从右极经电解液流入左极
C. 每产生,整个电解池中理论上转移电子数为
D. 若铁为阳极,则阳极的电极反应式为和
全钒液流电池充电时间短,续航能力强,其工作原理如图所示,反应的离子方程式为。以此电池电解溶液电极材料为石墨,可再生,同时得到,其原理如图所示。下列说法正确的是( )
A. 电解溶液时,极与电池负极相连,图中从右向左迁移
B. 电解时极的电极反应式为
C. 电池放电时,负极的电极反应式为
D. 若电解过程中图所有液体进出口密闭,则消耗,阴极区变化的质量为
近日,科学家发表了高温二氧化碳电解发展报告,利用固体氧化物电解池将和转化为合成气并联产高纯度,原理如图所示。下列说法正确的是( )
A. 极为电源正极
B. 当有电子流向极时,产生
C. 极的电极反应式:
D. 电解质中阴离子由极向极移动
三室式电渗析法处理含废水的原理如图所示,采用惰性电极,、均为离子交换膜,在直流电场的作用下,两膜中间的和可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是( )
A. 通电后中间隔室的向正极迁移,正极区溶液增大
B. 该法在处理含废水时可以得到和产品
C. 负极反应为,负极区溶液降低
D. 当电路中通过电子的电荷量时,会有的生成
电解饱和食盐水为饱和食盐水,若生成,则下列说法正确的是。( )
A. 在极生成
B. 在极生成
C. 在极生成
D. 在极生成
第II卷(非选择题)
二、流程题(本大题共1小题,共8.0分)
某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如图所示:
步骤的作用是清洗废铁屑表面的油污,其中加热的目的是 。
写出步骤中生成的离子方程式: 。写一个即可
步骤中“氯气”不引入杂质但有毒,可以用 代替填化学式。
溶液中只含有而不含,可证明该事实的实验操作是 。
步骤产生金属铜的化学方程式为 。
三、实验题(本大题共1小题,共10.0分)
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,、、、、、都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在极附近显红色。试回答下列问题:
电源极的名称是________。
甲装置中电解反应的总化学方程式是_____________________________。
如果收集乙装置中产生的气体,两种气体的体积比是________。
欲用丙装置精炼铜,应该是____填“纯铜”或“粗铜”,电解液的成分是____。
接通电源后装置丁中的现象是_____________________________。
在实验室电解的溶液,通电一段时间后溶液中设电解时溶液的体积变化忽略不计,阴极产生________标况气体,溶液中的浓度为__________。
四、简答题(本大题共2小题,共16.0分)
电解原理在物质制备、污水处理等领域应用广泛。以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图所示。
电源负极为________填“”或“”,写出阳极的电极反应式:________________。
若参加反应的为标准状况,制得的碳酸二甲酯的质量为________。
高剂量的亚硝酸盐有很大毒性,电化学降解的原理如图所示。
阴极的电极反应式为_____________________________。
若电解过程中转移了电子,则质子交换膜两侧电解液的质量变化差为________。
和都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
阴极上的反应式为 。
若生成的乙烯和乙烷的体积比为,则消耗的和体积比为 。
用如图所示装置除去含、废水中的时,控制溶液为,阳极产生的将氧化为两种无污染的气体。阳极的电极反应式是 ,阴极的电极反应式是 ,除去的反应为 。
电解制备,其工作原理如图所示。为使电解产物全部转化为,需补充物质。是 ,说明理由: 。
可由与次氯酸钠溶液反应制得,反应的离子方程式为 ;也可以通过石墨为电极,和的混合溶液为电解液电解制取。阳极发生的电极反应式为 ,阴极上观察到的现象是 ;若电解液中不加入,阴极发生的电极反应式为 ,这样做的主要缺点是 。
五、推断题(本大题共1小题,共10.0分)
、、、、是原子序数依次增大的短周期主族元素。的最外层电子数是内层电子数的两倍,可用于呼吸面具,的主族序数与周期数相等,的氢化物的分子式为。
在周期表中的位置是 , 的原子结构示意图是 。
的结构式是 ,的电子式是
溶液呈 性填“酸”“碱”或“中”,原因是用离子方程式表示 。
某传感器可以检测空气中的含量,工作原理如图所示。则其阴极电极反应式 。
答案和解析
1.【答案】
【解析】离子交换膜有选择性,根据题图可知,该离子交换膜只能让阳离子通过,不能让阴离子通过,故A正确;
根据题图知,左边电极上氯离子放电生成氯气,右边电极上氢离子放电生成氢气,所以装置中出口处的物质是氯气,出口处的物质是氢气,故B错误;
根据题图知,左边电极上氯离子放电生成氯气,右边电极上氢离子放电生成氢气,右边氢氧根离子浓度增加,碱性增强,所以除去杂质后的氢氧化钠溶液从出口处导出,故C正确;
电解总反应式为,转移电子时产生氢气,转移电子时产生氢气,标准状况下的体积是,故D正确。
2.【答案】
【解析】由甲图可知,为阳极,电极反应式为;为阴极,电极反应式为;总反应式为。结合乙图可知,转移电子生成和。
对,由电子与生成物的物质的量的关系可知,表示生成铜的物质的量。
对,由总反应结合电子与生成物的物质的量的关系可知,表示反应消耗水的物质的量。
对,由电子与生成物的物质的量的关系可知,表示反应生成氧气的物质的量。
错,由总反应结合电子与反应物的物质的量的关系可知,不能表示生成硫酸的物质的量。
3.【答案】
【解析】错,该装置是把电能转化为化学能的电解池,电子流入的电极为阴极,电子流出的电极为阳极,所以左极为阳极,右极为阴极;
错,电子不能通过电解质溶液,电解质溶液中通过离子的定向移动,在两极得失电子形成电流;
错,每产生,根据电极反应,代表金属和知,转移电子的物质的量大于,转移电子数大于;
对,根据题意,若铁为阳极,则阳极电极反应式为和。
故选:。
4.【答案】
【解析】A.由题图可知,电解溶液时向左迁移,电解池中阳离子向阴极迁移,则极为阴极,应与电池负极相连;由得,放电时,,化合价升高,所以题图中左侧电极为负极,右侧电极为正极,原电池中阳离子由负极向正极迁移,即题图中从左向右迁移,A错误。
B.电解时移向极阳极,失电子生成,B正确。
C.电池放电时,负极上发生失电子的氧化反应,电极反应式为,C错误。
D.消耗时,转移,有移入阴极区,同时在阴极得电子生成氢气,即阴极区变化的质量为,D错误。
5.【答案】
【解析】略
6.【答案】
【解析】电解池中,阴离子向阳极迁移,因此向阳极正极迁移,根据离子放电顺序,溶液中水电离出的在阳极正极失去电子发生氧化反应生成氧气,由于两端隔室中离子被阻挡不能进入中间隔室,因此水电离出的保留在正极区,最终导致该极区浓度增大,减小,项错误。
由于两端隔室中离子被阻挡不能进入中间隔室,因此在阳极正极区浓度增大,同时中间隔室的将迁移到正极区,最终会生成;在阴极负极,溶液中水电离出的得到电子发生还原反应生成氢气,水电离出的保留在该极区,最终导致该极区浓度增大,同时中间隔室的将迁移到负极区,最终会生成,项正确。
阴极负极电极反应式为,项错误。
每生成要转移电子,因此当电路中通过电子的电荷量时,生成的应为,项错误。
7.【答案】
【解析】由装置图可知为电解池的阳极,电极反应式为,为阴极,电极反应式为。电极为阴极,生成的是,项错误;生成,同时生成,项正确;电极为电解池阳极,生成,同时生成,项错误;阴极附近放电促进水电离,溶液中浓度增大,在极生成,项错误。
8.【答案】促进碳酸钠的水解,提高清洗效率
或
取少量溶液于试管中,先加溶液,不显红色,再而氯水后显红色
【解析】
溶液因水解呈碱性,加热能促进水解,使溶液碱性增强,从而提高油污的清洗效率。
与溶液或与盐酸反应均能生成。
步骤通入是为了将溶液中的氧化成,可用绿色氧化剂代替有毒的。
向溶液中加入溶液无明显现象,滴入氯水后出现红色,则可证明溶液中仅含而无。
步骤电解时,阳极和阴极分别为和放电,相当于电解溶液生成和。
9.【答案】正极;
;
:;
粗铜; 硫酸铜溶液;
极附近红褐色变深;
;。
【解析】
【分析】
本题考查电解原理的应用,侧重考查电解和电镀,掌握电极反应式以及化学方程式为解题关键,难度不大。
【解答】
向乙中滴入酚酞试液,在极附近显红色,说明该极上氢离子放电,则该电极是阴极,故E电极是阳极,电极是阴极,电极是阳极,电极是阳极,电极是阴极,电极是阳极,是阴极,是电源的正极,是原电池的负极,
故答案为:正极;
电解氯化铜溶液时的阳极是氯离子放电,阴极是铜离子放电,所以电解反应为:,
故答案为:;
电解饱和食盐水的电解原理是:,产生的氢气和氯气体积比为:,
故答案为::;
电解精炼铜时,粗铜作阳极,纯铜作阴极,含有铜离子的盐作电解质即可,
故答案为:粗铜;硫酸铜溶液;
根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的粒子会向阴极即极移动,所以极附近红褐色变深,
故答案为:极附近红褐色变深;
电解饱和食盐水时,阳极上是氯离子失电子,电极反应为:,阴极上是氢离子得电子,,通电一段时间后溶液中为,阴极产生,,
标况下的体积是:,
反应的氯离子的物质的量,
的溶液剩余的物质的量为:,
浓度,
故答案为:;。
10.【答案】
【解析】由题图知,右侧得电子被还原,则右侧为阴极室,为电源负极,为电源正极。左侧阳极室中的由价升高为价,则阳极反应式为。
阴极反应式主,总反应式为,则。
由题图知,右侧氮元素的化合价由降低到,发生还原反应,据此判断右侧为阴极区,则阴极反应式为。
转移电子时,有由左侧穿过质子交换膜进入右侧,。
左侧阳极区放氧生酸:
转移电子时,有由左侧穿过质子交换膜进入右侧,。。
11.【答案】;
;;
;根据反应,电解产生的多
;;石墨上包上红色镀层;;不能有效利用
【解析】结合题图可知在阴极发生还原反应生成,即阴极上的反应式为。设生成和的物质的量分别为和,则反应中转移电子的物质的量为,根据碳原子守恒,可知反应的为,,转移电子,需消耗,则反应中消耗和的体积比为。
在阳极被氧化为,阳极的电极反应式为 ;阴极为水得电子生成氢气,阴极的电极反应式为;根据题目信息提示,除去的反应为。
由题图知,阴极的被还原为,阳极的被氧化为,总反应方程式为:,补充适量可以使电解产生的转化为。由题意知,作还原剂,作氧化剂,反应的离子方程式为;根据阳极发生氧化反应知,阳极反应式为,阴极发生还原反应,放电生成,现象为石墨上包上红色镀层;若电解液中不加入,则溶液中的放电,这样就不能很好地转化为,导致的利用率降低。
12.【答案】第三周期第Ⅵ族
碱
【解析】
【分析】
本题考查物质结构与性质及电化学知识,考查的学科素养是化学观念、思维方法,难度一般,解题的关键是对元素的正确推断和对基础知识的灵活运用。
【解答】
的最外层电子数为内层电子数的两倍,则为能与水和二氧化碳反应生成氧气,常用于呼吸面具作氧气的来源,则为,为、、、、是原子序数依次增大的短周期主族元素,的主族序数与周期数相等,则为的氢化物的分子式为,则为。
为号元素,在周期表中位于第三周期第Ⅵ族为号元素,其原子结构示意图。
和的结构相似,均为直线形,其结构式为 为离子化合物,其电子式与相似,可表示为。
为强碱弱酸盐,其溶液因水解显碱性,其水解方程式为:。
电解池中阴极发生还原反应,由电解装置图可知电极为阴极,
其电极反应式为:。
第14页,共15页
21世纪教育网(www.21cnjy.com)
