探索酸的性质(全)
图片预览









文档简介
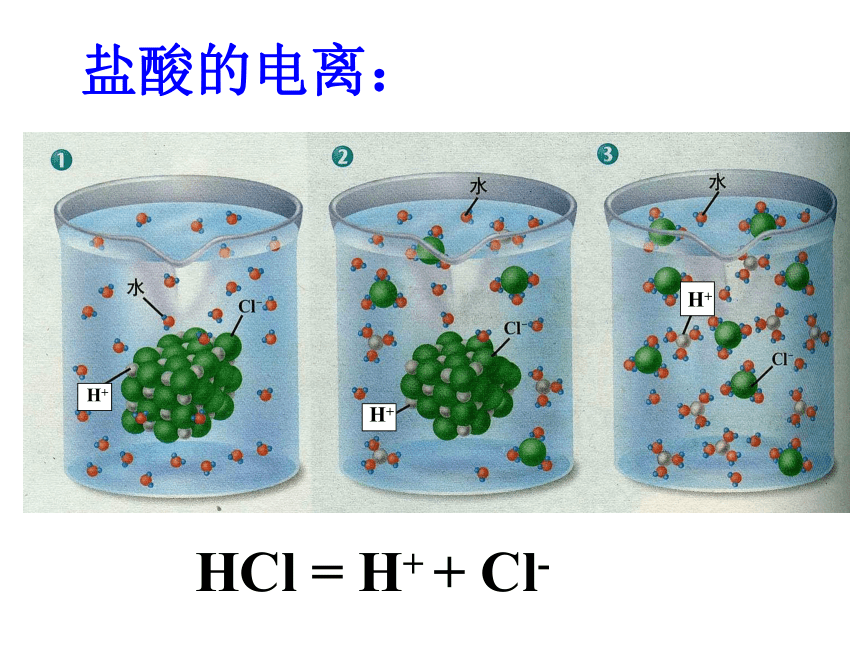
课件43张PPT。酸。一、什么是酸 你若有呕吐的经历,你会感受到胃液是酸的。在日常生活中,有酸味的物质还有醋、放置时间过长的面包、杏、苹果、橘子等。我们知道:食醋——醋酸,胃液——盐酸,柠檬、柑橘等水果中含有柠檬酸。含酸的水果第二节 探索酸的性质http://player.ku6.com/refer/tTMEBhPqUg66R94xVh6ldQ../v.swf这里是网址^v^ 这些物质在水中电离时,生成的阳离子全部都是氢离子(H+)。那么,为什么说这些物质都是酸呢?盐酸的电离:HCl = H+ + Cl-H+H+H+盐酸:
硝酸:
硫酸:HCI = H + + CI-电离方程式:H NO3 = H + + NO3-H2SO4 = 2H + + SO 42-
电离通式:酸= H + 酸根阴离子1、强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
2、弱酸:醋酸(CH3COOH)、碳酸(H2co3)第二节 探索酸的性质一、什么是酸:在水中电离时,生成的阳离子全部都是氢离子(H+)的化合物。板书:pH>7,碱性; pH =7,中性;pH<7,酸性。那么,你知道还有什么方法可以测定物质的酸碱性?二、酸碱指示剂:石蕊遇酸变红,遇碱变蓝;
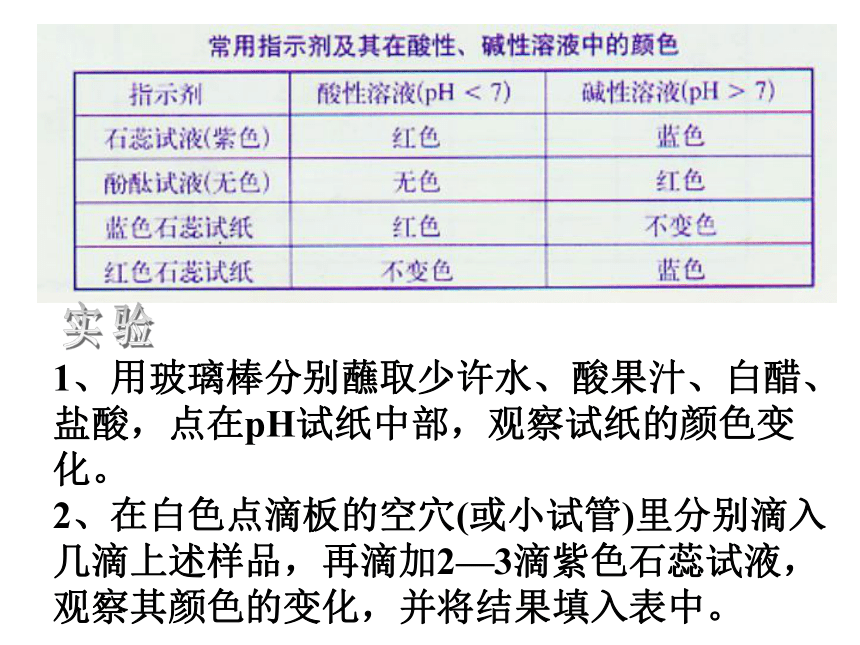
酚酞遇酸不变色,遇碱变红。1、用玻璃棒分别蘸取少许水、酸果汁、白醋、盐酸,点在pH试纸中部,观察试纸的颜色变化。
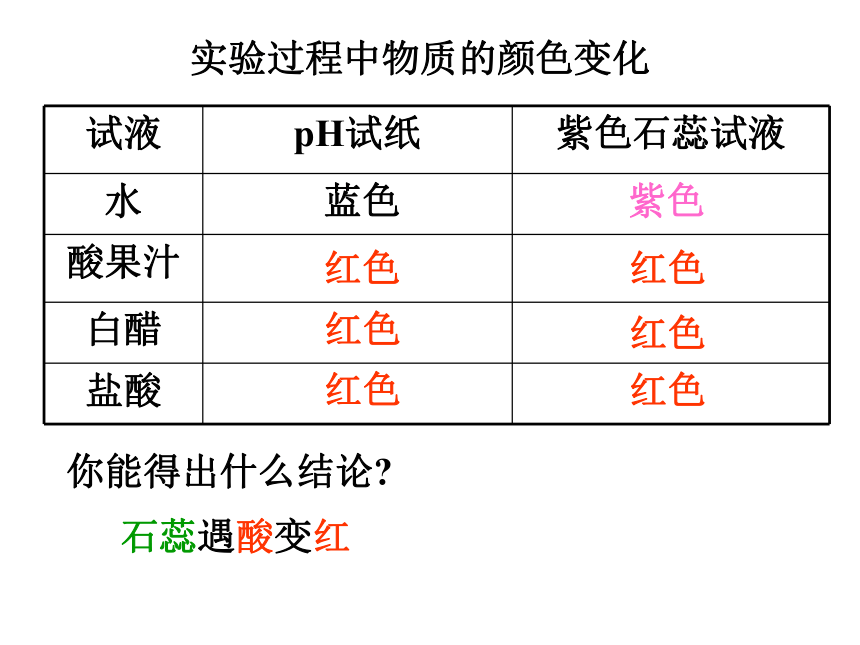
2、在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2—3滴紫色石蕊试液,观察其颜色的变化,并将结果填入表中。实验 实验过程中物质的颜色变化蓝色紫色红色红色红色红色红色红色你能得出什么结论?石蕊遇酸变红阅读P8自制酸碱指示剂1、下列物质不属于酸的是 ( )
A、HNO3 B、NaHCO3
C、H3PO4 D、HI
2、用简单的方法区别水和硫酸,并写出实验步骤。
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?B练习:思考 胃酸过多的病人常服用一种叫“胃舒平”的药片来治疗,药片的主要成份是氢氧化铝,为什么能用它来治疗胃酸过多呢? 3 HCI + Al(OH)3 〓 AlCI3 + 3H2O 请用化学方程式表示: 酸 + 碱 〓 盐 + 水 三、在氢氧化钠溶液中滴入2滴紫色石蕊试液,溶液呈________色;再逐滴滴入盐酸,溶液颜色有什么变化?______________________。蓝色由蓝色逐渐变成紫色 HCI + NaOH = NaCI + H2O 酸 + 碱 〓 盐 + 水 实验探究1第2课时盐酸有什么性质:如果继续滴入HCl呢?三、盐酸有哪些性质?实验探究2 a、把鸡蛋壳放入盛有盐酸的试管中,将燃着的火柴伸入试管口,你看到什么现象?
_________________________________.蛋壳表面产生气泡,燃着的木条伸入后会熄灭 2HCI + CaCO3 = CaCI2 + H2O + CO2↑ 酸 + 盐 = 新盐 + 新酸b、碳酸钠和盐酸的反应,产生的气体通过澄清石灰水,观察现象?HCI + Na2CO3 = NaCI + H2O + CO2 ↑ 酸 + 盐 = 新盐 + 新酸*? CO32-的检验:加盐酸,能产生使澄清石灰水变浑浊的气体(二氧化碳)
Ca(OH)2 + CO2 = CaCO3 ↓ + H2O三、盐酸有哪些性质?实验探究3 a、向盛有一枚生锈的铁钉的试管中加入盐酸,振荡,过会儿观察现象?
_______________________________________. 铁锈消失,溶液变成黄色 6HCI + Fe2O3 = 2FeCI3+3H2O 盐酸 +金属氧化物= 盐 + 水红棕色 黄色b、向盛有少量氧化铜粉末的试管中加入盐酸,微微加热,观察现象?
______________________________________ 黑色粉末消失,溶液变成蓝色2HCI + CuO = CuCI2 + H2O 盐酸 +金属氧化物= 盐 + 水黑色 蓝色 上述探究实验3中,除了铁锈消失外,还可以观察到什么现象?___________________ 探究实验4 铁钉表面产生气泡提出问题: 气体是否是盐酸和金属铁反应生成的?建立假设:____________________________.实验验证:结论:酸可以和某些活泼金属反应,
生成盐和氢气 2HCI + Fe = FeCI2 + H2↑酸 +金属 = 盐 + 氢气谁来归纳一下,盐酸主要有哪些
化学性质,能跟哪些物质反应。小结1、 酸能使紫色的石蕊变红,无色酚酞不变色。2、 酸 + 碱 〓 盐 + 水 3、酸 + 盐 = 新盐 + 新酸4、 盐酸 +金属氧化物= 盐 + 水5、酸 +金属 = 盐 + 氢气 3 HCI + Al(OH)3 〓 AlCI3 + 3H2O2HCI + CaCO3 = CaCI2 + H2O + CO2↑ 6HCI + Fe2O3 = 2FeCI3+3H2O2HCI + CuO = CuCI2 + H2O 2HCI + Fe = FeCI2 + H2↑三、硫酸有哪些性质?-H2SO4第3课时实验探究5 稀硫酸分别滴入盛有锌、氧化铁、氧化铜、氢氧化铜、氯化钡溶液的试管中,发现 :_____________________________。1、 Zn + H2SO4 = ZnSO4 + H2 ↑2、 Fe2O3 + H2SO4= Fe2(SO4)3+ H2 O3、CuO + H2SO4 =CuSO4+ H2 O4、Cu(OH)2 + H2SO4 = CuSO4 + 2H2 O5、BaCI2 + H2SO4 = BaSO4 ↓+ 2HCI你能说出硫酸有哪些性质?从盐酸、硫酸的实验中可以看到物质发生反应的证据有哪些?1、溶液颜色变化2、产生气体3、产生沉淀4、性质变化你能归纳出酸的一些共性吗?P12总结:
1、 酸能使指示剂变色
2、? 能与碱反应生成盐和水
3、 能与某些金属氧化物反应生成盐和水
4、 能与某些金属反应生成盐和氢气
5、能与盐反应生成新的盐和新的酸
1、下列物质中,能除去铁制品表面铁锈的是 ( )
A、稀硫酸 B、水 C、氢氧化钠溶液 D、硫酸铜溶液
2、写出下列方程式,并写出反应类型
反应类型
(1)Fe+H2SO4 ==___________________; _______________
(2)CuO+H2SO4==__________________; _______________
(3)2NaOH+H2SO4==________________; ______________
(4)H2SO4+BaCl2== _________________; _______________
(5)HCl+AgNO3==___________________; _______________
1、盐酸在工农业生产和日常生活中用途很大。下列各项用途是利用盐酸的哪些性质?试写出有关反应的化学方程式。
(1)电镀前用盐酸清洗钢铁表面的铁锈。
(2)制革工业中用熟石灰脱毛后,剩余的熟石灰[Ca(OH)2]用盐酸来除去。
(3)用稀盐酸清除锅炉中的水垢[主要成分为CaCO3,和Mg(OH)2]。
2、怎样鉴别3瓶分别盛有水、稀盐酸、稀硫酸的无色液体?
3、向稀盐酸中滴加石蕊试液,溶液显______色,稀盐酸的PH______7(填<、>、=)
4、鉴定某酸溶液为盐酸时需用试剂是:______ 盐酸的个性观 察1、物性:纯净的浓盐酸是无色的液体,有刺激性气味。工业品浓盐酸因含有杂质而带黄色。常用的浓盐酸中HCl的质量分数约为37%~38%,密度是1. 19g/㎝3 。一、浓盐酸的个性【猜一猜】
白雾是什么?怎样形成的?你猜想的依据是什么?2、浓盐酸具有挥发性。从浓盐酸挥发出来的氯化氢气体跟空气里的水蒸气接触,形成盐酸小液滴,从而形成白雾。【结论】P13观察3:瓶口出现白雾;盐酸具有刺激性气味。闻气体气味的方法雾是液滴悬浮在空气中的现象实 验1、稀盐酸中滴加硝酸银溶液,观察现象: HCl+AgNO3=AgCl↓+HNO3产生AgCl白色沉淀就凭这个实验能证明HCl的存在吗?2、Na2CO3中滴加硝酸银溶液,观察现象:产生Ag2CO3白色沉淀Na2CO3+ 2AgNO3=Ag2CO3 ↓+2NaNO3 CI-的检验:先加稀AgNO3出现沉淀,再加HNO3沉淀不消失。怎样才能判断生成的是AgCl沉淀,而不是Ag2CO3沉淀?在上述沉淀中再加入稀HNO3观察现象:1、在AgCl沉淀中沉淀不消失。2、在Ag2CO3沉淀中出现大量气泡(CO2),
白色沉淀消失。3、用NaCl+AgNO3反应证明1、物性:纯净的HNO3是一种无色的液体,具有刺激性气味。
2、硝酸具有挥发性。在空气里也能挥发出HNO3气体, HNO3气体与空气里的水蒸气结合形成硝酸小液滴,形成白雾。 3、硝酸具有很强的腐蚀性。二、硝酸(HNO3)4.常温下见光容易分解,受热时分解得更快。
4HNO3 = 2H2O+4NO2 ↑ +O2 ↑ 结论:硝酸具有不稳定性常把硝酸浓盛放在棕色玻璃瓶中,贮放在冷暗处光、热三、浓硫酸( H2SO4)三、
浓硫酸的个性2、化性:(1)浓硫酸具有强腐蚀性。【思考】如果浓硫酸不慎溅到皮肤上,应怎样处理?1、物性:纯净的浓硫酸是无色、粘稠、油状的液体,不容易挥发。常用的浓硫酸中H2SO4的质量分数是98%,密度为1.84g/㎝3
浓硫酸具有吸水性,可做干燥剂。要先用干布拭去,然后用大量水冲洗,最后用小苏打溶液冲洗,严重时应立即送医院2NaHCO3+H2SO4=Na2SO4 +2H2O+2CO2↑(2)浓硫酸具有脱水性。能使木材、纸张脱水碳化 三、
硫酸的个性怎样区分脱水性和吸水性?实验3:浓硫酸点在纸上现象:纸变黑能干燥哪些气体呢?硫酸的用途:重要的化工原料,应用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油、金属除锈等,实验室常用作干燥剂。干燥剂与被干燥的气体不能发生反应。三、
硫酸的个性浓硫酸的稀释实验 【现象】【结论】烧杯外壁很热。浓硫酸易溶于水,溶解时放出大量的热。错误操作稀释浓硫酸时,一定要把浓硫酸沿着器壁(或玻璃棒)慢慢地注入水里,并不断搅拌。正确操作不能把水倒入浓硫酸中【小结 】本节课今天我们学到了什么知识?掌握了什么学习方法?知识类: 三强酸的个性
方法类:观察实验现象,类比方法学习、分析推理归纳与小结【三强酸的个性】酸的个性【思考与讨论】
三强酸敝口放置,溶液质量增加的是_____,溶液质量减小的是_____,溶质的质量分数怎样变?放置一段时间后这些酸有无变质?【讨论与交流】你还认识哪些酸?它们有哪些特性巩固与拓展磷酸H3PO4:纯品为无色透明粘稠状液体或斜方晶体,无臭,味很酸。性质相对稳定,挥发性小;酸性中等。
醋酸CH3COOH:无色的液体,酸味很浓, 容易与水相混和,是有机酸。1、下列物质久置于空气中,它的PH会增大的是 -------------( )
A、 浓盐酸 B、石灰水
C、浓硫酸 D、浓食盐水
2、稀硝酸中混有小量的盐酸,为了除去盐酸,可以加入适量的---------( )
A、Fe B、AgNO3
C、BaCl2 D、KOH
3、打开盐酸的瓶塞可以在瓶口可以闻到____气味的气体,说明浓盐酸具有__________性。 4、怎样鉴别3瓶分别盛有水、稀盐酸、稀硫酸的无色液体?
5、鉴定某酸溶液为盐酸时需用试剂是:______ 再 见
硝酸:
硫酸:HCI = H + + CI-电离方程式:H NO3 = H + + NO3-H2SO4 = 2H + + SO 42-
电离通式:酸= H + 酸根阴离子1、强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
2、弱酸:醋酸(CH3COOH)、碳酸(H2co3)第二节 探索酸的性质一、什么是酸:在水中电离时,生成的阳离子全部都是氢离子(H+)的化合物。板书:pH>7,碱性; pH =7,中性;pH<7,酸性。那么,你知道还有什么方法可以测定物质的酸碱性?二、酸碱指示剂:石蕊遇酸变红,遇碱变蓝;
酚酞遇酸不变色,遇碱变红。1、用玻璃棒分别蘸取少许水、酸果汁、白醋、盐酸,点在pH试纸中部,观察试纸的颜色变化。
2、在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2—3滴紫色石蕊试液,观察其颜色的变化,并将结果填入表中。实验 实验过程中物质的颜色变化蓝色紫色红色红色红色红色红色红色你能得出什么结论?石蕊遇酸变红阅读P8自制酸碱指示剂1、下列物质不属于酸的是 ( )
A、HNO3 B、NaHCO3
C、H3PO4 D、HI
2、用简单的方法区别水和硫酸,并写出实验步骤。
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?B练习:思考 胃酸过多的病人常服用一种叫“胃舒平”的药片来治疗,药片的主要成份是氢氧化铝,为什么能用它来治疗胃酸过多呢? 3 HCI + Al(OH)3 〓 AlCI3 + 3H2O 请用化学方程式表示: 酸 + 碱 〓 盐 + 水 三、在氢氧化钠溶液中滴入2滴紫色石蕊试液,溶液呈________色;再逐滴滴入盐酸,溶液颜色有什么变化?______________________。蓝色由蓝色逐渐变成紫色 HCI + NaOH = NaCI + H2O 酸 + 碱 〓 盐 + 水 实验探究1第2课时盐酸有什么性质:如果继续滴入HCl呢?三、盐酸有哪些性质?实验探究2 a、把鸡蛋壳放入盛有盐酸的试管中,将燃着的火柴伸入试管口,你看到什么现象?
_________________________________.蛋壳表面产生气泡,燃着的木条伸入后会熄灭 2HCI + CaCO3 = CaCI2 + H2O + CO2↑ 酸 + 盐 = 新盐 + 新酸b、碳酸钠和盐酸的反应,产生的气体通过澄清石灰水,观察现象?HCI + Na2CO3 = NaCI + H2O + CO2 ↑ 酸 + 盐 = 新盐 + 新酸*? CO32-的检验:加盐酸,能产生使澄清石灰水变浑浊的气体(二氧化碳)
Ca(OH)2 + CO2 = CaCO3 ↓ + H2O三、盐酸有哪些性质?实验探究3 a、向盛有一枚生锈的铁钉的试管中加入盐酸,振荡,过会儿观察现象?
_______________________________________. 铁锈消失,溶液变成黄色 6HCI + Fe2O3 = 2FeCI3+3H2O 盐酸 +金属氧化物= 盐 + 水红棕色 黄色b、向盛有少量氧化铜粉末的试管中加入盐酸,微微加热,观察现象?
______________________________________ 黑色粉末消失,溶液变成蓝色2HCI + CuO = CuCI2 + H2O 盐酸 +金属氧化物= 盐 + 水黑色 蓝色 上述探究实验3中,除了铁锈消失外,还可以观察到什么现象?___________________ 探究实验4 铁钉表面产生气泡提出问题: 气体是否是盐酸和金属铁反应生成的?建立假设:____________________________.实验验证:结论:酸可以和某些活泼金属反应,
生成盐和氢气 2HCI + Fe = FeCI2 + H2↑酸 +金属 = 盐 + 氢气谁来归纳一下,盐酸主要有哪些
化学性质,能跟哪些物质反应。小结1、 酸能使紫色的石蕊变红,无色酚酞不变色。2、 酸 + 碱 〓 盐 + 水 3、酸 + 盐 = 新盐 + 新酸4、 盐酸 +金属氧化物= 盐 + 水5、酸 +金属 = 盐 + 氢气 3 HCI + Al(OH)3 〓 AlCI3 + 3H2O2HCI + CaCO3 = CaCI2 + H2O + CO2↑ 6HCI + Fe2O3 = 2FeCI3+3H2O2HCI + CuO = CuCI2 + H2O 2HCI + Fe = FeCI2 + H2↑三、硫酸有哪些性质?-H2SO4第3课时实验探究5 稀硫酸分别滴入盛有锌、氧化铁、氧化铜、氢氧化铜、氯化钡溶液的试管中,发现 :_____________________________。1、 Zn + H2SO4 = ZnSO4 + H2 ↑2、 Fe2O3 + H2SO4= Fe2(SO4)3+ H2 O3、CuO + H2SO4 =CuSO4+ H2 O4、Cu(OH)2 + H2SO4 = CuSO4 + 2H2 O5、BaCI2 + H2SO4 = BaSO4 ↓+ 2HCI你能说出硫酸有哪些性质?从盐酸、硫酸的实验中可以看到物质发生反应的证据有哪些?1、溶液颜色变化2、产生气体3、产生沉淀4、性质变化你能归纳出酸的一些共性吗?P12总结:
1、 酸能使指示剂变色
2、? 能与碱反应生成盐和水
3、 能与某些金属氧化物反应生成盐和水
4、 能与某些金属反应生成盐和氢气
5、能与盐反应生成新的盐和新的酸
1、下列物质中,能除去铁制品表面铁锈的是 ( )
A、稀硫酸 B、水 C、氢氧化钠溶液 D、硫酸铜溶液
2、写出下列方程式,并写出反应类型
反应类型
(1)Fe+H2SO4 ==___________________; _______________
(2)CuO+H2SO4==__________________; _______________
(3)2NaOH+H2SO4==________________; ______________
(4)H2SO4+BaCl2== _________________; _______________
(5)HCl+AgNO3==___________________; _______________
1、盐酸在工农业生产和日常生活中用途很大。下列各项用途是利用盐酸的哪些性质?试写出有关反应的化学方程式。
(1)电镀前用盐酸清洗钢铁表面的铁锈。
(2)制革工业中用熟石灰脱毛后,剩余的熟石灰[Ca(OH)2]用盐酸来除去。
(3)用稀盐酸清除锅炉中的水垢[主要成分为CaCO3,和Mg(OH)2]。
2、怎样鉴别3瓶分别盛有水、稀盐酸、稀硫酸的无色液体?
3、向稀盐酸中滴加石蕊试液,溶液显______色,稀盐酸的PH______7(填<、>、=)
4、鉴定某酸溶液为盐酸时需用试剂是:______ 盐酸的个性观 察1、物性:纯净的浓盐酸是无色的液体,有刺激性气味。工业品浓盐酸因含有杂质而带黄色。常用的浓盐酸中HCl的质量分数约为37%~38%,密度是1. 19g/㎝3 。一、浓盐酸的个性【猜一猜】
白雾是什么?怎样形成的?你猜想的依据是什么?2、浓盐酸具有挥发性。从浓盐酸挥发出来的氯化氢气体跟空气里的水蒸气接触,形成盐酸小液滴,从而形成白雾。【结论】P13观察3:瓶口出现白雾;盐酸具有刺激性气味。闻气体气味的方法雾是液滴悬浮在空气中的现象实 验1、稀盐酸中滴加硝酸银溶液,观察现象: HCl+AgNO3=AgCl↓+HNO3产生AgCl白色沉淀就凭这个实验能证明HCl的存在吗?2、Na2CO3中滴加硝酸银溶液,观察现象:产生Ag2CO3白色沉淀Na2CO3+ 2AgNO3=Ag2CO3 ↓+2NaNO3 CI-的检验:先加稀AgNO3出现沉淀,再加HNO3沉淀不消失。怎样才能判断生成的是AgCl沉淀,而不是Ag2CO3沉淀?在上述沉淀中再加入稀HNO3观察现象:1、在AgCl沉淀中沉淀不消失。2、在Ag2CO3沉淀中出现大量气泡(CO2),
白色沉淀消失。3、用NaCl+AgNO3反应证明1、物性:纯净的HNO3是一种无色的液体,具有刺激性气味。
2、硝酸具有挥发性。在空气里也能挥发出HNO3气体, HNO3气体与空气里的水蒸气结合形成硝酸小液滴,形成白雾。 3、硝酸具有很强的腐蚀性。二、硝酸(HNO3)4.常温下见光容易分解,受热时分解得更快。
4HNO3 = 2H2O+4NO2 ↑ +O2 ↑ 结论:硝酸具有不稳定性常把硝酸浓盛放在棕色玻璃瓶中,贮放在冷暗处光、热三、浓硫酸( H2SO4)三、
浓硫酸的个性2、化性:(1)浓硫酸具有强腐蚀性。【思考】如果浓硫酸不慎溅到皮肤上,应怎样处理?1、物性:纯净的浓硫酸是无色、粘稠、油状的液体,不容易挥发。常用的浓硫酸中H2SO4的质量分数是98%,密度为1.84g/㎝3
浓硫酸具有吸水性,可做干燥剂。要先用干布拭去,然后用大量水冲洗,最后用小苏打溶液冲洗,严重时应立即送医院2NaHCO3+H2SO4=Na2SO4 +2H2O+2CO2↑(2)浓硫酸具有脱水性。能使木材、纸张脱水碳化 三、
硫酸的个性怎样区分脱水性和吸水性?实验3:浓硫酸点在纸上现象:纸变黑能干燥哪些气体呢?硫酸的用途:重要的化工原料,应用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油、金属除锈等,实验室常用作干燥剂。干燥剂与被干燥的气体不能发生反应。三、
硫酸的个性浓硫酸的稀释实验 【现象】【结论】烧杯外壁很热。浓硫酸易溶于水,溶解时放出大量的热。错误操作稀释浓硫酸时,一定要把浓硫酸沿着器壁(或玻璃棒)慢慢地注入水里,并不断搅拌。正确操作不能把水倒入浓硫酸中【小结 】本节课今天我们学到了什么知识?掌握了什么学习方法?知识类: 三强酸的个性
方法类:观察实验现象,类比方法学习、分析推理归纳与小结【三强酸的个性】酸的个性【思考与讨论】
三强酸敝口放置,溶液质量增加的是_____,溶液质量减小的是_____,溶质的质量分数怎样变?放置一段时间后这些酸有无变质?【讨论与交流】你还认识哪些酸?它们有哪些特性巩固与拓展磷酸H3PO4:纯品为无色透明粘稠状液体或斜方晶体,无臭,味很酸。性质相对稳定,挥发性小;酸性中等。
醋酸CH3COOH:无色的液体,酸味很浓, 容易与水相混和,是有机酸。1、下列物质久置于空气中,它的PH会增大的是 -------------( )
A、 浓盐酸 B、石灰水
C、浓硫酸 D、浓食盐水
2、稀硝酸中混有小量的盐酸,为了除去盐酸,可以加入适量的---------( )
A、Fe B、AgNO3
C、BaCl2 D、KOH
3、打开盐酸的瓶塞可以在瓶口可以闻到____气味的气体,说明浓盐酸具有__________性。 4、怎样鉴别3瓶分别盛有水、稀盐酸、稀硫酸的无色液体?
5、鉴定某酸溶液为盐酸时需用试剂是:______ 再 见
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
