2022-2023学年九年级化学人教版上册第六单元 碳和碳的氧化物 同步质量检测卷(word版 有答案)
文档属性
| 名称 | 2022-2023学年九年级化学人教版上册第六单元 碳和碳的氧化物 同步质量检测卷(word版 有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 856.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-24 00:00:00 | ||
图片预览

文档简介
第六单元 碳和碳的氧化物 同步质量检测卷
一、单选题(本大题共14小题)
1.没有空气就没有生命。下列有关空气的说法错误的是
A.植物光合作用需要氮气 B.人体呼吸作用需要氧气
C.二氧化碳属于温室气体 D.稀有气体化学性质稳定
2.现有7g氧化铜、氧化铁和木炭粉的混合物,在高温条件下恰好完全反应,得到2.2g二氧化碳,则原混合物中氧化铜与氧化铁的质量比为
A.1:1 B.1:2 C.2:1 D.2:3
3.自然界中碳循环、氧循环如图,下列说法正确的是
A.植物呼吸作用放出氧气
B.化石燃料燃烧会大幅降低大气中氧气含量
C.植物光合作用可以将大气中CO2全部吸收
D.碳、氧循环失衡会导致人类生存环境恶化
4.实验室制取CO2、O2 和H2是初中化学必备知识。下列说法不正确的是
A.CO2和O2的发生装置可以相同 B.CO2和O2的发生装置可以不同
C.CO2和H2的收集装置完全相同 D.O2和H2的发生和收集装置可以相同
5.我国古代将炉甘石、赤铜和木炭粉混合加热到约800℃,可制得外观似金子的合金,其中发生的一个反应的文字表达式为,下列说法正确的是
A.X的化学式为CO B.Cu2O中铜原子与氧原子的个数比为2:1
C.Cu2O中Cu的化合价为+2 D.该反应体现了木炭的还原性
6.化学知识能反映出丰富的化学基本观念。某同学将化学知识与基本观念对应起来,整理出以下内容。其中认识错误的是
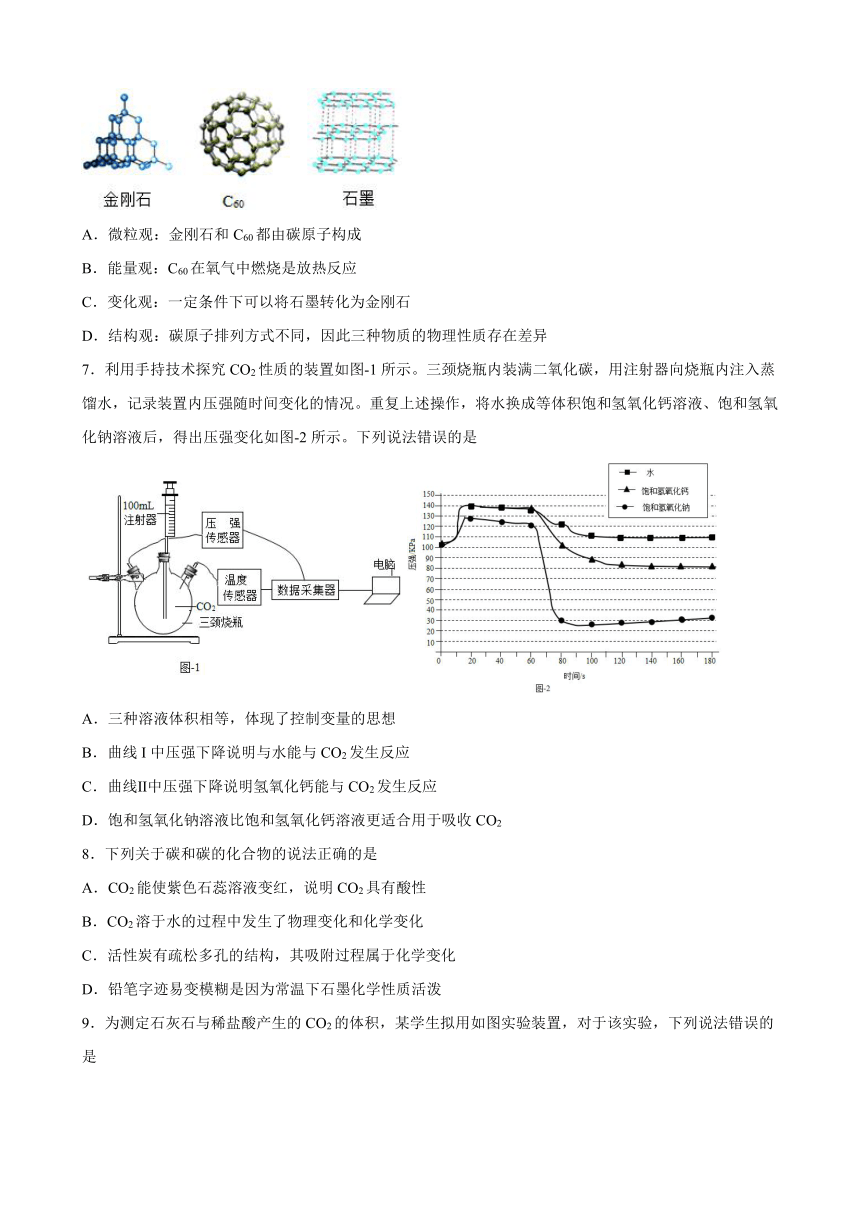
A.微粒观:金刚石和C60都由碳原子构成
B.能量观:C60在氧气中燃烧是放热反应
C.变化观:一定条件下可以将石墨转化为金刚石
D.结构观:碳原子排列方式不同,因此三种物质的物理性质存在差异
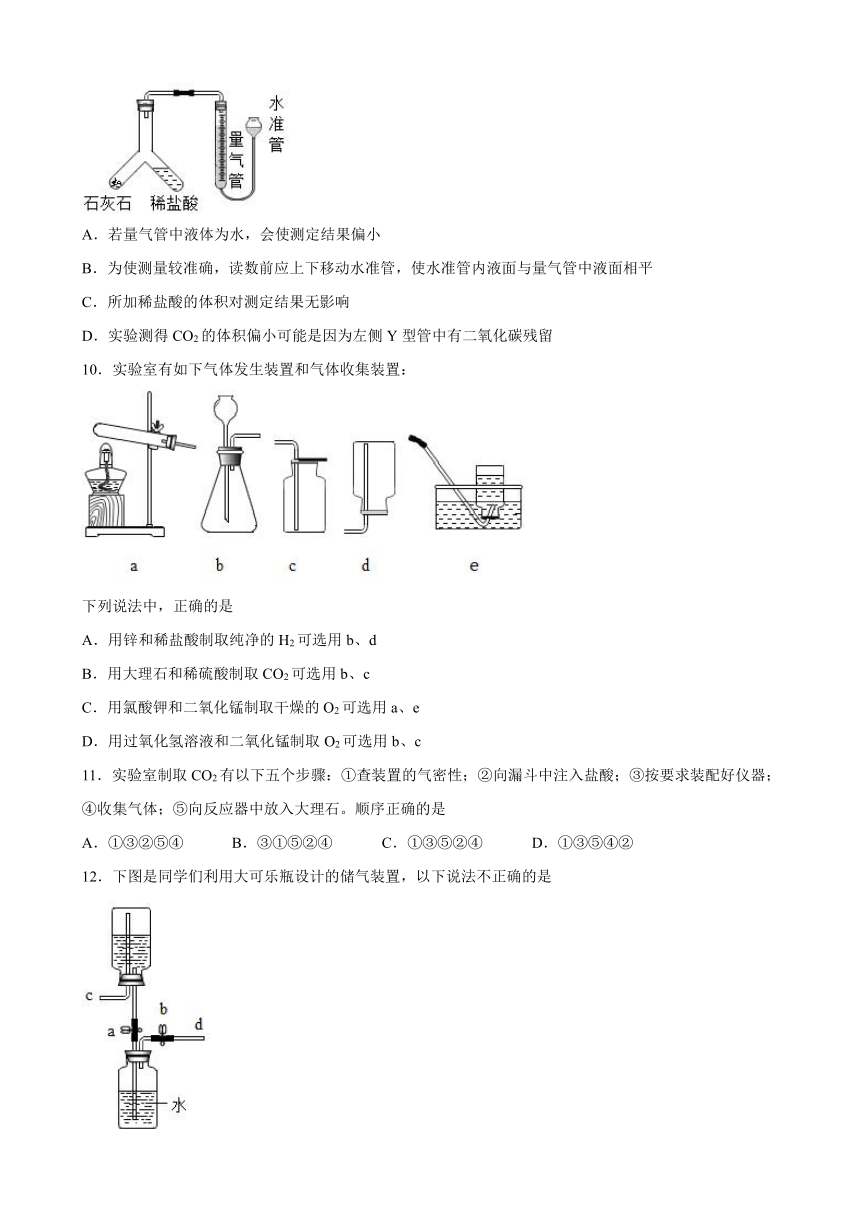
7.利用手持技术探究CO2性质的装置如图-1所示。三颈烧瓶内装满二氧化碳,用注射器向烧瓶内注入蒸馏水,记录装置内压强随时间变化的情况。重复上述操作,将水换成等体积饱和氢氧化钙溶液、饱和氢氧化钠溶液后,得出压强变化如图-2所示。下列说法错误的是
A.三种溶液体积相等,体现了控制变量的思想
B.曲线I中压强下降说明与水能与CO2发生反应
C.曲线Ⅱ中压强下降说明氢氧化钙能与CO2发生反应
D.饱和氢氧化钠溶液比饱和氢氧化钙溶液更适合用于吸收CO2
8.下列关于碳和碳的化合物的说法正确的是
A.CO2能使紫色石蕊溶液变红,说明CO2具有酸性
B.CO2溶于水的过程中发生了物理变化和化学变化
C.活性炭有疏松多孔的结构,其吸附过程属于化学变化
D.铅笔字迹易变模糊是因为常温下石墨化学性质活泼
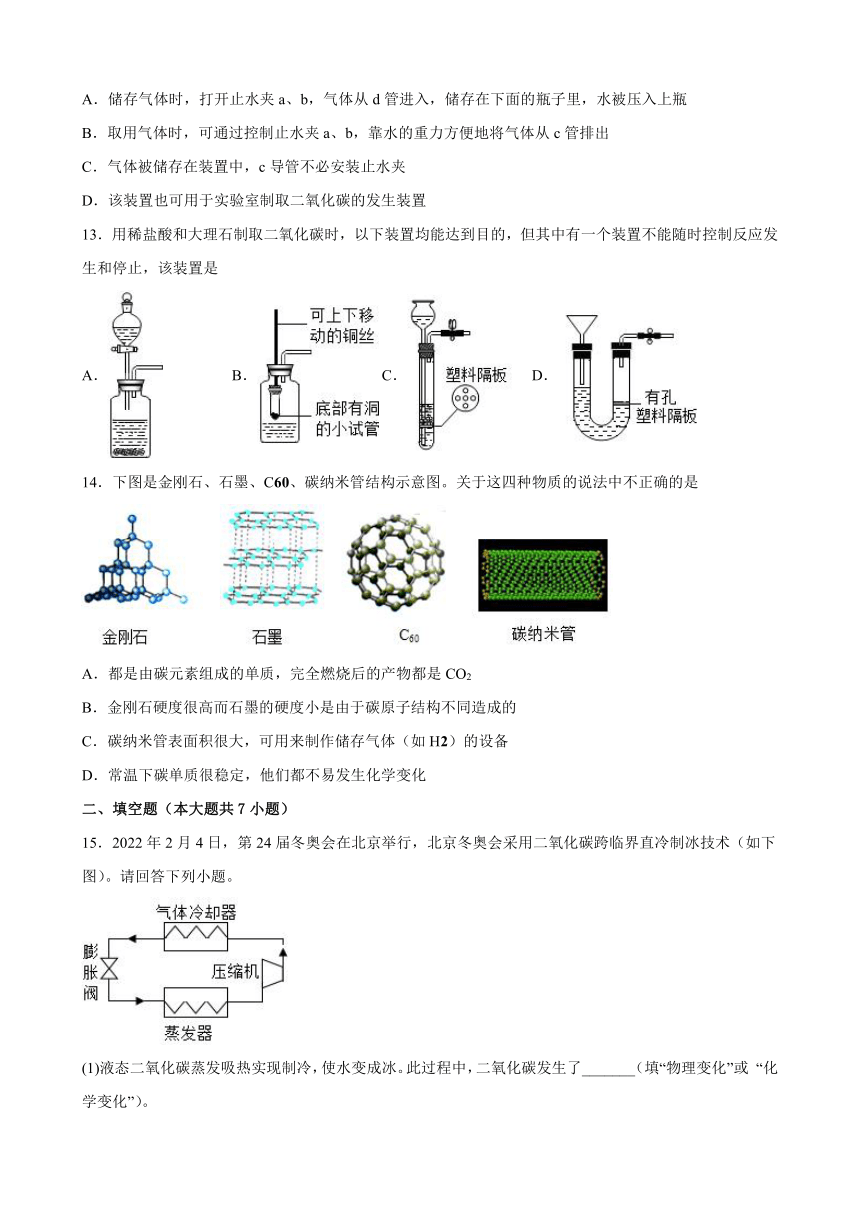
9.为测定石灰石与稀盐酸产生的CO2的体积,某学生拟用如图实验装置,对于该实验,下列说法错误的是
A.若量气管中液体为水,会使测定结果偏小
B.为使测量较准确,读数前应上下移动水准管,使水准管内液面与量气管中液面相平
C.所加稀盐酸的体积对测定结果无影响
D.实验测得CO2的体积偏小可能是因为左侧Y型管中有二氧化碳残留
10.实验室有如下气体发生装置和气体收集装置:
下列说法中,正确的是
A.用锌和稀盐酸制取纯净的H2可选用b、d
B.用大理石和稀硫酸制取CO2可选用b、c
C.用氯酸钾和二氧化锰制取干燥的O2可选用a、e
D.用过氧化氢溶液和二氧化锰制取O2可选用b、c
11.实验室制取CO2有以下五个步骤:①查装置的气密性;②向漏斗中注入盐酸;③按要求装配好仪器;④收集气体;⑤向反应器中放入大理石。顺序正确的是
A.①③②⑤④ B.③①⑤②④ C.①③⑤②④ D.①③⑤④②
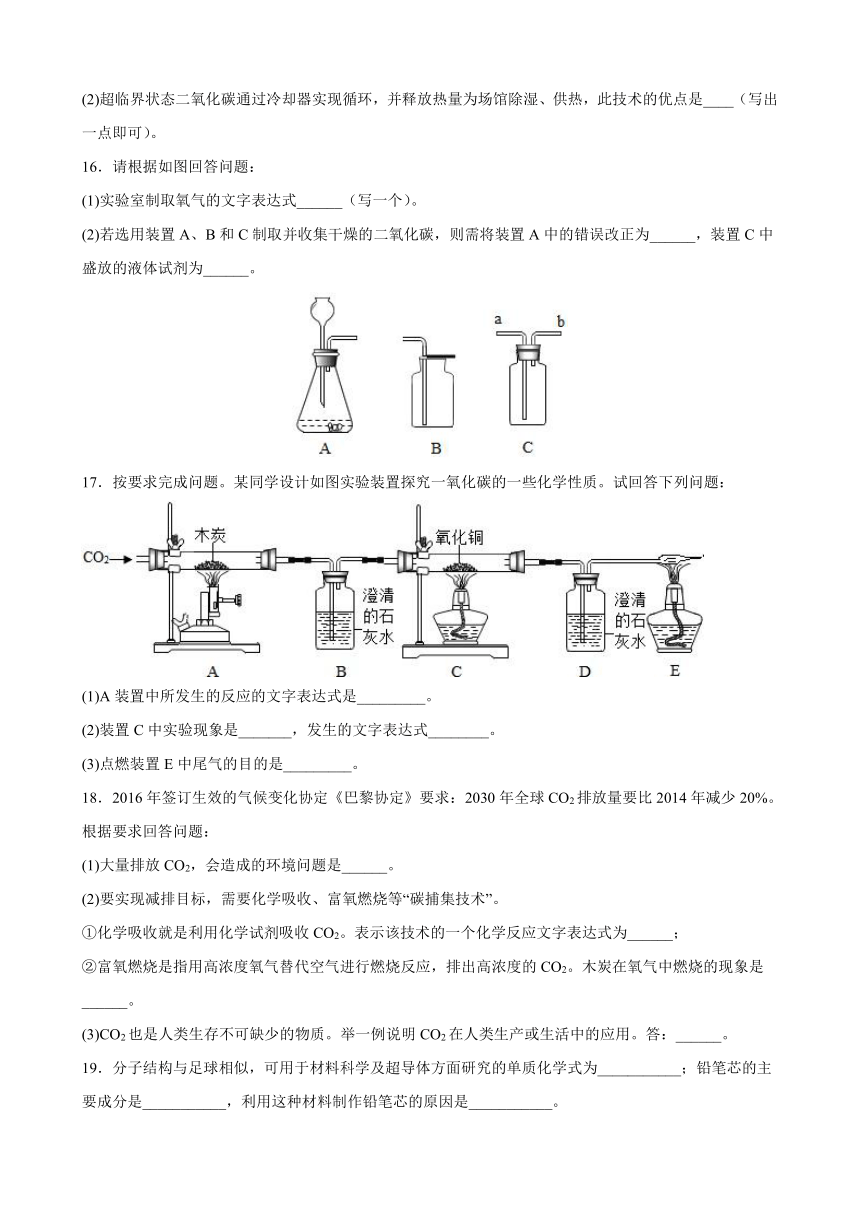
12.下图是同学们利用大可乐瓶设计的储气装置,以下说法不正确的是
A.储存气体时,打开止水夹a、b,气体从d管进入,储存在下面的瓶子里,水被压入上瓶
B.取用气体时,可通过控制止水夹a、b,靠水的重力方便地将气体从c管排出
C.气体被储存在装置中,c导管不必安装止水夹
D.该装置也可用于实验室制取二氧化碳的发生装置
13.用稀盐酸和大理石制取二氧化碳时,以下装置均能达到目的,但其中有一个装置不能随时控制反应发生和停止,该装置是
A. B. C. D.
14.下图是金刚石、石墨、C60、碳纳米管结构示意图。关于这四种物质的说法中不正确的是
A.都是由碳元素组成的单质,完全燃烧后的产物都是CO2
B.金刚石硬度很高而石墨的硬度小是由于碳原子结构不同造成的
C.碳纳米管表面积很大,可用来制作储存气体(如H2)的设备
D.常温下碳单质很稳定,他们都不易发生化学变化
二、填空题(本大题共7小题)
15.2022年2月4日,第24届冬奥会在北京举行,北京冬奥会采用二氧化碳跨临界直冷制冰技术(如下图)。请回答下列小题。
(1)液态二氧化碳蒸发吸热实现制冷,使水变成冰。此过程中,二氧化碳发生了_______(填“物理变化”或 “化学变化”)。
(2)超临界状态二氧化碳通过冷却器实现循环,并释放热量为场馆除湿、供热,此技术的优点是____(写出一点即可)。
16.请根据如图回答问题:
(1)实验室制取氧气的文字表达式______(写一个)。
(2)若选用装置A、B和C制取并收集干燥的二氧化碳,则需将装置A中的错误改正为______,装置C中盛放的液体试剂为______。
17.按要求完成问题。某同学设计如图实验装置探究一氧化碳的一些化学性质。试回答下列问题:
(1)A装置中所发生的反应的文字表达式是_________。
(2)装置C中实验现象是_______,发生的文字表达式________。
(3)点燃装置E中尾气的目的是_________。
18.2016年签订生效的气候变化协定《巴黎协定》要求:2030年全球CO2排放量要比2014年减少20%。根据要求回答问题:
(1)大量排放CO2,会造成的环境问题是______。
(2)要实现减排目标,需要化学吸收、富氧燃烧等“碳捕集技术”。
①化学吸收就是利用化学试剂吸收CO2。表示该技术的一个化学反应文字表达式为______;
②富氧燃烧是指用高浓度氧气替代空气进行燃烧反应,排出高浓度的CO2。木炭在氧气中燃烧的现象是______。
(3)CO2也是人类生存不可缺少的物质。举一例说明CO2在人类生产或生活中的应用。答:______。
19.分子结构与足球相似,可用于材料科学及超导体方面研究的单质化学式为___________;铅笔芯的主要成分是___________,利用这种材料制作铅笔芯的原因是___________。
20.中国画历史悠久、风格多样,是我国的文化艺术瑰宝。
(1)“文房四宝”之一的墨是中国传统水墨画的绘画材料。水墨画能长时间保存,是因为墨汁中的炭黑_______。
(2)敦煌壁画色彩艳丽,矿物颜料功不可没,其蓝色源于石青[Cu3(OH)2(CO3)x]。石青中铜元素(+2价)与碳元素的质量比为________(用不含x的比值表示)。
(3)油画促进了中国绘画的多元化发展。长期放置的油画色彩变暗,是因为生成了黑色的PbS。油画修复的方法是用H2O2将PbS变为白色的PbSO4,修复的文字表达式为________。
21.北京冬奥会虽已落幕,但是奥运会期间的科技元素让世界震撼。
(1)火炬“飞扬”采用氢气作燃料,完美诠释了绿色奥运理念。氢气燃烧的文字表达式为______;关闭火炬的燃气开关可使火炬熄灭,依据的灭火原理是______。
(2)领奖礼仪服一一冬奥中的“黑科技”。为增强保温效果,礼仪服里添加了石墨烯发热材料,由此可知石墨烯具有______性。
(3)“水立方”变身“冰立方”,在水结冰的过程中发生变化的是______(填字母序号)。
A.分子的种类 B.分子的质量 C.分子之间的间隔
三、实验题(本大题共3小题)
22.请结合如图回答问题:
(1)仪器①的名称是______。
(2)用高锰酸钾制取并收集氧气,可选用的装置是______(选填序号),反应文字表达式为______。
(3)为方便实验室制CO2控制反应的发生和停止,应选择的发生装置是______(选填序号),用E装置测定CO2气体的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值小,原因是______,为避免出现这样的情况,改进方法是______。
23.学习小组同学用下图装置进行实验,验证CO2的性质。
(1)打开止水夹I,关闭止水夹Ⅱ,通入潮湿的CO2气体一段时间后可观察到乙中干燥的紫色小花(用石蕊溶液染成)______。
(2)关闭止水夹I,打开止水夹Ⅱ,通入潮湿的CO2气体一段时间后观察到乙中干燥的紫色小花不变红。则甲瓶中所盛试剂的作用是______。
(3)若关闭止水夹I,打开止水夹Ⅱ,通入潮湿的CO2气体一段时间后观察到甲中溶液变浑浊,写出甲中发生反应的文字表达式:______。
24.对比法是进行科学实验的重要思想方法之一。完成下列关于“二氧化碳化学性质”探究活动的部分实验报告:
实验步骤 实验现象 实验结论
实验一 将一只短蜡烛固定在烧杯内,点燃。拿起收集满二氧化碳的集气瓶,向烧杯内缓缓倾倒二氧化碳 燃着蜡烛熄灭 ______
实验二 有两支分别盛有 2mL 蒸馏水的试管。实验步骤:(1)______;(2)______ 一支试管里的溶液颜色为紫色,另一只试管里的溶液______ 二氧化碳与水反应
实验三 取一支试管,向其中注入少量澄清石灰水,然后通入二氧化碳 ______ 二氧 化 碳与 石灰水 反 应
四、计算题(本大题共3小题)
25.河蚌是白洋淀一种常见的水生动物,河蚌壳的主要成分是 CaCO3,某课外活动小组为了测定其含量进行了如图所示实验,请计算:(计算结果精确至 0.1%,假设杂质不溶于水也不与稀盐酸反应)。
(1)反应中生成二氧化碳______g。
(2)该河蚌壳中碳酸钙的质量分数。
26.小明同学为测定含有碳粉的Cu的质量分数。将10g混合物放在如图1所示的装置中,不断通入O2,并将生成的气体用足量的澄清石灰水吸收。测得反应过程烧杯质量变化如表所示。
时间/s t0 t1 t2 t3 t4 t5 t6
烧杯及溶液质量/g 150 160 167 170 171 172 172
(1)求混合物中铜的质量分数______ (写出计算过程)。
(2)请在图2中画出CO2的质量随时间变化的曲线______。
(3)小芳同学认为,小明同学设计的实验装置不科学,导致测得的Cu的质量分数不准确。你认为是______(填“偏大”或“偏小”),理由是______。
27.某化学兴趣小组为测定实验室废弃的氧化铜样品中CuO的质量分数,称取5g该氧化铜样品,用下图所示的装置进行实验(样品中杂质不反应),充分反应后测得B装置的质量增加了2.2g。
回答下列问题:
(1)装置A中反应的文字表达式是____。
(2)生成CO2的质量为____g。
(3)计算该氧化铜样品中CuO的质量分数______(写出计算过程)。
参考答案:
1.A
2.A
3.D
4.C
5.D
6.A
7.B
8.B
9.D
10.D
11.B
12.B
13.A
14.B
15.(1)物理变化
(2)利用二氧化碳资源,不产生有毒有害物质,环保节约
16.(1)2H2O22H2O+O2↑或2KMnO4K2MnO4+MnO2+O2↑或2KClO32KCl+3O2↑
(2) 长颈漏斗下端伸入液面下 浓硫酸
17.(1)
(2) 黑色粉末变为红色
(3)处理尾气,防止空气污染
18.(1)温室效应
(2) (合理答案均可) 剧烈燃烧,发出白光,生成使澄清石灰水变浑浊气体
(3)灭火或人工降雨(合理答案均可)
19. C60 石墨 石墨质软、有深灰色
20.(1)常温下化学性质稳定
(2)8:1
(3)4H2O2+PbS=PbSO4+4H2O
21.(1) 隔离可燃物
(2)导热
(3)C
22.(1)集气瓶
(2) AD
(3) C 部分二氧化碳溶于水 在集气瓶中的水面上覆盖一层植物油
23.(1)变红
(2)干燥气体
(3)CO2+Ca(OH)2=CaCO3↓+H2O
24. CO2不可燃不助燃密度比空气大 向两支试管中各滴入1-2滴石蕊溶液; 向其中一支试管中通入二氧化碳 变红 澄清石灰水变浑浊
25.(1)8.8
(2)解:设 21g 河蚌壳中所含碳酸钙的质量为 x。
河蚌壳中碳酸钙的质量分数为
答:该河蚌壳中碳酸钙的质量分数为 95.2%。
26.(1)烧杯及溶液增加的质量即为反应生成二氧化碳的质量,生成二氧化碳的质量为:172g-150g=22g
解:设混合物中碳的质量为x
x=6g
故混合物中铜的质量分数为:
(2)
(3) 偏小 澄清石灰水溶液露置在空气中,会吸收空气中的二氧化碳
27.(1)
(2)2.2
(3)80%
解:设该氧化铜样品中CuO的质量分数为x
x=80%
答:该氧化铜样品中CuO的质量分数为80%。
一、单选题(本大题共14小题)
1.没有空气就没有生命。下列有关空气的说法错误的是
A.植物光合作用需要氮气 B.人体呼吸作用需要氧气
C.二氧化碳属于温室气体 D.稀有气体化学性质稳定
2.现有7g氧化铜、氧化铁和木炭粉的混合物,在高温条件下恰好完全反应,得到2.2g二氧化碳,则原混合物中氧化铜与氧化铁的质量比为
A.1:1 B.1:2 C.2:1 D.2:3
3.自然界中碳循环、氧循环如图,下列说法正确的是
A.植物呼吸作用放出氧气
B.化石燃料燃烧会大幅降低大气中氧气含量
C.植物光合作用可以将大气中CO2全部吸收
D.碳、氧循环失衡会导致人类生存环境恶化
4.实验室制取CO2、O2 和H2是初中化学必备知识。下列说法不正确的是
A.CO2和O2的发生装置可以相同 B.CO2和O2的发生装置可以不同
C.CO2和H2的收集装置完全相同 D.O2和H2的发生和收集装置可以相同
5.我国古代将炉甘石、赤铜和木炭粉混合加热到约800℃,可制得外观似金子的合金,其中发生的一个反应的文字表达式为,下列说法正确的是
A.X的化学式为CO B.Cu2O中铜原子与氧原子的个数比为2:1
C.Cu2O中Cu的化合价为+2 D.该反应体现了木炭的还原性
6.化学知识能反映出丰富的化学基本观念。某同学将化学知识与基本观念对应起来,整理出以下内容。其中认识错误的是
A.微粒观:金刚石和C60都由碳原子构成
B.能量观:C60在氧气中燃烧是放热反应
C.变化观:一定条件下可以将石墨转化为金刚石
D.结构观:碳原子排列方式不同,因此三种物质的物理性质存在差异
7.利用手持技术探究CO2性质的装置如图-1所示。三颈烧瓶内装满二氧化碳,用注射器向烧瓶内注入蒸馏水,记录装置内压强随时间变化的情况。重复上述操作,将水换成等体积饱和氢氧化钙溶液、饱和氢氧化钠溶液后,得出压强变化如图-2所示。下列说法错误的是
A.三种溶液体积相等,体现了控制变量的思想
B.曲线I中压强下降说明与水能与CO2发生反应
C.曲线Ⅱ中压强下降说明氢氧化钙能与CO2发生反应
D.饱和氢氧化钠溶液比饱和氢氧化钙溶液更适合用于吸收CO2
8.下列关于碳和碳的化合物的说法正确的是
A.CO2能使紫色石蕊溶液变红,说明CO2具有酸性
B.CO2溶于水的过程中发生了物理变化和化学变化
C.活性炭有疏松多孔的结构,其吸附过程属于化学变化
D.铅笔字迹易变模糊是因为常温下石墨化学性质活泼
9.为测定石灰石与稀盐酸产生的CO2的体积,某学生拟用如图实验装置,对于该实验,下列说法错误的是
A.若量气管中液体为水,会使测定结果偏小
B.为使测量较准确,读数前应上下移动水准管,使水准管内液面与量气管中液面相平
C.所加稀盐酸的体积对测定结果无影响
D.实验测得CO2的体积偏小可能是因为左侧Y型管中有二氧化碳残留
10.实验室有如下气体发生装置和气体收集装置:
下列说法中,正确的是
A.用锌和稀盐酸制取纯净的H2可选用b、d
B.用大理石和稀硫酸制取CO2可选用b、c
C.用氯酸钾和二氧化锰制取干燥的O2可选用a、e
D.用过氧化氢溶液和二氧化锰制取O2可选用b、c
11.实验室制取CO2有以下五个步骤:①查装置的气密性;②向漏斗中注入盐酸;③按要求装配好仪器;④收集气体;⑤向反应器中放入大理石。顺序正确的是
A.①③②⑤④ B.③①⑤②④ C.①③⑤②④ D.①③⑤④②
12.下图是同学们利用大可乐瓶设计的储气装置,以下说法不正确的是
A.储存气体时,打开止水夹a、b,气体从d管进入,储存在下面的瓶子里,水被压入上瓶
B.取用气体时,可通过控制止水夹a、b,靠水的重力方便地将气体从c管排出
C.气体被储存在装置中,c导管不必安装止水夹
D.该装置也可用于实验室制取二氧化碳的发生装置
13.用稀盐酸和大理石制取二氧化碳时,以下装置均能达到目的,但其中有一个装置不能随时控制反应发生和停止,该装置是
A. B. C. D.
14.下图是金刚石、石墨、C60、碳纳米管结构示意图。关于这四种物质的说法中不正确的是
A.都是由碳元素组成的单质,完全燃烧后的产物都是CO2
B.金刚石硬度很高而石墨的硬度小是由于碳原子结构不同造成的
C.碳纳米管表面积很大,可用来制作储存气体(如H2)的设备
D.常温下碳单质很稳定,他们都不易发生化学变化
二、填空题(本大题共7小题)
15.2022年2月4日,第24届冬奥会在北京举行,北京冬奥会采用二氧化碳跨临界直冷制冰技术(如下图)。请回答下列小题。
(1)液态二氧化碳蒸发吸热实现制冷,使水变成冰。此过程中,二氧化碳发生了_______(填“物理变化”或 “化学变化”)。
(2)超临界状态二氧化碳通过冷却器实现循环,并释放热量为场馆除湿、供热,此技术的优点是____(写出一点即可)。
16.请根据如图回答问题:
(1)实验室制取氧气的文字表达式______(写一个)。
(2)若选用装置A、B和C制取并收集干燥的二氧化碳,则需将装置A中的错误改正为______,装置C中盛放的液体试剂为______。
17.按要求完成问题。某同学设计如图实验装置探究一氧化碳的一些化学性质。试回答下列问题:
(1)A装置中所发生的反应的文字表达式是_________。
(2)装置C中实验现象是_______,发生的文字表达式________。
(3)点燃装置E中尾气的目的是_________。
18.2016年签订生效的气候变化协定《巴黎协定》要求:2030年全球CO2排放量要比2014年减少20%。根据要求回答问题:
(1)大量排放CO2,会造成的环境问题是______。
(2)要实现减排目标,需要化学吸收、富氧燃烧等“碳捕集技术”。
①化学吸收就是利用化学试剂吸收CO2。表示该技术的一个化学反应文字表达式为______;
②富氧燃烧是指用高浓度氧气替代空气进行燃烧反应,排出高浓度的CO2。木炭在氧气中燃烧的现象是______。
(3)CO2也是人类生存不可缺少的物质。举一例说明CO2在人类生产或生活中的应用。答:______。
19.分子结构与足球相似,可用于材料科学及超导体方面研究的单质化学式为___________;铅笔芯的主要成分是___________,利用这种材料制作铅笔芯的原因是___________。
20.中国画历史悠久、风格多样,是我国的文化艺术瑰宝。
(1)“文房四宝”之一的墨是中国传统水墨画的绘画材料。水墨画能长时间保存,是因为墨汁中的炭黑_______。
(2)敦煌壁画色彩艳丽,矿物颜料功不可没,其蓝色源于石青[Cu3(OH)2(CO3)x]。石青中铜元素(+2价)与碳元素的质量比为________(用不含x的比值表示)。
(3)油画促进了中国绘画的多元化发展。长期放置的油画色彩变暗,是因为生成了黑色的PbS。油画修复的方法是用H2O2将PbS变为白色的PbSO4,修复的文字表达式为________。
21.北京冬奥会虽已落幕,但是奥运会期间的科技元素让世界震撼。
(1)火炬“飞扬”采用氢气作燃料,完美诠释了绿色奥运理念。氢气燃烧的文字表达式为______;关闭火炬的燃气开关可使火炬熄灭,依据的灭火原理是______。
(2)领奖礼仪服一一冬奥中的“黑科技”。为增强保温效果,礼仪服里添加了石墨烯发热材料,由此可知石墨烯具有______性。
(3)“水立方”变身“冰立方”,在水结冰的过程中发生变化的是______(填字母序号)。
A.分子的种类 B.分子的质量 C.分子之间的间隔
三、实验题(本大题共3小题)
22.请结合如图回答问题:
(1)仪器①的名称是______。
(2)用高锰酸钾制取并收集氧气,可选用的装置是______(选填序号),反应文字表达式为______。
(3)为方便实验室制CO2控制反应的发生和停止,应选择的发生装置是______(选填序号),用E装置测定CO2气体的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值小,原因是______,为避免出现这样的情况,改进方法是______。
23.学习小组同学用下图装置进行实验,验证CO2的性质。
(1)打开止水夹I,关闭止水夹Ⅱ,通入潮湿的CO2气体一段时间后可观察到乙中干燥的紫色小花(用石蕊溶液染成)______。
(2)关闭止水夹I,打开止水夹Ⅱ,通入潮湿的CO2气体一段时间后观察到乙中干燥的紫色小花不变红。则甲瓶中所盛试剂的作用是______。
(3)若关闭止水夹I,打开止水夹Ⅱ,通入潮湿的CO2气体一段时间后观察到甲中溶液变浑浊,写出甲中发生反应的文字表达式:______。
24.对比法是进行科学实验的重要思想方法之一。完成下列关于“二氧化碳化学性质”探究活动的部分实验报告:
实验步骤 实验现象 实验结论
实验一 将一只短蜡烛固定在烧杯内,点燃。拿起收集满二氧化碳的集气瓶,向烧杯内缓缓倾倒二氧化碳 燃着蜡烛熄灭 ______
实验二 有两支分别盛有 2mL 蒸馏水的试管。实验步骤:(1)______;(2)______ 一支试管里的溶液颜色为紫色,另一只试管里的溶液______ 二氧化碳与水反应
实验三 取一支试管,向其中注入少量澄清石灰水,然后通入二氧化碳 ______ 二氧 化 碳与 石灰水 反 应
四、计算题(本大题共3小题)
25.河蚌是白洋淀一种常见的水生动物,河蚌壳的主要成分是 CaCO3,某课外活动小组为了测定其含量进行了如图所示实验,请计算:(计算结果精确至 0.1%,假设杂质不溶于水也不与稀盐酸反应)。
(1)反应中生成二氧化碳______g。
(2)该河蚌壳中碳酸钙的质量分数。
26.小明同学为测定含有碳粉的Cu的质量分数。将10g混合物放在如图1所示的装置中,不断通入O2,并将生成的气体用足量的澄清石灰水吸收。测得反应过程烧杯质量变化如表所示。
时间/s t0 t1 t2 t3 t4 t5 t6
烧杯及溶液质量/g 150 160 167 170 171 172 172
(1)求混合物中铜的质量分数______ (写出计算过程)。
(2)请在图2中画出CO2的质量随时间变化的曲线______。
(3)小芳同学认为,小明同学设计的实验装置不科学,导致测得的Cu的质量分数不准确。你认为是______(填“偏大”或“偏小”),理由是______。
27.某化学兴趣小组为测定实验室废弃的氧化铜样品中CuO的质量分数,称取5g该氧化铜样品,用下图所示的装置进行实验(样品中杂质不反应),充分反应后测得B装置的质量增加了2.2g。
回答下列问题:
(1)装置A中反应的文字表达式是____。
(2)生成CO2的质量为____g。
(3)计算该氧化铜样品中CuO的质量分数______(写出计算过程)。
参考答案:
1.A
2.A
3.D
4.C
5.D
6.A
7.B
8.B
9.D
10.D
11.B
12.B
13.A
14.B
15.(1)物理变化
(2)利用二氧化碳资源,不产生有毒有害物质,环保节约
16.(1)2H2O22H2O+O2↑或2KMnO4K2MnO4+MnO2+O2↑或2KClO32KCl+3O2↑
(2) 长颈漏斗下端伸入液面下 浓硫酸
17.(1)
(2) 黑色粉末变为红色
(3)处理尾气,防止空气污染
18.(1)温室效应
(2) (合理答案均可) 剧烈燃烧,发出白光,生成使澄清石灰水变浑浊气体
(3)灭火或人工降雨(合理答案均可)
19. C60 石墨 石墨质软、有深灰色
20.(1)常温下化学性质稳定
(2)8:1
(3)4H2O2+PbS=PbSO4+4H2O
21.(1) 隔离可燃物
(2)导热
(3)C
22.(1)集气瓶
(2) AD
(3) C 部分二氧化碳溶于水 在集气瓶中的水面上覆盖一层植物油
23.(1)变红
(2)干燥气体
(3)CO2+Ca(OH)2=CaCO3↓+H2O
24. CO2不可燃不助燃密度比空气大 向两支试管中各滴入1-2滴石蕊溶液; 向其中一支试管中通入二氧化碳 变红 澄清石灰水变浑浊
25.(1)8.8
(2)解:设 21g 河蚌壳中所含碳酸钙的质量为 x。
河蚌壳中碳酸钙的质量分数为
答:该河蚌壳中碳酸钙的质量分数为 95.2%。
26.(1)烧杯及溶液增加的质量即为反应生成二氧化碳的质量,生成二氧化碳的质量为:172g-150g=22g
解:设混合物中碳的质量为x
x=6g
故混合物中铜的质量分数为:
(2)
(3) 偏小 澄清石灰水溶液露置在空气中,会吸收空气中的二氧化碳
27.(1)
(2)2.2
(3)80%
解:设该氧化铜样品中CuO的质量分数为x
x=80%
答:该氧化铜样品中CuO的质量分数为80%。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
