化学人教版(2019)必修第一册1.1.3物质的转化(共21张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.3物质的转化(共21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-24 00:00:00 | ||
图片预览




文档简介
(共21张PPT)
第一章 物质的转化
核心素养
(1)能对酸、碱、盐、氧化物及它们之间的反应进行描述和符号表征。
(2)通过归纳相关物间的化学反应关系,建立物质转化模型,认识物质的变化规律。
酸碱盐的分类
一
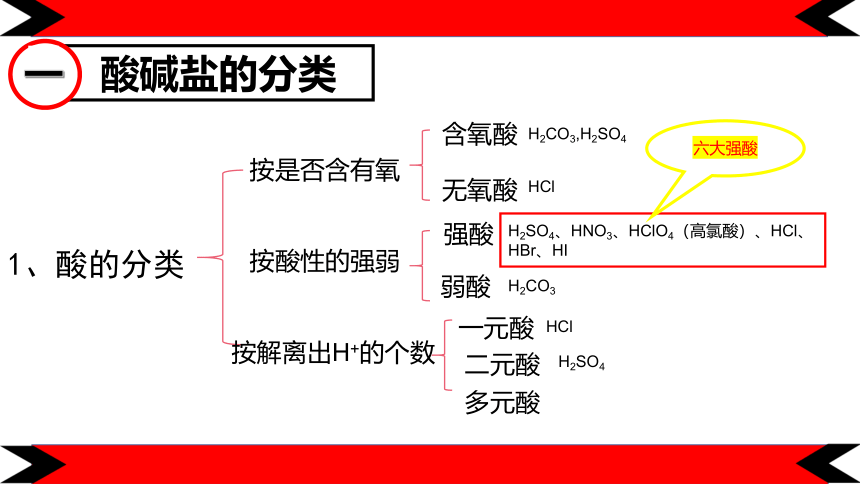
1、酸的分类
按是否含有氧
按酸性的强弱
按解离出H+的个数
含氧酸
无氧酸
强酸
弱酸
一元酸
二元酸
多元酸
H2CO3,H2SO4
HCl
H2SO4、HNO3、HClO4(高氯酸)、HCl、HBr、HI
H2CO3
HCl
H2SO4
六大强酸
Cu(OH)2、Mg(OH)2
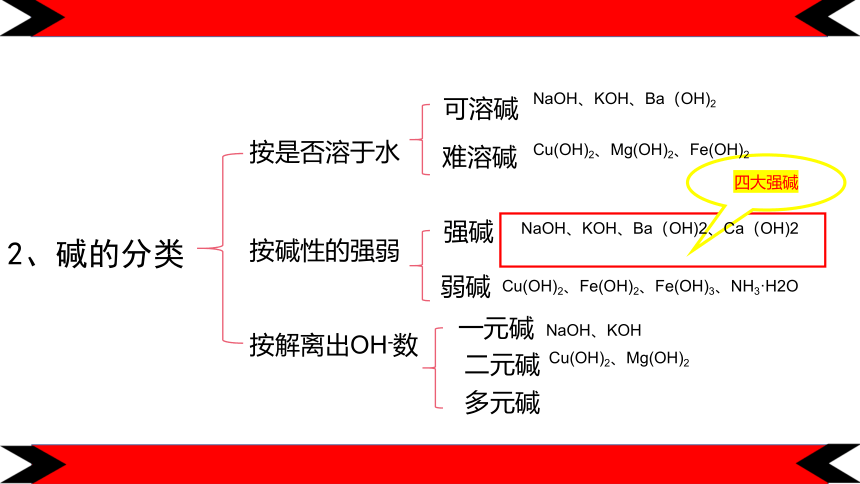
2、碱的分类
按是否溶于水
按碱性的强弱
按解离出OH-数
强碱
弱碱
可溶碱
难溶碱
一元碱
二元碱
多元碱
NaOH、KOH、Ba(OH)2
四大强碱
Cu(OH)2、Mg(OH)2、Fe(OH)2
NaOH、KOH、Ba(OH)2、Ca(OH)2
Cu(OH)2、Fe(OH)2、Fe(OH)3、NH3·H2O
NaOH、KOH
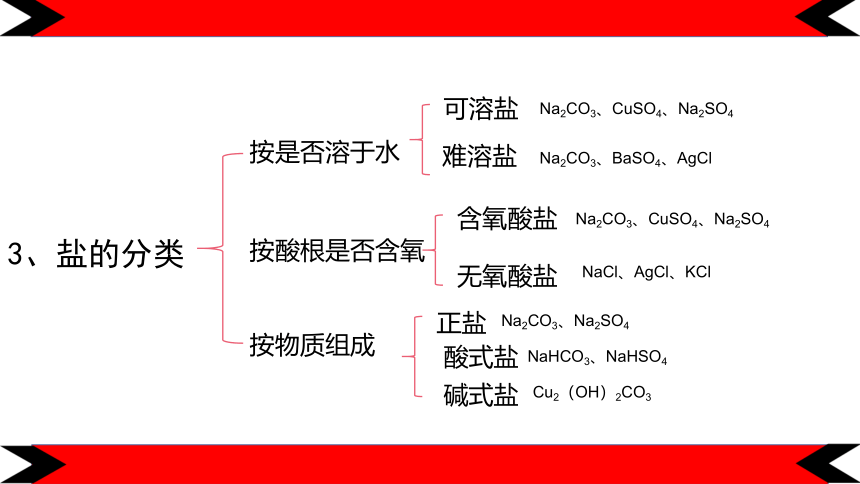
3、盐的分类
按是否溶于水
按酸根是否含氧
按物质组成
含氧酸盐
无氧酸盐
可溶盐
难溶盐
正盐
酸式盐
碱式盐
Na2CO3、CuSO4、Na2SO4
Na2CO3、BaSO4、AgCl
Na2CO3、CuSO4、Na2SO4
NaCl、AgCl、KCl
Na2CO3、Na2SO4
NaHCO3、NaHSO4
Cu2(OH)2CO3
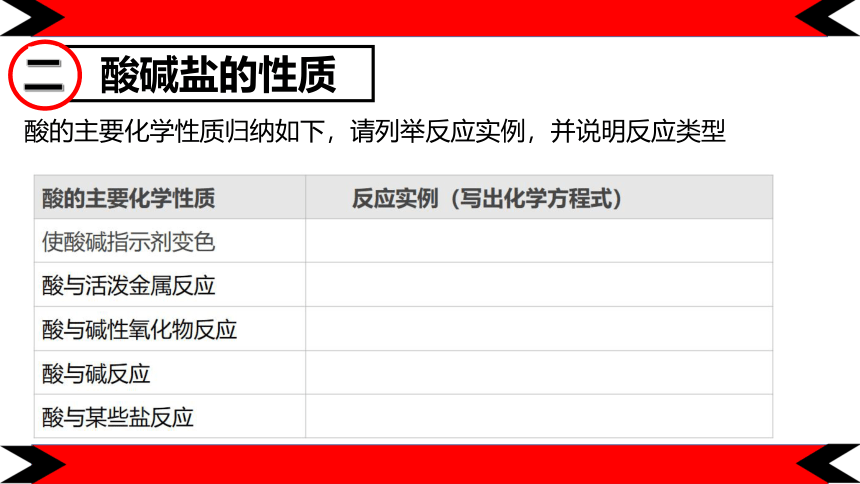
酸碱盐的性质
二
酸的主要化学性质归纳如下,请列举反应实例,并说明反应类型
远程教习
碱的主要化学性质归纳如下,请列举反应实例,并说明反应类型
盐的主要化学性质归纳如下,请列举反应实例,并说明反应类型
思考与讨论
?
1.为什么不同的酸(或碱)具有相似的化学性质?
解析:从微观角度看,不同的酸溶液中都会有H+,不同的碱溶液中都含有OH-,故具有相似的化学性质。
2.SO2和CO2同为酸性氧化物,试根据CO2的性质,推测二氧化硫具有的性质,用化学方程式表示:
解析: ①SO2+H2O = H2SO3
②SO2+CaO = CaSO3
③SO2+Ca(OH)2 = CaSO3↓+H2O
3.有同学认为向氯化钙溶液中通入二氧化碳气体会发生反应生成碳酸钙沉淀,反应的化学方程式为
CaCl2+H2O+CO2 = CaCO3↓+2HCl,该判断正确吗?
不正确。一般“强酸制弱酸”,即强酸与弱酸盐反应生成弱酸和强酸盐,
且难溶碳酸盐都易溶于强酸溶液中。
【思考与交流】写出下列物质之间转化的化学方程式:
物质的转化
三
从物质分类角度看,你发现了什么规律?
思考
工业上制取NaOH可以采用什么方法?
思考
工业生产中需要考虑反应进行的可能性、原料来源、成本高低和设备要求等因素
工业上常用熟石灰制备方法——石灰消化法,将石灰石煅烧成氧化钙后,经精选与水按1:(3~3.5)的比例混合,生成氢氧化钙料液,经净化分离除渣,再经离心、脱水、干燥,即制得氢氧化钙成品。反应的化学方程式:
该方法有什么优点?
小试牛刀
小试牛刀
2.采用三种不同的方法制取MgCl2,写出化学方程式并说明反应类型。
小试牛刀
3.物质之间的相互转化,可以直接实现,也可以间接实现,下列转化可以一步实现的是( )
小试牛刀
4.下列关于化学反应类型的叙述正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加或生成
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物中一定有单质
第一章 物质的转化
核心素养
(1)能对酸、碱、盐、氧化物及它们之间的反应进行描述和符号表征。
(2)通过归纳相关物间的化学反应关系,建立物质转化模型,认识物质的变化规律。
酸碱盐的分类
一
1、酸的分类
按是否含有氧
按酸性的强弱
按解离出H+的个数
含氧酸
无氧酸
强酸
弱酸
一元酸
二元酸
多元酸
H2CO3,H2SO4
HCl
H2SO4、HNO3、HClO4(高氯酸)、HCl、HBr、HI
H2CO3
HCl
H2SO4
六大强酸
Cu(OH)2、Mg(OH)2
2、碱的分类
按是否溶于水
按碱性的强弱
按解离出OH-数
强碱
弱碱
可溶碱
难溶碱
一元碱
二元碱
多元碱
NaOH、KOH、Ba(OH)2
四大强碱
Cu(OH)2、Mg(OH)2、Fe(OH)2
NaOH、KOH、Ba(OH)2、Ca(OH)2
Cu(OH)2、Fe(OH)2、Fe(OH)3、NH3·H2O
NaOH、KOH
3、盐的分类
按是否溶于水
按酸根是否含氧
按物质组成
含氧酸盐
无氧酸盐
可溶盐
难溶盐
正盐
酸式盐
碱式盐
Na2CO3、CuSO4、Na2SO4
Na2CO3、BaSO4、AgCl
Na2CO3、CuSO4、Na2SO4
NaCl、AgCl、KCl
Na2CO3、Na2SO4
NaHCO3、NaHSO4
Cu2(OH)2CO3
酸碱盐的性质
二
酸的主要化学性质归纳如下,请列举反应实例,并说明反应类型
远程教习
碱的主要化学性质归纳如下,请列举反应实例,并说明反应类型
盐的主要化学性质归纳如下,请列举反应实例,并说明反应类型
思考与讨论
?
1.为什么不同的酸(或碱)具有相似的化学性质?
解析:从微观角度看,不同的酸溶液中都会有H+,不同的碱溶液中都含有OH-,故具有相似的化学性质。
2.SO2和CO2同为酸性氧化物,试根据CO2的性质,推测二氧化硫具有的性质,用化学方程式表示:
解析: ①SO2+H2O = H2SO3
②SO2+CaO = CaSO3
③SO2+Ca(OH)2 = CaSO3↓+H2O
3.有同学认为向氯化钙溶液中通入二氧化碳气体会发生反应生成碳酸钙沉淀,反应的化学方程式为
CaCl2+H2O+CO2 = CaCO3↓+2HCl,该判断正确吗?
不正确。一般“强酸制弱酸”,即强酸与弱酸盐反应生成弱酸和强酸盐,
且难溶碳酸盐都易溶于强酸溶液中。
【思考与交流】写出下列物质之间转化的化学方程式:
物质的转化
三
从物质分类角度看,你发现了什么规律?
思考
工业上制取NaOH可以采用什么方法?
思考
工业生产中需要考虑反应进行的可能性、原料来源、成本高低和设备要求等因素
工业上常用熟石灰制备方法——石灰消化法,将石灰石煅烧成氧化钙后,经精选与水按1:(3~3.5)的比例混合,生成氢氧化钙料液,经净化分离除渣,再经离心、脱水、干燥,即制得氢氧化钙成品。反应的化学方程式:
该方法有什么优点?
小试牛刀
小试牛刀
2.采用三种不同的方法制取MgCl2,写出化学方程式并说明反应类型。
小试牛刀
3.物质之间的相互转化,可以直接实现,也可以间接实现,下列转化可以一步实现的是( )
小试牛刀
4.下列关于化学反应类型的叙述正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加或生成
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物中一定有单质
