第一章第一节第三课时《胶体》课件2022-2023学年高一上学期化学人教版(2019)必修第一册(22张ppt)
文档属性
| 名称 | 第一章第一节第三课时《胶体》课件2022-2023学年高一上学期化学人教版(2019)必修第一册(22张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-24 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
CLASSIFICATION AND TRANSFORMATION OF SUBSTANCES
物质的分类及转化
第三课时 胶体
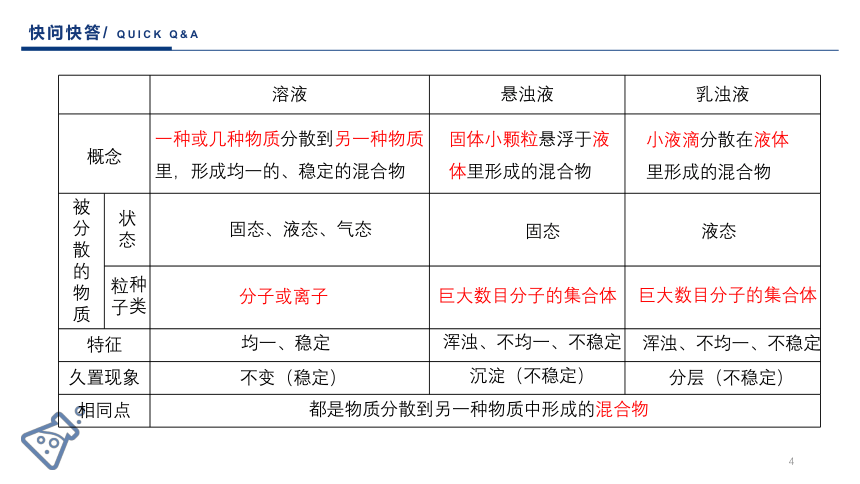
最强大脑/SUPERBRAIN为什么聚光灯可以在空气中照射出一条直线?温故知新/REVIEW溶液乳浊液悬浊液从物质分类的角度看,CuSO4溶液、振荡后的植物油与水的混合物、泥水属于什么类?思考:溶液、乳浊液、悬浊液的区别和联系快问快答/QUICKQ&A溶液悬浊液乳浊液概念被分散的物质状态粒子特征久置现象相同点一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物固体小颗粒悬浮于液体里形成的混合物小液滴分散在液体里形成的混合物分子或离子巨大数目分子的集合体巨大数目分子的集合体均一、稳定浑浊、不均一、不稳定浑浊、不均一、不稳定不变(稳定)沉淀(不稳定)分层(不稳定)都是物质分散到另一种物质中形成的混合物种类固态、液态、气态固态液态分散系/DISPERSIONSYSTEM1.分散系的概念及组成(1)概念化学上把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。(2)组成分散系中被分散成粒子的物质叫做分散质,另一种物质叫做分散剂。2.分散系的组合方式及分类(1)常见的三类分散系胶体分散质粒子的直径/nm溶液乳浊液或悬浊液01100① 分类依据:分散质粒子的直径大小② 类型:溶液、胶体、乳浊液或悬浊液分散系/DISPERSIONSYSTEM分散系/DISPERSIONSYSTEM2.分散系的组合方式及分类(2)分散质可以是气体、液体或固体,分散剂也可以是气体、液体或固体,因此分散系有____种组合方式。9分散质气液固分散剂气液固①②③④⑤⑥⑦⑧⑨胶体/COLLOID3.胶体的分类、制备与性质(1)胶体的分类根据分散剂的状态分类气溶胶:烟、云、雾液溶胶:Fe(OH)3胶体、豆浆、墨水、蛋白质溶液、淀粉溶液、血液固溶胶:烟水晶、有色玻璃胶体/COLLOID3.胶体的分类、制备与性质(2)胶体的性质① 丁达尔效应概念:当一束可见光通过胶体时,可以看到一条光亮的“通路”。这条光亮的“通路”是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,叫做丁达尔效应。3.胶体的分类、制备与性质(2)胶体的性质丁达尔效应可被用来区分胶体和溶液。Fe(OH)3胶体CuSO4溶液胶体/COLLOID3. 胶体的分类、制备与性质
(2)胶体的性质
常见的丁达尔效应:
胶体/COLLOID
美丽的夜景
树林中的晨曦
3. 胶体的分类、制备与性质
(2)胶体的性质
② 胶体的介稳性
溶液是稳定体系,浊液是不稳定体系,胶体属于介稳体系,在一定条件下能稳定存在。
静置前
静置后
CuSO4溶液
静置前
静置后
Fe(OH)3胶体
泥水
静置前
静置后
胶体/COLLOID
布朗运动/BROWNIANMOTION3. 胶体的分类、制备与性质
(2)胶体的性质
③ 聚沉
胶体聚沉的原理即中和胶体粒子的电荷或加快其胶体粒子的热运动以增加胶体粒子的结合机会。
常用方法有加入可溶性盐、加入带相反电荷胶粒的胶体或加热胶体。
向Fe(OH)3胶体中滴加NaCl溶液
胶体/COLLOID
3. 胶体的分类、制备与性质
(2)胶体的性质
④ 电泳
由于胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里作定向移动,这种现象叫做电泳。
Fe(OH)3胶体粒子带正电荷,在电场作用下,带正电荷的红褐色Fe(OH)3胶体粒子向负极移动。
负极
正极
胶体/COLLOID
胶体/COLLOID3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备FeCl3+ 3H2O Fe(OH)3(胶体) + 3HCl△实验原理:实验操作:取1个100 mL小烧杯,向烧杯中加入40 mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐渐滴加入5~6滴FeCl3饱和溶液。继续煮沸至液体呈红褐色,停止加热。3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备注意事项:① 实验中必须使用FeCl3饱和溶液和沸水,一定不能用FeCl3溶液和NaOH溶液反应,否则产生的是Fe(OH)3沉淀。② 当液体呈红褐色时应立即停止加热,因为过度加热会破坏胶体,生成Fe(OH)3沉淀。③ 制备过程中不能用玻璃棒搅拌,否则会使Fe(OH)3胶体粒子碰撞形成大颗粒,最后形成沉淀。胶体/COLLOID3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备通过渗析实验可以提纯Fe(OH)3胶体。使杂质离子或分子从胶体里分离出来的操作叫渗析(也叫透析)。FeCl3+ 3H2OFe(OH)3(胶体) + 3HCl△Fe(OH)3胶体中可能含有较多的H+、Cl-,如图所示,将其放在半透膜中,浸在蒸馏水中,一段时间后,在蒸馏水中加入AgNO3溶液出现白色沉淀,说明Cl-透过半透膜进入了蒸馏水中。胶体/COLLOID3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备半透膜:半透膜由膀胱、鸡蛋内膜、牛皮纸、胶棉薄膜、玻璃纸等制成,有非常细小的孔,只能允许较小的离子、分子透过,而胶体不能透过。胶体/COLLOIDq溶液、胶体、浊液三类分散系的比较 溶液胶体浊液分散质粒子的直径分散质粒子种类 性质外观稳定性能否透过滤纸能否透过半透膜是否有丁达尔效应实例<1 nm1~100 nm>100 nm分子或离子许多分子集合体或高分子巨大数目分子集合体均一、透明绝大部分均一、透明浑浊稳定较稳定不稳定能能不能能不能不能没有有没有NaCl溶液Fe(OH)3胶体泥水胶体/COLLOID3. 胶体的分类、制备与性质
请用胶体的性质解释自然及日常生活中的现象:
① 工业除尘
② 河流入海处“三角洲”的形成
③ 点豆腐
④ 明矾净水
⑤ 用FeCl3溶液止血
⑥ 用微波手术刀进行外科手术
⑦不同牌子的墨水混合会造成钢笔堵塞
⑧血液透析
⑨土壤保肥
胶体/COLLOID
思维导图
物质
纯净物
混合物
单质
化合物
非金属单质(如C)
金属单质(如Fe)
氧化物
酸
盐
碱
酸性氧化物(如CO )
碱性氧化物(如Na O)
按强弱
按电离出的H+数
强酸(如HCI)
弱酸(如CH COOH)
一元酸(如HCI)
二元酸(如H SO )
多元酸(如H PO )
按强弱
按电离出的OH-数
强碱(如NaOH)
弱碱(如NH ·H O)
一元碱(如NaOH)
二元碱(如Ba(OH) )
多元碱(如Fe(OH) )
正盐(如Na CO )
碱式盐(如Cu (OH) CO )
酸式盐(如NaHCO )
溶液(如NaCI溶液)
胶体[如Fe(OH) 胶体]
浊液
悬浊液(如泥水混合物)
乳浊液(如油水混合物)
CLASSIFICATION AND TRANSFORMATION OF SUBSTANCES
物质的分类及转化
第三课时 胶体
最强大脑/SUPERBRAIN为什么聚光灯可以在空气中照射出一条直线?温故知新/REVIEW溶液乳浊液悬浊液从物质分类的角度看,CuSO4溶液、振荡后的植物油与水的混合物、泥水属于什么类?思考:溶液、乳浊液、悬浊液的区别和联系快问快答/QUICKQ&A溶液悬浊液乳浊液概念被分散的物质状态粒子特征久置现象相同点一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物固体小颗粒悬浮于液体里形成的混合物小液滴分散在液体里形成的混合物分子或离子巨大数目分子的集合体巨大数目分子的集合体均一、稳定浑浊、不均一、不稳定浑浊、不均一、不稳定不变(稳定)沉淀(不稳定)分层(不稳定)都是物质分散到另一种物质中形成的混合物种类固态、液态、气态固态液态分散系/DISPERSIONSYSTEM1.分散系的概念及组成(1)概念化学上把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。(2)组成分散系中被分散成粒子的物质叫做分散质,另一种物质叫做分散剂。2.分散系的组合方式及分类(1)常见的三类分散系胶体分散质粒子的直径/nm溶液乳浊液或悬浊液01100① 分类依据:分散质粒子的直径大小② 类型:溶液、胶体、乳浊液或悬浊液分散系/DISPERSIONSYSTEM分散系/DISPERSIONSYSTEM2.分散系的组合方式及分类(2)分散质可以是气体、液体或固体,分散剂也可以是气体、液体或固体,因此分散系有____种组合方式。9分散质气液固分散剂气液固①②③④⑤⑥⑦⑧⑨胶体/COLLOID3.胶体的分类、制备与性质(1)胶体的分类根据分散剂的状态分类气溶胶:烟、云、雾液溶胶:Fe(OH)3胶体、豆浆、墨水、蛋白质溶液、淀粉溶液、血液固溶胶:烟水晶、有色玻璃胶体/COLLOID3.胶体的分类、制备与性质(2)胶体的性质① 丁达尔效应概念:当一束可见光通过胶体时,可以看到一条光亮的“通路”。这条光亮的“通路”是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,叫做丁达尔效应。3.胶体的分类、制备与性质(2)胶体的性质丁达尔效应可被用来区分胶体和溶液。Fe(OH)3胶体CuSO4溶液胶体/COLLOID3. 胶体的分类、制备与性质
(2)胶体的性质
常见的丁达尔效应:
胶体/COLLOID
美丽的夜景
树林中的晨曦
3. 胶体的分类、制备与性质
(2)胶体的性质
② 胶体的介稳性
溶液是稳定体系,浊液是不稳定体系,胶体属于介稳体系,在一定条件下能稳定存在。
静置前
静置后
CuSO4溶液
静置前
静置后
Fe(OH)3胶体
泥水
静置前
静置后
胶体/COLLOID
布朗运动/BROWNIANMOTION3. 胶体的分类、制备与性质
(2)胶体的性质
③ 聚沉
胶体聚沉的原理即中和胶体粒子的电荷或加快其胶体粒子的热运动以增加胶体粒子的结合机会。
常用方法有加入可溶性盐、加入带相反电荷胶粒的胶体或加热胶体。
向Fe(OH)3胶体中滴加NaCl溶液
胶体/COLLOID
3. 胶体的分类、制备与性质
(2)胶体的性质
④ 电泳
由于胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里作定向移动,这种现象叫做电泳。
Fe(OH)3胶体粒子带正电荷,在电场作用下,带正电荷的红褐色Fe(OH)3胶体粒子向负极移动。
负极
正极
胶体/COLLOID
胶体/COLLOID3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备FeCl3+ 3H2O Fe(OH)3(胶体) + 3HCl△实验原理:实验操作:取1个100 mL小烧杯,向烧杯中加入40 mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐渐滴加入5~6滴FeCl3饱和溶液。继续煮沸至液体呈红褐色,停止加热。3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备注意事项:① 实验中必须使用FeCl3饱和溶液和沸水,一定不能用FeCl3溶液和NaOH溶液反应,否则产生的是Fe(OH)3沉淀。② 当液体呈红褐色时应立即停止加热,因为过度加热会破坏胶体,生成Fe(OH)3沉淀。③ 制备过程中不能用玻璃棒搅拌,否则会使Fe(OH)3胶体粒子碰撞形成大颗粒,最后形成沉淀。胶体/COLLOID3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备通过渗析实验可以提纯Fe(OH)3胶体。使杂质离子或分子从胶体里分离出来的操作叫渗析(也叫透析)。FeCl3+ 3H2OFe(OH)3(胶体) + 3HCl△Fe(OH)3胶体中可能含有较多的H+、Cl-,如图所示,将其放在半透膜中,浸在蒸馏水中,一段时间后,在蒸馏水中加入AgNO3溶液出现白色沉淀,说明Cl-透过半透膜进入了蒸馏水中。胶体/COLLOID3.胶体的分类、制备与性质(3)Fe(OH)3胶体的制备半透膜:半透膜由膀胱、鸡蛋内膜、牛皮纸、胶棉薄膜、玻璃纸等制成,有非常细小的孔,只能允许较小的离子、分子透过,而胶体不能透过。胶体/COLLOIDq溶液、胶体、浊液三类分散系的比较 溶液胶体浊液分散质粒子的直径分散质粒子种类 性质外观稳定性能否透过滤纸能否透过半透膜是否有丁达尔效应实例<1 nm1~100 nm>100 nm分子或离子许多分子集合体或高分子巨大数目分子集合体均一、透明绝大部分均一、透明浑浊稳定较稳定不稳定能能不能能不能不能没有有没有NaCl溶液Fe(OH)3胶体泥水胶体/COLLOID3. 胶体的分类、制备与性质
请用胶体的性质解释自然及日常生活中的现象:
① 工业除尘
② 河流入海处“三角洲”的形成
③ 点豆腐
④ 明矾净水
⑤ 用FeCl3溶液止血
⑥ 用微波手术刀进行外科手术
⑦不同牌子的墨水混合会造成钢笔堵塞
⑧血液透析
⑨土壤保肥
胶体/COLLOID
思维导图
物质
纯净物
混合物
单质
化合物
非金属单质(如C)
金属单质(如Fe)
氧化物
酸
盐
碱
酸性氧化物(如CO )
碱性氧化物(如Na O)
按强弱
按电离出的H+数
强酸(如HCI)
弱酸(如CH COOH)
一元酸(如HCI)
二元酸(如H SO )
多元酸(如H PO )
按强弱
按电离出的OH-数
强碱(如NaOH)
弱碱(如NH ·H O)
一元碱(如NaOH)
二元碱(如Ba(OH) )
多元碱(如Fe(OH) )
正盐(如Na CO )
碱式盐(如Cu (OH) CO )
酸式盐(如NaHCO )
溶液(如NaCI溶液)
胶体[如Fe(OH) 胶体]
浊液
悬浊液(如泥水混合物)
乳浊液(如油水混合物)
