1.1物质的分类及转化+第二课时(分散系及胶体)课件2022-2023学年高一上学期化学人教版(2019)必修第一册(24张ppt)
文档属性
| 名称 | 1.1物质的分类及转化+第二课时(分散系及胶体)课件2022-2023学年高一上学期化学人教版(2019)必修第一册(24张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 11.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-27 21:20:34 | ||
图片预览





文档简介
(共24张PPT)
第一章 第一节
物质的分类及转化
第二课时 分散系及胶体
【学习任务一】学习分散系的分类
从物质分类的角度看,CuSO4溶液、泥水、振荡后的植物油与水的混合物属于什么类?
分散系:把一种(或多种)物质以粒子形式分散在另一种(或多种)物质中所得到的体系
乳浊液
【思考与交流1】
分散质:被分散的物质
分散剂:起容纳分散质作用的物质
一、分散系的概念
溶液
悬浊液
【学习任务二】学习分散系的分类
以CuSO4溶液、泥水、振荡后的植物油与水为例,说说这三种分散系有什么相同点和不同点
分散剂相同
粒子直径大小不同、稳定性不同
1. 按分散质的粒子直径大小分——本质区别
溶液
胶体
浊液
< 1 nm
1nm 至100nm
>100nm
稳定
不稳定
介稳性
稳定性如何?
【思考与交流2】
二、分散质的分类
【学习任务一】学习分散系的分类
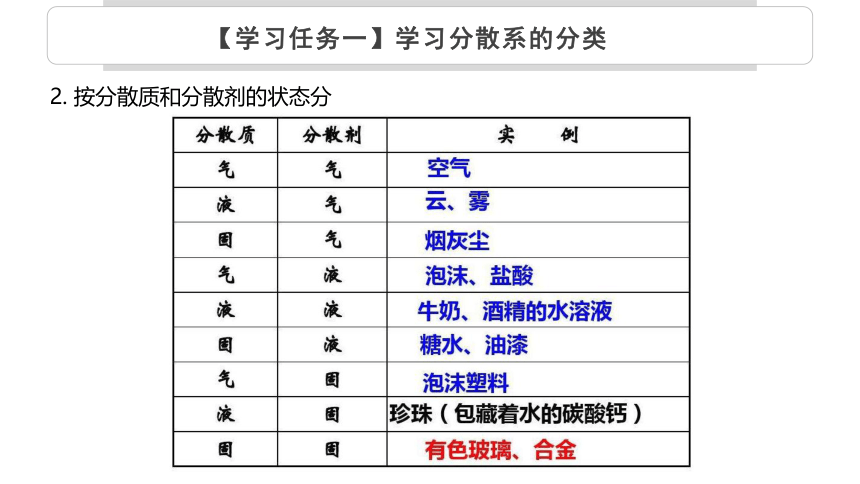
2. 按分散质和分散剂的状态分
【学习任务一】学习分散系的分类
【学习任务二】胶体的制备与性质
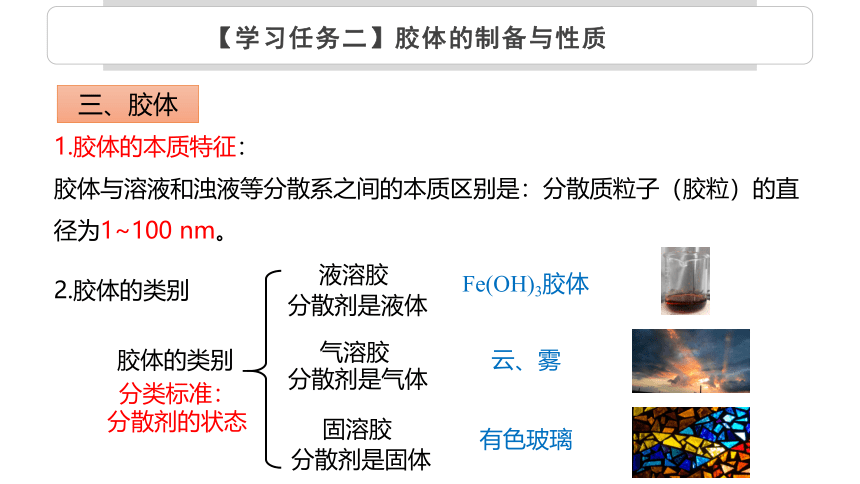
1.胶体的本质特征:
胶体与溶液和浊液等分散系之间的本质区别是:分散质粒子(胶粒)的直径为1~100 nm。
三、胶体
胶体的类别
气溶胶
分散剂是气体
固溶胶
分类标准:
分散剂的状态
分散剂是固体
Fe(OH)3胶体
云、雾
有色玻璃
液溶胶
分散剂是液体
2.胶体的类别
【学习任务二】胶体的制备与性质
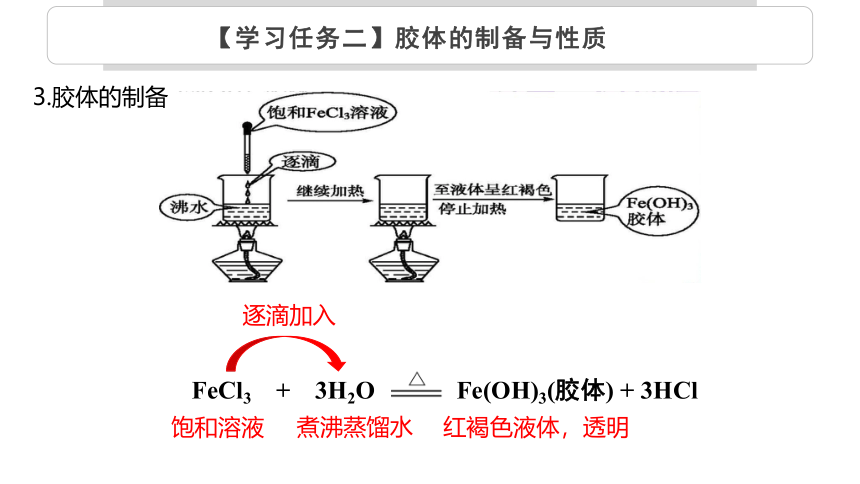
逐滴加入
饱和溶液
煮沸蒸馏水
红褐色液体,透明
FeCl3 + 3H2O Fe(OH)3(胶体) + 3HCl
3.胶体的制备
【学习任务二】胶体的制备与性质
(1)丁达尔效应——物理现象
当光束通过Fe(OH)3胶体时,可以看到一条光亮的“通路”,这条光亮的“通路”是由于胶体粒子对光线散射形成的,叫做丁达尔效应。
应用:区分胶体和溶液。
如何区分溶液和透明的胶体?
4.胶体的重要性质
【学习任务二】胶体的制备与性质
生活中的丁达尔效应
【学习任务二】胶体的制备与性质
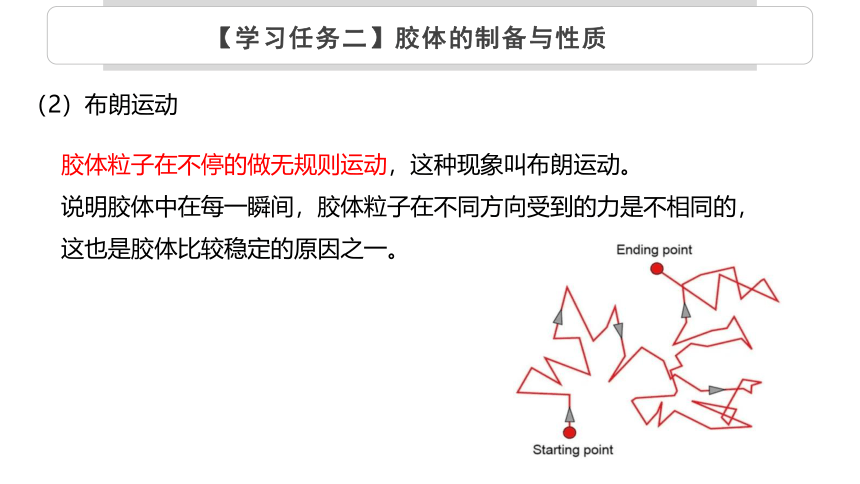
(2)布朗运动
胶体粒子在不停的做无规则运动,这种现象叫布朗运动。
说明胶体中在每一瞬间,胶体粒子在不同方向受到的力是不相同的,这也是胶体比较稳定的原因之一。
【学习任务二】胶体的制备与性质
通电前
通电后
问题1:观察到氢氧化铁胶体通电前后有什么变化?
问题2:产生这种变化的原因?
问题3:氢氧化铁胶体粒子带何种电荷?
【学习任务二】胶体的制备与性质
(3)电泳
在电场作用下,胶体粒子在分散剂中做定向移动的现象叫做电泳。
电泳现象证明,一些胶体粒子带有电荷。
注:(1)胶体不带电,呈电中性;
(2)不是所有胶体都有电泳现象,如淀粉胶体,因为淀粉胶粒不带电
应用:工厂静电除尘;冶金工业利用电泳原理选矿;利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上。
【学习任务二】胶体的制备与性质
胶体粒子聚集成较大颗粒,形成沉淀从分散剂里析出的过程。
(4)聚沉
聚沉的常用方法:
1、加热
原因:胶体粒子加速运动,增加碰撞机会,导致胶体凝聚而沉淀。
2、加电解质
原因:加入的离子中和了胶体粒子所带电荷,使胶粒聚集成较大颗粒而沉淀。
3、加带相反电荷胶体粒子的胶体
原因:带相反电荷胶粒相遇时互相中和电荷,从而聚集成大颗粒而沉积。
【学习任务二】胶体的制备与性质
应用:① 卤水点豆腐,②河流三角洲的形成、③用氯化铁溶液紧急止血、④制肥皂时在高级脂肪酸钠、甘油和水形成的混合物中加入食盐析出肥皂、⑤淀粉溶液加热后凝聚成了浆糊凝胶、⑥不同种类的墨水混合使用时有沉淀产生、⑦不同血型的人,不能相互输血等。
【学习任务二】胶体的制备与性质
【思考与交流3】某混合液中含泥沙、淀粉、氯化钠三种成分,如何将它们逐一分离开来?(提示:淀粉溶液是胶体)
【学习任务二】胶体的制备与性质
[实验一]
泥水的过滤
(固液分离)
[实验二]
泥沙
淀粉胶体
氯化钠溶液
过滤
泥沙
滤液
淀粉胶体
氯化钠溶液
渗析
胶体
(淀粉胶体)
(氯化钠溶液)
溶液
是一种提纯胶体方法
半透膜
怎样判断淀粉没有透过半透膜?
【学习任务二】胶体的制备与性质
利用半透膜分离胶体中的杂质分子或离子,提纯,精制胶体的操作称为渗析。
(5)渗析
应用:胶体的提纯,血液透析等。
透析(dialysis)是通过小分子经过半透膜扩散到水(或缓冲液)的原理,将小分子与生物大分子分开的一种分离技术。 血液透析是利用半透膜来清除患者体内多余的毒素以及水分,从而达到让血液净化的作用。
【小结】
分散系 溶液 胶体 浊液
分散质粒子直径大小 <1 nm 1~100 nm >100 nm
分散质粒子成分 离子或小分子 高分子化合物或分子集合体 巨大数目的分子集合体
性质 外观特征 均匀、透明 均匀、透明或半透明 不均匀、不透明
稳定性 稳定,静置无沉淀 较稳定 不稳定,静置有沉淀或分层
分散质能否透过滤纸 能 能 不能
分散质能否透过半透膜 能 不能 不能
鉴别 无丁达尔效应 丁达尔效应 静置沉降或分层
实例 食盐水、蔗糖溶液、酒精溶液 Fe(OH)3胶体、 淀粉溶胶 泥水、石灰乳、油水
【小结】
浊液
溶液
d<1nm
浊液
d>100nm
1nm胶体
【小结】
1、胶体粒子直径较溶质粒子大
2、胶体粒子直径较浊液粒子小
不能透过半透膜--渗析
丁达尔效应
能透过滤纸
比浊液稳定
吸附离子而带电
布朗运动
中和电荷
通直流电
聚沉
电泳
【课堂练习】
(1)溶液是纯净物,浊液是混合物。( )
(2)烟、雾、云都是气溶胶。( )
(3)溶液和胶体的本质区别是能否产生丁达尔效应。( )
(4)FeCl3溶液呈电中性,Fe(OH)3胶体带正电。( )
(5)江河入海口处易形成三角洲,这与胶体的性质有关。( )
1.判断题
2.选择题
(1)关于胶体和溶液的区别,下列叙述正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质微粒不能通过半透膜,胶体中分散质微粒能通过半透膜
C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线会出现光亮的通路
D.溶液稳定,放置后不会生成沉淀,胶体不稳定,放置后会生成沉淀
【课堂练习】
C
2.选择题
【课堂练习】
B
(2)某胶体中加入氯化镁的结晶水合物或石膏发生聚沉,而加入食盐水或硫酸钠溶液则聚沉效果差一些。下列有关说法正确的是( )
A.该胶体中胶粒的大小约是10-9~10-7 cm
B.该胶体遇氯化钡溶液或氢氧化铁胶体发生聚沉
C.电泳时该胶体粒子向阴极方向移动
D.氯离子对胶体聚沉的效果不如硫酸根离子
【视野拓展】
一、新冠病毒的传播
新型冠状病毒粒子直径约60-220nm,传播方式以飞沫传播和接触传播为主,也可能经气溶胶近距离传播。
飞沫、气溶胶等都属于分散系。胶体颗粒直径1nm-100nm, 胶体较稳定(介稳性),飞沫的颗粒直径>50um,在空气中悬浮时间较短。气溶胶可在空气中长时间悬浮达几个小时。
【视野拓展】
二、新冠病毒的检测
一款用于新型冠状病毒蛋白快速检测的试剂盒采用胶体金免疫层析法,做为免疫标记探针的胶体金粒子,其直径应在3-30nm范围内。检测时间短(15分钟以内),操作简单,肉眼可判断结果,可进行快速筛查,大大加快检测速度。
第一章 第一节
物质的分类及转化
第二课时 分散系及胶体
【学习任务一】学习分散系的分类
从物质分类的角度看,CuSO4溶液、泥水、振荡后的植物油与水的混合物属于什么类?
分散系:把一种(或多种)物质以粒子形式分散在另一种(或多种)物质中所得到的体系
乳浊液
【思考与交流1】
分散质:被分散的物质
分散剂:起容纳分散质作用的物质
一、分散系的概念
溶液
悬浊液
【学习任务二】学习分散系的分类
以CuSO4溶液、泥水、振荡后的植物油与水为例,说说这三种分散系有什么相同点和不同点
分散剂相同
粒子直径大小不同、稳定性不同
1. 按分散质的粒子直径大小分——本质区别
溶液
胶体
浊液
< 1 nm
1nm 至100nm
>100nm
稳定
不稳定
介稳性
稳定性如何?
【思考与交流2】
二、分散质的分类
【学习任务一】学习分散系的分类
2. 按分散质和分散剂的状态分
【学习任务一】学习分散系的分类
【学习任务二】胶体的制备与性质
1.胶体的本质特征:
胶体与溶液和浊液等分散系之间的本质区别是:分散质粒子(胶粒)的直径为1~100 nm。
三、胶体
胶体的类别
气溶胶
分散剂是气体
固溶胶
分类标准:
分散剂的状态
分散剂是固体
Fe(OH)3胶体
云、雾
有色玻璃
液溶胶
分散剂是液体
2.胶体的类别
【学习任务二】胶体的制备与性质
逐滴加入
饱和溶液
煮沸蒸馏水
红褐色液体,透明
FeCl3 + 3H2O Fe(OH)3(胶体) + 3HCl
3.胶体的制备
【学习任务二】胶体的制备与性质
(1)丁达尔效应——物理现象
当光束通过Fe(OH)3胶体时,可以看到一条光亮的“通路”,这条光亮的“通路”是由于胶体粒子对光线散射形成的,叫做丁达尔效应。
应用:区分胶体和溶液。
如何区分溶液和透明的胶体?
4.胶体的重要性质
【学习任务二】胶体的制备与性质
生活中的丁达尔效应
【学习任务二】胶体的制备与性质
(2)布朗运动
胶体粒子在不停的做无规则运动,这种现象叫布朗运动。
说明胶体中在每一瞬间,胶体粒子在不同方向受到的力是不相同的,这也是胶体比较稳定的原因之一。
【学习任务二】胶体的制备与性质
通电前
通电后
问题1:观察到氢氧化铁胶体通电前后有什么变化?
问题2:产生这种变化的原因?
问题3:氢氧化铁胶体粒子带何种电荷?
【学习任务二】胶体的制备与性质
(3)电泳
在电场作用下,胶体粒子在分散剂中做定向移动的现象叫做电泳。
电泳现象证明,一些胶体粒子带有电荷。
注:(1)胶体不带电,呈电中性;
(2)不是所有胶体都有电泳现象,如淀粉胶体,因为淀粉胶粒不带电
应用:工厂静电除尘;冶金工业利用电泳原理选矿;利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上。
【学习任务二】胶体的制备与性质
胶体粒子聚集成较大颗粒,形成沉淀从分散剂里析出的过程。
(4)聚沉
聚沉的常用方法:
1、加热
原因:胶体粒子加速运动,增加碰撞机会,导致胶体凝聚而沉淀。
2、加电解质
原因:加入的离子中和了胶体粒子所带电荷,使胶粒聚集成较大颗粒而沉淀。
3、加带相反电荷胶体粒子的胶体
原因:带相反电荷胶粒相遇时互相中和电荷,从而聚集成大颗粒而沉积。
【学习任务二】胶体的制备与性质
应用:① 卤水点豆腐,②河流三角洲的形成、③用氯化铁溶液紧急止血、④制肥皂时在高级脂肪酸钠、甘油和水形成的混合物中加入食盐析出肥皂、⑤淀粉溶液加热后凝聚成了浆糊凝胶、⑥不同种类的墨水混合使用时有沉淀产生、⑦不同血型的人,不能相互输血等。
【学习任务二】胶体的制备与性质
【思考与交流3】某混合液中含泥沙、淀粉、氯化钠三种成分,如何将它们逐一分离开来?(提示:淀粉溶液是胶体)
【学习任务二】胶体的制备与性质
[实验一]
泥水的过滤
(固液分离)
[实验二]
泥沙
淀粉胶体
氯化钠溶液
过滤
泥沙
滤液
淀粉胶体
氯化钠溶液
渗析
胶体
(淀粉胶体)
(氯化钠溶液)
溶液
是一种提纯胶体方法
半透膜
怎样判断淀粉没有透过半透膜?
【学习任务二】胶体的制备与性质
利用半透膜分离胶体中的杂质分子或离子,提纯,精制胶体的操作称为渗析。
(5)渗析
应用:胶体的提纯,血液透析等。
透析(dialysis)是通过小分子经过半透膜扩散到水(或缓冲液)的原理,将小分子与生物大分子分开的一种分离技术。 血液透析是利用半透膜来清除患者体内多余的毒素以及水分,从而达到让血液净化的作用。
【小结】
分散系 溶液 胶体 浊液
分散质粒子直径大小 <1 nm 1~100 nm >100 nm
分散质粒子成分 离子或小分子 高分子化合物或分子集合体 巨大数目的分子集合体
性质 外观特征 均匀、透明 均匀、透明或半透明 不均匀、不透明
稳定性 稳定,静置无沉淀 较稳定 不稳定,静置有沉淀或分层
分散质能否透过滤纸 能 能 不能
分散质能否透过半透膜 能 不能 不能
鉴别 无丁达尔效应 丁达尔效应 静置沉降或分层
实例 食盐水、蔗糖溶液、酒精溶液 Fe(OH)3胶体、 淀粉溶胶 泥水、石灰乳、油水
【小结】
浊液
溶液
d<1nm
浊液
d>100nm
1nm
【小结】
1、胶体粒子直径较溶质粒子大
2、胶体粒子直径较浊液粒子小
不能透过半透膜--渗析
丁达尔效应
能透过滤纸
比浊液稳定
吸附离子而带电
布朗运动
中和电荷
通直流电
聚沉
电泳
【课堂练习】
(1)溶液是纯净物,浊液是混合物。( )
(2)烟、雾、云都是气溶胶。( )
(3)溶液和胶体的本质区别是能否产生丁达尔效应。( )
(4)FeCl3溶液呈电中性,Fe(OH)3胶体带正电。( )
(5)江河入海口处易形成三角洲,这与胶体的性质有关。( )
1.判断题
2.选择题
(1)关于胶体和溶液的区别,下列叙述正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质微粒不能通过半透膜,胶体中分散质微粒能通过半透膜
C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线会出现光亮的通路
D.溶液稳定,放置后不会生成沉淀,胶体不稳定,放置后会生成沉淀
【课堂练习】
C
2.选择题
【课堂练习】
B
(2)某胶体中加入氯化镁的结晶水合物或石膏发生聚沉,而加入食盐水或硫酸钠溶液则聚沉效果差一些。下列有关说法正确的是( )
A.该胶体中胶粒的大小约是10-9~10-7 cm
B.该胶体遇氯化钡溶液或氢氧化铁胶体发生聚沉
C.电泳时该胶体粒子向阴极方向移动
D.氯离子对胶体聚沉的效果不如硫酸根离子
【视野拓展】
一、新冠病毒的传播
新型冠状病毒粒子直径约60-220nm,传播方式以飞沫传播和接触传播为主,也可能经气溶胶近距离传播。
飞沫、气溶胶等都属于分散系。胶体颗粒直径1nm-100nm, 胶体较稳定(介稳性),飞沫的颗粒直径>50um,在空气中悬浮时间较短。气溶胶可在空气中长时间悬浮达几个小时。
【视野拓展】
二、新冠病毒的检测
一款用于新型冠状病毒蛋白快速检测的试剂盒采用胶体金免疫层析法,做为免疫标记探针的胶体金粒子,其直径应在3-30nm范围内。检测时间短(15分钟以内),操作简单,肉眼可判断结果,可进行快速筛查,大大加快检测速度。
