沪教版(全国)化学九年级上册课课练:2.1 第3课时 用过氧化氢、氯酸钾制取氧气(word版有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册课课练:2.1 第3课时 用过氧化氢、氯酸钾制取氧气(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 282.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-28 00:00:00 | ||
图片预览

文档简介
第2章 第1节 第3课时 用过氧化氢、氯酸钾制取氧气 建议用时:25分钟]
一、选择题
1.实验室制取氧气的装置如所示,下列有关叙述合理的是 ( )
A.锥形瓶里加入少量二氧化锰粉末,分液漏斗里盛放6%的过氧化氢溶液
B.集满氧气的集气瓶从水槽里取出后盖上玻璃片
C.集满氧气的集气瓶从水槽里取出后倒放在桌面上
D.观察到发生装置中刚开始产生气泡时,即可开始收集
2.[2020·云南改编] 下列有关催化剂的说法正确的是 ( )
A.在化学反应后其质量减少
B.在化学反应前后其化学性质发生了变化
C.在化学反应后其质量增加
D.催化剂能加快化学反应速率
3.如所示,过氧化氢(H2O2)在催化剂二氧化锰(MnO2)的作用下,迅速分解放出大量氧气,出现的现象是 ( )
A.气球胀大,红墨水左移 B.气球缩小,红墨水右移
C.气球胀大,红墨水右移 D.气球缩小,红墨水左移
4.查阅资料得知:马铃薯可代替二氧化锰作过氧化氢溶液分解的催化剂。下列有关催化剂的说法正确的是 ( )
A.二氧化锰只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂能使原本不发生的反应快速进行
D.用作催化剂的物质不可能是其他反应的反应物或生成物
二、填空题
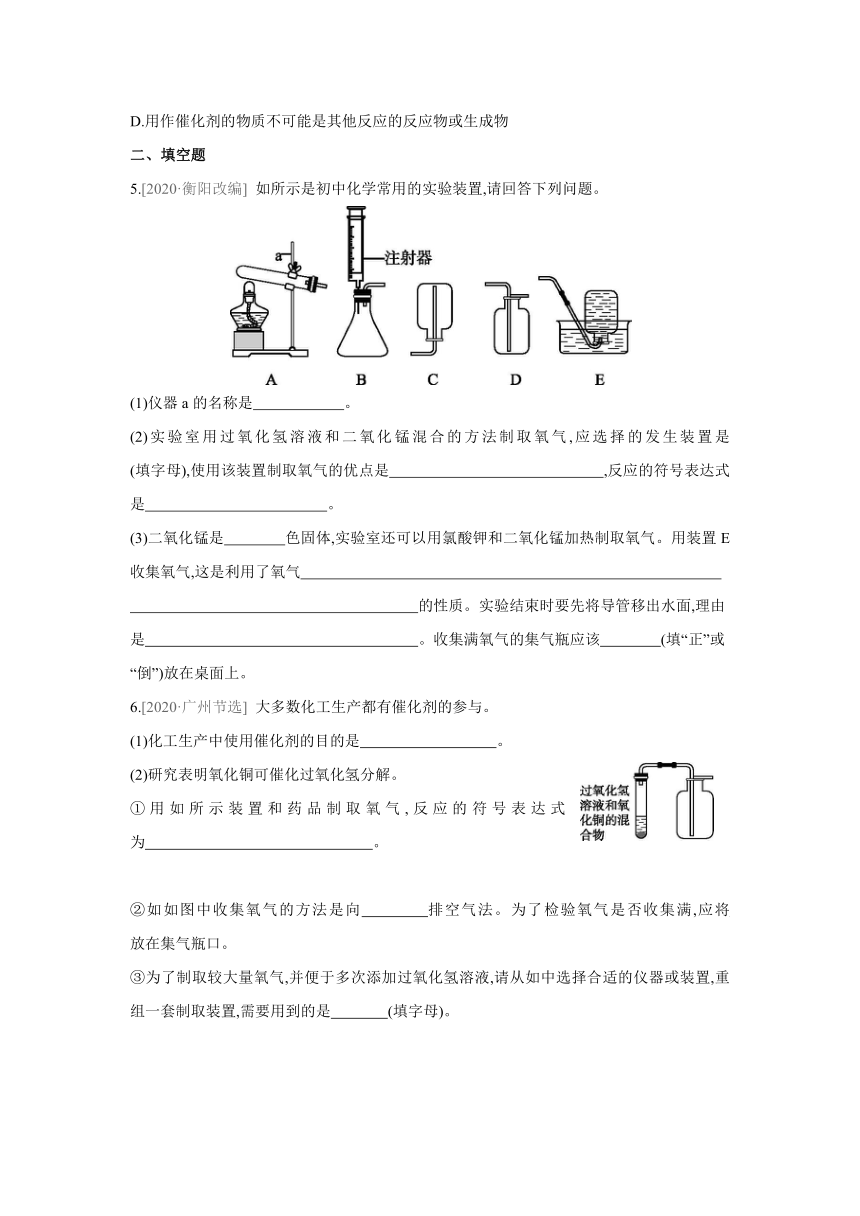
5.[2020·衡阳改编] 如所示是初中化学常用的实验装置,请回答下列问题。
(1)仪器a的名称是 。
(2)实验室用过氧化氢溶液和二氧化锰混合的方法制取氧气,应选择的发生装置是 (填字母),使用该装置制取氧气的优点是 ,反应的符号表达式是 。
(3)二氧化锰是 色固体,实验室还可以用氯酸钾和二氧化锰加热制取氧气。用装置E收集氧气,这是利用了氧气
的性质。实验结束时要先将导管移出水面,理由是 。收集满氧气的集气瓶应该 (填“正”或“倒”)放在桌面上。
6.[2020·广州节选] 大多数化工生产都有催化剂的参与。
(1)化工生产中使用催化剂的目的是 。
(2)研究表明氧化铜可催化过氧化氢分解。
①用如所示装置和药品制取氧气,反应的符号表达式为 。
②如如图中收集氧气的方法是向 排空气法。为了检验氧气是否收集满,应将 放在集气瓶口。
③为了制取较大量氧气,并便于多次添加过氧化氢溶液,请从如中选择合适的仪器或装置,重组一套制取装置,需要用到的是 (填字母)。
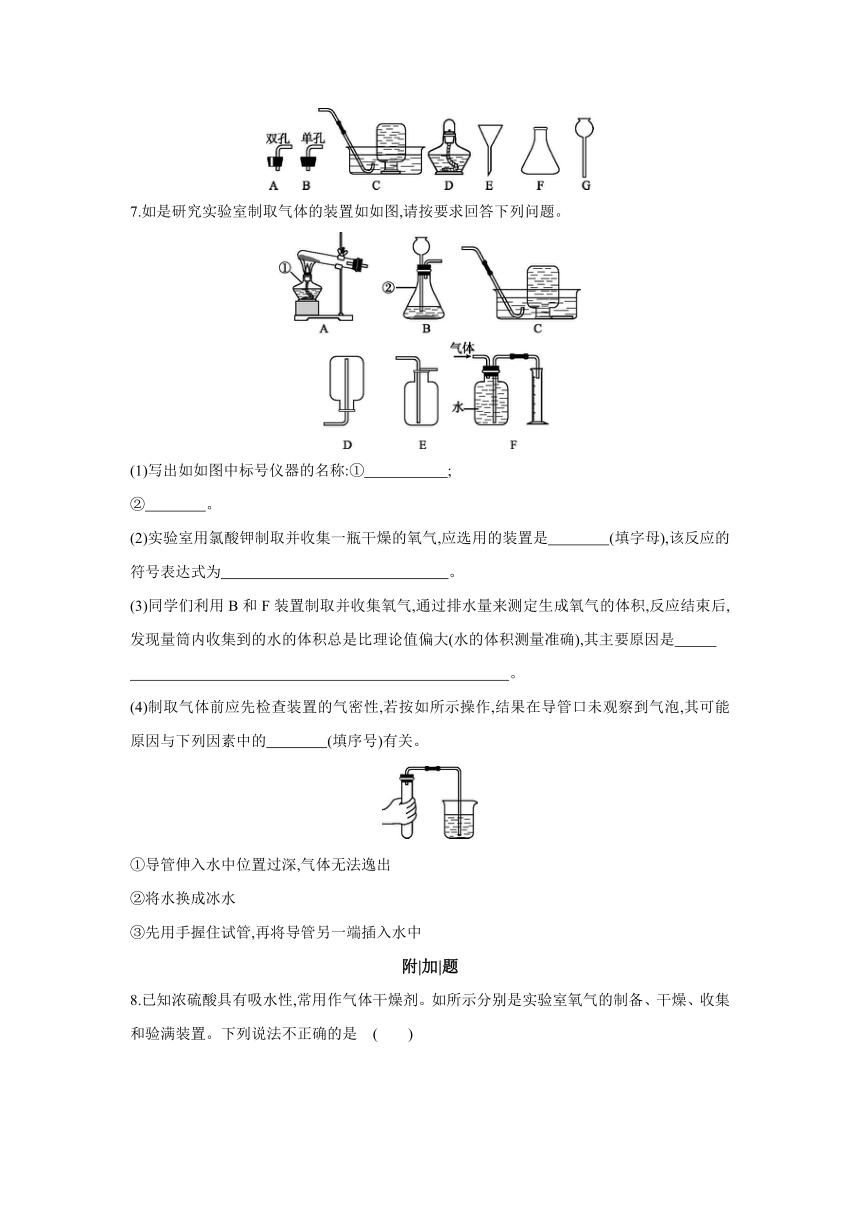
7.如是研究实验室制取气体的装置如如图,请按要求回答下列问题。
(1)写出如如图中标号仪器的名称:① ;
② 。
(2)实验室用氯酸钾制取并收集一瓶干燥的氧气,应选用的装置是 (填字母),该反应的符号表达式为 。
(3)同学们利用B和F装置制取并收集氧气,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是
。
(4)制取气体前应先检查装置的气密性,若按如所示操作,结果在导管口未观察到气泡,其可能原因与下列因素中的 (填序号)有关。
①导管伸入水中位置过深,气体无法逸出
②将水换成冰水
③先用手握住试管,再将导管另一端插入水中
附|加|题
8.已知浓硫酸具有吸水性,常用作气体干燥剂。如所示分别是实验室氧气的制备、干燥、收集和验满装置。下列说法不正确的是 ( )
A.装置①可作为制取氧气的发生装置 B.装置②干燥氧气时,气体由a端进b端出
C.装置③可用作制取氧气的收集装置 D.装置④是收集氧气的验满方法
9.取一定量的过氧化氢溶液于试管中,加入少量二氧化锰,充分反应后,中表示的反应过程与事实一致的是 ( )
10.某化学兴趣小组为比较氧化铜和二氧化锰对过氧化氢分解的催化效果,进行如下实验探究。
用如甲所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,再分别将注射器内盛有的3 mL 5%的过氧化氢溶液注入试管中,再利用注射器收集氧气,收集到氧气的体积和时间的关系如如如图乙所示。
(1)写出过氧化氢在二氧化锰的催化作用下制取氧气的符号表达式: ;
在检查装置的气密性后,小组同学开始实验时注入过氧化氢溶液的方法是 (填字母)。
A.快速推注射器活塞
B.缓慢推注射器活塞
实验中造成U形管内红墨水液面左低右高的原因是 。
(2)根据反应时 注射器中收集到氧气体积的不同,可比较两种催化剂的催化效果。通过如如图像除了能得出二氧化锰催化效果比氧化铜好外,还能得出的结论是
。
(3)由氧化铜催化的反应可知,t1~t2时间段反应速率逐渐变慢,原因是
。
答案
1.A 集满氧气的集气瓶从水槽里取出前,应在水面以下盖上玻璃片;氧气的密度比空气的大,集满氧气的集气瓶从水槽里取出后应正放在桌面上;发生装置中刚开始有气泡产生时,不能立即收集,要等到气泡连续均匀地放出时再收集。
2.D 催化剂是指能加快某些物质的化学反应速率,而自身的质量和化学性质在化学反应前后不变的物质,具有“一变,两不变”的特征。
3.D 过氧化氢在催化剂二氧化锰的作用下,迅速分解产生大量氧气,会造成瓶内压强增大,充气气球内的气体被挤压,故会观察到气球缩小,红墨水左移。
4.B 二氧化锰不是只能作为过氧化氢溶液分解的催化剂,还可以作氯酸钾分解的催化剂;根据题目的信息可知同一个化学反应可以有多种催化剂;催化剂只是加快化学反应的速率,不能使原本不发生的反应快速进行;用作催化剂的物质可能是其他反应的反应物或生成物,例如二氧化锰是高锰酸钾受热分解的生成物。
5.(1)铁架台
(2)B 可以控制化学反应的速率 H2O2H2O+O2
(3)黑 不易溶于水且不与水发生化学反应 防止冷水倒吸,使试管炸裂 正
(2)过氧化氢与二氧化锰混合制取氧气为固液反应且无需加热,所以发生装置为B;该装置中的注射器相当于分液漏斗,能控制液体的滴加速度,进而能控制反应速率;过氧化氢在二氧化锰催化作用下分解生成水和氧气,符号表达式为H2O2H2O+O2。(3)二氧化锰是黑色固体;氧气不易溶于水且不与水反应,决定了氧气可以采用排水法收集;结束时为了防止冷水倒吸,使试管炸裂,要先将导管移出水面;由于氧气的密度比空气稍大,所以收集满氧气的集气瓶应该正放在桌面上。
6.(1)加快化学反应速率
(2)①H2O2H2O+O2 ②上 带火星的木条 ③ACFG
(1)由催化剂的概念可知,化工生产使用催化剂的目的是加快化学反应速率。(2)①过氧化氢在氧化铜的催化作用下分解为水和氧气,符号表达式为H2O2H2O+O2。②如如图中收集氧气的方法是向上排空气法;氧气具有助燃性,为了检验氧气是否收集满,应将带火星的木条放在集气瓶口,若木条复燃,证明氧气已满。
7.(1)酒精灯 锥形瓶
(2)AE KClO3KCl+O2
(3)过氧化氢溶液进入锥形瓶中时,锥形瓶中一部分空气进入了F装置
(4)③
(3)当过氧化氢溶液从分液漏斗中流入锥形瓶中时,会将锥形瓶中的一部分空气排出并进入F装置,导致量筒内收集到的水的体积总是比理论值大。(4)检查装置气密性的方法:把导管的一端浸没在水里,双手紧握容器外壁,若导管口有气泡冒出,则装置不漏气。①导管伸入水中位置过深,②将水换成冰水,均不会影响气泡冒出;③先用手握住试管,试管内气体已经膨胀逸出,再将导管另一端插入水中会导致现象不明显。
8.D 利用装置①使用过氧化氢溶液和二氧化锰即可制取氧气;干燥氧气时,气体由a端进b端出,遵循“长进短出”的原则;氧气的密度比空气稍大,可以用装置③收集;验满时,应该把带火星的木条放在集气瓶口。
9.C 由于过氧化氢的质量一定,当其完全分解后,氧气的质量不会再发生变化;二氧化锰是过氧化氢分解的催化剂,反应前后质量不变;过氧化氢制取氧气时会放出大量的热,反应过程中溶液的温度会升高,当反应停止后,液体温度逐渐降低,直至降低至室温,不再变化;过氧化氢溶液中含有水,水的质量不能从0开始。
10.(1)H2O2H2O+O2 A 过氧化氢分解反应放热,使大试管内空气膨胀,压强变大
(2)单位(或相同)时间内 催化剂只能改变反应速率,不能改变生成氧气的总质量
(3)随着反应的进行,过氧化氢被消耗,t1~t2时间段过氧化氢浓度逐渐降低
(2)实验原理是利用单位(或相同)时间内注射器中收集到氧气体积的不同,从而比较两种催化剂的催化效果;分析如如图像可知,虽然二氧化锰的催化效果比氧化铜好,但最终生成氧气的总质量相同,所以还能得出的结论是催化剂只能改变反应速率,不能改变生成氧气的总质量。(3)反应物浓度越大,反应速率越快,分析如如图像可知,随着反应的进行过氧化氢被消耗,t1~t2时间段过氧化氢浓度逐渐降低,所以由氧化铜催化的反应,t1~t2时间段反应速率逐渐变慢。
一、选择题
1.实验室制取氧气的装置如所示,下列有关叙述合理的是 ( )
A.锥形瓶里加入少量二氧化锰粉末,分液漏斗里盛放6%的过氧化氢溶液
B.集满氧气的集气瓶从水槽里取出后盖上玻璃片
C.集满氧气的集气瓶从水槽里取出后倒放在桌面上
D.观察到发生装置中刚开始产生气泡时,即可开始收集
2.[2020·云南改编] 下列有关催化剂的说法正确的是 ( )
A.在化学反应后其质量减少
B.在化学反应前后其化学性质发生了变化
C.在化学反应后其质量增加
D.催化剂能加快化学反应速率
3.如所示,过氧化氢(H2O2)在催化剂二氧化锰(MnO2)的作用下,迅速分解放出大量氧气,出现的现象是 ( )
A.气球胀大,红墨水左移 B.气球缩小,红墨水右移
C.气球胀大,红墨水右移 D.气球缩小,红墨水左移
4.查阅资料得知:马铃薯可代替二氧化锰作过氧化氢溶液分解的催化剂。下列有关催化剂的说法正确的是 ( )
A.二氧化锰只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂能使原本不发生的反应快速进行
D.用作催化剂的物质不可能是其他反应的反应物或生成物
二、填空题
5.[2020·衡阳改编] 如所示是初中化学常用的实验装置,请回答下列问题。
(1)仪器a的名称是 。
(2)实验室用过氧化氢溶液和二氧化锰混合的方法制取氧气,应选择的发生装置是 (填字母),使用该装置制取氧气的优点是 ,反应的符号表达式是 。
(3)二氧化锰是 色固体,实验室还可以用氯酸钾和二氧化锰加热制取氧气。用装置E收集氧气,这是利用了氧气
的性质。实验结束时要先将导管移出水面,理由是 。收集满氧气的集气瓶应该 (填“正”或“倒”)放在桌面上。
6.[2020·广州节选] 大多数化工生产都有催化剂的参与。
(1)化工生产中使用催化剂的目的是 。
(2)研究表明氧化铜可催化过氧化氢分解。
①用如所示装置和药品制取氧气,反应的符号表达式为 。
②如如图中收集氧气的方法是向 排空气法。为了检验氧气是否收集满,应将 放在集气瓶口。
③为了制取较大量氧气,并便于多次添加过氧化氢溶液,请从如中选择合适的仪器或装置,重组一套制取装置,需要用到的是 (填字母)。
7.如是研究实验室制取气体的装置如如图,请按要求回答下列问题。
(1)写出如如图中标号仪器的名称:① ;
② 。
(2)实验室用氯酸钾制取并收集一瓶干燥的氧气,应选用的装置是 (填字母),该反应的符号表达式为 。
(3)同学们利用B和F装置制取并收集氧气,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是
。
(4)制取气体前应先检查装置的气密性,若按如所示操作,结果在导管口未观察到气泡,其可能原因与下列因素中的 (填序号)有关。
①导管伸入水中位置过深,气体无法逸出
②将水换成冰水
③先用手握住试管,再将导管另一端插入水中
附|加|题
8.已知浓硫酸具有吸水性,常用作气体干燥剂。如所示分别是实验室氧气的制备、干燥、收集和验满装置。下列说法不正确的是 ( )
A.装置①可作为制取氧气的发生装置 B.装置②干燥氧气时,气体由a端进b端出
C.装置③可用作制取氧气的收集装置 D.装置④是收集氧气的验满方法
9.取一定量的过氧化氢溶液于试管中,加入少量二氧化锰,充分反应后,中表示的反应过程与事实一致的是 ( )
10.某化学兴趣小组为比较氧化铜和二氧化锰对过氧化氢分解的催化效果,进行如下实验探究。
用如甲所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,再分别将注射器内盛有的3 mL 5%的过氧化氢溶液注入试管中,再利用注射器收集氧气,收集到氧气的体积和时间的关系如如如图乙所示。
(1)写出过氧化氢在二氧化锰的催化作用下制取氧气的符号表达式: ;
在检查装置的气密性后,小组同学开始实验时注入过氧化氢溶液的方法是 (填字母)。
A.快速推注射器活塞
B.缓慢推注射器活塞
实验中造成U形管内红墨水液面左低右高的原因是 。
(2)根据反应时 注射器中收集到氧气体积的不同,可比较两种催化剂的催化效果。通过如如图像除了能得出二氧化锰催化效果比氧化铜好外,还能得出的结论是
。
(3)由氧化铜催化的反应可知,t1~t2时间段反应速率逐渐变慢,原因是
。
答案
1.A 集满氧气的集气瓶从水槽里取出前,应在水面以下盖上玻璃片;氧气的密度比空气的大,集满氧气的集气瓶从水槽里取出后应正放在桌面上;发生装置中刚开始有气泡产生时,不能立即收集,要等到气泡连续均匀地放出时再收集。
2.D 催化剂是指能加快某些物质的化学反应速率,而自身的质量和化学性质在化学反应前后不变的物质,具有“一变,两不变”的特征。
3.D 过氧化氢在催化剂二氧化锰的作用下,迅速分解产生大量氧气,会造成瓶内压强增大,充气气球内的气体被挤压,故会观察到气球缩小,红墨水左移。
4.B 二氧化锰不是只能作为过氧化氢溶液分解的催化剂,还可以作氯酸钾分解的催化剂;根据题目的信息可知同一个化学反应可以有多种催化剂;催化剂只是加快化学反应的速率,不能使原本不发生的反应快速进行;用作催化剂的物质可能是其他反应的反应物或生成物,例如二氧化锰是高锰酸钾受热分解的生成物。
5.(1)铁架台
(2)B 可以控制化学反应的速率 H2O2H2O+O2
(3)黑 不易溶于水且不与水发生化学反应 防止冷水倒吸,使试管炸裂 正
(2)过氧化氢与二氧化锰混合制取氧气为固液反应且无需加热,所以发生装置为B;该装置中的注射器相当于分液漏斗,能控制液体的滴加速度,进而能控制反应速率;过氧化氢在二氧化锰催化作用下分解生成水和氧气,符号表达式为H2O2H2O+O2。(3)二氧化锰是黑色固体;氧气不易溶于水且不与水反应,决定了氧气可以采用排水法收集;结束时为了防止冷水倒吸,使试管炸裂,要先将导管移出水面;由于氧气的密度比空气稍大,所以收集满氧气的集气瓶应该正放在桌面上。
6.(1)加快化学反应速率
(2)①H2O2H2O+O2 ②上 带火星的木条 ③ACFG
(1)由催化剂的概念可知,化工生产使用催化剂的目的是加快化学反应速率。(2)①过氧化氢在氧化铜的催化作用下分解为水和氧气,符号表达式为H2O2H2O+O2。②如如图中收集氧气的方法是向上排空气法;氧气具有助燃性,为了检验氧气是否收集满,应将带火星的木条放在集气瓶口,若木条复燃,证明氧气已满。
7.(1)酒精灯 锥形瓶
(2)AE KClO3KCl+O2
(3)过氧化氢溶液进入锥形瓶中时,锥形瓶中一部分空气进入了F装置
(4)③
(3)当过氧化氢溶液从分液漏斗中流入锥形瓶中时,会将锥形瓶中的一部分空气排出并进入F装置,导致量筒内收集到的水的体积总是比理论值大。(4)检查装置气密性的方法:把导管的一端浸没在水里,双手紧握容器外壁,若导管口有气泡冒出,则装置不漏气。①导管伸入水中位置过深,②将水换成冰水,均不会影响气泡冒出;③先用手握住试管,试管内气体已经膨胀逸出,再将导管另一端插入水中会导致现象不明显。
8.D 利用装置①使用过氧化氢溶液和二氧化锰即可制取氧气;干燥氧气时,气体由a端进b端出,遵循“长进短出”的原则;氧气的密度比空气稍大,可以用装置③收集;验满时,应该把带火星的木条放在集气瓶口。
9.C 由于过氧化氢的质量一定,当其完全分解后,氧气的质量不会再发生变化;二氧化锰是过氧化氢分解的催化剂,反应前后质量不变;过氧化氢制取氧气时会放出大量的热,反应过程中溶液的温度会升高,当反应停止后,液体温度逐渐降低,直至降低至室温,不再变化;过氧化氢溶液中含有水,水的质量不能从0开始。
10.(1)H2O2H2O+O2 A 过氧化氢分解反应放热,使大试管内空气膨胀,压强变大
(2)单位(或相同)时间内 催化剂只能改变反应速率,不能改变生成氧气的总质量
(3)随着反应的进行,过氧化氢被消耗,t1~t2时间段过氧化氢浓度逐渐降低
(2)实验原理是利用单位(或相同)时间内注射器中收集到氧气体积的不同,从而比较两种催化剂的催化效果;分析如如图像可知,虽然二氧化锰的催化效果比氧化铜好,但最终生成氧气的总质量相同,所以还能得出的结论是催化剂只能改变反应速率,不能改变生成氧气的总质量。(3)反应物浓度越大,反应速率越快,分析如如图像可知,随着反应的进行过氧化氢被消耗,t1~t2时间段过氧化氢浓度逐渐降低,所以由氧化铜催化的反应,t1~t2时间段反应速率逐渐变慢。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
