沪教版(全国)化学九年级上册课课练:第1章 开启化学之门 自我综合评价(word版有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册课课练:第1章 开启化学之门 自我综合评价(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 212.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-28 00:00:00 | ||
图片预览




文档简介
自我综合评价
[测试范围:第1章 时间:40分钟 分值:100分]
一、选择题(每小题只有一个选项符合题意,每小题3分,共45分)
1.下列选项不是体现化学造福人类的是 ( )
A.新医药的研制 B.单晶硅的使用
C.隔水透气材料的发明 D.杂交水稻的成功
2.在实验室中,药品和仪器的存放应符合一定规范,如中物质存放在对应的容器中,符合规范的是 ( )
3.[2020·本溪] 下列如如图示实验操作中,正确的是 ( )
4.[2020·陕西] 变化无处不在。生活中的下列现象是由化学变化引起的是 ( )
A.柏油路面曝晒变软
B.水放冰箱结成冰块
C.铜器锈蚀颜色变绿
D.电流过大灯丝熔断
5.规范的操作是化学实验成功的保障。下列实验操作中正确的是 ( )
A.洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下,表明仪器已洗干净
B.固体药品可以直接放在天平的托盘上称量
C.加热后的试管应立即用冷水冲洗
D.为了便于观察,给试管里的液体加热时试管口对着自己
6.下列物质的用途,主要利用其化学性质的是 ( )
A.液氮用于医疗 B.用铝制作导线
C.石墨制铅笔芯 D.用煤炭作燃料
7.下列有关蜡烛燃烧的实验现象的叙述错误的是 ( )
A.蜡烛在空气中燃烧产生黄白色火焰,放热
B.在蜡烛火焰上方罩一个冷而干燥的烧杯,烧杯内壁有水珠出现
C.蜡烛燃烧时生成了二氧化碳和水
D.用火柴去引燃刚熄灭时蜡烛上方飘出的白烟,蜡烛重新燃烧
8.[2020·鸡西] 下列各组物质中,属于纯净物的是 ( )
A.医用生理盐水 B.瓶装矿泉水
C.冰水混合物 D.未经污染的空气
9.取8 mL的液体并加热,需要用到的仪器是 ( )
①烧杯 ②试管 ③胶头滴管 ④石棉网 ⑤试管夹 ⑥铁架台 ⑦10 mL量筒 ⑧50 mL量筒 ⑨酒精灯
A.①③④⑥⑦⑨ B.②⑤⑦⑨
C.②③⑤⑦⑨ D.②③⑤⑧⑨
10.用酒精灯给试管里的液体加热时,发现试管破裂,可能原因有:①用酒精灯的外焰给试管加热;②被加热的液体超过试管容积的;③加热时试管底部触及灯芯;④加热前没有擦干试管外壁的水;⑤没有进行预热,直接集中加热试管中的液体;⑥加热时没有不时地上下移动试管。其中与之相关的是 ( )
A.①③⑤⑥ B.②④ C.②③⑥ D.③④⑤
11.如所示,为防止燃气泄漏造成危险,可在食堂或家庭中安装报警器。下列燃气的性质中,能确定安装报警器位置的是 ( )
A.毒性 B.密度 C.气味 D.溶解性
12.在实验室中某同学把澄清石灰水滴入盛有人体呼出气体的集气瓶中,振荡。这一过程属于科学探究中的哪一重要环节 ( )
A.提出假设 B.进行实验
C.收集证据 D.得出结论
13.已知淀粉遇碘变蓝。小军同学在做唾液淀粉酶实验时,向热的面粉糊中加入碘酒,发现未变蓝。面对“异常”现象,他不应该采取的做法是 ( )
A.向老师请教 B.查找相关资料,探究原因
C.认为自己做错了,继续做其他实验 D.反复实验,并观察是否有相同现象
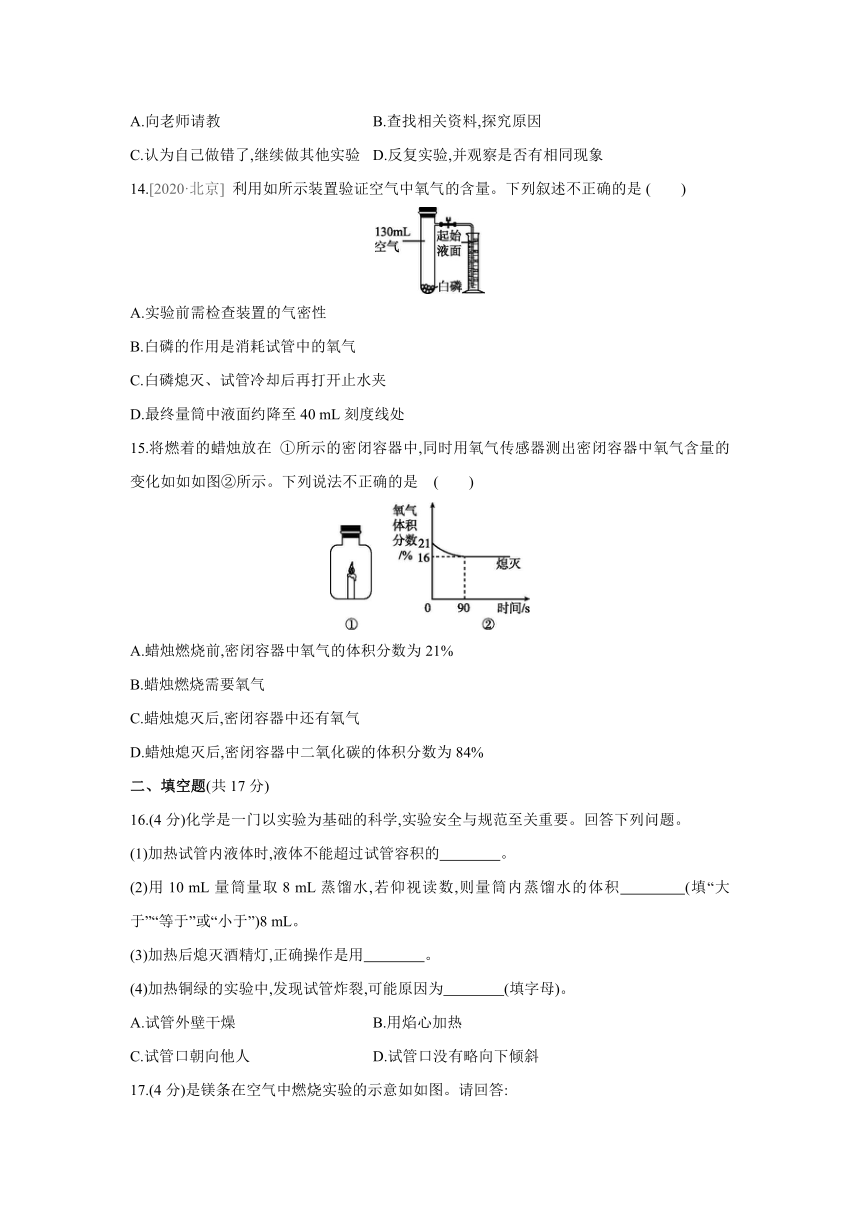
14.[2020·北京] 利用如所示装置验证空气中氧气的含量。下列叙述不正确的是 ( )
A.实验前需检查装置的气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄灭、试管冷却后再打开止水夹
D.最终量筒中液面约降至40 mL刻度线处
15.将燃着的蜡烛放在 ①所示的密闭容器中,同时用氧气传感器测出密闭容器中氧气含量的变化如如如图②所示。下列说法不正确的是 ( )
A.蜡烛燃烧前,密闭容器中氧气的体积分数为21%
B.蜡烛燃烧需要氧气
C.蜡烛熄灭后,密闭容器中还有氧气
D.蜡烛熄灭后,密闭容器中二氧化碳的体积分数为84%
二、填空题(共17分)
16.(4分)化学是一门以实验为基础的科学,实验安全与规范至关重要。回答下列问题。
(1)加热试管内液体时,液体不能超过试管容积的 。
(2)用10 mL量筒量取8 mL蒸馏水,若仰视读数,则量筒内蒸馏水的体积 (填“大于”“等于”或“小于”)8 mL。
(3)加热后熄灭酒精灯,正确操作是用 。
(4)加热铜绿的实验中,发现试管炸裂,可能原因为 (填字母)。
A.试管外壁干燥 B.用焰心加热
C.试管口朝向他人 D.试管口没有略向下倾斜
17.(4分)是镁条在空气中燃烧实验的示意如如图。请回答:
(1)夹持镁条的仪器名称是 。
(2)能说明镁条燃烧是化学变化的实验现象是 。
(3)实验完毕,发现桌面被烫坏了,原因可能是 。
(4)镁粉可用于军事上制作照明弹,是因为 。
18.(3分)根据材料,回答下列问题。
通常情况下,钾具有银白色光泽,质地十分柔软,可以用小刀切割。钾的熔点很低,只有63 ℃,也就是说,只要温度升高到63 ℃,金属钾就变成水银般的液体了。钾的密度很小,它比水还轻。钾的化学性质十分活泼,与水反应剧烈,当把一块钾放入水中时,你就会看到它不断地浮起落下,周身还冒出火焰;一会儿再看,水中的钾就消失了。原来,它跟水发生反应生成了氢氧化钾和氢气。钾与酸的水溶液反应更加剧烈,几乎能达到爆炸的程度。
(1)钾的物理性质有 。
(2)写出一条钾的化学性质: 。
(3)写出钾和水反应的文字表达式: 。
19.(6分)化学现象中包含发光、放热现象,许多物质燃烧时都伴随有发光、放热的现象。小明同学认为有发光、放热现象的变化不一定是化学变化,于是学习小组对此展开了探究与讨论。
(1)取适量红磷于燃烧匙中,在酒精灯上点燃。实验现象为产生黄白色火焰,放出大量热,生成大量白烟。
分析:红磷燃烧属于 变化,该反应的文字表达式为 。
(2)观察白炽灯(灯丝为钨丝):
通电前 通电中 通电后
灯丝为灰黑色固体 发出白光,手摸灯泡感觉发烫 灯丝为灰黑色固体
分析:根据通电前后,钨丝本身没有发生变化,灯泡通电发光、放热属于 变化。
三、实验探究题(共38分)
20.(14分)为了测定空气中氧气含量,某兴趣小组设计以下实验进行探究。
Ⅰ.燃烧红磷法测定空气中氧气的含量。
实验原理:利用红磷在空气中燃烧生成五氧化二磷固体,集气瓶内压强减小,使烧杯内水倒流入集气瓶中。写出红磷在空气中燃烧的符号表达式: 。
[实验步骤] (1)用弹簧夹夹紧乳胶管。
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞。
(3) (补全实验步骤)。
(4)观察到水倒流至集气瓶并记录水面的变化情况。
[实验结论] 多次实验发现,在实验操作完全规范时,集气瓶内进入的水的体积始终小于理论值,请你分析可能的原因: 。
Ⅱ.利用脱氧剂测定空气中氧气的含量。
使用如如图②装置进行实验,实验原理是利用脱氧剂在常温下能够消耗装置内的氧气。在实验前应先进行的操作是 。
[实验步骤] (1)在注射器中放入足量脱氧剂粉末,打开弹簧夹。
(2)注射器向右拉至一定刻度,关闭弹簧夹。
(3)待一段时间后活塞位置不再发生变化,记录数据。
[数据处理] (1)实验中需要记录的数据有 (填字母)。
A.反应前注射器中原有空气的体积
B.反应后注射器中剩余气体的体积
(2)上述实验测定过程至少需要重复两次,其目的是 ,
最终计算得出氧气约占空气的体积分数。
[实验评价] 与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是 。
21.(8分)某化学小组受英国科学家法拉第《蜡烛的化学史》的启发,对蜡烛的燃烧过程进行了一次探究。
[查阅资料] 无水硫酸铜(CuSO4)是一种白色粉末,吸水后变为蓝色。
[进行实验]
序号 实验步骤 实验现象 实验结论
Ⅰ 外焰处的铁纱窗出现红热的环,内焰及焰心处的铁纱窗无明显变化
Ⅱ 硫酸铜粉末变成 色,澄清石灰水 蜡烛燃烧的产物中有水和二氧化碳
[反思与评价]
实验Ⅱ是该小组同学对中乙所示实验的改进。与如如图乙所示实验相比,实验Ⅱ的优点是 。
22.(16分)在小英家的仓库里,堆放着一袋袋碳酸氢铵(NH4HCO3)化肥。过了一个夏天,小英发现这种化肥所特有的刺激性气味变得更浓烈了,有些化肥袋里碳酸氢铵变少了。检查发现,变少的化肥包装袋没有密封,化肥也没有撒落在地上,更没有人进过仓库开袋使用。
为了探究这些化肥减少的原因,小英在实验室取了一些碳酸氢铵粉末,放在蒸发皿中加热,过一会儿观察到粉末完全消失,同时也闻到了这种刺激性气味。
[提出问题] 碳酸氢铵粉末消失的原因是什么
[作出猜想]
猜想①:碳酸氢铵粉末在不加热或加热条件下由固态变成它的气态(升华)。
猜想②:碳酸氢铵在不加热或加热条件下发生分解反应,可能产生的物质有氨气和其他物质。
[查阅资料]
(1)碳酸氢铵属于氮肥,不具有升华的性质,说明上述猜想 (填序号)不成立。
(2)氨气(NH3)具有特殊的刺激性气味,极易溶于水,能使湿润的红色石蕊试纸变蓝。
(3)二氧化氮(NO2)为红棕色气体,一氧化氮(NO)为无色气体,在空气中易发生反应:NO+O2NO2。
[进行实验]
实验操作 实验现象 实验结论
Ⅰ.取适量碳酸氢铵于试管中加热,如甲所示,将干燥的红色石蕊试纸接近导管口 产生强烈的刺激性气味,试管壁上有无色液滴出现且试纸变蓝,但未见红棕色气体 分解产物中有 和 ,没有 或一氧化氮
Ⅱ.按如如图乙所示装置继续实验,直到反应完全 澄清石灰水变浑浊 分解产物中有
[应用]
(1)利用氨气的化学性质,检验某集气瓶内的气体是不是氨气。
实验操作 实验现象 实验结论
集气瓶内气体为氨气
(2)如果你家里有碳酸氢铵化肥,你应该如何保存 。
答案
1.D
2.C 液体应存放于细口瓶或滴瓶中,固体存放于广口瓶中。
3.C
4.C 柏油路面曝晒变软,没有新物质生成,属于物理变化;水放冰箱结成冰块,没有新物质生成,属于物理变化;铜器锈蚀颜色变绿,生成的铜锈是新物质,属于化学变化;电流过大灯丝熔断,没有新物质生成,属于物理变化。
5.A 洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下,表明仪器已洗干净;一般来说,固体药品应垫上纸片称量,而不能直接放在托盘上,以免药品被污染或托盘被腐蚀;加热后的试管不能立即用冷水冲洗,以防试管因骤冷而炸裂;给试管里的液体加热时试管口不能对着自己或他人,以防液体沸腾时喷出伤人。
6.D 液氮用于医疗是利用其沸点低的物理性质;用铝制作导线主要是利用铝能导电的物理性质;石墨制铅笔芯是利用石墨呈灰黑色、质软的物理性质;用煤炭作燃料是利用煤炭的可燃性,属于化学性质。
7.C 蜡烛在空气中燃烧产生黄白色火焰,放出大量的热;石蜡燃烧能生成水,故可看到烧杯内壁有水珠出现;蜡烛燃烧时生成了二氧化碳和水,是实验结论而不是实验现象;白烟是石蜡蒸气凝成的石蜡小颗粒,具有可燃性,用火柴点燃,蜡烛能重新燃烧。
8.C 医用生理盐水中有氯化钠和水,属于混合物;瓶装矿泉水中有可溶性杂质和水,属于混合物;冰水混合物中只有水,属于纯净物;未经污染的空气中有氧气、氮气等,属于混合物。
9.C 量取8 mL液体,应选用与8 mL相近的量程为10 mL的量筒,量取液体时,先倾倒至接近所要求的刻度,最后不足的用胶头滴管滴加;加热少量液体可用试管盛放液体,用酒精灯提供热量,并用试管夹夹持试管。
10.D ③因为外焰温度最高,焰心温度较低,会使试管受热不均而炸裂;④加热前没有擦干试管外壁的水,容易导致试管受热不均而炸裂;⑤没有进行预热,直接集中加热试管里液体的中下部,会使试管受热不均而炸裂。
11.B 气体的密度小于空气的密度,泄漏后会很快上升到上方,因此报警器应安装在房间内墙上方的位置;如果气体的密度大于空气的密度,泄漏后会聚集在下方,因此报警器应安装在房间内墙下方的位置,所以安装位置与气体的密度有关。
12.B 把澄清石灰水滴入盛有人体呼出气体的集气瓶中,振荡,应该属于科学探究环节中的进行实验。
13.C
14.D 实验前需检查装置气密性,以防止装置漏气造成结果不准确;白磷燃烧是与氧气反应生成五氧化二磷;白磷熄灭、试管冷却后再打开止水夹,以防止剩余的气体受热处于膨胀状态,使进入试管中的水减少,造成结果偏小;氧气约占空气总体积的,130 mL空气中氧气的体积约为130 mL×=26 mL,最终量筒中液面约降至50 mL-26 mL=24 mL刻度线处。
15.D 由如如图示可知,蜡烛燃烧前,密闭容器中氧气的体积分数为21%;反应前瓶内氧气的体积分数是21%,反应后氧气的体积分数为16%,氧气被消耗,说明蜡烛燃烧需要氧气;当氧气的体积分数达到16%时,蜡烛熄灭,密闭容器中还有氧气;蜡烛燃烧生成二氧化碳和水,燃烧结束后,除剩余氧气外,瓶内不会只剩下二氧化碳,还应有水蒸气和燃烧前瓶内的其他气体,体积分数不可能为84%。
16.(1)
(2)大于
(3)灯帽盖灭
(4)BD
17.(1)坩埚钳
(2)生成白色固体
(3)实验时没有在桌面上垫石棉网,高温生成物溅落(合理即可)
(4)镁粉燃烧时发出耀眼的白光
18.(1)具有银白色光泽、质软、熔点低、密度比水小
(2)钾能跟水发生反应(或钾能与酸的水溶液反应)
(3)钾+水氢氧化钾+氢气
(1)物理性质可以通过感知器官直接感知或通过仪器进行测量,不需要通过化学性质体现,如物质的颜色、状态、气味、密度等。(2)化学性质需要通过化学变化才能体现,钾能跟水、酸溶液发生反应就属于钾的化学性质。(3)钾和水反应生成了氢氧化钾和氢气,故文字表达式为钾+水氢氧化钾+氢气。
19.(1)化学 红磷+氧气五氧化二磷
(2)物理
20.Ⅰ.P+O2P2O5
[实验步骤] (3)红磷熄灭,冷却至室温,打开弹簧夹
[实验结论] 氧气不能完全反应(合理即可)
Ⅱ.检查装置的气密性
[数据处理] (1)AB (2)减小误差
[实验评价] 实验结果更准确,更环保(合理即可)
Ⅰ.红磷在空气中燃烧生成五氧化二磷,反应的符号表达式为P+O2P2O5。[实验步骤] (3)为避免瓶内气体受热膨胀,影响进入集气瓶的水的体积,应在红磷熄灭,冷却至室温后,再打开弹簧夹。[实验结论] 多次实验发现,在实验操作完全规范时,集气瓶内进入的水的体积始终小于理论值,可能的原因是氧气不能完全反应。Ⅱ.实验前应先进行的操作是检查装置气密性。[数据处理] (1)实验中需要记录的数据:反应前注射器中原有空气的体积、反应后注射器中剩余气体的体积,减少的体积即为氧气体积,进一步可以计算氧气含量。[实验评价] 与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点:防止燃烧匙伸入集气瓶中时导致的部分气体受热膨胀逸出,使实验结果更准确,同时防止反应生成的五氧化二磷扩散到空气中污染 环境。
21.[进行实验]Ⅰ.蜡烛火焰外焰的温度高于内焰及焰心的温度(合理即可)
Ⅱ.蓝 变浑浊
[反思与评价] 能够同时检验是否有水和二氧化碳生成
22.[查阅资料] (1)①
[进行实验] 水 氨气 二氧化氮 二氧化碳
[应用] (1)将湿润的红色石蕊试纸伸入集气瓶中 试纸变为蓝色
(2)密封、低温保存
[查阅资料] 碳酸氢铵不具有升华的性质,即不能由固态变成它的气态,故猜想①错误。[进行实验] 氨气能使湿润的红色石蕊试纸变蓝,而操作Ⅰ中使用干燥的红色石蕊试纸检验且试纸变为蓝色,可以说明碳酸氢铵分解生成了水,也生成了氨气;由于没有红棕色气体产生,结合题中信息可知,生成的气体中不含二氧化氮或一氧化氮;澄清石灰水可以检验二氧化碳,结合实验现象可知,碳酸氢铵分解还生成了二氧化碳。[应用] (1)根据氨气的性质,可以用湿润的红色石蕊试纸检验瓶内气体是否为氨气。(2)碳酸氢铵受热易分解,故需要密封、低温保存。
[测试范围:第1章 时间:40分钟 分值:100分]
一、选择题(每小题只有一个选项符合题意,每小题3分,共45分)
1.下列选项不是体现化学造福人类的是 ( )
A.新医药的研制 B.单晶硅的使用
C.隔水透气材料的发明 D.杂交水稻的成功
2.在实验室中,药品和仪器的存放应符合一定规范,如中物质存放在对应的容器中,符合规范的是 ( )
3.[2020·本溪] 下列如如图示实验操作中,正确的是 ( )
4.[2020·陕西] 变化无处不在。生活中的下列现象是由化学变化引起的是 ( )
A.柏油路面曝晒变软
B.水放冰箱结成冰块
C.铜器锈蚀颜色变绿
D.电流过大灯丝熔断
5.规范的操作是化学实验成功的保障。下列实验操作中正确的是 ( )
A.洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下,表明仪器已洗干净
B.固体药品可以直接放在天平的托盘上称量
C.加热后的试管应立即用冷水冲洗
D.为了便于观察,给试管里的液体加热时试管口对着自己
6.下列物质的用途,主要利用其化学性质的是 ( )
A.液氮用于医疗 B.用铝制作导线
C.石墨制铅笔芯 D.用煤炭作燃料
7.下列有关蜡烛燃烧的实验现象的叙述错误的是 ( )
A.蜡烛在空气中燃烧产生黄白色火焰,放热
B.在蜡烛火焰上方罩一个冷而干燥的烧杯,烧杯内壁有水珠出现
C.蜡烛燃烧时生成了二氧化碳和水
D.用火柴去引燃刚熄灭时蜡烛上方飘出的白烟,蜡烛重新燃烧
8.[2020·鸡西] 下列各组物质中,属于纯净物的是 ( )
A.医用生理盐水 B.瓶装矿泉水
C.冰水混合物 D.未经污染的空气
9.取8 mL的液体并加热,需要用到的仪器是 ( )
①烧杯 ②试管 ③胶头滴管 ④石棉网 ⑤试管夹 ⑥铁架台 ⑦10 mL量筒 ⑧50 mL量筒 ⑨酒精灯
A.①③④⑥⑦⑨ B.②⑤⑦⑨
C.②③⑤⑦⑨ D.②③⑤⑧⑨
10.用酒精灯给试管里的液体加热时,发现试管破裂,可能原因有:①用酒精灯的外焰给试管加热;②被加热的液体超过试管容积的;③加热时试管底部触及灯芯;④加热前没有擦干试管外壁的水;⑤没有进行预热,直接集中加热试管中的液体;⑥加热时没有不时地上下移动试管。其中与之相关的是 ( )
A.①③⑤⑥ B.②④ C.②③⑥ D.③④⑤
11.如所示,为防止燃气泄漏造成危险,可在食堂或家庭中安装报警器。下列燃气的性质中,能确定安装报警器位置的是 ( )
A.毒性 B.密度 C.气味 D.溶解性
12.在实验室中某同学把澄清石灰水滴入盛有人体呼出气体的集气瓶中,振荡。这一过程属于科学探究中的哪一重要环节 ( )
A.提出假设 B.进行实验
C.收集证据 D.得出结论
13.已知淀粉遇碘变蓝。小军同学在做唾液淀粉酶实验时,向热的面粉糊中加入碘酒,发现未变蓝。面对“异常”现象,他不应该采取的做法是 ( )
A.向老师请教 B.查找相关资料,探究原因
C.认为自己做错了,继续做其他实验 D.反复实验,并观察是否有相同现象
14.[2020·北京] 利用如所示装置验证空气中氧气的含量。下列叙述不正确的是 ( )
A.实验前需检查装置的气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄灭、试管冷却后再打开止水夹
D.最终量筒中液面约降至40 mL刻度线处
15.将燃着的蜡烛放在 ①所示的密闭容器中,同时用氧气传感器测出密闭容器中氧气含量的变化如如如图②所示。下列说法不正确的是 ( )
A.蜡烛燃烧前,密闭容器中氧气的体积分数为21%
B.蜡烛燃烧需要氧气
C.蜡烛熄灭后,密闭容器中还有氧气
D.蜡烛熄灭后,密闭容器中二氧化碳的体积分数为84%
二、填空题(共17分)
16.(4分)化学是一门以实验为基础的科学,实验安全与规范至关重要。回答下列问题。
(1)加热试管内液体时,液体不能超过试管容积的 。
(2)用10 mL量筒量取8 mL蒸馏水,若仰视读数,则量筒内蒸馏水的体积 (填“大于”“等于”或“小于”)8 mL。
(3)加热后熄灭酒精灯,正确操作是用 。
(4)加热铜绿的实验中,发现试管炸裂,可能原因为 (填字母)。
A.试管外壁干燥 B.用焰心加热
C.试管口朝向他人 D.试管口没有略向下倾斜
17.(4分)是镁条在空气中燃烧实验的示意如如图。请回答:
(1)夹持镁条的仪器名称是 。
(2)能说明镁条燃烧是化学变化的实验现象是 。
(3)实验完毕,发现桌面被烫坏了,原因可能是 。
(4)镁粉可用于军事上制作照明弹,是因为 。
18.(3分)根据材料,回答下列问题。
通常情况下,钾具有银白色光泽,质地十分柔软,可以用小刀切割。钾的熔点很低,只有63 ℃,也就是说,只要温度升高到63 ℃,金属钾就变成水银般的液体了。钾的密度很小,它比水还轻。钾的化学性质十分活泼,与水反应剧烈,当把一块钾放入水中时,你就会看到它不断地浮起落下,周身还冒出火焰;一会儿再看,水中的钾就消失了。原来,它跟水发生反应生成了氢氧化钾和氢气。钾与酸的水溶液反应更加剧烈,几乎能达到爆炸的程度。
(1)钾的物理性质有 。
(2)写出一条钾的化学性质: 。
(3)写出钾和水反应的文字表达式: 。
19.(6分)化学现象中包含发光、放热现象,许多物质燃烧时都伴随有发光、放热的现象。小明同学认为有发光、放热现象的变化不一定是化学变化,于是学习小组对此展开了探究与讨论。
(1)取适量红磷于燃烧匙中,在酒精灯上点燃。实验现象为产生黄白色火焰,放出大量热,生成大量白烟。
分析:红磷燃烧属于 变化,该反应的文字表达式为 。
(2)观察白炽灯(灯丝为钨丝):
通电前 通电中 通电后
灯丝为灰黑色固体 发出白光,手摸灯泡感觉发烫 灯丝为灰黑色固体
分析:根据通电前后,钨丝本身没有发生变化,灯泡通电发光、放热属于 变化。
三、实验探究题(共38分)
20.(14分)为了测定空气中氧气含量,某兴趣小组设计以下实验进行探究。
Ⅰ.燃烧红磷法测定空气中氧气的含量。
实验原理:利用红磷在空气中燃烧生成五氧化二磷固体,集气瓶内压强减小,使烧杯内水倒流入集气瓶中。写出红磷在空气中燃烧的符号表达式: 。
[实验步骤] (1)用弹簧夹夹紧乳胶管。
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞。
(3) (补全实验步骤)。
(4)观察到水倒流至集气瓶并记录水面的变化情况。
[实验结论] 多次实验发现,在实验操作完全规范时,集气瓶内进入的水的体积始终小于理论值,请你分析可能的原因: 。
Ⅱ.利用脱氧剂测定空气中氧气的含量。
使用如如图②装置进行实验,实验原理是利用脱氧剂在常温下能够消耗装置内的氧气。在实验前应先进行的操作是 。
[实验步骤] (1)在注射器中放入足量脱氧剂粉末,打开弹簧夹。
(2)注射器向右拉至一定刻度,关闭弹簧夹。
(3)待一段时间后活塞位置不再发生变化,记录数据。
[数据处理] (1)实验中需要记录的数据有 (填字母)。
A.反应前注射器中原有空气的体积
B.反应后注射器中剩余气体的体积
(2)上述实验测定过程至少需要重复两次,其目的是 ,
最终计算得出氧气约占空气的体积分数。
[实验评价] 与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是 。
21.(8分)某化学小组受英国科学家法拉第《蜡烛的化学史》的启发,对蜡烛的燃烧过程进行了一次探究。
[查阅资料] 无水硫酸铜(CuSO4)是一种白色粉末,吸水后变为蓝色。
[进行实验]
序号 实验步骤 实验现象 实验结论
Ⅰ 外焰处的铁纱窗出现红热的环,内焰及焰心处的铁纱窗无明显变化
Ⅱ 硫酸铜粉末变成 色,澄清石灰水 蜡烛燃烧的产物中有水和二氧化碳
[反思与评价]
实验Ⅱ是该小组同学对中乙所示实验的改进。与如如图乙所示实验相比,实验Ⅱ的优点是 。
22.(16分)在小英家的仓库里,堆放着一袋袋碳酸氢铵(NH4HCO3)化肥。过了一个夏天,小英发现这种化肥所特有的刺激性气味变得更浓烈了,有些化肥袋里碳酸氢铵变少了。检查发现,变少的化肥包装袋没有密封,化肥也没有撒落在地上,更没有人进过仓库开袋使用。
为了探究这些化肥减少的原因,小英在实验室取了一些碳酸氢铵粉末,放在蒸发皿中加热,过一会儿观察到粉末完全消失,同时也闻到了这种刺激性气味。
[提出问题] 碳酸氢铵粉末消失的原因是什么
[作出猜想]
猜想①:碳酸氢铵粉末在不加热或加热条件下由固态变成它的气态(升华)。
猜想②:碳酸氢铵在不加热或加热条件下发生分解反应,可能产生的物质有氨气和其他物质。
[查阅资料]
(1)碳酸氢铵属于氮肥,不具有升华的性质,说明上述猜想 (填序号)不成立。
(2)氨气(NH3)具有特殊的刺激性气味,极易溶于水,能使湿润的红色石蕊试纸变蓝。
(3)二氧化氮(NO2)为红棕色气体,一氧化氮(NO)为无色气体,在空气中易发生反应:NO+O2NO2。
[进行实验]
实验操作 实验现象 实验结论
Ⅰ.取适量碳酸氢铵于试管中加热,如甲所示,将干燥的红色石蕊试纸接近导管口 产生强烈的刺激性气味,试管壁上有无色液滴出现且试纸变蓝,但未见红棕色气体 分解产物中有 和 ,没有 或一氧化氮
Ⅱ.按如如图乙所示装置继续实验,直到反应完全 澄清石灰水变浑浊 分解产物中有
[应用]
(1)利用氨气的化学性质,检验某集气瓶内的气体是不是氨气。
实验操作 实验现象 实验结论
集气瓶内气体为氨气
(2)如果你家里有碳酸氢铵化肥,你应该如何保存 。
答案
1.D
2.C 液体应存放于细口瓶或滴瓶中,固体存放于广口瓶中。
3.C
4.C 柏油路面曝晒变软,没有新物质生成,属于物理变化;水放冰箱结成冰块,没有新物质生成,属于物理变化;铜器锈蚀颜色变绿,生成的铜锈是新物质,属于化学变化;电流过大灯丝熔断,没有新物质生成,属于物理变化。
5.A 洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下,表明仪器已洗干净;一般来说,固体药品应垫上纸片称量,而不能直接放在托盘上,以免药品被污染或托盘被腐蚀;加热后的试管不能立即用冷水冲洗,以防试管因骤冷而炸裂;给试管里的液体加热时试管口不能对着自己或他人,以防液体沸腾时喷出伤人。
6.D 液氮用于医疗是利用其沸点低的物理性质;用铝制作导线主要是利用铝能导电的物理性质;石墨制铅笔芯是利用石墨呈灰黑色、质软的物理性质;用煤炭作燃料是利用煤炭的可燃性,属于化学性质。
7.C 蜡烛在空气中燃烧产生黄白色火焰,放出大量的热;石蜡燃烧能生成水,故可看到烧杯内壁有水珠出现;蜡烛燃烧时生成了二氧化碳和水,是实验结论而不是实验现象;白烟是石蜡蒸气凝成的石蜡小颗粒,具有可燃性,用火柴点燃,蜡烛能重新燃烧。
8.C 医用生理盐水中有氯化钠和水,属于混合物;瓶装矿泉水中有可溶性杂质和水,属于混合物;冰水混合物中只有水,属于纯净物;未经污染的空气中有氧气、氮气等,属于混合物。
9.C 量取8 mL液体,应选用与8 mL相近的量程为10 mL的量筒,量取液体时,先倾倒至接近所要求的刻度,最后不足的用胶头滴管滴加;加热少量液体可用试管盛放液体,用酒精灯提供热量,并用试管夹夹持试管。
10.D ③因为外焰温度最高,焰心温度较低,会使试管受热不均而炸裂;④加热前没有擦干试管外壁的水,容易导致试管受热不均而炸裂;⑤没有进行预热,直接集中加热试管里液体的中下部,会使试管受热不均而炸裂。
11.B 气体的密度小于空气的密度,泄漏后会很快上升到上方,因此报警器应安装在房间内墙上方的位置;如果气体的密度大于空气的密度,泄漏后会聚集在下方,因此报警器应安装在房间内墙下方的位置,所以安装位置与气体的密度有关。
12.B 把澄清石灰水滴入盛有人体呼出气体的集气瓶中,振荡,应该属于科学探究环节中的进行实验。
13.C
14.D 实验前需检查装置气密性,以防止装置漏气造成结果不准确;白磷燃烧是与氧气反应生成五氧化二磷;白磷熄灭、试管冷却后再打开止水夹,以防止剩余的气体受热处于膨胀状态,使进入试管中的水减少,造成结果偏小;氧气约占空气总体积的,130 mL空气中氧气的体积约为130 mL×=26 mL,最终量筒中液面约降至50 mL-26 mL=24 mL刻度线处。
15.D 由如如图示可知,蜡烛燃烧前,密闭容器中氧气的体积分数为21%;反应前瓶内氧气的体积分数是21%,反应后氧气的体积分数为16%,氧气被消耗,说明蜡烛燃烧需要氧气;当氧气的体积分数达到16%时,蜡烛熄灭,密闭容器中还有氧气;蜡烛燃烧生成二氧化碳和水,燃烧结束后,除剩余氧气外,瓶内不会只剩下二氧化碳,还应有水蒸气和燃烧前瓶内的其他气体,体积分数不可能为84%。
16.(1)
(2)大于
(3)灯帽盖灭
(4)BD
17.(1)坩埚钳
(2)生成白色固体
(3)实验时没有在桌面上垫石棉网,高温生成物溅落(合理即可)
(4)镁粉燃烧时发出耀眼的白光
18.(1)具有银白色光泽、质软、熔点低、密度比水小
(2)钾能跟水发生反应(或钾能与酸的水溶液反应)
(3)钾+水氢氧化钾+氢气
(1)物理性质可以通过感知器官直接感知或通过仪器进行测量,不需要通过化学性质体现,如物质的颜色、状态、气味、密度等。(2)化学性质需要通过化学变化才能体现,钾能跟水、酸溶液发生反应就属于钾的化学性质。(3)钾和水反应生成了氢氧化钾和氢气,故文字表达式为钾+水氢氧化钾+氢气。
19.(1)化学 红磷+氧气五氧化二磷
(2)物理
20.Ⅰ.P+O2P2O5
[实验步骤] (3)红磷熄灭,冷却至室温,打开弹簧夹
[实验结论] 氧气不能完全反应(合理即可)
Ⅱ.检查装置的气密性
[数据处理] (1)AB (2)减小误差
[实验评价] 实验结果更准确,更环保(合理即可)
Ⅰ.红磷在空气中燃烧生成五氧化二磷,反应的符号表达式为P+O2P2O5。[实验步骤] (3)为避免瓶内气体受热膨胀,影响进入集气瓶的水的体积,应在红磷熄灭,冷却至室温后,再打开弹簧夹。[实验结论] 多次实验发现,在实验操作完全规范时,集气瓶内进入的水的体积始终小于理论值,可能的原因是氧气不能完全反应。Ⅱ.实验前应先进行的操作是检查装置气密性。[数据处理] (1)实验中需要记录的数据:反应前注射器中原有空气的体积、反应后注射器中剩余气体的体积,减少的体积即为氧气体积,进一步可以计算氧气含量。[实验评价] 与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点:防止燃烧匙伸入集气瓶中时导致的部分气体受热膨胀逸出,使实验结果更准确,同时防止反应生成的五氧化二磷扩散到空气中污染 环境。
21.[进行实验]Ⅰ.蜡烛火焰外焰的温度高于内焰及焰心的温度(合理即可)
Ⅱ.蓝 变浑浊
[反思与评价] 能够同时检验是否有水和二氧化碳生成
22.[查阅资料] (1)①
[进行实验] 水 氨气 二氧化氮 二氧化碳
[应用] (1)将湿润的红色石蕊试纸伸入集气瓶中 试纸变为蓝色
(2)密封、低温保存
[查阅资料] 碳酸氢铵不具有升华的性质,即不能由固态变成它的气态,故猜想①错误。[进行实验] 氨气能使湿润的红色石蕊试纸变蓝,而操作Ⅰ中使用干燥的红色石蕊试纸检验且试纸变为蓝色,可以说明碳酸氢铵分解生成了水,也生成了氨气;由于没有红棕色气体产生,结合题中信息可知,生成的气体中不含二氧化氮或一氧化氮;澄清石灰水可以检验二氧化碳,结合实验现象可知,碳酸氢铵分解还生成了二氧化碳。[应用] (1)根据氨气的性质,可以用湿润的红色石蕊试纸检验瓶内气体是否为氨气。(2)碳酸氢铵受热易分解,故需要密封、低温保存。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
