沪教版(全国)化学九年级上册课课练:第3章 物质构成的奥秘 自我综合评价(word版有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册课课练:第3章 物质构成的奥秘 自我综合评价(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 249.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-28 00:00:00 | ||
图片预览



文档简介
自我综合评价
[测试范围:第3章 时间:40分钟 分值:100分]
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Fe—56
一、选择题(每小题只有一个选项符合题意,每小题2分,共30分)
1.能保持氢气化学性质的微粒是 ( )
A.2H B.H C.H+ D.H2
2.[2020·吉林] 对下列现象解释正确的是 ( )
A.汽油挥发——分子可分 B.花香四溢——分子不断运动
C.冰雪融化——分子很小 D.氧气液化——分子体积变小
3.“农夫山泉”矿泉水里含有的下列成分中,指“元素”的是 ( )
A.偏硅酸 B.天然矿物盐
C.溶解性总固体 D.钾、钠、钙、镁
4.[2020·常州] 下列人体所缺元素与引起的健康问题关系错误的是 ( )
A.缺锌会使儿童智力低下 B.缺碘会引起龋齿
C.缺钙会引起骨质疏松 D.缺铁会引起贫血
5.“中国芯”已在许多领域广泛应用。制造芯片的重要材料是硅,它在元素周期表中的信息如,有关说法正确的是 ( )
A.硅属于金属元素 B.硅原子的质子数为14
C.硅元素在地壳中含量最多 D.硅的相对原子质量为28.09 g
6.下列有关原子与离子的说法不正确的是 ( )
A.原子变成离子,电子层数一定发生改变
B.原子、离子都可以构成物质
C.同种元素的原子与离子可以相互转化
D.离子是指带电的原子或原子团
7.如是四位同学对某化学式意义的描述,他们描述的化学式是 ( )
A.O2 B.3H C.KClO3 D.H2O
8.思维导如如图有助于建构知识,如是小金建立的有关物质宏观组成和微观构成的思维导如如图,其中“▲”应填入的是 ( )
A.原子 B.中子
C.电子 D.质子
9.下列有关化学用语中数字“2”意义的说法正确的是 ( )
①SO2 ②2NH3 ③S2- ④Ca2+ ⑤ ⑥N2
A.表示离子所带电荷数的是③④ B.表示分子个数的是①②
C.表示化合价数值的是①⑥ D.表示1个分子中含有某种原子个数的是⑤
10.学习化学必须正确使用和理解化学用语。下列有关化学用语说法正确的是 ( )
A.SO2、CO2中均含有氧分子
B.KMnO4、K2MnO4中锰元素的化合价不相同
C.Mg、Mg2+的化学性质相同
D.Na+、Mg2+、Al3+原子核内质子数均为10
11.日常生活中我们经常使用肥皂来清洗衣物,肥皂的主要成分是硬脂酸钠(化学式为C17H35COONa)。下列有关硬脂酸钠的说法正确的是 ( )
A.从微观上看:硬脂酸钠含有18个碳原子、35个氢原子、2个氧原子和1个钠原子
B.从宏观上看:硬脂酸钠分子是由碳、氢、氧、钠四种元素组成的
C.从分类上看:硬脂酸钠属于化合物
D.从质量上看:硬脂酸钠中碳、氧元素的质量比为9∶1
12.模型认知是科学研究的一种方法。1911年物理学家卢瑟福完成著名的α粒子轰击金箔实验,提出了有核原子模型。下列说法中错误的是 ( )
A.原子中质子数一定等于中子数 B.原子的质量几乎全部集中在原子核上
C.原子核带正电荷 D.电子在原子核外很大空间中运动
13.[2020·黑龙江] 如表示两种气体发生的化学反应,其中相同的球代表同种原子,下列说法正确的是 ( )
A.生成物一定是混合物 B.分子在化学变化中不可分
C.化学反应前后原子的种类不变 D.该反应既不是化合反应也不是分解反应
14.[2020·嘉兴] 某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如所示。由如如图可判断该化合物可能是 ( )
A.CaCl2 B.Al(NO3)3 C.NaOH D.H2SO4
15.葡萄糖溶液是将葡萄糖(化学式为C6H12O6)溶于水形成的。某温度下一定质量的葡萄糖溶液中氢元素的质量分数为10%,则该溶液中碳元素的质量分数为 ( )
A.5% B.10% C.25% D.60%
二、填空题(共46分)
16.(8分)[2020·宿迁] 用化学用语填空。
(1)铝原子: 。
(2)标出NH3中氮元素的化合价: ,
(3)对应的微粒符号: 。
(4)相对分子质量为128的硫单质蒸气的化学式: 。
17.(6分)下列几种元素及对应化合价为g、、、,选择适当的元素写出一个符合下列条件的化学式。
(1)非金属单质 。
(2)氧化物 。
(3)金属单质 。
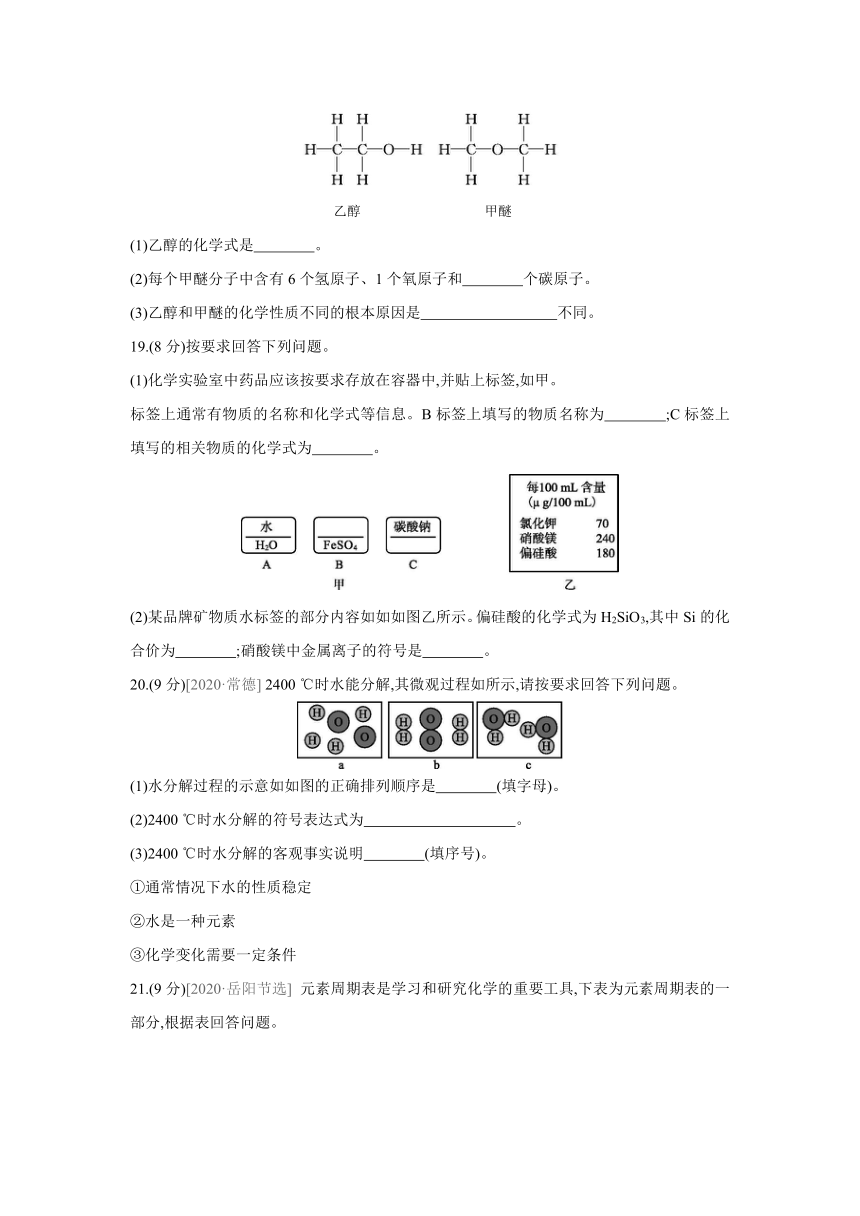
18.(6分)分析给出的乙醇、甲醚的分子结构,回答下列问题。
乙醇 甲醚
(1)乙醇的化学式是 。
(2)每个甲醚分子中含有6个氢原子、1个氧原子和 个碳原子。
(3)乙醇和甲醚的化学性质不同的根本原因是 不同。
19.(8分)按要求回答下列问题。
(1)化学实验室中药品应该按要求存放在容器中,并贴上标签,如甲。
标签上通常有物质的名称和化学式等信息。B标签上填写的物质名称为 ;C标签上填写的相关物质的化学式为 。
(2)某品牌矿物质水标签的部分内容如如如图乙所示。偏硅酸的化学式为H2SiO3,其中Si的化合价为 ;硝酸镁中金属离子的符号是 。
20.(9分)[2020·常德] 2400 ℃时水能分解,其微观过程如所示,请按要求回答下列问题。
(1)水分解过程的示意如如图的正确排列顺序是 (填字母)。
(2)2400 ℃时水分解的符号表达式为 。
(3)2400 ℃时水分解的客观事实说明 (填序号)。
①通常情况下水的性质稳定
②水是一种元素
③化学变化需要一定条件
21.(9分)[2020·岳阳节选] 元素周期表是学习和研究化学的重要工具,下表为元素周期表的一部分,根据表回答问题。
(1)11号元素与17号元素组成化合物的化学式为 。
(2)某粒子结构示意如如图为,该粒子所表示的符号是 。
(3)煤、石油、天然气等化石燃料中主要含有上表中的 (填元素符号)。
三、计算题(共24分)
22.(6分)香烟的烟气中含有几百种有毒物质,其中的一氧化碳能与血红蛋白结合,可能导致人体缺氧窒息。血红素是血红蛋白中的主要稳定结构,为血红蛋白、肌红蛋白等的辅基,其化学式是C34H32N4FeO4。请回答下列问题。
(1)一个血红素分子中含有 个原子。
(2)经测定血红蛋白中铁的质量分数为0.335%,每个血红蛋白分子中含有n个铁原子,则血红蛋白的相对分子质量可用含n的代数式表示为 。(不必化简)
23.(8分)苯(化学式为C6H6)是一种重要的有机溶剂,它的部分同系列物质如下表。
碳原子数 6 7 8 9 10
化学式 C6H6 C7H8 X C9H12 C10H14
(1)比较归纳是学好化学的重要方法,据表推断X的化学式为 。
(2)在C6H6中,碳、氢元素的质量比为 。
(3)156 g C6H6 中含碳元素多少克 (要求写出计算过程)
24.(10分)某品牌化肥尿素包装袋上部分信息如所示,请根据相关信息计算并回答下列问题。
(1)尿素中氮元素的质量分数是 。(结果精确到0.1%)
(2)通过计算判断该化肥属于 (填“纯净物”或“混合物”)。
(3)某农田原计划施用上述品牌的尿素[化学式CO(NH2)2]120 kg,但由于货源短缺,现改用硝酸铵(化学式NH4NO3),为保证含氮量相当,所需硝酸铵的质量是多少千克 (写出计算过程,结果保留一位小数)
答案
1.D 2.B 3.D 4.B
5.B 硅为“石”字旁,属于固态非金属元素;原子序数为14,在原子中,原子序数=质子数,则硅原子的质子数为14;氧元素在地壳中含量最多;硅元素的相对原子质量为28.09,相对原子质量的单位是“1”,不是“g”。
6.A 原子变成离子,电子层数不一定发生改变,如氯原子得到电子形成氯离子,电子层数不变;原子、离子都是构成物质的粒子,都可以构成物质;同种元素的原子与离子可以通过得失电子相互转化;离子是指带电的原子或原子团。
7.A O2由同种元素组成,且1个氧分子由2个氧原子构成。
8.A 原子构成分子;原子通过得失电子变成离子;具有相同核电荷数的一类原子的总称为元素,所以“▲”应填入的是原子。
9.A 标在元素符号右上角的数字表示1个离子所带的电荷数,表示离子所带电荷数的是③④;标在分子前面的数字表示分子的个数,②中的“2”表示氨分子的个数,①中的“2”表示1个二氧化硫分子中含有2个氧原子;标在元素符号正上方的数字表示该元素化合价的数值,①⑥中的“2”均表示1个分子中含有2个原子,均不能表示化合价数值;标在化学式中元素符号右下角的数字表示1个分子中所含原子的数目,表示1个分子中含有某种原子个数的是①⑥,⑤中的“2”表示镁元素的化合价为+2。
10.B SO2、CO2中不含有氧分子;KMnO4、K2MnO4中锰元素的化合价分别是+7和+6;决定元素化学性质的是最外层电子数,Mg、Mg2+的最外层电子数不相同,化学性质不相似;Na+、Mg2+、Al3+属于不同种元素,核内质子数不相同。
11.C 硬脂酸钠是由硬脂酸钠分子构成的,1个硬脂酸钠分子是由18个碳原子、35个氢原子、2个氧原子和1个钠原子构成的;硬脂酸钠分子是由碳原子、氢原子、氧原子和钠原子构成的;硬脂酸钠是由碳、氢、氧、钠四种元素组成的纯净物,属于化合物;硬脂酸钠中碳元素和氧元素的质量比为(12×18)∶(16×2)=27∶4。
12.A 在原子中质子数一定等于电子数,但不一定等于中子数;原子的质量几乎全部集中在原子核上,电子的质量相对要小得多;一般情况下,原子核中含有质子和中子,质子带正电,中子不带电,所以原子核带正电荷;原子中含有电子,电子在原子核外做高速运动。
13.C 由反应的如如图示可知反应后生成的分子种类只有一种,所以生成物是纯净物;该反应前后分子的种类发生了改变,所以化学反应中分子可分;反应前后都含有两种原子,且原子的种类没有改变;该反应的反应物是两种、生成物是一种,所以该反应是化合反应。
14.C 由如如图可知,该溶液中阳离子和阴离子的个数比为1∶1。CaCl2中钙离子和氯离子的个数比为1∶2;Al(NO3)3中铝离子和硝酸根离子的个数比为1∶3;氢氧化钠中钠离子和氢氧根离子的个数比为1∶1;H2SO4中氢离子和硫酸根离子的个数比为2∶1。
15.B 由葡萄糖和水的化学式可知,葡萄糖和水中氢元素与氧元素的质量比均为1∶8,所以葡萄糖溶液中氢元素的质量分数为10%,则溶液中氧元素的质量分数为80%,因此,该葡萄糖溶液中碳元素的质量分数为1-80%-10%=10%。
16.(1)Al (2)H3 (3)O2- (4)S4
17.(1)H2 (2)K2O (3)Mg
18.(1)C2H5OH (2)2 (3)构成它们的分子
(1)1个乙醇分子由2个碳原子、6个氢原子和1个氧原子构成,其化学式为C2H5OH。(2)根据甲醚的分子结构可知,每个甲醚分子中含有2个碳原子。(3)乙醇和甲醛的化学性质不同的根本原因是构成它们的分子不同。
19.(1)硫酸亚铁 Na2CO3 (2)+4 Mg2+
20.(1)cab (2)H2OH2+O2 (3)①③
21.(1)NaCl (2)Mg2+ (3)C
22.(1)75 (2)
23.(1)C8H10 (2)12∶1
(3)解:156 g C6H6中含碳元素的质量为
156 g×=144 g。
答:156 g C6H6中含碳元素144 g。
(1)分析表中苯的部分同系列物质的化学式,可发现当碳原子增加1个时,氢原子增加2个,因此可得物质X的分子中含8个碳原子和10个氢原子,则物质X的化学式为C8H10。
24.(1)46.7% (2)混合物
(3)解:设需要硝酸铵的质量为x。
120 kg×44.2%=×x
x=151.5 kg。
答:要保证含氮量相当,所需硝酸铵的质量是151.5 kg。
(1)尿素中氮元素的质量分数为×100%=46.7%。(2)因为纯尿素中氮元素的质量分数为46.7%,而该化肥尿素包装袋上标明含氮量为44.2%,所以该化肥属于混合物。
[测试范围:第3章 时间:40分钟 分值:100分]
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Fe—56
一、选择题(每小题只有一个选项符合题意,每小题2分,共30分)
1.能保持氢气化学性质的微粒是 ( )
A.2H B.H C.H+ D.H2
2.[2020·吉林] 对下列现象解释正确的是 ( )
A.汽油挥发——分子可分 B.花香四溢——分子不断运动
C.冰雪融化——分子很小 D.氧气液化——分子体积变小
3.“农夫山泉”矿泉水里含有的下列成分中,指“元素”的是 ( )
A.偏硅酸 B.天然矿物盐
C.溶解性总固体 D.钾、钠、钙、镁
4.[2020·常州] 下列人体所缺元素与引起的健康问题关系错误的是 ( )
A.缺锌会使儿童智力低下 B.缺碘会引起龋齿
C.缺钙会引起骨质疏松 D.缺铁会引起贫血
5.“中国芯”已在许多领域广泛应用。制造芯片的重要材料是硅,它在元素周期表中的信息如,有关说法正确的是 ( )
A.硅属于金属元素 B.硅原子的质子数为14
C.硅元素在地壳中含量最多 D.硅的相对原子质量为28.09 g
6.下列有关原子与离子的说法不正确的是 ( )
A.原子变成离子,电子层数一定发生改变
B.原子、离子都可以构成物质
C.同种元素的原子与离子可以相互转化
D.离子是指带电的原子或原子团
7.如是四位同学对某化学式意义的描述,他们描述的化学式是 ( )
A.O2 B.3H C.KClO3 D.H2O
8.思维导如如图有助于建构知识,如是小金建立的有关物质宏观组成和微观构成的思维导如如图,其中“▲”应填入的是 ( )
A.原子 B.中子
C.电子 D.质子
9.下列有关化学用语中数字“2”意义的说法正确的是 ( )
①SO2 ②2NH3 ③S2- ④Ca2+ ⑤ ⑥N2
A.表示离子所带电荷数的是③④ B.表示分子个数的是①②
C.表示化合价数值的是①⑥ D.表示1个分子中含有某种原子个数的是⑤
10.学习化学必须正确使用和理解化学用语。下列有关化学用语说法正确的是 ( )
A.SO2、CO2中均含有氧分子
B.KMnO4、K2MnO4中锰元素的化合价不相同
C.Mg、Mg2+的化学性质相同
D.Na+、Mg2+、Al3+原子核内质子数均为10
11.日常生活中我们经常使用肥皂来清洗衣物,肥皂的主要成分是硬脂酸钠(化学式为C17H35COONa)。下列有关硬脂酸钠的说法正确的是 ( )
A.从微观上看:硬脂酸钠含有18个碳原子、35个氢原子、2个氧原子和1个钠原子
B.从宏观上看:硬脂酸钠分子是由碳、氢、氧、钠四种元素组成的
C.从分类上看:硬脂酸钠属于化合物
D.从质量上看:硬脂酸钠中碳、氧元素的质量比为9∶1
12.模型认知是科学研究的一种方法。1911年物理学家卢瑟福完成著名的α粒子轰击金箔实验,提出了有核原子模型。下列说法中错误的是 ( )
A.原子中质子数一定等于中子数 B.原子的质量几乎全部集中在原子核上
C.原子核带正电荷 D.电子在原子核外很大空间中运动
13.[2020·黑龙江] 如表示两种气体发生的化学反应,其中相同的球代表同种原子,下列说法正确的是 ( )
A.生成物一定是混合物 B.分子在化学变化中不可分
C.化学反应前后原子的种类不变 D.该反应既不是化合反应也不是分解反应
14.[2020·嘉兴] 某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如所示。由如如图可判断该化合物可能是 ( )
A.CaCl2 B.Al(NO3)3 C.NaOH D.H2SO4
15.葡萄糖溶液是将葡萄糖(化学式为C6H12O6)溶于水形成的。某温度下一定质量的葡萄糖溶液中氢元素的质量分数为10%,则该溶液中碳元素的质量分数为 ( )
A.5% B.10% C.25% D.60%
二、填空题(共46分)
16.(8分)[2020·宿迁] 用化学用语填空。
(1)铝原子: 。
(2)标出NH3中氮元素的化合价: ,
(3)对应的微粒符号: 。
(4)相对分子质量为128的硫单质蒸气的化学式: 。
17.(6分)下列几种元素及对应化合价为g、、、,选择适当的元素写出一个符合下列条件的化学式。
(1)非金属单质 。
(2)氧化物 。
(3)金属单质 。
18.(6分)分析给出的乙醇、甲醚的分子结构,回答下列问题。
乙醇 甲醚
(1)乙醇的化学式是 。
(2)每个甲醚分子中含有6个氢原子、1个氧原子和 个碳原子。
(3)乙醇和甲醚的化学性质不同的根本原因是 不同。
19.(8分)按要求回答下列问题。
(1)化学实验室中药品应该按要求存放在容器中,并贴上标签,如甲。
标签上通常有物质的名称和化学式等信息。B标签上填写的物质名称为 ;C标签上填写的相关物质的化学式为 。
(2)某品牌矿物质水标签的部分内容如如如图乙所示。偏硅酸的化学式为H2SiO3,其中Si的化合价为 ;硝酸镁中金属离子的符号是 。
20.(9分)[2020·常德] 2400 ℃时水能分解,其微观过程如所示,请按要求回答下列问题。
(1)水分解过程的示意如如图的正确排列顺序是 (填字母)。
(2)2400 ℃时水分解的符号表达式为 。
(3)2400 ℃时水分解的客观事实说明 (填序号)。
①通常情况下水的性质稳定
②水是一种元素
③化学变化需要一定条件
21.(9分)[2020·岳阳节选] 元素周期表是学习和研究化学的重要工具,下表为元素周期表的一部分,根据表回答问题。
(1)11号元素与17号元素组成化合物的化学式为 。
(2)某粒子结构示意如如图为,该粒子所表示的符号是 。
(3)煤、石油、天然气等化石燃料中主要含有上表中的 (填元素符号)。
三、计算题(共24分)
22.(6分)香烟的烟气中含有几百种有毒物质,其中的一氧化碳能与血红蛋白结合,可能导致人体缺氧窒息。血红素是血红蛋白中的主要稳定结构,为血红蛋白、肌红蛋白等的辅基,其化学式是C34H32N4FeO4。请回答下列问题。
(1)一个血红素分子中含有 个原子。
(2)经测定血红蛋白中铁的质量分数为0.335%,每个血红蛋白分子中含有n个铁原子,则血红蛋白的相对分子质量可用含n的代数式表示为 。(不必化简)
23.(8分)苯(化学式为C6H6)是一种重要的有机溶剂,它的部分同系列物质如下表。
碳原子数 6 7 8 9 10
化学式 C6H6 C7H8 X C9H12 C10H14
(1)比较归纳是学好化学的重要方法,据表推断X的化学式为 。
(2)在C6H6中,碳、氢元素的质量比为 。
(3)156 g C6H6 中含碳元素多少克 (要求写出计算过程)
24.(10分)某品牌化肥尿素包装袋上部分信息如所示,请根据相关信息计算并回答下列问题。
(1)尿素中氮元素的质量分数是 。(结果精确到0.1%)
(2)通过计算判断该化肥属于 (填“纯净物”或“混合物”)。
(3)某农田原计划施用上述品牌的尿素[化学式CO(NH2)2]120 kg,但由于货源短缺,现改用硝酸铵(化学式NH4NO3),为保证含氮量相当,所需硝酸铵的质量是多少千克 (写出计算过程,结果保留一位小数)
答案
1.D 2.B 3.D 4.B
5.B 硅为“石”字旁,属于固态非金属元素;原子序数为14,在原子中,原子序数=质子数,则硅原子的质子数为14;氧元素在地壳中含量最多;硅元素的相对原子质量为28.09,相对原子质量的单位是“1”,不是“g”。
6.A 原子变成离子,电子层数不一定发生改变,如氯原子得到电子形成氯离子,电子层数不变;原子、离子都是构成物质的粒子,都可以构成物质;同种元素的原子与离子可以通过得失电子相互转化;离子是指带电的原子或原子团。
7.A O2由同种元素组成,且1个氧分子由2个氧原子构成。
8.A 原子构成分子;原子通过得失电子变成离子;具有相同核电荷数的一类原子的总称为元素,所以“▲”应填入的是原子。
9.A 标在元素符号右上角的数字表示1个离子所带的电荷数,表示离子所带电荷数的是③④;标在分子前面的数字表示分子的个数,②中的“2”表示氨分子的个数,①中的“2”表示1个二氧化硫分子中含有2个氧原子;标在元素符号正上方的数字表示该元素化合价的数值,①⑥中的“2”均表示1个分子中含有2个原子,均不能表示化合价数值;标在化学式中元素符号右下角的数字表示1个分子中所含原子的数目,表示1个分子中含有某种原子个数的是①⑥,⑤中的“2”表示镁元素的化合价为+2。
10.B SO2、CO2中不含有氧分子;KMnO4、K2MnO4中锰元素的化合价分别是+7和+6;决定元素化学性质的是最外层电子数,Mg、Mg2+的最外层电子数不相同,化学性质不相似;Na+、Mg2+、Al3+属于不同种元素,核内质子数不相同。
11.C 硬脂酸钠是由硬脂酸钠分子构成的,1个硬脂酸钠分子是由18个碳原子、35个氢原子、2个氧原子和1个钠原子构成的;硬脂酸钠分子是由碳原子、氢原子、氧原子和钠原子构成的;硬脂酸钠是由碳、氢、氧、钠四种元素组成的纯净物,属于化合物;硬脂酸钠中碳元素和氧元素的质量比为(12×18)∶(16×2)=27∶4。
12.A 在原子中质子数一定等于电子数,但不一定等于中子数;原子的质量几乎全部集中在原子核上,电子的质量相对要小得多;一般情况下,原子核中含有质子和中子,质子带正电,中子不带电,所以原子核带正电荷;原子中含有电子,电子在原子核外做高速运动。
13.C 由反应的如如图示可知反应后生成的分子种类只有一种,所以生成物是纯净物;该反应前后分子的种类发生了改变,所以化学反应中分子可分;反应前后都含有两种原子,且原子的种类没有改变;该反应的反应物是两种、生成物是一种,所以该反应是化合反应。
14.C 由如如图可知,该溶液中阳离子和阴离子的个数比为1∶1。CaCl2中钙离子和氯离子的个数比为1∶2;Al(NO3)3中铝离子和硝酸根离子的个数比为1∶3;氢氧化钠中钠离子和氢氧根离子的个数比为1∶1;H2SO4中氢离子和硫酸根离子的个数比为2∶1。
15.B 由葡萄糖和水的化学式可知,葡萄糖和水中氢元素与氧元素的质量比均为1∶8,所以葡萄糖溶液中氢元素的质量分数为10%,则溶液中氧元素的质量分数为80%,因此,该葡萄糖溶液中碳元素的质量分数为1-80%-10%=10%。
16.(1)Al (2)H3 (3)O2- (4)S4
17.(1)H2 (2)K2O (3)Mg
18.(1)C2H5OH (2)2 (3)构成它们的分子
(1)1个乙醇分子由2个碳原子、6个氢原子和1个氧原子构成,其化学式为C2H5OH。(2)根据甲醚的分子结构可知,每个甲醚分子中含有2个碳原子。(3)乙醇和甲醛的化学性质不同的根本原因是构成它们的分子不同。
19.(1)硫酸亚铁 Na2CO3 (2)+4 Mg2+
20.(1)cab (2)H2OH2+O2 (3)①③
21.(1)NaCl (2)Mg2+ (3)C
22.(1)75 (2)
23.(1)C8H10 (2)12∶1
(3)解:156 g C6H6中含碳元素的质量为
156 g×=144 g。
答:156 g C6H6中含碳元素144 g。
(1)分析表中苯的部分同系列物质的化学式,可发现当碳原子增加1个时,氢原子增加2个,因此可得物质X的分子中含8个碳原子和10个氢原子,则物质X的化学式为C8H10。
24.(1)46.7% (2)混合物
(3)解:设需要硝酸铵的质量为x。
120 kg×44.2%=×x
x=151.5 kg。
答:要保证含氮量相当,所需硝酸铵的质量是151.5 kg。
(1)尿素中氮元素的质量分数为×100%=46.7%。(2)因为纯尿素中氮元素的质量分数为46.7%,而该化肥尿素包装袋上标明含氮量为44.2%,所以该化肥属于混合物。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
