沪教版(全国)化学九年级上册课课练:专题训练 分子、原子、离子和元素(word版有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册课课练:专题训练 分子、原子、离子和元素(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 278.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-28 00:00:00 | ||
图片预览


文档简介
专题训练
分子、原子、离子和元素
一、选择题
1.人体中含量最高的金属元素是( )
A.O B.Fe C.Ca D.Na
2.下列物质由离子构成的是 ( )
A.水 B.汞 C.氢气 D.氯化钠
3.从分子、原子的角度解释下列事实,其中不正确的是 ( )
选项 事实 解释
A 6000 L氧气加压后可装入40 L的钢瓶 相同条件下,气体分子间的空隙较大
B 香水、汽油要密闭保存 分子在不断运动
C 物体具有热胀冷缩现象 分子受热变大,遇冷变小
D 氧气和臭氧(O3)的化学性质不同 构成氧气和臭氧两物质的分子不同
4.[2020·怀化] 决定元素化学性质的是原子的( )
A.核内中子数 B.核内质子数 C.最外层电子数 D.核外电子数
5.[2020·金昌] 2020年1月14日,C919大型客机第二架机迎来了进入2020年后的第一次飞行。C919部分机身采用了新型的铝锂合金,铝锂合金中的铝元素与锂元素的本质区别是 ( )
A.相对原子质量不同
B.原子的质子数不同
C.原子的电子数不同
D.原子的中子数不同
6.如为某粒子结构示意如如图,下列说法错误的是 ( )
A.该粒子属于非金属元素
B.该粒子核外电子数为17
C.该粒子具有3个电子层
D.在化学反应中,该元素原子易得电子形成Cl-
7.[2020·潍坊] 下列有关粒子的说法中正确的是 ( )
A.分子可分,原子不可分 B.原子得到电子后带正电荷
C.分子、原子和离子都可以直接构成物质 D.原子的原子核都是由质子和中子构成的
8.有一种近些年发现的元素,其原子核外电子数为 117,中子数为 177,相对原子质量为 294,元素名称为,元素符号为 Ts。对照甲,如如图乙中“①”处应填 ( )
A.117 B.177 C.294 D.60
9.北宋王希孟创作的绢本设色画《千里江山如如图》比采用同样颜料的《蒙娜丽莎》早300多年,下表是《千里江山如如图》所用的部分矿物颜料,其主要成分属于氧化物的是( )
矿物 蓝铜矿 朱砂 赭石 砗磲
颜色 深蓝色 大红色 暗棕红色或灰黑色 白色
主要成分 2CuCO3 Cu(OH)2 HgS Fe2O3 CaCO3
A.蓝铜矿 B.朱砂 C.赭石 D.砗磲
10.同素异形体是指由同种元素组成的不同单质。下列和氧气互为同素异形体的是( )
A.臭氧 B.液氧 C.石墨 D.二氧化碳
11.我们是微观世界的“小不点”,是人们用肉眼无法看见的微粒,但我们是真实存在的,对人类的贡献功不可没。下列四种微粒有一种是与众不同的,它是 ( )
二、填空题
12.用化学用语填空。
(1)氧元素 。 (2)2个铁原子 。
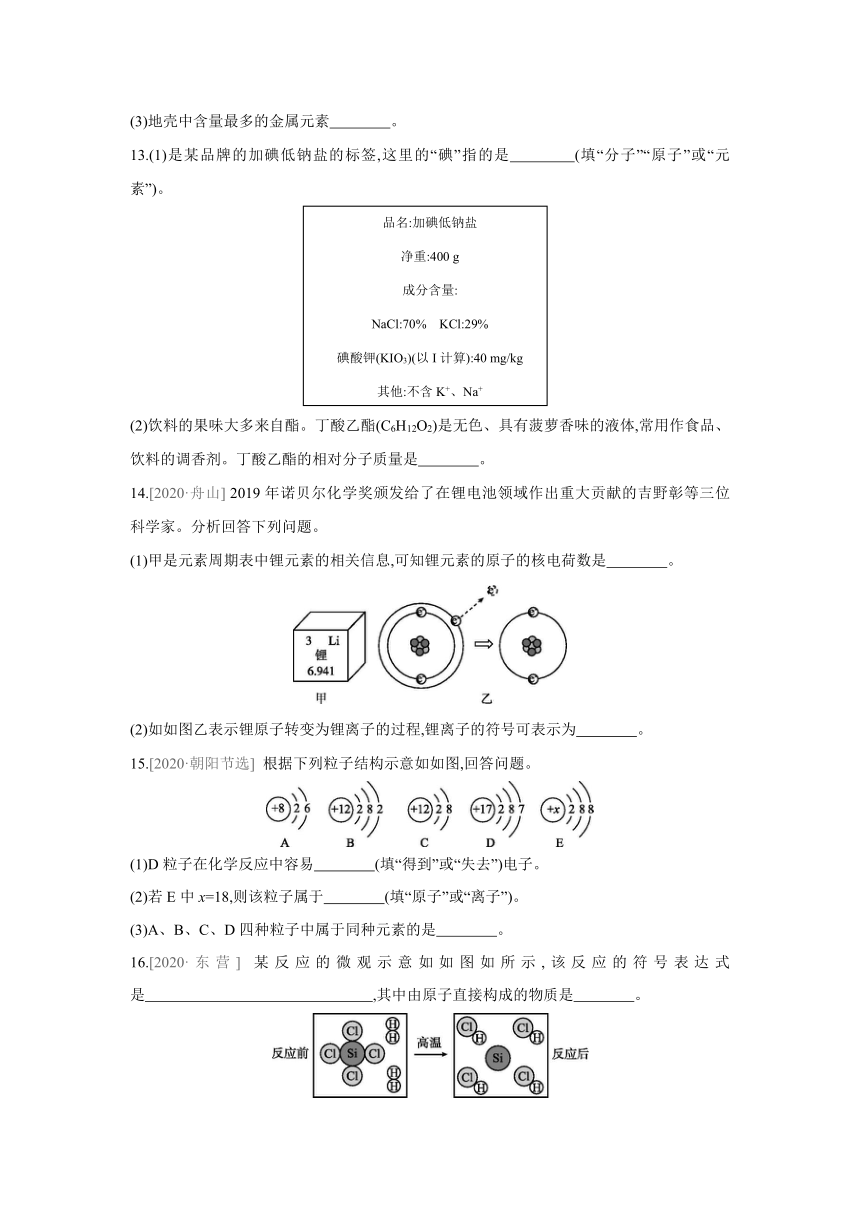
(3)地壳中含量最多的金属元素 。
13.(1)是某品牌的加碘低钠盐的标签,这里的“碘”指的是 (填“分子”“原子”或“元素”)。
品名:加碘低钠盐
净重:400 g
成分含量:
NaCl:70% KCl:29%
碘酸钾(KIO3)(以I计算):40 mg/kg
其他:不含K+、Na+
(2)饮料的果味大多来自酯。丁酸乙酯(C6H12O2)是无色、具有菠萝香味的液体,常用作食品、饮料的调香剂。丁酸乙酯的相对分子质量是 。
14.[2020·舟山] 2019年诺贝尔化学奖颁发给了在锂电池领域作出重大贡献的吉野彰等三位科学家。分析回答下列问题。
(1)甲是元素周期表中锂元素的相关信息,可知锂元素的原子的核电荷数是 。
(2)如如图乙表示锂原子转变为锂离子的过程,锂离子的符号可表示为 。
15.[2020·朝阳节选] 根据下列粒子结构示意如如图,回答问题。
(1)D粒子在化学反应中容易 (填“得到”或“失去”)电子。
(2)若E中x=18,则该粒子属于 (填“原子”或“离子”)。
(3)A、B、C、D四种粒子中属于同种元素的是 。
16.[2020·东营] 某反应的微观示意如如图如所示,该反应的符号表达式是 ,其中由原子直接构成的物质是 。
请结合如如图示,从微观的角度谈一下对化学反应的认识: 。
17.在宏观、微观和符号之间建立联系是化学学科的特点。是某物质发生反应的微观示意如如图。
(1)丙中所示物质都是由 (填“分子”“原子”或“离子”)构成的。
(2)结合如如图示分析,化学变化中的最小粒子是 。
(3)画出氧原子的结构示意如如图: 。
(4)甲所表示的意义是 (用化学用语表示)。
18.[2019·恩施州] 恩施州具有丰富的硒资源。研究发现,硒(Se)在铁死亡过程中可增强基因的转录,对中风的营养和治疗有重要意义。甲是元素周期表的一部分,如如图乙是硒原子的结构示意如如图,请根据要求填空。
(1)硒的相对原子质量是 ,如如图中x= 。
(2)硒原子和硫原子具有相同的 ,所以化学性质相似,都能形成阴离子,则硒的阴离子符号为 。
答案
1.C 2.D
3.C 6000 L氧气加压后可装入40 L的钢瓶,是因为相同条件下,气体分子间的空隙较大,气体受压后,分子间的空隙变小;香水、汽油要密闭保存,是因为分子在不断运动,密封保存是为防止运动到空气中造成浪费;物体具有热胀冷缩现象,是因为分子间的空隙受热增大,遇冷缩小;氧气和臭氧(O3)的化学性质不同,是因为构成氧气和臭氧两物质的分子不同,不同种的分子化学性质不同。
4.C 元素的化学性质取决于原子的最外层电子数。
5.B 元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是核电荷数(即核内质子数)不同。
6.B 该元素的核内质子数为17,为氯元素,属于非金属元素;该粒子核外电子数是2+8+8=18;由如如图示可知,该粒子核外有3个电子层;该粒子是原子得到1个电子得到的,其原子的最外层电子数为7,在化学反应中易得到1个电子形成带1个单位负电荷的阴离子,其离子符号为Cl-。
7.C 分子可分,原子也可以再分,原子可以分成原子核和核外电子;电子带负电,所以原子得到电子后带负电荷;分子、原子和离子都可以直接构成物质,如水是由水分子构成的,铁是由铁原子构成的,氯化钠是由钠离子和氯离子构成的;原子核不一定都是由质子和中子构成的,如氢原子的原子核内只有质子,没有中子。
8.A 根据元素周期表中的一格可知,左上角的数字表示原子序数,在原子中,原子序数=核电荷数=质子数=核外电子数,其原子核外电子数为 117,则该元素的原子序数为117。
9.C 赭石的主要成分是由两种元素组成的化合物,其中一种元素是氧元素,属于氧化物。
10.A 判断同素异形体,关键把握两点:①由同种元素组成;②不同单质。臭氧和氧气是由氧元素组成的不同单质,互为同素异形体。
11.C 构成物质A、B、D的分子都是不同种原子,它们属于化合物;构成物质C的分子是同种原子,属于单质,单质与化合物属于纯净物的两种不同类别。
12.(1)O (2)2Fe (3)Al
13.(1)元素 (2)116
14.(1)3 (2)Li+
(1)根据元素周期表中的一格可知,左上角的数字为3,表示原子序数为3。在原子中,原子序数=核电荷数=质子数=核外电子数,则锂元素的原子的核电荷数是3。(2)如如图乙表示锂原子转变为锂离子的过程,锂原子失去1个电子形成带1个单位正电荷的锂离子,其离子符号为Li+。
15.(1)得到 (2)原子 (3)B和C
(1)D粒子的最外层电子数是7,大于4,在化学反应中容易得到电子。(2)若E中x=18,则该粒子中质子数等于电子数,属于原子。(3)A、B、C、D四种粒子中B和C的质子数相同,属于同种元素。
16.SiCl4+H2HCl+Si Si 化学反应前后原子的种类、数目均不变(合理即可)
由微观反应示意如如图可知,该反应的符号表达式为SiCl4+H2HCl+Si。硅是一种固态非金属,是由硅原子直接构成的。由化学反应的实质可知,化学反应前后原子的种类、数目均不变;在化学反应中,分子分成原子,原子再重新组合成新的分子等。
17.(1)分子 (2)原子
(3) (4)2H2O2
18.(1)78.96 6
(2)最外层电子数 Se2-
分子、原子、离子和元素
一、选择题
1.人体中含量最高的金属元素是( )
A.O B.Fe C.Ca D.Na
2.下列物质由离子构成的是 ( )
A.水 B.汞 C.氢气 D.氯化钠
3.从分子、原子的角度解释下列事实,其中不正确的是 ( )
选项 事实 解释
A 6000 L氧气加压后可装入40 L的钢瓶 相同条件下,气体分子间的空隙较大
B 香水、汽油要密闭保存 分子在不断运动
C 物体具有热胀冷缩现象 分子受热变大,遇冷变小
D 氧气和臭氧(O3)的化学性质不同 构成氧气和臭氧两物质的分子不同
4.[2020·怀化] 决定元素化学性质的是原子的( )
A.核内中子数 B.核内质子数 C.最外层电子数 D.核外电子数
5.[2020·金昌] 2020年1月14日,C919大型客机第二架机迎来了进入2020年后的第一次飞行。C919部分机身采用了新型的铝锂合金,铝锂合金中的铝元素与锂元素的本质区别是 ( )
A.相对原子质量不同
B.原子的质子数不同
C.原子的电子数不同
D.原子的中子数不同
6.如为某粒子结构示意如如图,下列说法错误的是 ( )
A.该粒子属于非金属元素
B.该粒子核外电子数为17
C.该粒子具有3个电子层
D.在化学反应中,该元素原子易得电子形成Cl-
7.[2020·潍坊] 下列有关粒子的说法中正确的是 ( )
A.分子可分,原子不可分 B.原子得到电子后带正电荷
C.分子、原子和离子都可以直接构成物质 D.原子的原子核都是由质子和中子构成的
8.有一种近些年发现的元素,其原子核外电子数为 117,中子数为 177,相对原子质量为 294,元素名称为,元素符号为 Ts。对照甲,如如图乙中“①”处应填 ( )
A.117 B.177 C.294 D.60
9.北宋王希孟创作的绢本设色画《千里江山如如图》比采用同样颜料的《蒙娜丽莎》早300多年,下表是《千里江山如如图》所用的部分矿物颜料,其主要成分属于氧化物的是( )
矿物 蓝铜矿 朱砂 赭石 砗磲
颜色 深蓝色 大红色 暗棕红色或灰黑色 白色
主要成分 2CuCO3 Cu(OH)2 HgS Fe2O3 CaCO3
A.蓝铜矿 B.朱砂 C.赭石 D.砗磲
10.同素异形体是指由同种元素组成的不同单质。下列和氧气互为同素异形体的是( )
A.臭氧 B.液氧 C.石墨 D.二氧化碳
11.我们是微观世界的“小不点”,是人们用肉眼无法看见的微粒,但我们是真实存在的,对人类的贡献功不可没。下列四种微粒有一种是与众不同的,它是 ( )
二、填空题
12.用化学用语填空。
(1)氧元素 。 (2)2个铁原子 。
(3)地壳中含量最多的金属元素 。
13.(1)是某品牌的加碘低钠盐的标签,这里的“碘”指的是 (填“分子”“原子”或“元素”)。
品名:加碘低钠盐
净重:400 g
成分含量:
NaCl:70% KCl:29%
碘酸钾(KIO3)(以I计算):40 mg/kg
其他:不含K+、Na+
(2)饮料的果味大多来自酯。丁酸乙酯(C6H12O2)是无色、具有菠萝香味的液体,常用作食品、饮料的调香剂。丁酸乙酯的相对分子质量是 。
14.[2020·舟山] 2019年诺贝尔化学奖颁发给了在锂电池领域作出重大贡献的吉野彰等三位科学家。分析回答下列问题。
(1)甲是元素周期表中锂元素的相关信息,可知锂元素的原子的核电荷数是 。
(2)如如图乙表示锂原子转变为锂离子的过程,锂离子的符号可表示为 。
15.[2020·朝阳节选] 根据下列粒子结构示意如如图,回答问题。
(1)D粒子在化学反应中容易 (填“得到”或“失去”)电子。
(2)若E中x=18,则该粒子属于 (填“原子”或“离子”)。
(3)A、B、C、D四种粒子中属于同种元素的是 。
16.[2020·东营] 某反应的微观示意如如图如所示,该反应的符号表达式是 ,其中由原子直接构成的物质是 。
请结合如如图示,从微观的角度谈一下对化学反应的认识: 。
17.在宏观、微观和符号之间建立联系是化学学科的特点。是某物质发生反应的微观示意如如图。
(1)丙中所示物质都是由 (填“分子”“原子”或“离子”)构成的。
(2)结合如如图示分析,化学变化中的最小粒子是 。
(3)画出氧原子的结构示意如如图: 。
(4)甲所表示的意义是 (用化学用语表示)。
18.[2019·恩施州] 恩施州具有丰富的硒资源。研究发现,硒(Se)在铁死亡过程中可增强基因的转录,对中风的营养和治疗有重要意义。甲是元素周期表的一部分,如如图乙是硒原子的结构示意如如图,请根据要求填空。
(1)硒的相对原子质量是 ,如如图中x= 。
(2)硒原子和硫原子具有相同的 ,所以化学性质相似,都能形成阴离子,则硒的阴离子符号为 。
答案
1.C 2.D
3.C 6000 L氧气加压后可装入40 L的钢瓶,是因为相同条件下,气体分子间的空隙较大,气体受压后,分子间的空隙变小;香水、汽油要密闭保存,是因为分子在不断运动,密封保存是为防止运动到空气中造成浪费;物体具有热胀冷缩现象,是因为分子间的空隙受热增大,遇冷缩小;氧气和臭氧(O3)的化学性质不同,是因为构成氧气和臭氧两物质的分子不同,不同种的分子化学性质不同。
4.C 元素的化学性质取决于原子的最外层电子数。
5.B 元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是核电荷数(即核内质子数)不同。
6.B 该元素的核内质子数为17,为氯元素,属于非金属元素;该粒子核外电子数是2+8+8=18;由如如图示可知,该粒子核外有3个电子层;该粒子是原子得到1个电子得到的,其原子的最外层电子数为7,在化学反应中易得到1个电子形成带1个单位负电荷的阴离子,其离子符号为Cl-。
7.C 分子可分,原子也可以再分,原子可以分成原子核和核外电子;电子带负电,所以原子得到电子后带负电荷;分子、原子和离子都可以直接构成物质,如水是由水分子构成的,铁是由铁原子构成的,氯化钠是由钠离子和氯离子构成的;原子核不一定都是由质子和中子构成的,如氢原子的原子核内只有质子,没有中子。
8.A 根据元素周期表中的一格可知,左上角的数字表示原子序数,在原子中,原子序数=核电荷数=质子数=核外电子数,其原子核外电子数为 117,则该元素的原子序数为117。
9.C 赭石的主要成分是由两种元素组成的化合物,其中一种元素是氧元素,属于氧化物。
10.A 判断同素异形体,关键把握两点:①由同种元素组成;②不同单质。臭氧和氧气是由氧元素组成的不同单质,互为同素异形体。
11.C 构成物质A、B、D的分子都是不同种原子,它们属于化合物;构成物质C的分子是同种原子,属于单质,单质与化合物属于纯净物的两种不同类别。
12.(1)O (2)2Fe (3)Al
13.(1)元素 (2)116
14.(1)3 (2)Li+
(1)根据元素周期表中的一格可知,左上角的数字为3,表示原子序数为3。在原子中,原子序数=核电荷数=质子数=核外电子数,则锂元素的原子的核电荷数是3。(2)如如图乙表示锂原子转变为锂离子的过程,锂原子失去1个电子形成带1个单位正电荷的锂离子,其离子符号为Li+。
15.(1)得到 (2)原子 (3)B和C
(1)D粒子的最外层电子数是7,大于4,在化学反应中容易得到电子。(2)若E中x=18,则该粒子中质子数等于电子数,属于原子。(3)A、B、C、D四种粒子中B和C的质子数相同,属于同种元素。
16.SiCl4+H2HCl+Si Si 化学反应前后原子的种类、数目均不变(合理即可)
由微观反应示意如如图可知,该反应的符号表达式为SiCl4+H2HCl+Si。硅是一种固态非金属,是由硅原子直接构成的。由化学反应的实质可知,化学反应前后原子的种类、数目均不变;在化学反应中,分子分成原子,原子再重新组合成新的分子等。
17.(1)分子 (2)原子
(3) (4)2H2O2
18.(1)78.96 6
(2)最外层电子数 Se2-
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
