沪教版(全国)化学九年级上册课课练:专题训练 分子、原子和离子(word版 有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册课课练:专题训练 分子、原子和离子(word版 有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 198.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-28 00:00:00 | ||
图片预览


文档简介
专题训练
分子、原子和离子
一、选择题
1.物质由微观粒子构成,下列物质由离子构成的是 ( )
A.He B.NH3 C.C60 D.NaCl
2.[2020·泰州] 制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为 ( )
A.22 B.48 C.70 D.26
3.下列微观示意如如图中,黑球代表氢原子,白球代表氯原子,其中代表混合物的是 ( )
4.[2020·杭州] 2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C18,这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个 ( )
A.原子 B.质子
C.中子 D.电子
5.下列事实的微观解释中,不正确的是 ( )
A.墙内开花墙外可闻到花香——分子在不断地运动
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——构成物质的分子相同,其化学性质相同
D.水壶中的水沸腾时,壶盖被顶起——水分子间的空隙增大
6.如所示结构示意如如图表示的粒子中,属于阴离子的是 ( )
7.已知某物质的化学式是RNO3,相对分子质量是85,则R元素的相对原子质量是 ( )
A.55 B.55 g
C.23 D.23 g
8.[2020·淄博] 化学是在原子、分子水平上研究物质及其变化规律的一门学科,它能指导我们更好地认识、改造和应用物质。以下说法正确的是 ( )
A.质子、中子、电子都可以直接构成物质
B.原子、分子、离子都可以直接构成物质
C.分子是由原子构成的,水由氢原子和氧原子构成
D.分子是构成物质的基本粒子,空气由空气分子构成
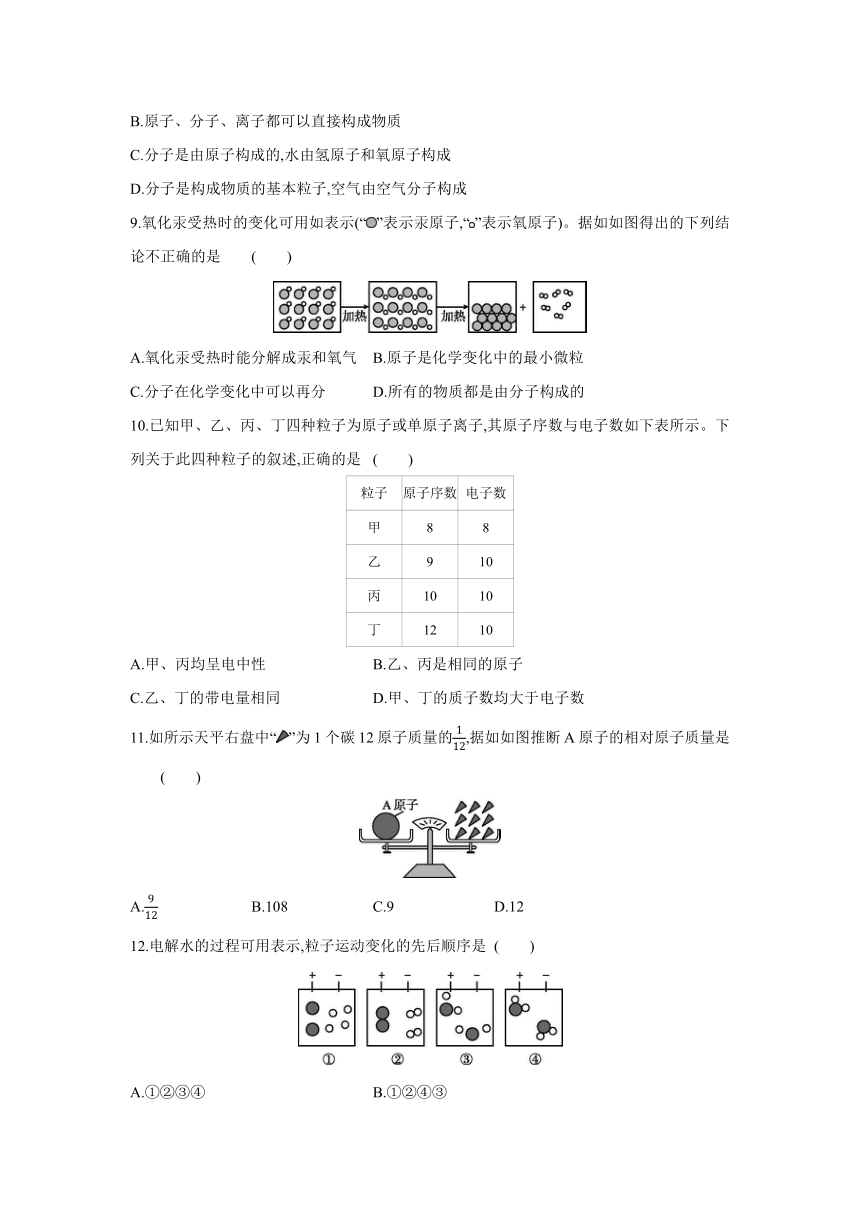
9.氧化汞受热时的变化可用如表示(“”表示汞原子,“”表示氧原子)。据如如图得出的下列结论不正确的是 ( )
A.氧化汞受热时能分解成汞和氧气 B.原子是化学变化中的最小微粒
C.分子在化学变化中可以再分 D.所有的物质都是由分子构成的
10.已知甲、乙、丙、丁四种粒子为原子或单原子离子,其原子序数与电子数如下表所示。下列关于此四种粒子的叙述,正确的是 ( )
粒子 原子序数 电子数
甲 8 8
乙 9 10
丙 10 10
丁 12 10
A.甲、丙均呈电中性 B.乙、丙是相同的原子
C.乙、丁的带电量相同 D.甲、丁的质子数均大于电子数
11.如所示天平右盘中“”为1个碳12原子质量的,据如如图推断A原子的相对原子质量是 ( )
A. B.108 C.9 D.12
12.电解水的过程可用表示,粒子运动变化的先后顺序是 ( )
A.①②③④ B.①②④③
C.④③①② D.④①②③
二、填空题
13.用如所示装置研究分子的性质。
(1)挤出浓氨水,A实验中观察到的实验现象是 。说明的分子性质是 。
(2)写出设计A、B实验的目的: 。
14.在①分子、②原子、③质子、④中子、⑤电子、⑥离子这些微粒中,选择相应微粒的序号填空。
(1)能构成物质的微粒有 。
(2)显电中性的微粒有 。
(3)质量最小的微粒是 。
(4)一定带正电荷的微粒是 。
(5)一定带负电荷的微粒是 。
15.[2019·铁岭改编] 丁香油酚(化学式C10H12O2)是玫瑰花中含有的主要物质,请回答下列 问题。
(1)构成丁香油酚的微粒是 (填微粒种类)。
(2)丁香油酚的相对分子质量是 。
16.人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911年物理学家卢瑟福用带正电的α粒子轰击金箔。实验发现:多数α粒子穿过金箔后仍保持原来的运动方向,绝少数α粒子发生了较大角度的偏转。
(1)卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的 。
(2)当α粒子轰击金箔时,中四条运动轨迹不可能出现的是 (填字母)。
17.[2020·赤峰节选] 如是某化学反应的微观示意如如图,根据如如图示回答下列问题。
(1)A到C的过程中发生改变的粒子是 (填符号)。
(2)该变化过程中的最小粒子是 (填符号)。
(3)该反应的符号表达式为 。
18.碘是一种由碘分子构成的固体物质,某同学利用碘进行了如下的实验:
①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝(提示:碘分子能与馒头中的淀粉作用而呈蓝色)。
②再取少量的碘溶解在水中,用馒头去蘸取碘液,发现馒头也会变蓝。
(1)取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头 (填“会”或“不会”)变蓝。
(2)由上述三个实验可知,分子是 。
(3)市场上买来的食盐一般是加碘盐,含有碘酸钾(KIO3),用馒头沾取少量的食盐水 (填“会”或“不会”)变蓝。
19.模型是联系宏观与微观的桥梁。
(1)如中甲是钠原子的结构示意如如图。
①x的数值为 。
②“11”指的是 。
③钠原子在化学反应中易失去1个电子,形成 (填离子符号)。
(2)如如如图乙是氢分子和氧分子运动的示意如如图。
①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是 (填字母)。
②从如如图中可见,影响分子运动速率的因素除温度外,还有 。
③举一个能说明“温度升高,分子运动速率加快”的生活事例: 。
答案
1.D 2.A 3.D 4.A 5.B
6.D 若质子数=核外电子数,该粒子为原子;若质子数>核外电子数,该粒子为阳离子;若质子数<核外电子数,该粒子为阴离子。
7.C 设R的相对原子质量为x,则有x+14+16×3=85,解得x=23。
8.B 质子、中子和电子构成了原子;原子、分子、离子都可以直接构成物质;分子是由原子构成的,水分子由氢原子和氧原子构成;分子是构成物质的基本粒子,空气是混合物,不存在空气分子。
9.D
10.A 甲和丙的原子序数等于核外电子数,为原子,均呈电中性;乙和丙的原子序数不同,属于不同种原子;乙中原子序数<电子数,带一个单位的负电荷,丁中原子序数>电子数,带两个单位的正电荷,可知乙、丁带电量不同;甲中质子数=电子数,丁中质子数>电子数。
11.C 由如如图可知,天平平衡,故右盘中9个小块的总质量等于一个A原子的质量,每个小块对应的是一个碳12原子质量的,根据相对原子质量计算公式可知,A原子的相对原子质量为9。
12.C
13.(1)滴有酚酞试液的棉花变红
分子在不断运动
(2)研究温度对分子运动速率的影响
(1)氨水显碱性,能使酚酞试液变红,挤出浓氨水后氨分子不断运动,与滴有酚酞试液的棉花接触时,滴有酚酞试液的棉花变红,说明了分子在不断运动。(2)对照A、B实验可知,二者的温度不同,其他条件相同,所以目的是研究温度对分子运动速率的影响。
14.(1)①②⑥ (2)①②④ (3)⑤ (4)③
(5)⑤
15.(1)分子 (2)164
16.(1)原子核 (2)C
(1)卢瑟福认为原子的中心有一个很小的原子核。(2)当α粒子轰击金箔时,如如图中四条运动轨迹不可能出现的是C,因为粒子都带正电荷,相互排斥,轨迹应该和D相似,向上偏转。
17.(1)H2、O2
(2)O、H
(3)H2+O2H2O
(1)在化学变化中,分子种类发生改变,故A到C的过程中发生改变的粒子是氢分子和氧分子,符号分别为H2、O2。(2)原子在化学变化中不发生改变,该变化过程中的最小粒子是氧原子和氢原子,符号分别为O、H。(3)由化学反应的微观示意如如图可知,该反应是氢气和氧气在一定条件下反应生成了水,符号表达式为H2+O2H2O。
18.(1)会
(2)不断运动的
(3)不会
(1)碘升华变成的碘蒸气是由碘分子构成的,都能使淀粉变蓝,所以馒头会变蓝。(2)由上述三个实验可知,分子是不断运动的。(3)加碘盐中不含碘分子,所以用馒头沾取少量的食盐水不会变蓝。
19.(1)①8
②钠原子的质子数(或核电荷数)为11
③Na+
(2)①BC
②分子种类
③湿衣服在阳光下比在阴凉处干得快(合理即可)
(1)①根据在原子中,核内质子数等于核外电子数,可得x=11-2-1=8;③钠原子在化学反应中易失去1个电子,形成带1个单位正电荷的钠离子,其符号为Na+。(2)①比较B和C,分子种类相同,但温度不同的条件下,分子的运动速率不同;②由A和B可知,温度相同,分子不同,运动速率不同,故影响分子运动速率的因素除温度外,还有分子种类。
分子、原子和离子
一、选择题
1.物质由微观粒子构成,下列物质由离子构成的是 ( )
A.He B.NH3 C.C60 D.NaCl
2.[2020·泰州] 制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为 ( )
A.22 B.48 C.70 D.26
3.下列微观示意如如图中,黑球代表氢原子,白球代表氯原子,其中代表混合物的是 ( )
4.[2020·杭州] 2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C18,这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个 ( )
A.原子 B.质子
C.中子 D.电子
5.下列事实的微观解释中,不正确的是 ( )
A.墙内开花墙外可闻到花香——分子在不断地运动
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——构成物质的分子相同,其化学性质相同
D.水壶中的水沸腾时,壶盖被顶起——水分子间的空隙增大
6.如所示结构示意如如图表示的粒子中,属于阴离子的是 ( )
7.已知某物质的化学式是RNO3,相对分子质量是85,则R元素的相对原子质量是 ( )
A.55 B.55 g
C.23 D.23 g
8.[2020·淄博] 化学是在原子、分子水平上研究物质及其变化规律的一门学科,它能指导我们更好地认识、改造和应用物质。以下说法正确的是 ( )
A.质子、中子、电子都可以直接构成物质
B.原子、分子、离子都可以直接构成物质
C.分子是由原子构成的,水由氢原子和氧原子构成
D.分子是构成物质的基本粒子,空气由空气分子构成
9.氧化汞受热时的变化可用如表示(“”表示汞原子,“”表示氧原子)。据如如图得出的下列结论不正确的是 ( )
A.氧化汞受热时能分解成汞和氧气 B.原子是化学变化中的最小微粒
C.分子在化学变化中可以再分 D.所有的物质都是由分子构成的
10.已知甲、乙、丙、丁四种粒子为原子或单原子离子,其原子序数与电子数如下表所示。下列关于此四种粒子的叙述,正确的是 ( )
粒子 原子序数 电子数
甲 8 8
乙 9 10
丙 10 10
丁 12 10
A.甲、丙均呈电中性 B.乙、丙是相同的原子
C.乙、丁的带电量相同 D.甲、丁的质子数均大于电子数
11.如所示天平右盘中“”为1个碳12原子质量的,据如如图推断A原子的相对原子质量是 ( )
A. B.108 C.9 D.12
12.电解水的过程可用表示,粒子运动变化的先后顺序是 ( )
A.①②③④ B.①②④③
C.④③①② D.④①②③
二、填空题
13.用如所示装置研究分子的性质。
(1)挤出浓氨水,A实验中观察到的实验现象是 。说明的分子性质是 。
(2)写出设计A、B实验的目的: 。
14.在①分子、②原子、③质子、④中子、⑤电子、⑥离子这些微粒中,选择相应微粒的序号填空。
(1)能构成物质的微粒有 。
(2)显电中性的微粒有 。
(3)质量最小的微粒是 。
(4)一定带正电荷的微粒是 。
(5)一定带负电荷的微粒是 。
15.[2019·铁岭改编] 丁香油酚(化学式C10H12O2)是玫瑰花中含有的主要物质,请回答下列 问题。
(1)构成丁香油酚的微粒是 (填微粒种类)。
(2)丁香油酚的相对分子质量是 。
16.人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911年物理学家卢瑟福用带正电的α粒子轰击金箔。实验发现:多数α粒子穿过金箔后仍保持原来的运动方向,绝少数α粒子发生了较大角度的偏转。
(1)卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的 。
(2)当α粒子轰击金箔时,中四条运动轨迹不可能出现的是 (填字母)。
17.[2020·赤峰节选] 如是某化学反应的微观示意如如图,根据如如图示回答下列问题。
(1)A到C的过程中发生改变的粒子是 (填符号)。
(2)该变化过程中的最小粒子是 (填符号)。
(3)该反应的符号表达式为 。
18.碘是一种由碘分子构成的固体物质,某同学利用碘进行了如下的实验:
①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝(提示:碘分子能与馒头中的淀粉作用而呈蓝色)。
②再取少量的碘溶解在水中,用馒头去蘸取碘液,发现馒头也会变蓝。
(1)取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头 (填“会”或“不会”)变蓝。
(2)由上述三个实验可知,分子是 。
(3)市场上买来的食盐一般是加碘盐,含有碘酸钾(KIO3),用馒头沾取少量的食盐水 (填“会”或“不会”)变蓝。
19.模型是联系宏观与微观的桥梁。
(1)如中甲是钠原子的结构示意如如图。
①x的数值为 。
②“11”指的是 。
③钠原子在化学反应中易失去1个电子,形成 (填离子符号)。
(2)如如如图乙是氢分子和氧分子运动的示意如如图。
①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是 (填字母)。
②从如如图中可见,影响分子运动速率的因素除温度外,还有 。
③举一个能说明“温度升高,分子运动速率加快”的生活事例: 。
答案
1.D 2.A 3.D 4.A 5.B
6.D 若质子数=核外电子数,该粒子为原子;若质子数>核外电子数,该粒子为阳离子;若质子数<核外电子数,该粒子为阴离子。
7.C 设R的相对原子质量为x,则有x+14+16×3=85,解得x=23。
8.B 质子、中子和电子构成了原子;原子、分子、离子都可以直接构成物质;分子是由原子构成的,水分子由氢原子和氧原子构成;分子是构成物质的基本粒子,空气是混合物,不存在空气分子。
9.D
10.A 甲和丙的原子序数等于核外电子数,为原子,均呈电中性;乙和丙的原子序数不同,属于不同种原子;乙中原子序数<电子数,带一个单位的负电荷,丁中原子序数>电子数,带两个单位的正电荷,可知乙、丁带电量不同;甲中质子数=电子数,丁中质子数>电子数。
11.C 由如如图可知,天平平衡,故右盘中9个小块的总质量等于一个A原子的质量,每个小块对应的是一个碳12原子质量的,根据相对原子质量计算公式可知,A原子的相对原子质量为9。
12.C
13.(1)滴有酚酞试液的棉花变红
分子在不断运动
(2)研究温度对分子运动速率的影响
(1)氨水显碱性,能使酚酞试液变红,挤出浓氨水后氨分子不断运动,与滴有酚酞试液的棉花接触时,滴有酚酞试液的棉花变红,说明了分子在不断运动。(2)对照A、B实验可知,二者的温度不同,其他条件相同,所以目的是研究温度对分子运动速率的影响。
14.(1)①②⑥ (2)①②④ (3)⑤ (4)③
(5)⑤
15.(1)分子 (2)164
16.(1)原子核 (2)C
(1)卢瑟福认为原子的中心有一个很小的原子核。(2)当α粒子轰击金箔时,如如图中四条运动轨迹不可能出现的是C,因为粒子都带正电荷,相互排斥,轨迹应该和D相似,向上偏转。
17.(1)H2、O2
(2)O、H
(3)H2+O2H2O
(1)在化学变化中,分子种类发生改变,故A到C的过程中发生改变的粒子是氢分子和氧分子,符号分别为H2、O2。(2)原子在化学变化中不发生改变,该变化过程中的最小粒子是氧原子和氢原子,符号分别为O、H。(3)由化学反应的微观示意如如图可知,该反应是氢气和氧气在一定条件下反应生成了水,符号表达式为H2+O2H2O。
18.(1)会
(2)不断运动的
(3)不会
(1)碘升华变成的碘蒸气是由碘分子构成的,都能使淀粉变蓝,所以馒头会变蓝。(2)由上述三个实验可知,分子是不断运动的。(3)加碘盐中不含碘分子,所以用馒头沾取少量的食盐水不会变蓝。
19.(1)①8
②钠原子的质子数(或核电荷数)为11
③Na+
(2)①BC
②分子种类
③湿衣服在阳光下比在阴凉处干得快(合理即可)
(1)①根据在原子中,核内质子数等于核外电子数,可得x=11-2-1=8;③钠原子在化学反应中易失去1个电子,形成带1个单位正电荷的钠离子,其符号为Na+。(2)①比较B和C,分子种类相同,但温度不同的条件下,分子的运动速率不同;②由A和B可知,温度相同,分子不同,运动速率不同,故影响分子运动速率的因素除温度外,还有分子种类。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
