粤教版化学九年级上册课课练:专题训练 质量守恒定律的应用(一)—— 图表类题(word版 有答案)
文档属性
| 名称 | 粤教版化学九年级上册课课练:专题训练 质量守恒定律的应用(一)—— 图表类题(word版 有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-28 00:00:00 | ||
图片预览

文档简介
专题训练 质量守恒定律的应用(一)—— 图表类题
类型一 表格型
1.在一密闭容器中,有甲、乙、丙、丁四种物质,令其在一定条件下充分反应,反应前后各物质的质量如图下表,根据质量守恒定律判断x的值为( )
物质 甲 乙 丙 丁
反应前的质量/g 20 50 80 30
反应后的质量/g 0 100 10 x
A.50 B.40 C.10 D.70
2.2020·怀化将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如图下,下列有关说法正确的是( )
物质 甲 乙 丙 丁
反应前的质量/g 30 10 5 5
反应后的质量/g 2 4 m 39
A.m=0
B.发生反应的甲、乙质量比为3∶1
C.该反应是化合反应
D.丙一定作催化剂
3.在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如图下表。下列说法正确的是( )
物质 a b c d
反应前的质量/g 12 100 10 0
反应后的质量/g 40 x 10 32
A.x等于60
B.b一定是化合物
C.c一定是催化剂
D.反应生成的a与d的质量比为5∶4
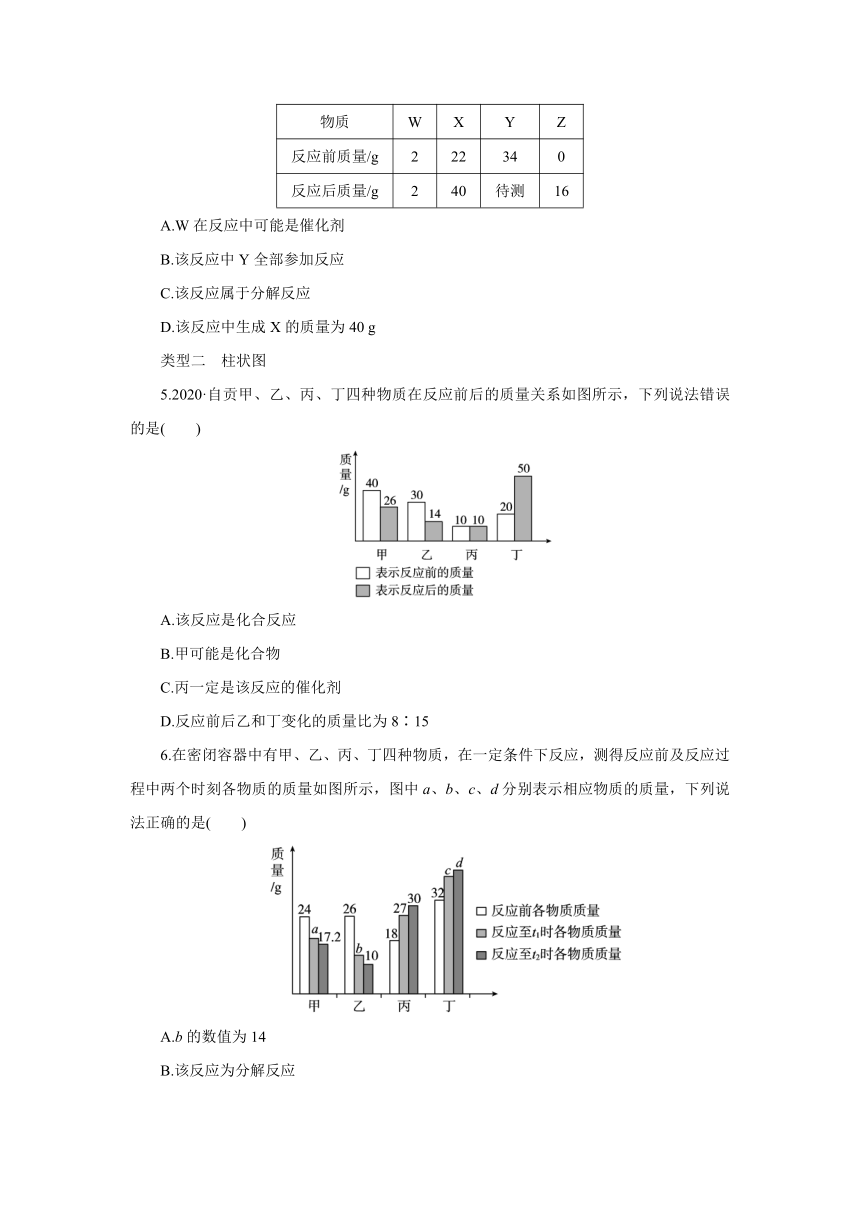
4.在一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图下表所示,下列说法中错误的是( )
物质 W X Y Z
反应前质量/g 2 22 34 0
反应后质量/g 2 40 待测 16
A.W在反应中可能是催化剂
B.该反应中Y全部参加反应
C.该反应属于分解反应
D.该反应中生成X的质量为40 g
类型二 柱状图
5.2020·自贡甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列说法错误的是( )
A.该反应是化合反应
B.甲可能是化合物
C.丙一定是该反应的催化剂
D.反应前后乙和丁变化的质量比为8∶15
6.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量,下列说法正确的是( )
A.b的数值为14
B.该反应为分解反应
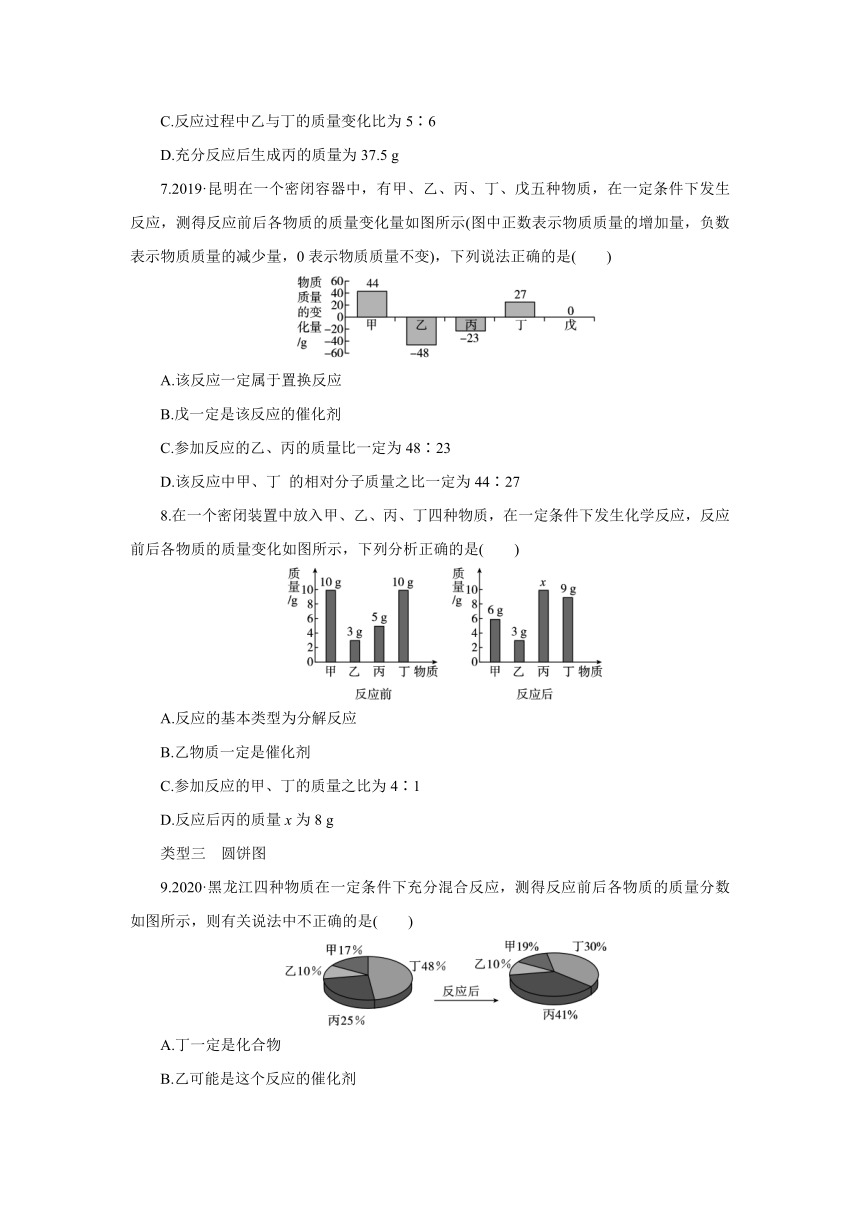
C.反应过程中乙与丁的质量变化比为5∶6
D.充分反应后生成丙的质量为37.5 g
7.2019·昆明在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0表示物质质量不变),下列说法正确的是( )
A.该反应一定属于置换反应
B.戊一定是该反应的催化剂
C.参加反应的乙、丙的质量比一定为48∶23
D.该反应中甲、丁 的相对分子质量之比一定为44∶27
8.在一个密闭装置中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图所示,下列分析正确的是( )
A.反应的基本类型为分解反应
B.乙物质一定是催化剂
C.参加反应的甲、丁的质量之比为4∶1
D.反应后丙的质量x为8 g
类型三 圆饼图
9.2020·黑龙江四种物质在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法中不正确的是( )
A.丁一定是化合物
B.乙可能是这个反应的催化剂
C.生成的甲、丙两物质的质量比为8∶1
D.参加反应的丁的质量一定等于生成甲和丙的质量之和
类型四 折线图
10.2020·宜昌某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了一个化学反应,容器中乙、丙、丁的质量随甲的质量变化的情况如图 所示。下列说法错误的是( )
A.a的值为12
B.丁属于化合物
C.当丁的质量为5 g时,容器中乙的质量为11 g
D.当甲的质量为2 g时,容器中丙与丁的质量之比为12∶5
类型五 其他类型
11.2020·昆明在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如图所示(例如图:d的质量为2 g)。在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )
A.反应结束后c的质量为14 g
B.该反应可能为化合反应
C.a、b变化的质量比一定为9∶17
D.a、d的相对分子质量之比一定为9∶8
答案
1.D 由表中数据分析可知,反应前后甲的质量减少了20 g-0 g=20 g,故是反应物,参加反应的质量为20 g;同理可以确定乙是生成物,生成的质量为100 g-50 g=50 g;丙是反应物,参加反应的质量为80 g-10 g=70 g;由质量守恒定律可知,丁应是生成物,生成的质量为20 g+70 g-50 g=40 g,故x的数值为30+40=70。
2.C 由表中数据分析可知,反应前后甲的质量减少了30 g-2 g=28 g,故是反应物,参加反应的质量为28 g;同理可以确定乙是反应物,参加反应的质量为10 g-4 g=6 g;丁是生成物,生成的质量为39 g-5 g=34 g;由质量守恒定律可知,丙的质量不变,可能作该反应的催化剂,也可能没有参加反应。丙的质量不变,m的数值为5;反应中甲、乙的质量比为28 g∶6 g=14∶3;该反应的反应物为甲和乙,生成物是丁,符合“多变一”的特征,属于化合反应。
3.B
4.D 由表中数据分析可知,反应前后W的质量不变,可能作该反应的催化剂,也可能没有参加反应。X的质量增加了40 g-22 g=18 g,故是生成物,生成的质量为18 g;同理可以确定Z是生成物,生成的质量为16 g-0 g=16 g;由质量守恒定律可知,Y应是反应物,且参加反应的质量为16 g+18 g=34 g,故Y全部参加反应。该反应中生成X的质量为40 g-22 g=18 g。
5.C 由图中数据分析可知,反应前后甲的质量减少了40 g-26 g=14 g,是反应物;反应前后乙的质量减少了30 g-14 g=16 g,是反应物;反应前后丙的质量不变,可能是该反应的催化剂,也可能没有参加反应;反应前后丁的质量增加了50 g-20 g=30 g,是生成物。该反应的反应物为甲和乙,生成物是丁,属于化合反应;甲是化合反应的反应物,可能是化合物,也可能是单质;反应前后乙和丁变化的质量比为16 g∶30 g=8∶15。
6.A 由四种物质反应前后各物质的质量可知,反应前后甲的质量减少了24 g-17.2 g=6.8 g,所以甲是反应物;反应前后乙的质量减少了26 g-10 g=16 g,所以乙是反应物;反应前后丙的质量增加了30 g-18 g=12 g,所以丙是生成物;反应前后丁的质量增加了6.8 g+16 g-12 g=10.8 g,所以丁是生成物,d的数值为32+10.8=42.8,反应过程中参加反应的乙和生成的丙的质量比为16 g∶12 g=4∶3,当生成丙的质量为27 g-18 g=9 g时,参加反应的乙的质量为12 g,所以b的数值为26-12=14。该反应的反应物是甲和乙,生成物是丙和丁,不符合“一变多”的特征,不属于分解反应。该反应的过程中乙与丁的质量变化比为16 g∶10.8 g=40∶27。
7.C
8.C 由图中数据分析可知,反应前后甲的质量减少了10 g-6 g=4 g,故是反应物,参加反应的质量为4 g;同理可以确定乙的质量不变,可能作该反应的催化剂,也可能没有参加反应;丁是反应物,参加反应的质量为10 g-9 g=1 g;由质量守恒定律可知,丙应是生成物,且生成的质量为4 g+1 g=5 g,故反应后丙的质量x为5 g+5 g=10 g。
9.C 由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数增加了19%-17%=2%,故甲是生成物;乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应;丁的质量分数减少了48%-30%=18%,故丁是反应物;丙的质量分数增加了41%-25%=16%,故丙是生成物,生成的甲、丙两物质的质量比为2%∶16%=1∶8。
10.D 由图中信息可知,反应前后丙的质量不变,反应前乙、丁的质量都是10 g,反应后生成8 g甲,丁完全反应,生成了一定质量的乙,生成乙的质量为10 g-8 g=2 g,故a=10+2=12;丁分解生成甲和乙,是化合物;反应过程中,丁、乙、甲三种物质的质量比是10 g∶2 g∶8 g=5∶1∶4,当丁的质量为5 g时,即丁反应了5 g,生成1 g乙,容器中乙的质量为10 g+1 g=11 g;当甲的质量为2 g时,反应的丁质量是2.5 g,容器中丙与丁的质量之比为6 g∶(10 g-2.5 g)=4∶5。
11.C 由图示可知,每一格的质量为1 g;反应前a的质量为5 g,b的质量为22 g-5 g=17 g,c的质量为28 g-22 g=6 g,d的质量为30 g-28 g=2 g。刻度线Ⅰ右移9格,a物质质量增加9 g;刻度线Ⅱ左移8格,同时刻度线Ⅰ右移9格,则b物质质量减少了8 g+9 g=17 g;刻度线Ⅲ左移8格,同时刻度线Ⅱ左移8格,则c物质质量不变;刻度线Ⅲ左移8格,d物质的质量增加了8 g。该反应可表示为b―→a+d,为分解反应。由于不知道化学方程式中化学计量数之比,故无法确定a、d的相对分子质量之比。
类型一 表格型
1.在一密闭容器中,有甲、乙、丙、丁四种物质,令其在一定条件下充分反应,反应前后各物质的质量如图下表,根据质量守恒定律判断x的值为( )
物质 甲 乙 丙 丁
反应前的质量/g 20 50 80 30
反应后的质量/g 0 100 10 x
A.50 B.40 C.10 D.70
2.2020·怀化将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如图下,下列有关说法正确的是( )
物质 甲 乙 丙 丁
反应前的质量/g 30 10 5 5
反应后的质量/g 2 4 m 39
A.m=0
B.发生反应的甲、乙质量比为3∶1
C.该反应是化合反应
D.丙一定作催化剂
3.在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如图下表。下列说法正确的是( )
物质 a b c d
反应前的质量/g 12 100 10 0
反应后的质量/g 40 x 10 32
A.x等于60
B.b一定是化合物
C.c一定是催化剂
D.反应生成的a与d的质量比为5∶4
4.在一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图下表所示,下列说法中错误的是( )
物质 W X Y Z
反应前质量/g 2 22 34 0
反应后质量/g 2 40 待测 16
A.W在反应中可能是催化剂
B.该反应中Y全部参加反应
C.该反应属于分解反应
D.该反应中生成X的质量为40 g
类型二 柱状图
5.2020·自贡甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列说法错误的是( )
A.该反应是化合反应
B.甲可能是化合物
C.丙一定是该反应的催化剂
D.反应前后乙和丁变化的质量比为8∶15
6.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量,下列说法正确的是( )
A.b的数值为14
B.该反应为分解反应
C.反应过程中乙与丁的质量变化比为5∶6
D.充分反应后生成丙的质量为37.5 g
7.2019·昆明在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0表示物质质量不变),下列说法正确的是( )
A.该反应一定属于置换反应
B.戊一定是该反应的催化剂
C.参加反应的乙、丙的质量比一定为48∶23
D.该反应中甲、丁 的相对分子质量之比一定为44∶27
8.在一个密闭装置中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图所示,下列分析正确的是( )
A.反应的基本类型为分解反应
B.乙物质一定是催化剂
C.参加反应的甲、丁的质量之比为4∶1
D.反应后丙的质量x为8 g
类型三 圆饼图
9.2020·黑龙江四种物质在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法中不正确的是( )
A.丁一定是化合物
B.乙可能是这个反应的催化剂
C.生成的甲、丙两物质的质量比为8∶1
D.参加反应的丁的质量一定等于生成甲和丙的质量之和
类型四 折线图
10.2020·宜昌某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了一个化学反应,容器中乙、丙、丁的质量随甲的质量变化的情况如图 所示。下列说法错误的是( )
A.a的值为12
B.丁属于化合物
C.当丁的质量为5 g时,容器中乙的质量为11 g
D.当甲的质量为2 g时,容器中丙与丁的质量之比为12∶5
类型五 其他类型
11.2020·昆明在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如图所示(例如图:d的质量为2 g)。在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )
A.反应结束后c的质量为14 g
B.该反应可能为化合反应
C.a、b变化的质量比一定为9∶17
D.a、d的相对分子质量之比一定为9∶8
答案
1.D 由表中数据分析可知,反应前后甲的质量减少了20 g-0 g=20 g,故是反应物,参加反应的质量为20 g;同理可以确定乙是生成物,生成的质量为100 g-50 g=50 g;丙是反应物,参加反应的质量为80 g-10 g=70 g;由质量守恒定律可知,丁应是生成物,生成的质量为20 g+70 g-50 g=40 g,故x的数值为30+40=70。
2.C 由表中数据分析可知,反应前后甲的质量减少了30 g-2 g=28 g,故是反应物,参加反应的质量为28 g;同理可以确定乙是反应物,参加反应的质量为10 g-4 g=6 g;丁是生成物,生成的质量为39 g-5 g=34 g;由质量守恒定律可知,丙的质量不变,可能作该反应的催化剂,也可能没有参加反应。丙的质量不变,m的数值为5;反应中甲、乙的质量比为28 g∶6 g=14∶3;该反应的反应物为甲和乙,生成物是丁,符合“多变一”的特征,属于化合反应。
3.B
4.D 由表中数据分析可知,反应前后W的质量不变,可能作该反应的催化剂,也可能没有参加反应。X的质量增加了40 g-22 g=18 g,故是生成物,生成的质量为18 g;同理可以确定Z是生成物,生成的质量为16 g-0 g=16 g;由质量守恒定律可知,Y应是反应物,且参加反应的质量为16 g+18 g=34 g,故Y全部参加反应。该反应中生成X的质量为40 g-22 g=18 g。
5.C 由图中数据分析可知,反应前后甲的质量减少了40 g-26 g=14 g,是反应物;反应前后乙的质量减少了30 g-14 g=16 g,是反应物;反应前后丙的质量不变,可能是该反应的催化剂,也可能没有参加反应;反应前后丁的质量增加了50 g-20 g=30 g,是生成物。该反应的反应物为甲和乙,生成物是丁,属于化合反应;甲是化合反应的反应物,可能是化合物,也可能是单质;反应前后乙和丁变化的质量比为16 g∶30 g=8∶15。
6.A 由四种物质反应前后各物质的质量可知,反应前后甲的质量减少了24 g-17.2 g=6.8 g,所以甲是反应物;反应前后乙的质量减少了26 g-10 g=16 g,所以乙是反应物;反应前后丙的质量增加了30 g-18 g=12 g,所以丙是生成物;反应前后丁的质量增加了6.8 g+16 g-12 g=10.8 g,所以丁是生成物,d的数值为32+10.8=42.8,反应过程中参加反应的乙和生成的丙的质量比为16 g∶12 g=4∶3,当生成丙的质量为27 g-18 g=9 g时,参加反应的乙的质量为12 g,所以b的数值为26-12=14。该反应的反应物是甲和乙,生成物是丙和丁,不符合“一变多”的特征,不属于分解反应。该反应的过程中乙与丁的质量变化比为16 g∶10.8 g=40∶27。
7.C
8.C 由图中数据分析可知,反应前后甲的质量减少了10 g-6 g=4 g,故是反应物,参加反应的质量为4 g;同理可以确定乙的质量不变,可能作该反应的催化剂,也可能没有参加反应;丁是反应物,参加反应的质量为10 g-9 g=1 g;由质量守恒定律可知,丙应是生成物,且生成的质量为4 g+1 g=5 g,故反应后丙的质量x为5 g+5 g=10 g。
9.C 由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数增加了19%-17%=2%,故甲是生成物;乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应;丁的质量分数减少了48%-30%=18%,故丁是反应物;丙的质量分数增加了41%-25%=16%,故丙是生成物,生成的甲、丙两物质的质量比为2%∶16%=1∶8。
10.D 由图中信息可知,反应前后丙的质量不变,反应前乙、丁的质量都是10 g,反应后生成8 g甲,丁完全反应,生成了一定质量的乙,生成乙的质量为10 g-8 g=2 g,故a=10+2=12;丁分解生成甲和乙,是化合物;反应过程中,丁、乙、甲三种物质的质量比是10 g∶2 g∶8 g=5∶1∶4,当丁的质量为5 g时,即丁反应了5 g,生成1 g乙,容器中乙的质量为10 g+1 g=11 g;当甲的质量为2 g时,反应的丁质量是2.5 g,容器中丙与丁的质量之比为6 g∶(10 g-2.5 g)=4∶5。
11.C 由图示可知,每一格的质量为1 g;反应前a的质量为5 g,b的质量为22 g-5 g=17 g,c的质量为28 g-22 g=6 g,d的质量为30 g-28 g=2 g。刻度线Ⅰ右移9格,a物质质量增加9 g;刻度线Ⅱ左移8格,同时刻度线Ⅰ右移9格,则b物质质量减少了8 g+9 g=17 g;刻度线Ⅲ左移8格,同时刻度线Ⅱ左移8格,则c物质质量不变;刻度线Ⅲ左移8格,d物质的质量增加了8 g。该反应可表示为b―→a+d,为分解反应。由于不知道化学方程式中化学计量数之比,故无法确定a、d的相对分子质量之比。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
