第一章第一节物质的分类与转化-课时1(课件)2022-2023学年上学期高一化学人教版(2019)必修第一册(30张ppt)
文档属性
| 名称 | 第一章第一节物质的分类与转化-课时1(课件)2022-2023学年上学期高一化学人教版(2019)必修第一册(30张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 20.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-31 00:00:00 | ||
图片预览





文档简介
(共30张PPT)
第一节 物质的分类及转化
第一章物质及其变化
目录
CONTENT
第一课时 物质的分类
第二课时 物质的转化
学习目标与核心素养
学习目标
核心素养
认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
了解分散系的概念及分散系的分类
认识丁达尔效应在生活中的应用
1
2
3
微观探析:能利用元素的种类以及存在形态将物质分为不同类别;能利用分散系粒子的大小区分分散系
宏观辨识:能从微观粒子的角度认识胶体的特征
1
2
【小组讨论】
同学们都去过图书馆和超市对吧,如果你想买一样商品,在没有服务员的前提下,怎样快速找到你需要的商品呢?
图书馆里有许许多多的书籍,你怎么样找到你需要的书?
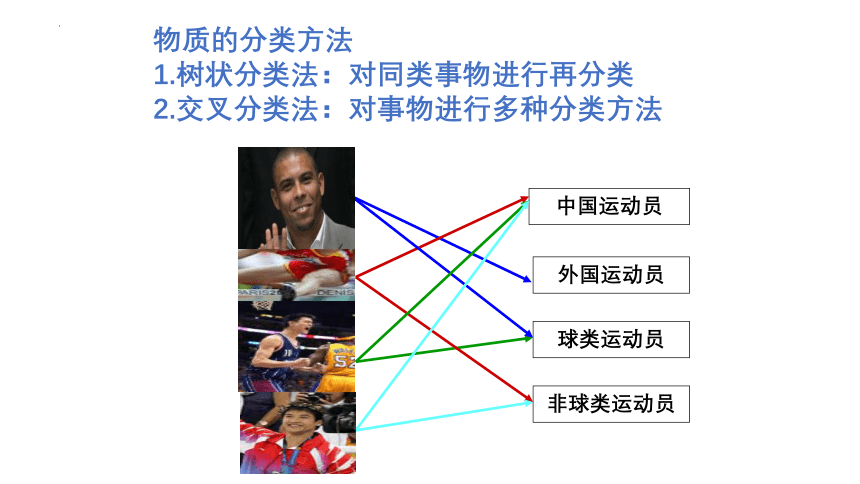
物质的分类方法
1.树状分类法:对同类事物进行再分类
2.交叉分类法:对事物进行多种分类方法
中国运动员
外国运动员
球类运动员
非球类运动员
一、物质的分类
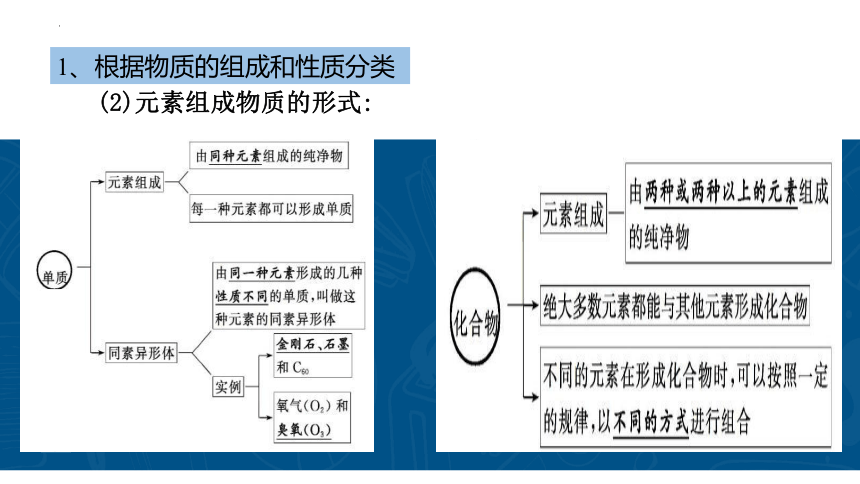
1、根据物质的组成和性质分类
由同一种元素形成几种性质不同的单质,叫做这种元素的同素异形体
例如:C60 、金刚石、石墨 O2和O3
请尝试对你所学过的化学物质和化学反应进行分类,并与同学交流。
1.根据物质的组成分类
(1)化学研究的基础:根据元素组成对物质进行分类是化学研究的基础。
(2)元素组成物质的形式:
1、根据物质的组成和性质分类
1、根据物质的组成和性质分类
物质
纯净物
金属单质
非金属单质
化合物
酸
碱
盐
氧化物
单 质
混合物
稀有气体
无机物
有机物
树状分类法
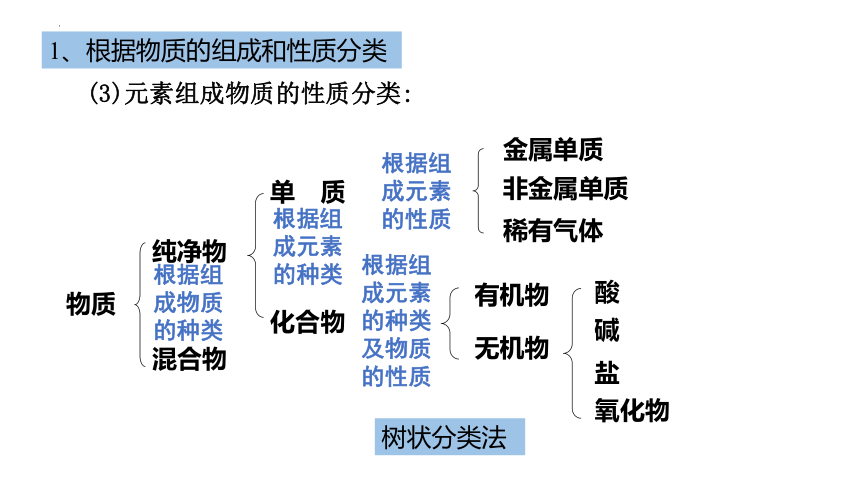
(3)元素组成物质的性质分类:
根据组成物质的种类
根据组成元素的种类
根据组成元素的种类及物质的性质
根据组成元素的性质
树状分类法
树状分类法就是对分类后的各类事物再分类的多层次分类方法。
树状分类法的分类原则:同一层次的物质类别间一般是相互独立,没有交叉的。
优点:体现了对事物认识逐渐深入的过程。
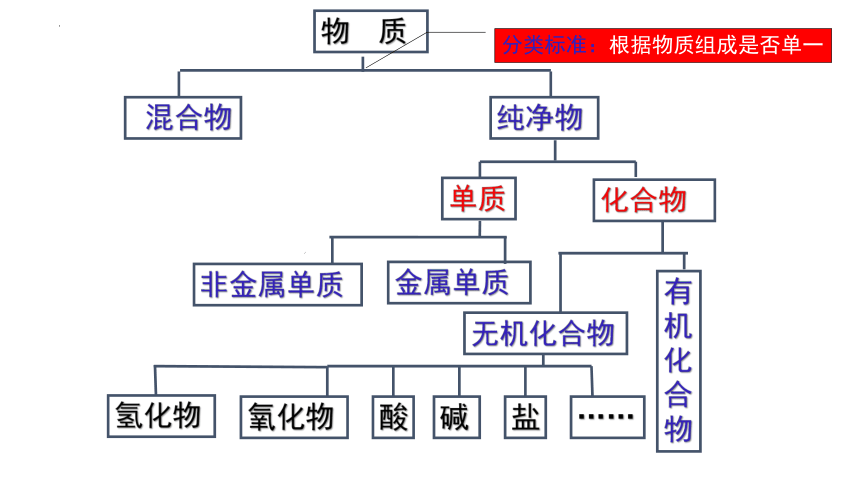
物 质
混合物
纯净物
单质
化合物
非金属单质
金属单质
无机化合物
有机化合物
氧化物
……
盐
酸
碱
氢化物
分类标准:根据物质组成是否单一
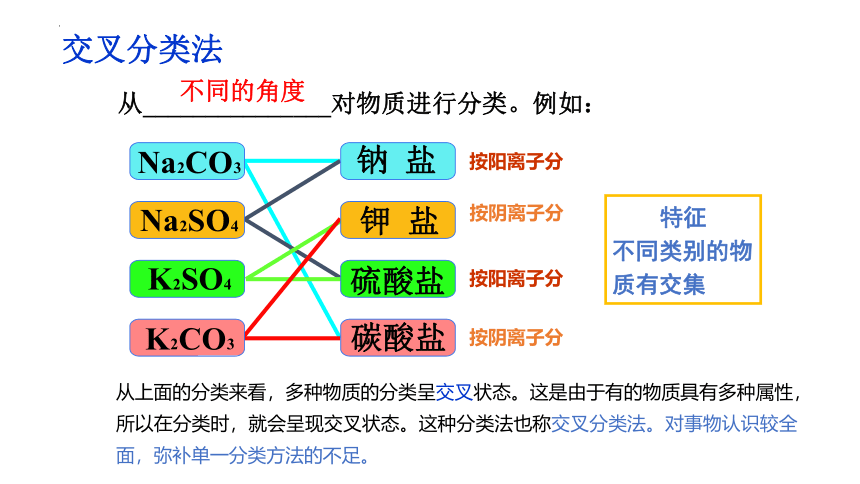
不同的角度
交叉分类法
从_______________对物质进行分类。例如:
按阳离子分
按阳离子分
按阴离子分
按阴离子分
特征
不同类别的物质有交集
从上面的分类来看,多种物质的分类呈交叉状态。这是由于有的物质具有多种属性,所以在分类时,就会呈现交叉状态。这种分类法也称交叉分类法。对事物认识较全面,弥补单一分类方法的不足。
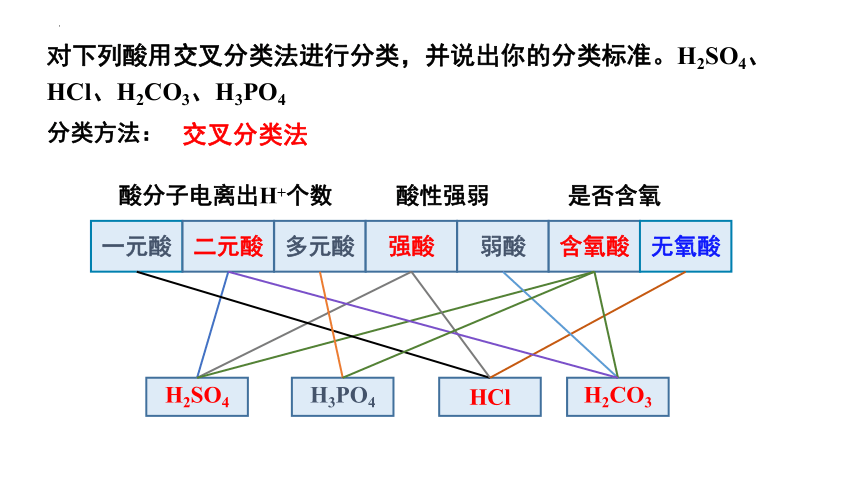
对下列酸用交叉分类法进行分类,并说出你的分类标准。H2SO4、HCl、H2CO3、H3PO4
一元酸
二元酸
多元酸
强酸
弱酸
含氧酸
无氧酸
H2SO4
H2CO3
H3PO4
HCl
是否含氧
酸性强弱
酸分子电离出H+个数
分类方法:
交叉分类法
一、物质的分类
氧化物的分类:
① 按组成元素分类
② 按化学性质分类
金属氧化物( CuO )
非金属氧化物( CO2 )
酸性氧化物(CO2、SO2)
碱性氧化物(Fe2O3、CuO)
两性氧化物(Al2O3)
不成盐氧化物(CO、NO)
酸性氧化物:与碱反应生成相应的盐和水的氧化物
碱性氧化物:与酸反应生成相应的盐和水的氧化物
知识拓展:NO、CO等氧化物既不能与酸反应又不能与碱反应生成相应的盐和水,属于不成盐氧化物
金属氧化物与碱性氧化物的关系
金属氧化物不一定是碱性氧化物,碱性氧化物一定是金属氧化物;
非金属氧化物与酸性氧化物的关系
非金属氧化物不一定是酸性氧化物,酸性氧化物不一定是非金属氧化物。
初中时所学“溶液”的概念:
一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液.
溶剂:能溶解其他物质的物质.
溶质:被溶解的物质
同学们能回顾初中学过的知识溶液吗?
从物质分类的角度看,CuSO4溶液、泥水、振荡后的植物油与水的混合物属于什么类?
一、物质的分类
2、分散系和胶体
分散系:把一种(或多种)物质分散在另一种 (或多种)物质中所得到的体系。
分散质:被分散的物质
分散剂:起容纳分散质作用的物质
分散系 分散质 分散剂
溶液 NaCl溶液 _____ ___
浊液 泥水 ___________ ___
牛奶 不溶于水的有机 物小液滴 水
一、物质的分类
2、分散系和胶体
分散质
分散剂
气
气
液
液
固
固
思考:你能用交叉分类法说出它们能组成哪些种分散系吗?
9种分散系
分散质 分散剂 实例
气 气
液
固
气 液
液
固
气 固
液
固
空气
云、雾
烟
盐酸
牛奶、酒精
糖水
泡沫塑料
珍珠
有色玻璃、合金
分散系 分散质 分散剂
烟 __________________ ____________
雾 ____________ ____________
碘酒 ____________ ____________
食盐水 ____________ ______
有色玻璃 __________________ ____________
常见分散系及其组成
微小尘埃(固)
空气(气)
微小水滴(液)
空气(气)
碘(固)
酒精(液)
食盐(固)
水(液)
金属氧化物(固)
玻璃(固)
一、物质的分类
2、分散系和胶体
分散系的分类:按照分散质粒子的大小来分:
分散系
溶液
浊液
胶体
(<1nm)
(1~100nm)
(>100nm)
胶体:分散质微粒的直径大小在1-100nm之间的分散系。
稳定
不稳定
介稳性
胶体:分散质粒子的直径为1~100 nm的分散系是胶体。
胶体的分类
液溶胶
气溶胶
分散剂是液体
分散剂是气体
固溶胶
标准:
分散剂的状态
分散剂是固体
Fe(OH)3胶体
云、雾
有色玻璃
一、物质的分类
2、分散系和胶体
【思考】有些液溶胶是透明的,用肉眼很难与溶液和胶体。那么,用什么方法能够将它们区分开呢?
【实验1-1】Fe(OH)3胶体的制备
(1) 实验操作
(2) 实验现象:烧杯中液体呈 色。
红褐
逐滴加入到
红褐色液体,透明
FeCl3 + 3H2O Fe(OH)3(胶体) + 3HCl
Fe(OH)3胶体的制备实验
溶液
一条光亮的“通路”
散射
胶体的性质
应用:区分胶体与溶液
光束照射时的现象
Fe(OH)3胶体
CuSO4溶液
形成一条光亮的通路
无现象产生
生活中的丁达尔效应
分散系 溶液 悬浊液 乳浊液 胶体
举例 NaCl溶液 泥水 牛奶 Fe(OH)3胶体
分散质粒子组成 离子 巨大数目的分子集合体 众多分子的集合,单个大分子
分散质粒子直径 <1 nm >100 nm 1~100 nm之间
外观特点 均一,透明 不均一,不透明 均一,有的透明
稳定性 稳定 不稳定 较稳定
能否透过滤纸 能透过 不能透过 不能透过 能透过
能否透过半透膜 能透过 不能透过 不能透过 不能透过
1)溶液、浊液和胶体三种分散系的本质区别是什么
提示:三种分散系的本质区别是分散质粒子大小。
2)胶体是不是都是均匀透明的液体
提示:胶体根据分散剂状态可分为气溶胶、固溶胶和液溶胶,胶体不一定是液体。
3).关于分散系的“两个”大小比较
分散质粒子的大小:溶液<胶体<浊液;
分散系稳定性大小:溶液>胶体>浊液。
4).关于分散质的“两个”只有
只有浊液不能透过滤纸,溶液和胶体能透过;
只有溶液能透过半透膜,浊液和胶体不能透过。
1、分类是一种科学的学习方法
2、分类方法:树状分类法、交叉分类法
3、酸性氧化物、碱性氧化物的概念
4、分散系的概念
5、胶体的概念与分类
6、氢氧化铁胶体的制备
7、丁达尔效应
课堂总结
1.某气体经过检验只含有一种元素,则该气体是( )
A.一种单质
B.一种化合物
C.单质与化合物的混合物
D.可能是一种单质,也可能是几种单质的混合物
当堂训练
2.下列分散系属于胶体的是( )
①肥皂水②豆浆③食盐水④蔗糖水⑤泥水⑥淀粉液
A.只有② B.①②⑥ C.①②③ D.①②③④⑥
3.下列事实与胶体性质无关的是( )
A.在豆浆里加入盐卤做豆腐
B.河流入海处易形成沙洲
C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路
D.FeCl3溶液中加入NaOH溶液出现红褐色沉淀
谢谢
第一节 物质的分类及转化
第一章物质及其变化
目录
CONTENT
第一课时 物质的分类
第二课时 物质的转化
学习目标与核心素养
学习目标
核心素养
认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
了解分散系的概念及分散系的分类
认识丁达尔效应在生活中的应用
1
2
3
微观探析:能利用元素的种类以及存在形态将物质分为不同类别;能利用分散系粒子的大小区分分散系
宏观辨识:能从微观粒子的角度认识胶体的特征
1
2
【小组讨论】
同学们都去过图书馆和超市对吧,如果你想买一样商品,在没有服务员的前提下,怎样快速找到你需要的商品呢?
图书馆里有许许多多的书籍,你怎么样找到你需要的书?
物质的分类方法
1.树状分类法:对同类事物进行再分类
2.交叉分类法:对事物进行多种分类方法
中国运动员
外国运动员
球类运动员
非球类运动员
一、物质的分类
1、根据物质的组成和性质分类
由同一种元素形成几种性质不同的单质,叫做这种元素的同素异形体
例如:C60 、金刚石、石墨 O2和O3
请尝试对你所学过的化学物质和化学反应进行分类,并与同学交流。
1.根据物质的组成分类
(1)化学研究的基础:根据元素组成对物质进行分类是化学研究的基础。
(2)元素组成物质的形式:
1、根据物质的组成和性质分类
1、根据物质的组成和性质分类
物质
纯净物
金属单质
非金属单质
化合物
酸
碱
盐
氧化物
单 质
混合物
稀有气体
无机物
有机物
树状分类法
(3)元素组成物质的性质分类:
根据组成物质的种类
根据组成元素的种类
根据组成元素的种类及物质的性质
根据组成元素的性质
树状分类法
树状分类法就是对分类后的各类事物再分类的多层次分类方法。
树状分类法的分类原则:同一层次的物质类别间一般是相互独立,没有交叉的。
优点:体现了对事物认识逐渐深入的过程。
物 质
混合物
纯净物
单质
化合物
非金属单质
金属单质
无机化合物
有机化合物
氧化物
……
盐
酸
碱
氢化物
分类标准:根据物质组成是否单一
不同的角度
交叉分类法
从_______________对物质进行分类。例如:
按阳离子分
按阳离子分
按阴离子分
按阴离子分
特征
不同类别的物质有交集
从上面的分类来看,多种物质的分类呈交叉状态。这是由于有的物质具有多种属性,所以在分类时,就会呈现交叉状态。这种分类法也称交叉分类法。对事物认识较全面,弥补单一分类方法的不足。
对下列酸用交叉分类法进行分类,并说出你的分类标准。H2SO4、HCl、H2CO3、H3PO4
一元酸
二元酸
多元酸
强酸
弱酸
含氧酸
无氧酸
H2SO4
H2CO3
H3PO4
HCl
是否含氧
酸性强弱
酸分子电离出H+个数
分类方法:
交叉分类法
一、物质的分类
氧化物的分类:
① 按组成元素分类
② 按化学性质分类
金属氧化物( CuO )
非金属氧化物( CO2 )
酸性氧化物(CO2、SO2)
碱性氧化物(Fe2O3、CuO)
两性氧化物(Al2O3)
不成盐氧化物(CO、NO)
酸性氧化物:与碱反应生成相应的盐和水的氧化物
碱性氧化物:与酸反应生成相应的盐和水的氧化物
知识拓展:NO、CO等氧化物既不能与酸反应又不能与碱反应生成相应的盐和水,属于不成盐氧化物
金属氧化物与碱性氧化物的关系
金属氧化物不一定是碱性氧化物,碱性氧化物一定是金属氧化物;
非金属氧化物与酸性氧化物的关系
非金属氧化物不一定是酸性氧化物,酸性氧化物不一定是非金属氧化物。
初中时所学“溶液”的概念:
一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液.
溶剂:能溶解其他物质的物质.
溶质:被溶解的物质
同学们能回顾初中学过的知识溶液吗?
从物质分类的角度看,CuSO4溶液、泥水、振荡后的植物油与水的混合物属于什么类?
一、物质的分类
2、分散系和胶体
分散系:把一种(或多种)物质分散在另一种 (或多种)物质中所得到的体系。
分散质:被分散的物质
分散剂:起容纳分散质作用的物质
分散系 分散质 分散剂
溶液 NaCl溶液 _____ ___
浊液 泥水 ___________ ___
牛奶 不溶于水的有机 物小液滴 水
一、物质的分类
2、分散系和胶体
分散质
分散剂
气
气
液
液
固
固
思考:你能用交叉分类法说出它们能组成哪些种分散系吗?
9种分散系
分散质 分散剂 实例
气 气
液
固
气 液
液
固
气 固
液
固
空气
云、雾
烟
盐酸
牛奶、酒精
糖水
泡沫塑料
珍珠
有色玻璃、合金
分散系 分散质 分散剂
烟 __________________ ____________
雾 ____________ ____________
碘酒 ____________ ____________
食盐水 ____________ ______
有色玻璃 __________________ ____________
常见分散系及其组成
微小尘埃(固)
空气(气)
微小水滴(液)
空气(气)
碘(固)
酒精(液)
食盐(固)
水(液)
金属氧化物(固)
玻璃(固)
一、物质的分类
2、分散系和胶体
分散系的分类:按照分散质粒子的大小来分:
分散系
溶液
浊液
胶体
(<1nm)
(1~100nm)
(>100nm)
胶体:分散质微粒的直径大小在1-100nm之间的分散系。
稳定
不稳定
介稳性
胶体:分散质粒子的直径为1~100 nm的分散系是胶体。
胶体的分类
液溶胶
气溶胶
分散剂是液体
分散剂是气体
固溶胶
标准:
分散剂的状态
分散剂是固体
Fe(OH)3胶体
云、雾
有色玻璃
一、物质的分类
2、分散系和胶体
【思考】有些液溶胶是透明的,用肉眼很难与溶液和胶体。那么,用什么方法能够将它们区分开呢?
【实验1-1】Fe(OH)3胶体的制备
(1) 实验操作
(2) 实验现象:烧杯中液体呈 色。
红褐
逐滴加入到
红褐色液体,透明
FeCl3 + 3H2O Fe(OH)3(胶体) + 3HCl
Fe(OH)3胶体的制备实验
溶液
一条光亮的“通路”
散射
胶体的性质
应用:区分胶体与溶液
光束照射时的现象
Fe(OH)3胶体
CuSO4溶液
形成一条光亮的通路
无现象产生
生活中的丁达尔效应
分散系 溶液 悬浊液 乳浊液 胶体
举例 NaCl溶液 泥水 牛奶 Fe(OH)3胶体
分散质粒子组成 离子 巨大数目的分子集合体 众多分子的集合,单个大分子
分散质粒子直径 <1 nm >100 nm 1~100 nm之间
外观特点 均一,透明 不均一,不透明 均一,有的透明
稳定性 稳定 不稳定 较稳定
能否透过滤纸 能透过 不能透过 不能透过 能透过
能否透过半透膜 能透过 不能透过 不能透过 不能透过
1)溶液、浊液和胶体三种分散系的本质区别是什么
提示:三种分散系的本质区别是分散质粒子大小。
2)胶体是不是都是均匀透明的液体
提示:胶体根据分散剂状态可分为气溶胶、固溶胶和液溶胶,胶体不一定是液体。
3).关于分散系的“两个”大小比较
分散质粒子的大小:溶液<胶体<浊液;
分散系稳定性大小:溶液>胶体>浊液。
4).关于分散质的“两个”只有
只有浊液不能透过滤纸,溶液和胶体能透过;
只有溶液能透过半透膜,浊液和胶体不能透过。
1、分类是一种科学的学习方法
2、分类方法:树状分类法、交叉分类法
3、酸性氧化物、碱性氧化物的概念
4、分散系的概念
5、胶体的概念与分类
6、氢氧化铁胶体的制备
7、丁达尔效应
课堂总结
1.某气体经过检验只含有一种元素,则该气体是( )
A.一种单质
B.一种化合物
C.单质与化合物的混合物
D.可能是一种单质,也可能是几种单质的混合物
当堂训练
2.下列分散系属于胶体的是( )
①肥皂水②豆浆③食盐水④蔗糖水⑤泥水⑥淀粉液
A.只有② B.①②⑥ C.①②③ D.①②③④⑥
3.下列事实与胶体性质无关的是( )
A.在豆浆里加入盐卤做豆腐
B.河流入海处易形成沙洲
C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路
D.FeCl3溶液中加入NaOH溶液出现红褐色沉淀
谢谢
