浙教版科学九年级上册同步提优训练:2.2 金属的化学性质 第1课时(含解析)
文档属性
| 名称 | 浙教版科学九年级上册同步提优训练:2.2 金属的化学性质 第1课时(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-08-04 00:00:00 | ||
图片预览


文档简介
第2节 金属的化学性质
第1课时 金属与氧气的反应 金属防腐
请判断下列说法的正误(正确的在括号内画“√”,错误的画“×”):
(1)金属在一定条件下,都能与氧气发生反应。( )
(2)将一根铜丝放在酒精灯的外焰处加热,铜丝没有燃烧,说明铜不与氧气反应。( )
(3)金属腐蚀都是因为金属直接跟空气中的氧气化合生成金属氧化物。( )
(4)防止金属腐蚀只能用隔绝氧气的方法来实现。( )
(5)铁在氧气中燃烧的化学方程式为4Fe+3O22Fe2O3。( )
(6)洗涤铝制容器时,应用钢丝球擦洗,使其恢复光亮。( )
[核心知识]
1.金属生锈的条件:金属与氧气、水等物质同时接触。
2.防止金属生锈的方法:
(1)保持金属表面洁净、干燥;
(2)隔绝空气(如涂油、刷漆等);
(3)改变金属的内部结构。
1.下列有关金属性质的说法错误的是( )
A. 常温下所有金属都是银白色的固体
B.在空气中灼烧铜丝,其表面会变黑
C.铜、银等金属具有良好的导电性
D.埋在潮湿、疏松、透气的酸性土壤中的铸铁管容易被腐蚀
2.通常铝制品很耐腐蚀,其主要原因是( )
A.铝不易发生化学反应
B.铝表面致密的氧化膜阻止铝进一步被氧化
C.铝在空气中不易被氧化
D.铝的氧化物容易在空气中生成铝
3.银制容器在空气中放置一段时间后表面会变黑,原因是发生了反应:4Ag+2H2S+O2=== 2X+2H2O,则X的化学式为( )
A. AgS B.Ag2O C.Ag2S D.Ag2O2
4.取三枚洁净无锈的铁钉,分别放入三支试管中,用如所示的物质进行实验,试管中铁钉锈蚀速率由快到慢的顺序为( )
A. ②①③ B.①②③
C.②③① D.③①②
5.2020·徐州 纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,如所示是纳米铁粉在锥形瓶中燃烧的实验。下列说法不正确的是( )
A.纳米铁粉燃烧的化学方程式为3Fe+2O2Fe3O4
B.水可防止生成物溅落炸裂瓶底
C.激光手电照射使纳米铁粉的着火点降低
D.气球先膨胀后又变瘪
6.2021·杭州 海绵铁是多孔隙的块状固体物质,主要成分是铁单质,常用于除工业循环冷却水中的溶解氧,当含有氧气的水通过海绵铁时,其中铁单质跟氧气等物质发生化合反应,生成不溶于水的红褐色氢氧化物。请回答:
(1)写出上述生成红褐色氢氧化物的化学方程式: _____________________________________。
(2)海绵铁除去溶解氧的反应中,氧气表现了________(填“氧化”或“还原”)性,跟成分相同的普通铁块相比较,海绵铁除氧效果要好得多,原因是_____________________________
________________________________________________________________________。
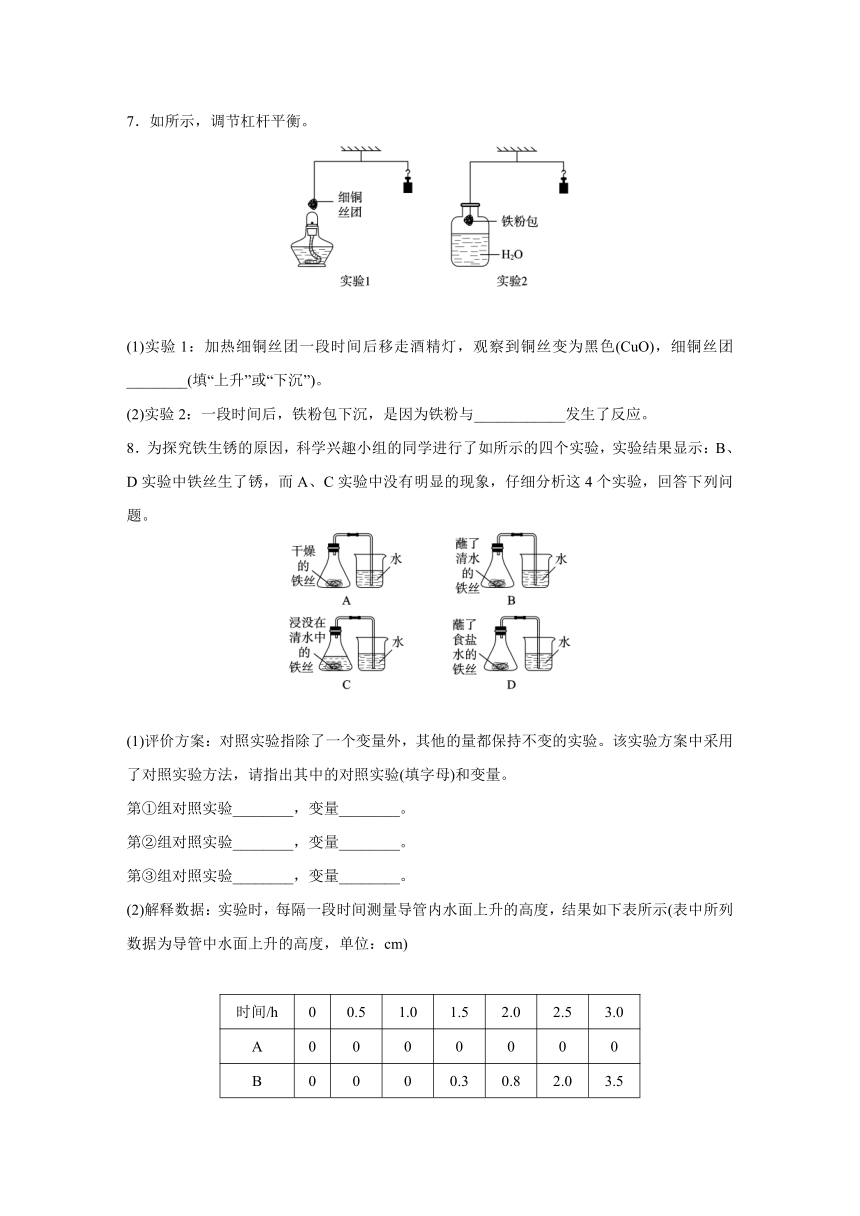
7.如所示,调节杠杆平衡。
(1)实验1:加热细铜丝团一段时间后移走酒精灯,观察到铜丝变为黑色(CuO),细铜丝团________(填“上升”或“下沉”)。
(2)实验2:一段时间后,铁粉包下沉,是因为铁粉与____________发生了反应。
8.为探究铁生锈的原因,科学兴趣小组的同学进行了如所示的四个实验,实验结果显示:B、D实验中铁丝生了锈,而A、C实验中没有明显的现象,仔细分析这4个实验,回答下列问题。
(1)评价方案:对照实验指除了一个变量外,其他的量都保持不变的实验。该实验方案中采用了对照实验方法,请指出其中的对照实验(填字母)和变量。
第①组对照实验________,变量________。
第②组对照实验________,变量________。
第③组对照实验________,变量________。
(2)解释数据:实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度,单位:cm)
时间/h 0 0.5 1.0 1.5 2.0 2.5 3.0
A 0 0 0 0 0 0 0
B 0 0 0 0.3 0.8 2.0 3.5
C 0 0 0 0 0 0 0
D 0 0.4 1.2 3.4 7.6 9.5 9.8
导致B、D实验装置中导管内水面上升的原因是______________________________________
________________________________________________________________________。
(3)获得结论:根据本实验,你认为导致铁生锈的物质有__________,能加快铁生锈的物质是________________________________________________________________________。
9.在氧化亚铁、氧化铁和四氧化三铁三种化合物中,与等质量的铁元素相结合的氧元素的质量比为( )
A. 1∶3∶4 B.2∶3∶6
C.6∶9∶8 D.3∶8∶9
10.冬天,同学们流行买“暖蛋”御寒,“暖蛋”的主要成分有铁粉、活性炭粉、氯化钠等,通过氧化反应放热取暖。取部分“暖蛋”的混合粉末润湿,并按 中乙所示连接好实验装置。下列叙述错误的是( )
A. 红色的水缓慢进入锥形瓶中
B.实验过程中锥形瓶底部发热
C.该实验装置可用来测定空气中氧气的体积分数
D.食盐水可增大铁生锈的速率
11.铁制品在我们家庭中应用广泛,现有从洗澡间拆下的两根生锈的铁管,A管里面生了很多锈,B管外面生锈严重,请根据所学知识回答问题。
(1)铁生锈的条件是____________________,铁锈的主要成分的化学式为__________。
(2)请判断:A、B两管中________管原来是供热水的管道,理由是___________________
________________________________________________________________________。
(3)稀盐酸可用来除铁锈,请写出反应的化学方程式:________________________________________________________________________。
答案
核心·易错
(1)× 金即使在高温条件下,也不与氧气反应。
(2)×
(3)× 金属腐蚀是一个比较复杂的过程,有些直接和氧气化合;有些需要氧气和水共同作用,如铁的腐蚀;有些还需要其他物质参与,如铜的锈蚀需要氧气、水、二氧化碳共同作用。
(4)×
(5)× 铁在氧气中燃烧的化学方程式为3Fe+2O2Fe3O4。
(6)×
能力提升拔尖练
1.A 金属都有金属光泽,但不是所有金属都是银白色的固体。
了解金属的物理共性和个性,大多数金属常温下为固体,汞却为液体;金属具有导电性、导热性和延展性。知道金属的一些化学性质:如绝大多数金属能与氧气反应,金属在潮湿的空气中易生锈。
2.B 铝的化学性质比较活泼,在常温下就能与氧气反应,生成一层致密的氧化物薄膜,从而阻止铝进一步被氧化。
3.C 由4Ag+2H2S+O2===2X+2H2O可知,反应前银原子是4个,反应后应该也是4个,包含在2X中;反应前氢原子是4个,反应后氢原子也是4个;反应前硫原子是2个,反应后硫原子也是2个,包含在2X中;反应前氧原子是2个,反应后氧原子也是2个;由此分析可知,X的化学式是Ag2S。
4.A ①中铁钉与水和较少量的氧气接触,生锈速率较慢;②中铁钉与水和氧气充分接触,生锈速率较快;③中铁钉与水和很少量的氧气接触,生锈速率很慢。
铁生锈的条件是与氧气和水同时接触,只满足其中一个条件铁是不会生锈的。植物油在题中有防止空气中的氧气继续溶解于水的作用。
5.C 物质的着火点是一定的,一般不会降低;纳米铁粉燃烧放出大量的热,使锥形瓶内压强增大,气球膨胀,装置冷却后由于消耗氧气,锥形瓶内压强减小,气球又变瘪。
6.(1)4Fe+3O2+6H2O===4Fe(OH)3
(2)氧化 海绵铁中多孔隙,增大了反应物之间的接触面积,加快了反应速率
(1)由题意可知,海绵铁能与氧气、水反应生成氢氧化铁,反应的化学方程式是4Fe+3O2+6H2O===4Fe(OH)3。(2)海绵铁除去溶解氧的反应中,氧气提供了氧,表现了氧化性,跟成分相同的普通铁块相比较,海绵铁除氧效果要好得多,原因是海绵铁中多孔隙,增大了反应物之间的接触面积,加快了反应速率。
7.(1)下沉
(2)水、氧气
(1)根据质量守恒,铜在加热的条件下与氧气反应生成氧化铜,加热前是细铜丝团的质量,加热后是生成的氧化铜的质量,质量增加,故细铜丝团下沉。(2)铁粉在潮湿的空气中与氧气和水反应而锈蚀,反应后固体的质量增加,所以铁粉包下沉。
8.(1)AB 水 BC 氧气 BD 食盐
(2)铁丝生锈消耗了装置中的氧气,导致压强减小,水面上升
(3)水和氧气 食盐
培优初探拓展练
9.C 由于比较的是氧元素与等质量的铁元素相结合,故可以把FeO、Fe2O3、Fe3O4看作FeO、FeO、FeO,则氧原子的个数比是1∶∶,即质量比为6∶9∶8。
解答此题时还可以假设铁元素的质量为m,根据这三种化合物中的铁、氧元素的质量比求出氧元素的质量,进而求出质量比。
10.C 该实验不可用来测定空气中氧气的体积分数,因为当烧杯中的水倒吸入锥形瓶中,铁粉与氧气不能充分接触时,锥形瓶中的氧气消耗缓慢,耗时较长。
11.(1)与氧气和水同时接触 Fe2O3
(2)B 热水管中的水含氧量少,内部不容易生锈,而外面温度高,铁易生锈
(3)Fe2O3+6HCl===2FeCl3+3H2O
第1课时 金属与氧气的反应 金属防腐
请判断下列说法的正误(正确的在括号内画“√”,错误的画“×”):
(1)金属在一定条件下,都能与氧气发生反应。( )
(2)将一根铜丝放在酒精灯的外焰处加热,铜丝没有燃烧,说明铜不与氧气反应。( )
(3)金属腐蚀都是因为金属直接跟空气中的氧气化合生成金属氧化物。( )
(4)防止金属腐蚀只能用隔绝氧气的方法来实现。( )
(5)铁在氧气中燃烧的化学方程式为4Fe+3O22Fe2O3。( )
(6)洗涤铝制容器时,应用钢丝球擦洗,使其恢复光亮。( )
[核心知识]
1.金属生锈的条件:金属与氧气、水等物质同时接触。
2.防止金属生锈的方法:
(1)保持金属表面洁净、干燥;
(2)隔绝空气(如涂油、刷漆等);
(3)改变金属的内部结构。
1.下列有关金属性质的说法错误的是( )
A. 常温下所有金属都是银白色的固体
B.在空气中灼烧铜丝,其表面会变黑
C.铜、银等金属具有良好的导电性
D.埋在潮湿、疏松、透气的酸性土壤中的铸铁管容易被腐蚀
2.通常铝制品很耐腐蚀,其主要原因是( )
A.铝不易发生化学反应
B.铝表面致密的氧化膜阻止铝进一步被氧化
C.铝在空气中不易被氧化
D.铝的氧化物容易在空气中生成铝
3.银制容器在空气中放置一段时间后表面会变黑,原因是发生了反应:4Ag+2H2S+O2=== 2X+2H2O,则X的化学式为( )
A. AgS B.Ag2O C.Ag2S D.Ag2O2
4.取三枚洁净无锈的铁钉,分别放入三支试管中,用如所示的物质进行实验,试管中铁钉锈蚀速率由快到慢的顺序为( )
A. ②①③ B.①②③
C.②③① D.③①②
5.2020·徐州 纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,如所示是纳米铁粉在锥形瓶中燃烧的实验。下列说法不正确的是( )
A.纳米铁粉燃烧的化学方程式为3Fe+2O2Fe3O4
B.水可防止生成物溅落炸裂瓶底
C.激光手电照射使纳米铁粉的着火点降低
D.气球先膨胀后又变瘪
6.2021·杭州 海绵铁是多孔隙的块状固体物质,主要成分是铁单质,常用于除工业循环冷却水中的溶解氧,当含有氧气的水通过海绵铁时,其中铁单质跟氧气等物质发生化合反应,生成不溶于水的红褐色氢氧化物。请回答:
(1)写出上述生成红褐色氢氧化物的化学方程式: _____________________________________。
(2)海绵铁除去溶解氧的反应中,氧气表现了________(填“氧化”或“还原”)性,跟成分相同的普通铁块相比较,海绵铁除氧效果要好得多,原因是_____________________________
________________________________________________________________________。
7.如所示,调节杠杆平衡。
(1)实验1:加热细铜丝团一段时间后移走酒精灯,观察到铜丝变为黑色(CuO),细铜丝团________(填“上升”或“下沉”)。
(2)实验2:一段时间后,铁粉包下沉,是因为铁粉与____________发生了反应。
8.为探究铁生锈的原因,科学兴趣小组的同学进行了如所示的四个实验,实验结果显示:B、D实验中铁丝生了锈,而A、C实验中没有明显的现象,仔细分析这4个实验,回答下列问题。
(1)评价方案:对照实验指除了一个变量外,其他的量都保持不变的实验。该实验方案中采用了对照实验方法,请指出其中的对照实验(填字母)和变量。
第①组对照实验________,变量________。
第②组对照实验________,变量________。
第③组对照实验________,变量________。
(2)解释数据:实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度,单位:cm)
时间/h 0 0.5 1.0 1.5 2.0 2.5 3.0
A 0 0 0 0 0 0 0
B 0 0 0 0.3 0.8 2.0 3.5
C 0 0 0 0 0 0 0
D 0 0.4 1.2 3.4 7.6 9.5 9.8
导致B、D实验装置中导管内水面上升的原因是______________________________________
________________________________________________________________________。
(3)获得结论:根据本实验,你认为导致铁生锈的物质有__________,能加快铁生锈的物质是________________________________________________________________________。
9.在氧化亚铁、氧化铁和四氧化三铁三种化合物中,与等质量的铁元素相结合的氧元素的质量比为( )
A. 1∶3∶4 B.2∶3∶6
C.6∶9∶8 D.3∶8∶9
10.冬天,同学们流行买“暖蛋”御寒,“暖蛋”的主要成分有铁粉、活性炭粉、氯化钠等,通过氧化反应放热取暖。取部分“暖蛋”的混合粉末润湿,并按 中乙所示连接好实验装置。下列叙述错误的是( )
A. 红色的水缓慢进入锥形瓶中
B.实验过程中锥形瓶底部发热
C.该实验装置可用来测定空气中氧气的体积分数
D.食盐水可增大铁生锈的速率
11.铁制品在我们家庭中应用广泛,现有从洗澡间拆下的两根生锈的铁管,A管里面生了很多锈,B管外面生锈严重,请根据所学知识回答问题。
(1)铁生锈的条件是____________________,铁锈的主要成分的化学式为__________。
(2)请判断:A、B两管中________管原来是供热水的管道,理由是___________________
________________________________________________________________________。
(3)稀盐酸可用来除铁锈,请写出反应的化学方程式:________________________________________________________________________。
答案
核心·易错
(1)× 金即使在高温条件下,也不与氧气反应。
(2)×
(3)× 金属腐蚀是一个比较复杂的过程,有些直接和氧气化合;有些需要氧气和水共同作用,如铁的腐蚀;有些还需要其他物质参与,如铜的锈蚀需要氧气、水、二氧化碳共同作用。
(4)×
(5)× 铁在氧气中燃烧的化学方程式为3Fe+2O2Fe3O4。
(6)×
能力提升拔尖练
1.A 金属都有金属光泽,但不是所有金属都是银白色的固体。
了解金属的物理共性和个性,大多数金属常温下为固体,汞却为液体;金属具有导电性、导热性和延展性。知道金属的一些化学性质:如绝大多数金属能与氧气反应,金属在潮湿的空气中易生锈。
2.B 铝的化学性质比较活泼,在常温下就能与氧气反应,生成一层致密的氧化物薄膜,从而阻止铝进一步被氧化。
3.C 由4Ag+2H2S+O2===2X+2H2O可知,反应前银原子是4个,反应后应该也是4个,包含在2X中;反应前氢原子是4个,反应后氢原子也是4个;反应前硫原子是2个,反应后硫原子也是2个,包含在2X中;反应前氧原子是2个,反应后氧原子也是2个;由此分析可知,X的化学式是Ag2S。
4.A ①中铁钉与水和较少量的氧气接触,生锈速率较慢;②中铁钉与水和氧气充分接触,生锈速率较快;③中铁钉与水和很少量的氧气接触,生锈速率很慢。
铁生锈的条件是与氧气和水同时接触,只满足其中一个条件铁是不会生锈的。植物油在题中有防止空气中的氧气继续溶解于水的作用。
5.C 物质的着火点是一定的,一般不会降低;纳米铁粉燃烧放出大量的热,使锥形瓶内压强增大,气球膨胀,装置冷却后由于消耗氧气,锥形瓶内压强减小,气球又变瘪。
6.(1)4Fe+3O2+6H2O===4Fe(OH)3
(2)氧化 海绵铁中多孔隙,增大了反应物之间的接触面积,加快了反应速率
(1)由题意可知,海绵铁能与氧气、水反应生成氢氧化铁,反应的化学方程式是4Fe+3O2+6H2O===4Fe(OH)3。(2)海绵铁除去溶解氧的反应中,氧气提供了氧,表现了氧化性,跟成分相同的普通铁块相比较,海绵铁除氧效果要好得多,原因是海绵铁中多孔隙,增大了反应物之间的接触面积,加快了反应速率。
7.(1)下沉
(2)水、氧气
(1)根据质量守恒,铜在加热的条件下与氧气反应生成氧化铜,加热前是细铜丝团的质量,加热后是生成的氧化铜的质量,质量增加,故细铜丝团下沉。(2)铁粉在潮湿的空气中与氧气和水反应而锈蚀,反应后固体的质量增加,所以铁粉包下沉。
8.(1)AB 水 BC 氧气 BD 食盐
(2)铁丝生锈消耗了装置中的氧气,导致压强减小,水面上升
(3)水和氧气 食盐
培优初探拓展练
9.C 由于比较的是氧元素与等质量的铁元素相结合,故可以把FeO、Fe2O3、Fe3O4看作FeO、FeO、FeO,则氧原子的个数比是1∶∶,即质量比为6∶9∶8。
解答此题时还可以假设铁元素的质量为m,根据这三种化合物中的铁、氧元素的质量比求出氧元素的质量,进而求出质量比。
10.C 该实验不可用来测定空气中氧气的体积分数,因为当烧杯中的水倒吸入锥形瓶中,铁粉与氧气不能充分接触时,锥形瓶中的氧气消耗缓慢,耗时较长。
11.(1)与氧气和水同时接触 Fe2O3
(2)B 热水管中的水含氧量少,内部不容易生锈,而外面温度高,铁易生锈
(3)Fe2O3+6HCl===2FeCl3+3H2O
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
