2.1. 空气(1)课件--2022-2023学年九年级化学人教版上册(共21张PPT)
文档属性
| 名称 | 2.1. 空气(1)课件--2022-2023学年九年级化学人教版上册(共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 845.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-03 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
我们周围的空气
课题1 空气(1)
空气
知识 与技能 了解空气的组成;掌握探究氧气含量的实验;学会区分纯净物、混合物
过程 与方法 通过红磷燃烧测定空气中氧气含量的实验,培养用实验探究的能力
情感态度与价值观 体验科学家严肃认真的科学态度,初步学会科学实验的方法。联系生活实际,激发学习化学的兴趣
学习目标
重点 探究空气的组成、空气中氧气含量的实验;物质的简单分类
难点 测定空气中氧气体积含量的实验
重点难点
1. 很久以前,人们认为空气只是单一的某种物质.
2. 18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气.
空气发现史
1.酥脆的饼干放置在空气中会变软,说明空气中含有___,蜡烛能在空气中燃烧,说明空气中含有____。
2.按右图①和②进行实验。实验操作:将注射器的活塞从0刻度拉至25 mL。瓶内空气抽走了___ mL。烧杯中的水将_______,体积约为___ mL。
红墨水
红墨水
水
25
25
氧气
倒流
①
②
课前预习
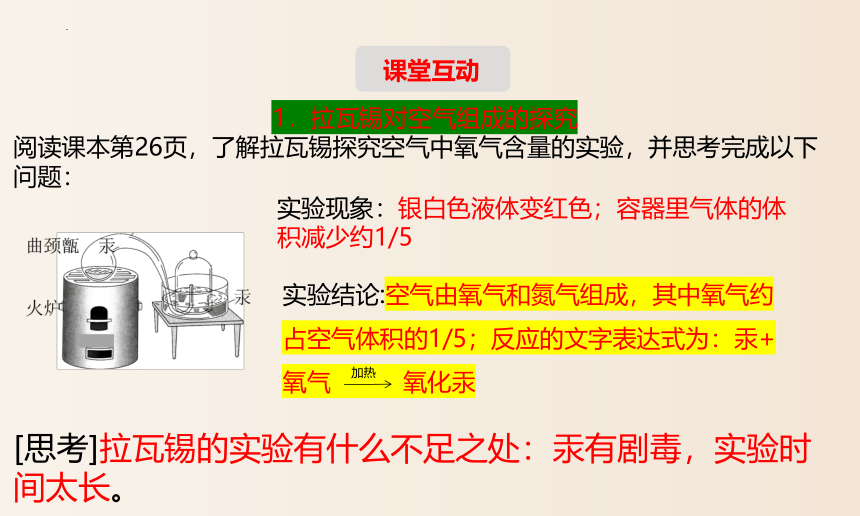
1.拉瓦锡对空气组成的探究
阅读课本第26页,了解拉瓦锡探究空气中氧气含量的实验,并思考完成以下问题:
[思考]拉瓦锡的实验有什么不足之处:汞有剧毒,实验时间太长。
课堂互动
实验现象:银白色液体变红色;容器里气体的体积减少约1/5
实验结论:空气由氧气和氮气组成,其中氧气约占空气体积的1/5;反应的文字表达式为:汞+氧气 氧化汞
加热
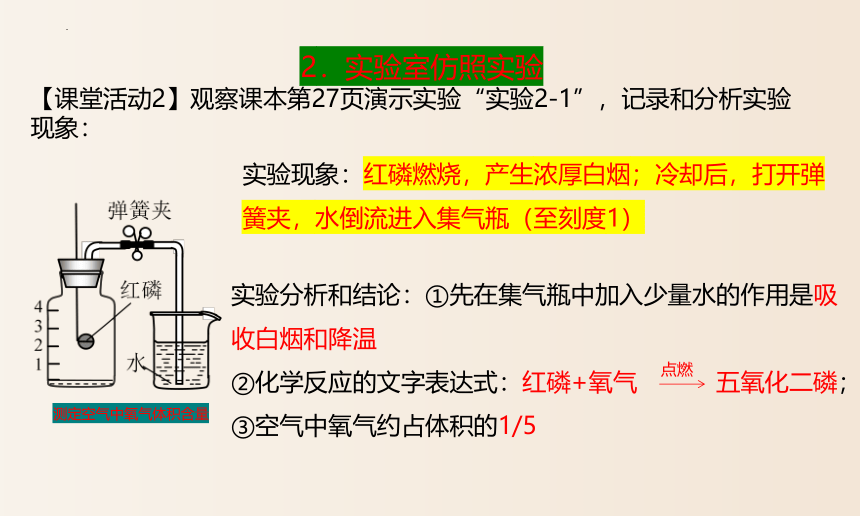
2.实验室仿照实验
【课堂活动2】观察课本第27页演示实验“实验2-1”,记录和分析实验现象:
测定空气中氧气体积含量
实验现象:红磷燃烧,产生浓厚白烟;冷却后,打开弹簧夹,水倒流进入集气瓶(至刻度1)
实验分析和结论:①先在集气瓶中加入少量水的作用是吸收白烟和降温
②化学反应的文字表达式:红磷+氧气 五氧化二磷;
③空气中氧气约占体积的1/5
点燃
[结论]实验的原理是:利用红磷燃烧消耗瓶内的氧气生成固体物质,使瓶内气体体积减少压强减小,烧杯中的水会被压入集气瓶,来推测空气里氧气的含量。
[思考]测定氧气含量的实验中,集气瓶内剩余的气体主要是氮气。
(1)氮气的性质:红磷熄灭了,这种现象说明氮气具有的化学性质是不支持燃烧(或不与红磷反应或化学性质不活泼);集气瓶内水面上升一定高度后,不能继续上升,得到氮气的物理性质是难溶于水
。
(2)实验误差分析
①点燃的红磷为什么要迅速伸入集气瓶内?
避免瓶内空气受热逸出;
②如果装置漏气,测出氧气的含量会偏小;如果红磷的量很少,实验中测出氧气的含量会偏小;如果装置没有冷却就打开弹簧夹,测出氧气的含量会偏小;点燃红磷后,若将燃烧匙伸入集气瓶中的速度稍慢,会导致测出氧气的含量偏大。
【课堂练习1】下列有关刚完成的空气中氧气含量测定实验的说法中,正确的是( )
A.实验时,红磷取量的多少不影响实验结果
B.红磷熄灭后,应立即打开弹簧夹
C.将点燃的红磷放入瓶内,用弹簧夹夹紧胶管
D.反应后,瓶中剩余的气体主要是氮气
D
知识点2 空气的组成
【课堂活动3】阅读课本第27页,了解空气的组成成分并填写下表:
成分
体积分数
氧气
21%
0.94%
0.03%
稀有气体
0.03%
二氧化碳
稀有气体
78%
氮气
知识点3 纯净物和混合物
【课堂活动4】分析下列物质的组成,其中由同种物质组成的是_______________(填序号,下同),由不同物质组成的是__________。
①氧气 ②氮气 ③二氧化碳 ④清新的空气
⑤澄清石灰水 ⑥水 ⑦五氧化二磷 ⑧稀盐酸
[小结]纯净物:___________________________;混合物:___________________________。
①②③⑥⑦
由不同种物质组成的物质
由同种物质组成的物质
④⑤⑧
【课堂练习2】下列物质中,属于纯净物的有____________(填序号)。
a.海水 b.二氧化碳 c.矿泉水
d.氢氧化铜 e.加碘食盐 f.冰红茶
g.石灰石 h.冰水混合物
bdh
1.空气是一种宝贵的资源,下列气体不是来自空气的是( )
A.氮气 B.氧气
C.氢气 D.稀有气体
2.下列属于纯净物的是( )
A.新鲜的空气 B.湖水
C.海天酱油 D.液氧
C
D
测评反馈
3.空气中含量较少,且跟植物的光合作用有关的气体是( )
A.氮气 B.氧气
C.二氧化碳 D.稀有气体
4.空气中氧气和氮气的体积比约为( )
A.1∶4 B.1∶5
C.4∶1 D.5∶1
C
A
5.空气中氧气含量测定的实验如右图所示。下列说法错误的是( )
A.集气瓶和烧杯中的水,在本实验中作用有所不同
B.红磷燃烧产生大量的白烟
C.红磷燃烧只消耗集气瓶中的氧气
D.该实验证明,氧气约占空气总质量的1/5
D
1.空气中氧气体积分数测定的探究实验解析。
(1)药品选择:①只能与空气中O2反应;②生成物没有气体(如不选蜡烛),选择红磷等物质。
(2)实验结论的表达:氧气约占空气中体积的1/5。关键词:“约”“体积”(不是“质量”)。
名师点睛
(3)操作注意点:
①点燃红磷之前要用弹簧夹夹紧胶管;
②点燃红磷后要立即伸入瓶中,迅速塞紧塞子,目的是防止瓶内空气受热逸出,导致结果偏大;
③瓶中加水的目的:降温、吸收五氧化二磷。
(4)实验误差:
①偏小:装置漏气、红磷不足等;
②偏大:点燃红磷后伸入集气瓶中不够迅速等。
(5)实验的改进:改进总的目的是提高实验的精确度,减少对空气的污染。主要思路如下:
①在装置内点燃红磷,避免瓶内空气受热膨胀逸出,同时避免五氧化二磷扩散到空气中污染空气;
②使用量筒或有刻度的玻璃管,主要是便于计算出实验结果。
2.易错点:
①“烟”“雾”“气”的判断(“烟”是固体小颗粒分散在空气中;“雾”是小液滴分散在空气中。红磷在空气中燃烧产生浓厚的白烟,不是“白雾”);
②氧气、氮气等在空气中的含量是“体积分数”不是“质量分数”;
③“稀有气体”为混合物,“冰水混合物”为纯净物。
我们周围的空气
课题1 空气(1)
空气
知识 与技能 了解空气的组成;掌握探究氧气含量的实验;学会区分纯净物、混合物
过程 与方法 通过红磷燃烧测定空气中氧气含量的实验,培养用实验探究的能力
情感态度与价值观 体验科学家严肃认真的科学态度,初步学会科学实验的方法。联系生活实际,激发学习化学的兴趣
学习目标
重点 探究空气的组成、空气中氧气含量的实验;物质的简单分类
难点 测定空气中氧气体积含量的实验
重点难点
1. 很久以前,人们认为空气只是单一的某种物质.
2. 18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气.
空气发现史
1.酥脆的饼干放置在空气中会变软,说明空气中含有___,蜡烛能在空气中燃烧,说明空气中含有____。
2.按右图①和②进行实验。实验操作:将注射器的活塞从0刻度拉至25 mL。瓶内空气抽走了___ mL。烧杯中的水将_______,体积约为___ mL。
红墨水
红墨水
水
25
25
氧气
倒流
①
②
课前预习
1.拉瓦锡对空气组成的探究
阅读课本第26页,了解拉瓦锡探究空气中氧气含量的实验,并思考完成以下问题:
[思考]拉瓦锡的实验有什么不足之处:汞有剧毒,实验时间太长。
课堂互动
实验现象:银白色液体变红色;容器里气体的体积减少约1/5
实验结论:空气由氧气和氮气组成,其中氧气约占空气体积的1/5;反应的文字表达式为:汞+氧气 氧化汞
加热
2.实验室仿照实验
【课堂活动2】观察课本第27页演示实验“实验2-1”,记录和分析实验现象:
测定空气中氧气体积含量
实验现象:红磷燃烧,产生浓厚白烟;冷却后,打开弹簧夹,水倒流进入集气瓶(至刻度1)
实验分析和结论:①先在集气瓶中加入少量水的作用是吸收白烟和降温
②化学反应的文字表达式:红磷+氧气 五氧化二磷;
③空气中氧气约占体积的1/5
点燃
[结论]实验的原理是:利用红磷燃烧消耗瓶内的氧气生成固体物质,使瓶内气体体积减少压强减小,烧杯中的水会被压入集气瓶,来推测空气里氧气的含量。
[思考]测定氧气含量的实验中,集气瓶内剩余的气体主要是氮气。
(1)氮气的性质:红磷熄灭了,这种现象说明氮气具有的化学性质是不支持燃烧(或不与红磷反应或化学性质不活泼);集气瓶内水面上升一定高度后,不能继续上升,得到氮气的物理性质是难溶于水
。
(2)实验误差分析
①点燃的红磷为什么要迅速伸入集气瓶内?
避免瓶内空气受热逸出;
②如果装置漏气,测出氧气的含量会偏小;如果红磷的量很少,实验中测出氧气的含量会偏小;如果装置没有冷却就打开弹簧夹,测出氧气的含量会偏小;点燃红磷后,若将燃烧匙伸入集气瓶中的速度稍慢,会导致测出氧气的含量偏大。
【课堂练习1】下列有关刚完成的空气中氧气含量测定实验的说法中,正确的是( )
A.实验时,红磷取量的多少不影响实验结果
B.红磷熄灭后,应立即打开弹簧夹
C.将点燃的红磷放入瓶内,用弹簧夹夹紧胶管
D.反应后,瓶中剩余的气体主要是氮气
D
知识点2 空气的组成
【课堂活动3】阅读课本第27页,了解空气的组成成分并填写下表:
成分
体积分数
氧气
21%
0.94%
0.03%
稀有气体
0.03%
二氧化碳
稀有气体
78%
氮气
知识点3 纯净物和混合物
【课堂活动4】分析下列物质的组成,其中由同种物质组成的是_______________(填序号,下同),由不同物质组成的是__________。
①氧气 ②氮气 ③二氧化碳 ④清新的空气
⑤澄清石灰水 ⑥水 ⑦五氧化二磷 ⑧稀盐酸
[小结]纯净物:___________________________;混合物:___________________________。
①②③⑥⑦
由不同种物质组成的物质
由同种物质组成的物质
④⑤⑧
【课堂练习2】下列物质中,属于纯净物的有____________(填序号)。
a.海水 b.二氧化碳 c.矿泉水
d.氢氧化铜 e.加碘食盐 f.冰红茶
g.石灰石 h.冰水混合物
bdh
1.空气是一种宝贵的资源,下列气体不是来自空气的是( )
A.氮气 B.氧气
C.氢气 D.稀有气体
2.下列属于纯净物的是( )
A.新鲜的空气 B.湖水
C.海天酱油 D.液氧
C
D
测评反馈
3.空气中含量较少,且跟植物的光合作用有关的气体是( )
A.氮气 B.氧气
C.二氧化碳 D.稀有气体
4.空气中氧气和氮气的体积比约为( )
A.1∶4 B.1∶5
C.4∶1 D.5∶1
C
A
5.空气中氧气含量测定的实验如右图所示。下列说法错误的是( )
A.集气瓶和烧杯中的水,在本实验中作用有所不同
B.红磷燃烧产生大量的白烟
C.红磷燃烧只消耗集气瓶中的氧气
D.该实验证明,氧气约占空气总质量的1/5
D
1.空气中氧气体积分数测定的探究实验解析。
(1)药品选择:①只能与空气中O2反应;②生成物没有气体(如不选蜡烛),选择红磷等物质。
(2)实验结论的表达:氧气约占空气中体积的1/5。关键词:“约”“体积”(不是“质量”)。
名师点睛
(3)操作注意点:
①点燃红磷之前要用弹簧夹夹紧胶管;
②点燃红磷后要立即伸入瓶中,迅速塞紧塞子,目的是防止瓶内空气受热逸出,导致结果偏大;
③瓶中加水的目的:降温、吸收五氧化二磷。
(4)实验误差:
①偏小:装置漏气、红磷不足等;
②偏大:点燃红磷后伸入集气瓶中不够迅速等。
(5)实验的改进:改进总的目的是提高实验的精确度,减少对空气的污染。主要思路如下:
①在装置内点燃红磷,避免瓶内空气受热膨胀逸出,同时避免五氧化二磷扩散到空气中污染空气;
②使用量筒或有刻度的玻璃管,主要是便于计算出实验结果。
2.易错点:
①“烟”“雾”“气”的判断(“烟”是固体小颗粒分散在空气中;“雾”是小液滴分散在空气中。红磷在空气中燃烧产生浓厚的白烟,不是“白雾”);
②氧气、氮气等在空气中的含量是“体积分数”不是“质量分数”;
③“稀有气体”为混合物,“冰水混合物”为纯净物。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
