第三章 晶体结构与性质-单元测试-2021-2022学年高二下学期化学人教版(2019)选择性必修第二册(Word含答案)
文档属性
| 名称 | 第三章 晶体结构与性质-单元测试-2021-2022学年高二下学期化学人教版(2019)选择性必修第二册(Word含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 235.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-04 00:00:00 | ||
图片预览

文档简介
第三章晶体结构与性质
题号 一 二 三 四 总分
得分
一、单选题
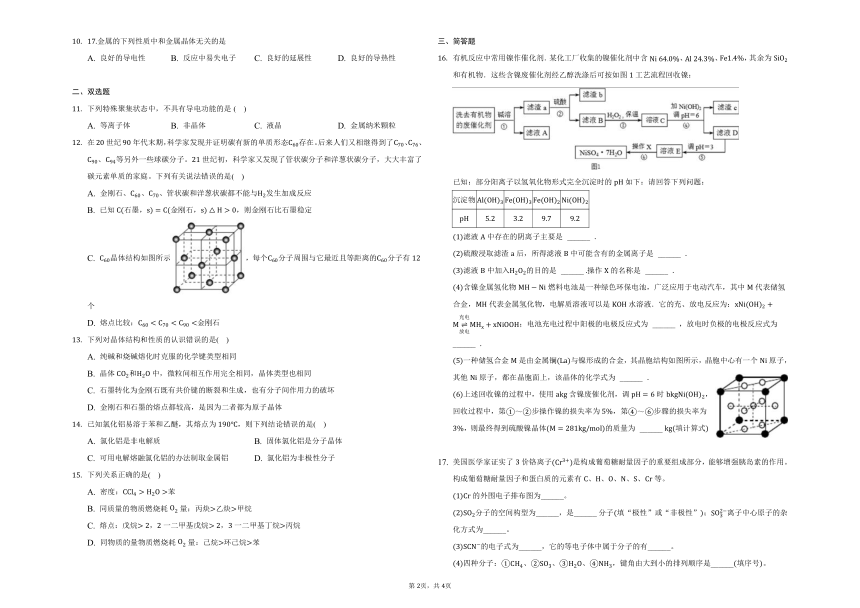
有关晶体的结构如图所示,下列说法中不正确的是( )
A. 在晶体中,距最近的形成正八面体
B. 在晶体中,每个晶胞平均占有个
C. 在金刚石晶体中,碳原子与碳碳键个数的比为:
D. 该气态团簇分子的分子式为或
下列关于晶体的说法中,不正确的是( )
晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
含有金属阳离子的晶体一定是离子晶体
共价键可决定分子晶体的熔、沸点
的晶格能远比大,这是因为前者离子所带的电荷数多,离子半径小
晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
晶体尽可能采取紧密堆积方式,以使其变得比较稳定
干冰晶体中,一个分子周围有个分子紧邻.
A. B. C. D.
金属晶体密度大,原子配位数大,能充分利用空间的原因是( )
A. 金属原子价电子数少 B. 金属晶体中有自由电子
C. 金属原子的半径大 D. 金属键没有饱和性和方向性
如图是、两种不同物质的熔化曲线,下列说法中正确的是( )
是晶体 是非晶体 是晶体 是非晶体
A. B. C. D.
下列变化需克服相同类型作用力的是( )
A. 碘和干冰的升华 B. 硅和的熔化
C. 氯化氢和氯化钠的溶解 D. 溴和汞的气化
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位。阳离子位于此晶胞的中心,阴离子位于个顶点,该离子化合物中,阴、阳离子个数比是
A. B. C. D.
下面关于晶体网状结构的叙述正确的是( )
A. 最小的环上,有个原子和个原子
B. 最小的环上,和原子数之比为:
C. 最小的环上,有个原子和个原子
D. 存在四面体结构单元,处于中心,处于个顶角
美国国家实验室在高压条件下合成了原子型二氧化碳,其晶体结构类似于二氧化硅,下列对该晶体叙述错误的是( )
A. 该晶体中碳原子和氧原子的个数比为
B. 晶体的空间最小环共有个原子构成
C. 此晶体的熔点高于二氧化硅
D. 该品体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状结构
如图所示是晶体结构中具有代表性的最小重复单元晶胞的排列方式,其对应的化学式正确的是图中:,,( )
A. B. C. D.
金属的下列性质中和金属晶体无关的是
A. 良好的导电性 B. 反应中易失电子 C. 良好的延展性 D. 良好的导热性
二、双选题
下列特殊聚集状态中,不具有导电功能的是( )
A. 等离子体 B. 非晶体 C. 液晶 D. 金属纳米颗粒
在世纪年代末期,科学家发现并证明碳有新的单质形态存在。后来人们又相继得到了、、、等另外一些球碳分子。世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了碳元素单质的家庭。下列有关说法错误的是( )
A. 金刚石、、、管状碳和洋葱状碳都不能与发生加成反应
B. 已知石墨,金刚石,,则金刚石比石墨稳定
C. 晶体结构如图所示,每个分子周围与它最近且等距离的分子有个
D. 熔点比较:金刚石
下列对晶体结构和性质的认识错误的是( )
A. 纯碱和烧碱熔化时克服的化学键类型相同
B. 晶体和中,微粒间相互作用完全相同,晶体类型也相同
C. 石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
D. 金刚石和石墨的熔点都较高,是因为二者都为原子晶体
已知氯化铝易溶于苯和乙醚,其熔点为,则下列结论错误的是( )
A. 氯化铝是非电解质 B. 固体氯化铝是分子晶体
C. 可用电解熔融氯化铝的办法制取金属铝 D. 氯化铝为非极性分子
下列关系正确的是( )
A. 密度:苯
B. 同质量的物质燃烧耗 量:丙炔乙炔甲烷
C. 熔点:戊烷, 一二甲基戊烷, 一二甲基丁烷丙烷
D. 同物质的量物质燃烧耗 量:己烷环己烷苯
三、简答题
有机反应中常用镍作催化剂.某化工厂收集的镍催化剂中含、、,其余为和有机物.这些含镍废催化剂经乙醇洗涤后可按如图工艺流程回收镍:
已知:部分阳离子以氢氧化物形式完全沉淀时的如下:请回答下列问题:
沉淀物
滤液中存在的阴离子主要是 ______ .
硫酸浸取滤渣后,所得滤液中可能含有的金属离子是 ______ .
滤液中加入的目的是 ______ 操作的名称是 ______ .
含镍金属氢化物燃料电池是一种绿色环保电池,广泛应用于电动汽车,其中代表储氢合金,代表金属氢化物,电解质溶液可以是水溶液.它的充、放电反应为:;电池充电过程中阳极的电极反应式为 ______ ,放电时负极的电极反应式为 ______ .
一种储氢合金是由金属镧与镍形成的合金,其晶胞结构如图所示,晶胞中心有一个原子,其他原子,都在晶胞面上,该晶体的化学式为 ______ .
上述回收镍的过程中,使用含镍废催化剂,调时,回收过程中,第步操作镍的损失率为,第步骤的损失率为,则最终得到硫酸镍晶体的质量为 ______ 填计算式.
美国医学家证实了价铬离子是构成葡萄糖耐量因子的重要组成部分,能够增强胰岛素的作用。构成葡萄糖耐量因子和蛋白质的元素有、、、、、等。
的外围电子排布图为______。
分子的空间构型为______,是______ 分子填“极性”或“非极性”;离子中心原子的杂化方式为______。
的电子式为______,它的等电子体中属于分子的有______。
四种分子:、、、,键角由大到小的排列顺序是______填序号。
分子可以与结合生成,这个过程发生改变的是______
微粒的空间构型 原子的杂化类型 的键角 微粒的电子数
由碳元素形成的某种单质的片状和层状结构如图所示,由碳元素形成的某种晶体的晶胞结构如图所示,试回答:
在图中,碳原子所形成的六元环数、原子数、键数之比为______;
在图中,已知阿伏加德罗常数为,晶体密度为 ,则该晶体的棱长为______只列式,不计算。
铬、钛及其化合物在工业上有重要用途,回答下列问题:
基态原子价层电子的轨道表达式电子排布图为______。
氮化铬在超级电容器领域具有良好的应用前景,可由与尿素反应先得到配合物,然后在通有和混合气体的反应炉内热分解制得。尿素构成元素中电负性由大到小的顺序为______,中心碳原子的杂化类型为______;含有的化学键类型有______。
氮化铬的晶体结构类型与氯化钠的相同,氮化铬熔点比氯化钠的高,主要原因是______。
钙钛矿型的结构可看作氧化物超导相结构的基本单元。
图为立方钙钛矿结构的晶胞,晶胞边长为 处于晶胞的顶点,则处于______位置,处于______位置;与紧邻的个数为______,与间的最短距离为______。
在图中画出立方钙钛矿晶胞结构的另一种表示要求:处于晶胞的顶点;,, 所代表的原子种类与图相同。
铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题:
铁在元素周期表中的位置是______,基态铜原子的核外电子排布式为______.
配合物常温下呈液态,熔点为,沸点为,易溶于非极性溶剂,据此可判断晶体属于______填晶体类型.
写出的一种常见等电子体分子的结构式______,两者相比较沸点较高的为______填化学式中碳原子杂化轨道类型为______,、、三元素的第一电离能最大的为______用元素符号表示.
铜晶体中铜原子的堆积方式如图所示.
原子的价电子排布式为,铜与形成化合物的晶胞如图所示黑点代表铜原子.
该晶体的化学式为______.
已知铜和的电负性分别为和,则铜与形成的化合物属于______填“离子”、“共价”化合物.
已知该晶体的密度为,阿伏伽德罗常数为,已知该晶体中铜原子和原子之间的最短距离为体对角线的,则该晶体中铜原子和原子之间的最短距离为______只写计算式.
氮化硅耐高温、硬度大,可用石英与焦炭在的氮气中合成:
在一定条件下,向密闭容器中加入反应物,后达到平衡。
完成下列问题:
上述反应所涉及的属于第三周期的元素,其原子的最外层电子轨道表示式为______。其中一种元素的原子核外电子数与电子数相等,其原子的核外电子能量不同的有______种。
上述反应混合物中的极性分子是______,写出非极性分子的电子式______。分析用氮化硅制造轴承和发动机中耐热部件的原因是______。
该反应的平衡常数表达式为______。可以提高二氧化硅转化率的措施是______任写一条,该措施对平衡常数的影响为______填“增大”、“减小”或“保持不变”。
测得平衡时固体质量减少了,则用氮气表示的平均反应速率为______。
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
16.【答案】、、;、、;将氧化为、有利于分离;蒸发结晶;;;;
17.【答案】;
形;极性;
;;;
;
;
::;
18.【答案】;;;配位键、共价键、离子键;氮化铬的离子电荷数较多,晶格能较大;体心;棱心;;
19.【答案】第四周期第Ⅷ族;或;
分子晶体;
;;杂化;;
;共价;
20.【答案】 氮化硅是原子晶体、熔点高 升高温度 增大
第2页,共4页
第3页,共4页
题号 一 二 三 四 总分
得分
一、单选题
有关晶体的结构如图所示,下列说法中不正确的是( )
A. 在晶体中,距最近的形成正八面体
B. 在晶体中,每个晶胞平均占有个
C. 在金刚石晶体中,碳原子与碳碳键个数的比为:
D. 该气态团簇分子的分子式为或
下列关于晶体的说法中,不正确的是( )
晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
含有金属阳离子的晶体一定是离子晶体
共价键可决定分子晶体的熔、沸点
的晶格能远比大,这是因为前者离子所带的电荷数多,离子半径小
晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
晶体尽可能采取紧密堆积方式,以使其变得比较稳定
干冰晶体中,一个分子周围有个分子紧邻.
A. B. C. D.
金属晶体密度大,原子配位数大,能充分利用空间的原因是( )
A. 金属原子价电子数少 B. 金属晶体中有自由电子
C. 金属原子的半径大 D. 金属键没有饱和性和方向性
如图是、两种不同物质的熔化曲线,下列说法中正确的是( )
是晶体 是非晶体 是晶体 是非晶体
A. B. C. D.
下列变化需克服相同类型作用力的是( )
A. 碘和干冰的升华 B. 硅和的熔化
C. 氯化氢和氯化钠的溶解 D. 溴和汞的气化
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位。阳离子位于此晶胞的中心,阴离子位于个顶点,该离子化合物中,阴、阳离子个数比是
A. B. C. D.
下面关于晶体网状结构的叙述正确的是( )
A. 最小的环上,有个原子和个原子
B. 最小的环上,和原子数之比为:
C. 最小的环上,有个原子和个原子
D. 存在四面体结构单元,处于中心,处于个顶角
美国国家实验室在高压条件下合成了原子型二氧化碳,其晶体结构类似于二氧化硅,下列对该晶体叙述错误的是( )
A. 该晶体中碳原子和氧原子的个数比为
B. 晶体的空间最小环共有个原子构成
C. 此晶体的熔点高于二氧化硅
D. 该品体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状结构
如图所示是晶体结构中具有代表性的最小重复单元晶胞的排列方式,其对应的化学式正确的是图中:,,( )
A. B. C. D.
金属的下列性质中和金属晶体无关的是
A. 良好的导电性 B. 反应中易失电子 C. 良好的延展性 D. 良好的导热性
二、双选题
下列特殊聚集状态中,不具有导电功能的是( )
A. 等离子体 B. 非晶体 C. 液晶 D. 金属纳米颗粒
在世纪年代末期,科学家发现并证明碳有新的单质形态存在。后来人们又相继得到了、、、等另外一些球碳分子。世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了碳元素单质的家庭。下列有关说法错误的是( )
A. 金刚石、、、管状碳和洋葱状碳都不能与发生加成反应
B. 已知石墨,金刚石,,则金刚石比石墨稳定
C. 晶体结构如图所示,每个分子周围与它最近且等距离的分子有个
D. 熔点比较:金刚石
下列对晶体结构和性质的认识错误的是( )
A. 纯碱和烧碱熔化时克服的化学键类型相同
B. 晶体和中,微粒间相互作用完全相同,晶体类型也相同
C. 石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
D. 金刚石和石墨的熔点都较高,是因为二者都为原子晶体
已知氯化铝易溶于苯和乙醚,其熔点为,则下列结论错误的是( )
A. 氯化铝是非电解质 B. 固体氯化铝是分子晶体
C. 可用电解熔融氯化铝的办法制取金属铝 D. 氯化铝为非极性分子
下列关系正确的是( )
A. 密度:苯
B. 同质量的物质燃烧耗 量:丙炔乙炔甲烷
C. 熔点:戊烷, 一二甲基戊烷, 一二甲基丁烷丙烷
D. 同物质的量物质燃烧耗 量:己烷环己烷苯
三、简答题
有机反应中常用镍作催化剂.某化工厂收集的镍催化剂中含、、,其余为和有机物.这些含镍废催化剂经乙醇洗涤后可按如图工艺流程回收镍:
已知:部分阳离子以氢氧化物形式完全沉淀时的如下:请回答下列问题:
沉淀物
滤液中存在的阴离子主要是 ______ .
硫酸浸取滤渣后,所得滤液中可能含有的金属离子是 ______ .
滤液中加入的目的是 ______ 操作的名称是 ______ .
含镍金属氢化物燃料电池是一种绿色环保电池,广泛应用于电动汽车,其中代表储氢合金,代表金属氢化物,电解质溶液可以是水溶液.它的充、放电反应为:;电池充电过程中阳极的电极反应式为 ______ ,放电时负极的电极反应式为 ______ .
一种储氢合金是由金属镧与镍形成的合金,其晶胞结构如图所示,晶胞中心有一个原子,其他原子,都在晶胞面上,该晶体的化学式为 ______ .
上述回收镍的过程中,使用含镍废催化剂,调时,回收过程中,第步操作镍的损失率为,第步骤的损失率为,则最终得到硫酸镍晶体的质量为 ______ 填计算式.
美国医学家证实了价铬离子是构成葡萄糖耐量因子的重要组成部分,能够增强胰岛素的作用。构成葡萄糖耐量因子和蛋白质的元素有、、、、、等。
的外围电子排布图为______。
分子的空间构型为______,是______ 分子填“极性”或“非极性”;离子中心原子的杂化方式为______。
的电子式为______,它的等电子体中属于分子的有______。
四种分子:、、、,键角由大到小的排列顺序是______填序号。
分子可以与结合生成,这个过程发生改变的是______
微粒的空间构型 原子的杂化类型 的键角 微粒的电子数
由碳元素形成的某种单质的片状和层状结构如图所示,由碳元素形成的某种晶体的晶胞结构如图所示,试回答:
在图中,碳原子所形成的六元环数、原子数、键数之比为______;
在图中,已知阿伏加德罗常数为,晶体密度为 ,则该晶体的棱长为______只列式,不计算。
铬、钛及其化合物在工业上有重要用途,回答下列问题:
基态原子价层电子的轨道表达式电子排布图为______。
氮化铬在超级电容器领域具有良好的应用前景,可由与尿素反应先得到配合物,然后在通有和混合气体的反应炉内热分解制得。尿素构成元素中电负性由大到小的顺序为______,中心碳原子的杂化类型为______;含有的化学键类型有______。
氮化铬的晶体结构类型与氯化钠的相同,氮化铬熔点比氯化钠的高,主要原因是______。
钙钛矿型的结构可看作氧化物超导相结构的基本单元。
图为立方钙钛矿结构的晶胞,晶胞边长为 处于晶胞的顶点,则处于______位置,处于______位置;与紧邻的个数为______,与间的最短距离为______。
在图中画出立方钙钛矿晶胞结构的另一种表示要求:处于晶胞的顶点;,, 所代表的原子种类与图相同。
铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题:
铁在元素周期表中的位置是______,基态铜原子的核外电子排布式为______.
配合物常温下呈液态,熔点为,沸点为,易溶于非极性溶剂,据此可判断晶体属于______填晶体类型.
写出的一种常见等电子体分子的结构式______,两者相比较沸点较高的为______填化学式中碳原子杂化轨道类型为______,、、三元素的第一电离能最大的为______用元素符号表示.
铜晶体中铜原子的堆积方式如图所示.
原子的价电子排布式为,铜与形成化合物的晶胞如图所示黑点代表铜原子.
该晶体的化学式为______.
已知铜和的电负性分别为和,则铜与形成的化合物属于______填“离子”、“共价”化合物.
已知该晶体的密度为,阿伏伽德罗常数为,已知该晶体中铜原子和原子之间的最短距离为体对角线的,则该晶体中铜原子和原子之间的最短距离为______只写计算式.
氮化硅耐高温、硬度大,可用石英与焦炭在的氮气中合成:
在一定条件下,向密闭容器中加入反应物,后达到平衡。
完成下列问题:
上述反应所涉及的属于第三周期的元素,其原子的最外层电子轨道表示式为______。其中一种元素的原子核外电子数与电子数相等,其原子的核外电子能量不同的有______种。
上述反应混合物中的极性分子是______,写出非极性分子的电子式______。分析用氮化硅制造轴承和发动机中耐热部件的原因是______。
该反应的平衡常数表达式为______。可以提高二氧化硅转化率的措施是______任写一条,该措施对平衡常数的影响为______填“增大”、“减小”或“保持不变”。
测得平衡时固体质量减少了,则用氮气表示的平均反应速率为______。
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
16.【答案】、、;、、;将氧化为、有利于分离;蒸发结晶;;;;
17.【答案】;
形;极性;
;;;
;
;
::;
18.【答案】;;;配位键、共价键、离子键;氮化铬的离子电荷数较多,晶格能较大;体心;棱心;;
19.【答案】第四周期第Ⅷ族;或;
分子晶体;
;;杂化;;
;共价;
20.【答案】 氮化硅是原子晶体、熔点高 升高温度 增大
第2页,共4页
第3页,共4页
