鲁科版 高中化学 必修第一册 第1章 第3节 第3课时 物质的量浓度 课件(75张ppt)
文档属性
| 名称 | 鲁科版 高中化学 必修第一册 第1章 第3节 第3课时 物质的量浓度 课件(75张ppt) |  | |
| 格式 | ppt | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-07 18:10:00 | ||
图片预览









文档简介
(共75张PPT)
第3课时 物质的量浓度
课前自主学习
学习任务一 物质的量浓度
任务驱动:
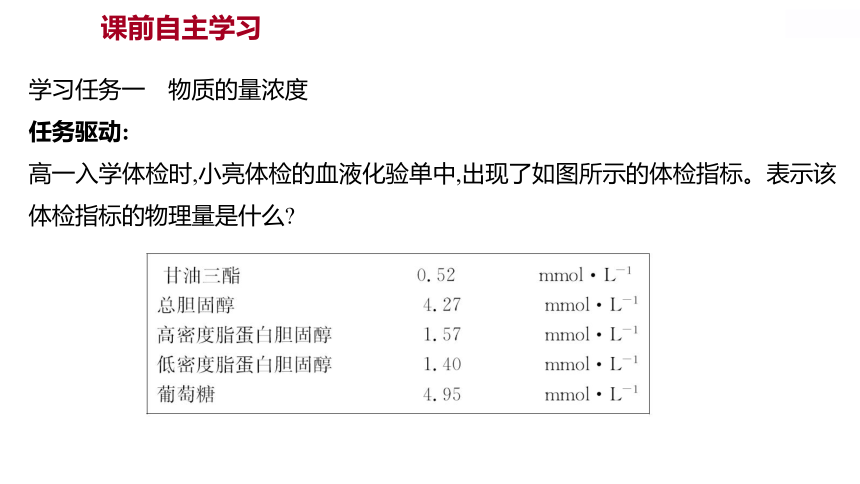
高一入学体检时,小亮体检的血液化验单中,出现了如图所示的体检指标。表示该体检指标的物理量是什么
1.概念:以_________溶液中所含溶质B的_________来表示溶液组成的物理量,
叫溶质B的物质的量浓度。
2.符号及单位:符号为__,单位为________或_________。
3.表达式:_________。
单位体积
物质的量
cB
mol·L-1
mol·m-3
【想一想】1 L溶液里含有20 g NaOH,则NaOH溶液的物质的量浓度为多少
学习任务二 一定物质的量浓度的溶液的配制
任务驱动:
初中我们学过一定溶质的质量分数溶液配制过程,那么一定物质的量浓度的溶液是怎么配制的呢
1.主要仪器
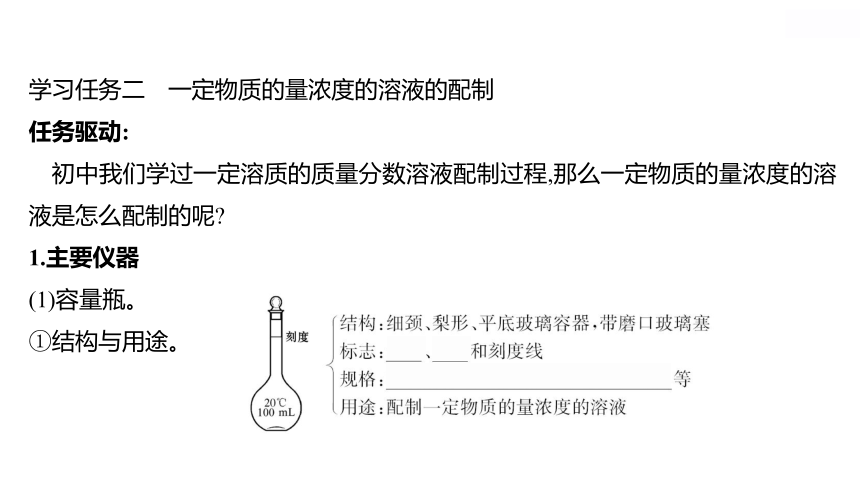
(1)容量瓶。
①结构与用途。
②使用注意事项。
a.使用前要检查瓶塞是否漏水。
b.定容时要使液体的_______与刻度线_____。
c.容量瓶的使用“六忌”:一忌用容量瓶溶解固体;二忌用容量瓶稀释浓溶液;三忌把
容量瓶加热;四忌把容量瓶当作反应容器;五忌用容量瓶长期存放溶液;六忌瓶塞
互换。
(2)其他仪器。
量筒、_____________________________________等。
凹液面
相切
托盘天平、烧杯、玻璃棒、胶头滴管
2.配制过程:以配制100 mL 0.4 mol·L-1 NaCl溶液为例。
【做一做】(1)2 mol·L-1的NaCl溶液1 000 mL,含溶质NaCl的物质的量为_____。
(2)已知某硫酸钠溶液的物质的量浓度为1 mol·L-1,该溶液中含硫酸钠的物质的量
为3 mol,则该溶液的体积为___。
(3)将342 g C12H22O11(蔗糖)溶解在1 L水中,所得溶液中溶质的物质的量浓度是否
为1 mol·L-1 ___。
(4)从1 L 1 mol·L-1的NaNO3溶液中取出100 mL,取出的NaNO3溶液的物质的量浓
度是________。
2 mol
3 L
否
1 mol·L-1
课堂合作探究
浓度变化 引起误差的可能原因
偏高 砝码沾有其他物质或生锈
用量筒量取已计算出体积的浓溶液时仰视读数
用水洗涤量筒
定容时俯视刻度线
用标准液润洗容量瓶
偏低 称量药品时,“左码右物”(需用到游码时)
转移时有少量液体洒在容量瓶外
未洗涤烧杯和玻璃棒
定容时仰视刻度线
在敞口容器中称量易潮解的物质
课堂素养达标
第3课时 物质的量浓度
课前自主学习
学习任务一 物质的量浓度
任务驱动:
高一入学体检时,小亮体检的血液化验单中,出现了如图所示的体检指标。表示该体检指标的物理量是什么
1.概念:以_________溶液中所含溶质B的_________来表示溶液组成的物理量,
叫溶质B的物质的量浓度。
2.符号及单位:符号为__,单位为________或_________。
3.表达式:_________。
单位体积
物质的量
cB
mol·L-1
mol·m-3
【想一想】1 L溶液里含有20 g NaOH,则NaOH溶液的物质的量浓度为多少
学习任务二 一定物质的量浓度的溶液的配制
任务驱动:
初中我们学过一定溶质的质量分数溶液配制过程,那么一定物质的量浓度的溶液是怎么配制的呢
1.主要仪器
(1)容量瓶。
①结构与用途。
②使用注意事项。
a.使用前要检查瓶塞是否漏水。
b.定容时要使液体的_______与刻度线_____。
c.容量瓶的使用“六忌”:一忌用容量瓶溶解固体;二忌用容量瓶稀释浓溶液;三忌把
容量瓶加热;四忌把容量瓶当作反应容器;五忌用容量瓶长期存放溶液;六忌瓶塞
互换。
(2)其他仪器。
量筒、_____________________________________等。
凹液面
相切
托盘天平、烧杯、玻璃棒、胶头滴管
2.配制过程:以配制100 mL 0.4 mol·L-1 NaCl溶液为例。
【做一做】(1)2 mol·L-1的NaCl溶液1 000 mL,含溶质NaCl的物质的量为_____。
(2)已知某硫酸钠溶液的物质的量浓度为1 mol·L-1,该溶液中含硫酸钠的物质的量
为3 mol,则该溶液的体积为___。
(3)将342 g C12H22O11(蔗糖)溶解在1 L水中,所得溶液中溶质的物质的量浓度是否
为1 mol·L-1 ___。
(4)从1 L 1 mol·L-1的NaNO3溶液中取出100 mL,取出的NaNO3溶液的物质的量浓
度是________。
2 mol
3 L
否
1 mol·L-1
课堂合作探究
浓度变化 引起误差的可能原因
偏高 砝码沾有其他物质或生锈
用量筒量取已计算出体积的浓溶液时仰视读数
用水洗涤量筒
定容时俯视刻度线
用标准液润洗容量瓶
偏低 称量药品时,“左码右物”(需用到游码时)
转移时有少量液体洒在容量瓶外
未洗涤烧杯和玻璃棒
定容时仰视刻度线
在敞口容器中称量易潮解的物质
课堂素养达标
