1.1.1原子结构 课件 2022-2023学年高一化学鲁科版(2019)必修第二册(34张ppt)
文档属性
| 名称 | 1.1.1原子结构 课件 2022-2023学年高一化学鲁科版(2019)必修第二册(34张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-11 13:34:14 | ||
图片预览










文档简介
(共34张PPT)
第1章 原子结构 元素周期律
第1节 原子结构与元素性质
第1课时 原子结构
【思考】(1)你知道考古学家是根据什么进一步推断一些出土文物和化石的年代的吗?
(2)你知道14C与12C有什么异同吗?
人类的发展经历了漫长的历史时期,考古学家通过测定过去材料的放射性元素14C的含量,可以推断生物死后经过的年代。
1.认识原子核的结构。
2.知道质量数和 X 的含义,掌握构成原子的各微粒间的关系。
3.知道元素、核素、同位素的含义。
1.能从元素和原子水平上认识物质的组成和结构。(宏观辨识与微观探析)
2.具有证据意识,能基于证据对物质组成、结构及其变化提出可能的假设,通过分析推理加以证实或证伪。(证据推理与模型认知)
A
Z
体会课堂探究的乐趣,
汲取新知识的营养,
让我们一起 吧!
进
走
课
堂
科学史话:原子结构模型的演变
1803年道尔顿模型
原子是构成物质的基本粒子,是坚实的、不可再分的实心球。
1904年汤姆孙原子模型
原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。
1911年卢瑟福原子模型
在原子的中心有一个带正电的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。
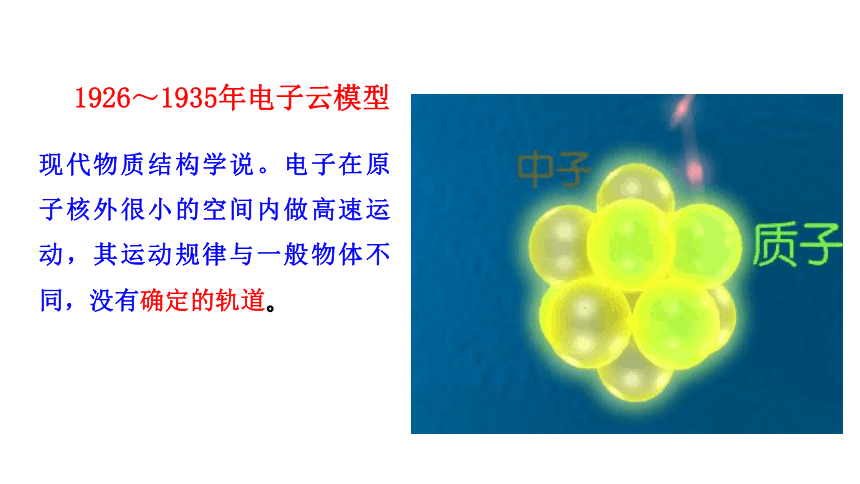
1926~1935年电子云模型
现代物质结构学说。电子在原子核外很小的空间内做高速运动,其运动规律与一般物体不同,没有确定的轨道。
1.原子是构成物质的一种微粒。
原子核
3.原子
核外电子
质子
中子
2.原子是化学变化中的最小微粒。
【知识回顾】
一、原子结构
一个质子带一个单位正电荷
一个电子带一个单位负电荷
中子不带电荷
原子
原子核
核外电子:
质子:
中子:
1.原子及构成微粒
1.原子核带电吗?
提示:原子核中的质子带正电,中子不带电,因此原子核带正电。
2.原子的相对原子质量和原子的质量是同一个概念吗?
提示:不是,原子的相对原子质量是原子的质量与12C原子质量的1/12的比值,因此两者不同。
【思考与交流】
微粒 电子 质子 中子
相对质量 0.000 548 4 1.007 1.008
3.下表是原子中微粒的相对质量。
根据上表分析原子的质量集中在原子的哪一部分?
提示:原子的质量集中在原子核上,原子的质量大体上等于质子和中子的质量之和。
【思考与交流】
(3)阴离子:质子数 < 核外电子数
质子数 = 核外电子数 - 电荷数
2.电性关系
(1)原子:质子数 = 核电荷数 = 核外电子数
(2)阳离子:质子数 > 核外电子数
质子数 = 核外电子数 + 电荷数
3.质量数
原子核中质子数和中子数之和
A
A =Z + N
公式
定义
质
量
数
符号
中子数
质子数
3.原子的表示方法
X
A
Z
质子数
质量数
元素符号
中子数=质量数-质子数
核电荷数=质子数=核外电子数
如:
提示:表示质子数为17 ,质量数为35的氯原子。
1. 表示的含义是什么?
2.原子的相对原子质量和原子的质量数相同吗?
提示:不同,质量数和原子的相对原子质量是不同的,质量数一定是整数,而相对原子质量是某一原子的质量与12C原子质量的1/12的比值,一般不是整数。
【思考与交流】
3.原子符号 中各个字母表示什么含义?
X离子所带的电荷数
一个分子中所含X原子
的个数
X原子的质量数
X原子的质子数
X元素的化合价
提示:
【思考与交流】
二者是同种元素吗?是同种原子吗?
【提示】质子数相同、中子数不同。
是同种元素,不是同种原子。
6 C
12
6 C
13
在结构上有什么区别?
和
结合原子的表示方法和元素的概念,思考下面
的问题:
【想一想】
新华网曾报道,加拿大开发出生产医用放射性同位素 Tc 的简单方法。下列关于 Tc的叙述正确的是( )
A.原子序数是99 B.核外电子数是43
C.中子数是99 D.质量数是43
99
43
99
43
【及时巩固】
B
质子数相同而中子数不同
的同一种元素的不同核素互
为同位素。
具有一定数目质子和一定
数目中子的一种原子。
同位素
核 素
二、认识核素、同位素
1.定义:
(1)同一种元素的各种同位素的化学性质几乎完全相同,物理性质不同。
2.同位素的特征
(2)在天然存在的某种元素里,各种同位素原子所占的百分数一般是不变的。
3.元素、核素、同位素之间的关系
具有相同质子数的同一类原子的总称,一种元素可以有多种核素。
具有一定数目质子和一定数目中子的一种原子。
质子数相同而中子数不同的同一种元素的不同核素互为同位素。
元素
核素1
核素n
同位素
…
4.原子结构中各微粒之间的关系:
原子核
质子
中子
核电荷数
元素
种类
质子数
决定
决定
与质子数共同决定
原子种类
决定
近似相对原子质量
质量数
5.重要的核素:
(1)用以制造氢弹的是 、 ;
(2)核反应堆的燃料是 ;
(3)考古时用于测定文物年代的是 ;
(4)用以同位素示踪的是 P。
1H
2
1H
3
6C
14
15
32
1.构成原子的基本微粒是质子、中子和电子,那么一个原子中,是否都存在这三种微粒?
2.质子数相同,中子数不同的原子是同种元素的原子吗?
提示:属于同种元素,但不是同种原子。
【思考与交流】
不是,如 中无中子。
1H
1
提示:
3.因为 的质量数是35,因此氯元素的相对原子质量约为35。
提示:不对,通常所说的元素的相对原子质量,是指该元素中各核素的平均相对原子质量,而不是指该元素的某种核素的质量数。
17Cl
35
4.互为同位素的原子有何异同点?
质子数、核外电子数相同
化学性质相同
相同点
中子数、质量数不同
物理性质不同
不同点
【思考与交流】
提示:
1.“三同”的区别与联系
同分异构体 同素异形体 同位素
概念
对象
化学
性质
实例
分子式相同,结构
不同的化合物之间
互为同分异构体
同种元素形成结构
不同的单质之间互
为同素异形体
质子数相同而中子
数不同的同一元素
的不同核素互为
同位素
一般为有机化合物之间
单质之间
原子之间
可能相似也可能不同
相似,一定条件下可以相互转变
几乎完全相同
CH3COOH与HCOOCH3
金刚石与石墨、C60;
红磷与白磷;O2与O3
1H
1
1H
2
与
【拓展延伸】
宏观辨识与微观探析
2.核素的相对原子质量与元素的相对原子质量的比较
核素的相对原子质量 元素的相对原子质量
概念 该核素原子的真实质量与12C原子质量的1/12相比所得的比值 按该元素所含天然核素原子所占的一定百分比算出来的平均值
计算方法 核素的相对原子质量=
元素的相对原子质量= M1×a%+ M2×b% +……其中M1、M2……为各同位素的相对原子质量,a% 、b%……为各同位素的原子个数百分比
近似值 数值等于核素的质量数 元素的近似相对原子质量= A1×a%+ A2×b% +……其中,A1、A2 ……为各同位素的质量数
镁有三种天然同位素:24Mg、25Mg、26Mg,其中24Mg
原子占镁元素的原子百分数为78.70%,又知镁的相
对原子质量是24.325,则26Mg在自然界镁元素中的
原子百分比是________。
【提示】设26Mg的原子百分含量为x,则:
24×78.70%+25(100%-78.70%-x)+26x=24.325
x=0.112=11.2%。
【例题】
11.2%
电子
中子
原子的相对原子质量
元素的相对原子质量
同位素
核素
元素
占有体积关系
电性关系
质量关系
数量关系
电子数决定元素
的化学性质
中子数决定同一
元素的不同核素
质子数决定
元素种类
质子
构成微粒
的关系
构成
原
子
结
构
1.美国科学家将两种元素铅和氢的原子核对撞,获
得了一种质子数为118,中子数为175的超重元素,
该元素原子核内的中子数与核外电子数之差是( ) A.57 B.47
C.61 D.293
A
2.下列关于原子的几种描述中不正确的是( )
A.18O与19F具有相同的中子数
B.16O与17O具有相同的电子数
C.12C与13C具有相同的质量数
D.15N与14N具有相同的质子数
C
3.“玉兔”号月球车用作为 Pu热源材料。下列关于 Pu的说法正确的是( )
A. Pu与 U互为同位素
B. Pu与 Pu互为同素异形体
C. Pu与 U具有完全相同的化学性质
D. Pu与 Pu具有相同的最外层电子数
D
4.杜布纳联合核研究所使用粒子回旋加速器,用
轰击 (锫)生成 和 ,Up就是科学家一直寻
找的第117号元素。下列有关说法正确的是( )
A. 表示一种核素,其中子数为97
B. 和 互为同位素
C. 轰击 (锫)生成 和 是化学变化
D. 、 、 、 属于4种元素
B
5.原子的质量主要由原子核决定。已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为( )
A.A-X B.A-X-n C.A-X+n D.A+X-n
D
第1章 原子结构 元素周期律
第1节 原子结构与元素性质
第1课时 原子结构
【思考】(1)你知道考古学家是根据什么进一步推断一些出土文物和化石的年代的吗?
(2)你知道14C与12C有什么异同吗?
人类的发展经历了漫长的历史时期,考古学家通过测定过去材料的放射性元素14C的含量,可以推断生物死后经过的年代。
1.认识原子核的结构。
2.知道质量数和 X 的含义,掌握构成原子的各微粒间的关系。
3.知道元素、核素、同位素的含义。
1.能从元素和原子水平上认识物质的组成和结构。(宏观辨识与微观探析)
2.具有证据意识,能基于证据对物质组成、结构及其变化提出可能的假设,通过分析推理加以证实或证伪。(证据推理与模型认知)
A
Z
体会课堂探究的乐趣,
汲取新知识的营养,
让我们一起 吧!
进
走
课
堂
科学史话:原子结构模型的演变
1803年道尔顿模型
原子是构成物质的基本粒子,是坚实的、不可再分的实心球。
1904年汤姆孙原子模型
原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。
1911年卢瑟福原子模型
在原子的中心有一个带正电的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。
1926~1935年电子云模型
现代物质结构学说。电子在原子核外很小的空间内做高速运动,其运动规律与一般物体不同,没有确定的轨道。
1.原子是构成物质的一种微粒。
原子核
3.原子
核外电子
质子
中子
2.原子是化学变化中的最小微粒。
【知识回顾】
一、原子结构
一个质子带一个单位正电荷
一个电子带一个单位负电荷
中子不带电荷
原子
原子核
核外电子:
质子:
中子:
1.原子及构成微粒
1.原子核带电吗?
提示:原子核中的质子带正电,中子不带电,因此原子核带正电。
2.原子的相对原子质量和原子的质量是同一个概念吗?
提示:不是,原子的相对原子质量是原子的质量与12C原子质量的1/12的比值,因此两者不同。
【思考与交流】
微粒 电子 质子 中子
相对质量 0.000 548 4 1.007 1.008
3.下表是原子中微粒的相对质量。
根据上表分析原子的质量集中在原子的哪一部分?
提示:原子的质量集中在原子核上,原子的质量大体上等于质子和中子的质量之和。
【思考与交流】
(3)阴离子:质子数 < 核外电子数
质子数 = 核外电子数 - 电荷数
2.电性关系
(1)原子:质子数 = 核电荷数 = 核外电子数
(2)阳离子:质子数 > 核外电子数
质子数 = 核外电子数 + 电荷数
3.质量数
原子核中质子数和中子数之和
A
A =Z + N
公式
定义
质
量
数
符号
中子数
质子数
3.原子的表示方法
X
A
Z
质子数
质量数
元素符号
中子数=质量数-质子数
核电荷数=质子数=核外电子数
如:
提示:表示质子数为17 ,质量数为35的氯原子。
1. 表示的含义是什么?
2.原子的相对原子质量和原子的质量数相同吗?
提示:不同,质量数和原子的相对原子质量是不同的,质量数一定是整数,而相对原子质量是某一原子的质量与12C原子质量的1/12的比值,一般不是整数。
【思考与交流】
3.原子符号 中各个字母表示什么含义?
X离子所带的电荷数
一个分子中所含X原子
的个数
X原子的质量数
X原子的质子数
X元素的化合价
提示:
【思考与交流】
二者是同种元素吗?是同种原子吗?
【提示】质子数相同、中子数不同。
是同种元素,不是同种原子。
6 C
12
6 C
13
在结构上有什么区别?
和
结合原子的表示方法和元素的概念,思考下面
的问题:
【想一想】
新华网曾报道,加拿大开发出生产医用放射性同位素 Tc 的简单方法。下列关于 Tc的叙述正确的是( )
A.原子序数是99 B.核外电子数是43
C.中子数是99 D.质量数是43
99
43
99
43
【及时巩固】
B
质子数相同而中子数不同
的同一种元素的不同核素互
为同位素。
具有一定数目质子和一定
数目中子的一种原子。
同位素
核 素
二、认识核素、同位素
1.定义:
(1)同一种元素的各种同位素的化学性质几乎完全相同,物理性质不同。
2.同位素的特征
(2)在天然存在的某种元素里,各种同位素原子所占的百分数一般是不变的。
3.元素、核素、同位素之间的关系
具有相同质子数的同一类原子的总称,一种元素可以有多种核素。
具有一定数目质子和一定数目中子的一种原子。
质子数相同而中子数不同的同一种元素的不同核素互为同位素。
元素
核素1
核素n
同位素
…
4.原子结构中各微粒之间的关系:
原子核
质子
中子
核电荷数
元素
种类
质子数
决定
决定
与质子数共同决定
原子种类
决定
近似相对原子质量
质量数
5.重要的核素:
(1)用以制造氢弹的是 、 ;
(2)核反应堆的燃料是 ;
(3)考古时用于测定文物年代的是 ;
(4)用以同位素示踪的是 P。
1H
2
1H
3
6C
14
15
32
1.构成原子的基本微粒是质子、中子和电子,那么一个原子中,是否都存在这三种微粒?
2.质子数相同,中子数不同的原子是同种元素的原子吗?
提示:属于同种元素,但不是同种原子。
【思考与交流】
不是,如 中无中子。
1H
1
提示:
3.因为 的质量数是35,因此氯元素的相对原子质量约为35。
提示:不对,通常所说的元素的相对原子质量,是指该元素中各核素的平均相对原子质量,而不是指该元素的某种核素的质量数。
17Cl
35
4.互为同位素的原子有何异同点?
质子数、核外电子数相同
化学性质相同
相同点
中子数、质量数不同
物理性质不同
不同点
【思考与交流】
提示:
1.“三同”的区别与联系
同分异构体 同素异形体 同位素
概念
对象
化学
性质
实例
分子式相同,结构
不同的化合物之间
互为同分异构体
同种元素形成结构
不同的单质之间互
为同素异形体
质子数相同而中子
数不同的同一元素
的不同核素互为
同位素
一般为有机化合物之间
单质之间
原子之间
可能相似也可能不同
相似,一定条件下可以相互转变
几乎完全相同
CH3COOH与HCOOCH3
金刚石与石墨、C60;
红磷与白磷;O2与O3
1H
1
1H
2
与
【拓展延伸】
宏观辨识与微观探析
2.核素的相对原子质量与元素的相对原子质量的比较
核素的相对原子质量 元素的相对原子质量
概念 该核素原子的真实质量与12C原子质量的1/12相比所得的比值 按该元素所含天然核素原子所占的一定百分比算出来的平均值
计算方法 核素的相对原子质量=
元素的相对原子质量= M1×a%+ M2×b% +……其中M1、M2……为各同位素的相对原子质量,a% 、b%……为各同位素的原子个数百分比
近似值 数值等于核素的质量数 元素的近似相对原子质量= A1×a%+ A2×b% +……其中,A1、A2 ……为各同位素的质量数
镁有三种天然同位素:24Mg、25Mg、26Mg,其中24Mg
原子占镁元素的原子百分数为78.70%,又知镁的相
对原子质量是24.325,则26Mg在自然界镁元素中的
原子百分比是________。
【提示】设26Mg的原子百分含量为x,则:
24×78.70%+25(100%-78.70%-x)+26x=24.325
x=0.112=11.2%。
【例题】
11.2%
电子
中子
原子的相对原子质量
元素的相对原子质量
同位素
核素
元素
占有体积关系
电性关系
质量关系
数量关系
电子数决定元素
的化学性质
中子数决定同一
元素的不同核素
质子数决定
元素种类
质子
构成微粒
的关系
构成
原
子
结
构
1.美国科学家将两种元素铅和氢的原子核对撞,获
得了一种质子数为118,中子数为175的超重元素,
该元素原子核内的中子数与核外电子数之差是( ) A.57 B.47
C.61 D.293
A
2.下列关于原子的几种描述中不正确的是( )
A.18O与19F具有相同的中子数
B.16O与17O具有相同的电子数
C.12C与13C具有相同的质量数
D.15N与14N具有相同的质子数
C
3.“玉兔”号月球车用作为 Pu热源材料。下列关于 Pu的说法正确的是( )
A. Pu与 U互为同位素
B. Pu与 Pu互为同素异形体
C. Pu与 U具有完全相同的化学性质
D. Pu与 Pu具有相同的最外层电子数
D
4.杜布纳联合核研究所使用粒子回旋加速器,用
轰击 (锫)生成 和 ,Up就是科学家一直寻
找的第117号元素。下列有关说法正确的是( )
A. 表示一种核素,其中子数为97
B. 和 互为同位素
C. 轰击 (锫)生成 和 是化学变化
D. 、 、 、 属于4种元素
B
5.原子的质量主要由原子核决定。已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为( )
A.A-X B.A-X-n C.A-X+n D.A+X-n
D
