3.2.2 碳酸钠 碳酸氢钠 课件(22张) 2022-2023 苏教版 高中化学 必修第一册
文档属性
| 名称 | 3.2.2 碳酸钠 碳酸氢钠 课件(22张) 2022-2023 苏教版 高中化学 必修第一册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-12 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
第二单元 金属钠及钠的化合物
第2课时 碳酸钠 碳酸氢钠
“苏打水”为什么用的是“小苏打”,而不是“苏打”?
小苏打
苏打水
1.了解碳酸钠和碳酸氢钠的性质和重要用途。
2.掌握碳酸钠和碳酸氢钠的性质和鉴别方法。
1.通过观察、实验等方法对比研究解碳酸钠、碳酸氢钠的性质,并知道它们在生产生活中的用途。(宏观辨识与微观探析)
2.通过实验探究碳酸钠、碳酸氢钠的化学性质,初步形成基于物质构成对物质性质进行预测和检验的认识模型。(证据推理与模型认知)
3.通过体验实验探究和问题讨论的过程,了解实验研究化学物质的一般方法,初步形成分析推理、综合归纳的能力。(科学探究与创新意识)
4.通过对侯氏制碱法的学习,培养科学态度与社会责任核心素养。(科学态度与社会责任)
体会课堂探究的乐趣,
汲取新知识的营养,
让我们一起 吧!
进
走
课
堂
【试一试】你能填出表格中的内容吗?
Na2CO3
NaHCO3
白色、固态
白色、固态
纯碱、苏打
小苏打
碳酸钠和碳酸氢钠
俗名
颜色、状态
化学式
物 质
碳酸钠
碳酸氢钠
【拓展延伸】化学上的“苏氏三兄弟”:大苏打Na2S2O3、苏打Na2CO3、小苏打NaHCO3。
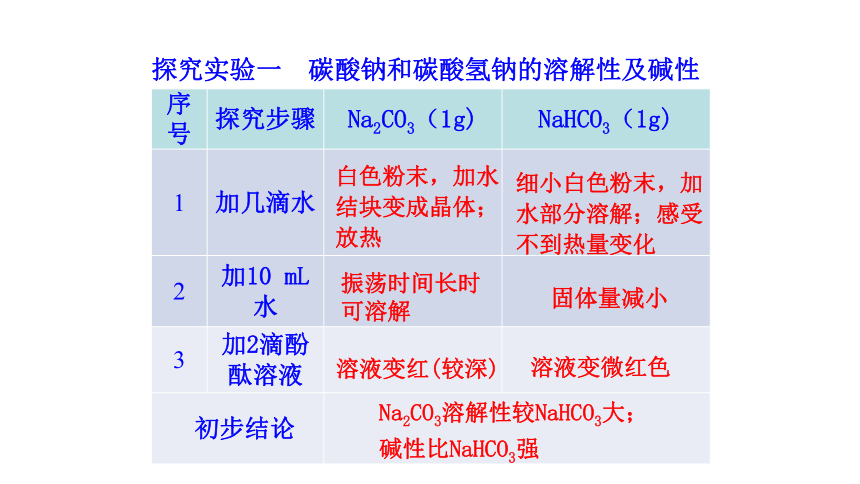
探究实验一 碳酸钠和碳酸氢钠的溶解性及碱性
序号 探究步骤 Na2CO3(1g) NaHCO3(1g)
1 加几滴水
2 加10 mL水
3 加2滴酚
酞溶液
初步结论
白色粉末,加水
结块变成晶体;
放热
细小白色粉末,加
水部分溶解;感受
不到热量变化
振荡时间长时
可溶解
固体量减小
溶液变红(较深)
溶液变微红色
Na2CO3溶解性较NaHCO3大;
碱性比NaHCO3强
【理论分析】
你能根据知识背景进行科学假设,猜测碳酸钠与碳酸氢钠的热稳定性差异吗?
知识背景:
1.碳酸钙在高温下才分解;
2.碳酸氢钙受热分解生成碳酸钙、二氧化碳和水。
探究实验二 碳酸钠和碳酸氢钠的热稳定性
【验证猜想】
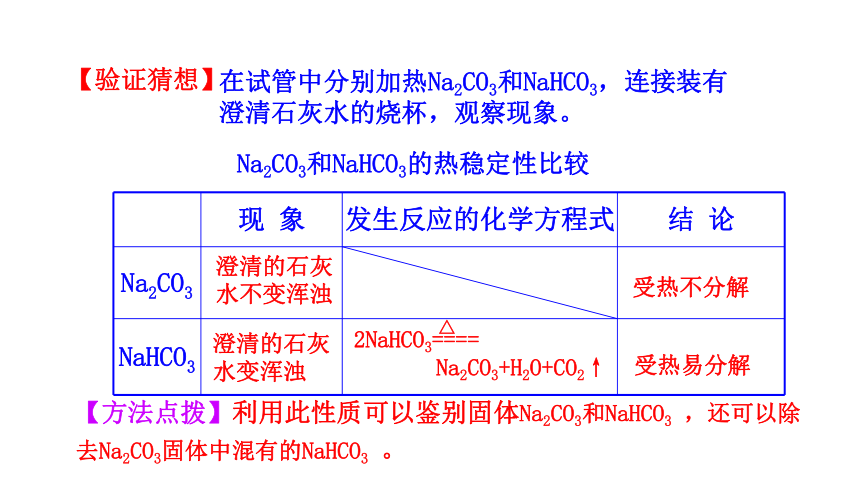
现 象 发生反应的化学方程式 结 论
Na2CO3
NaHCO3
△
2NaHCO3====
Na2CO3+H2O+CO2↑
澄清的石灰
水不变浑浊
澄清的石灰
水变浑浊
受热不分解
受热易分解
在试管中分别加热Na2CO3和NaHCO3,连接装有澄清石灰水的烧杯,观察现象。
Na2CO3和NaHCO3的热稳定性比较
【方法点拨】利用此性质可以鉴别固体Na2CO3和NaHCO3 ,还可以除去Na2CO3固体中混有的NaHCO3 。
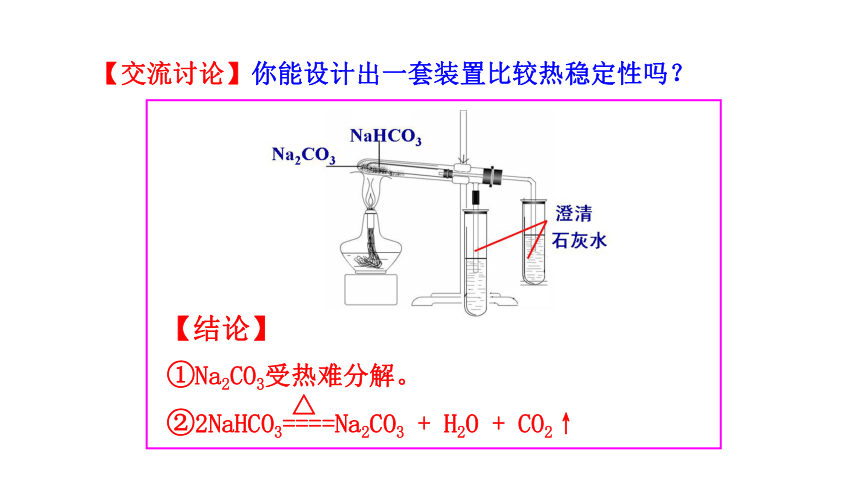
【结论】
①Na2CO3受热难分解。
②2NaHCO3====Na2CO3 + H2O + CO2↑
△
【交流讨论】你能设计出一套装置比较热稳定性吗?
现象:
结论:
两只气球都鼓起来,但是装碳酸氢钠的气球鼓起得更快
都能和盐酸反应产生二氧化碳,但是碳酸氢钠和盐酸反应更快
探究实验三 Na2CO3和NaHCO3与盐酸的反应
在两只试管中分别加入足量且等物质
的量浓度的稀盐酸,将两只各装有等
量Na2CO3和NaHCO3固体的小气球分
别套在两只试管口,同时把固体粉末
抖入试管,观察现象。
为什么NaHCO3与酸反应比Na2CO3剧烈呢?
CO32-
H+
HCO3-
H+
CO2 ↑ + H2O
H2CO3
【深度分析】
提示:
试写出Na2CO3和NaHCO3与盐酸反应的方程式。
Na2CO3与盐酸反应的方程式:
Na2CO3 + HCl ==== NaCl + NaHCO3
NaHCO3 + HCl ==== NaCl + H2O + CO2↑
总反应方程式:
Na2CO3 + 2HCl ==== 2NaCl + H2O + CO2↑
NaHCO3与盐酸反应的方程式:
NaHCO3 + HCl ==== NaCl + H2O + CO2↑
Na2CO3、NaHCO3均可与胃酸(盐酸)反应,为何不选用Na2CO3作抗酸药 ?
原因:碱性 Na2CO3>NaHCO3
注意:
胃溃疡患者不能过多服用碳酸氢钠治疗胃酸,产生的CO2会导致胃穿孔!
【学以致用】
向盐酸中逐滴加入碳酸钠溶液与向碳酸钠溶液中逐滴加入盐酸现象一样吗?
向碳酸钠溶液中滴加盐酸
开始没有明显现象,后来从溶液里产生无色无味的气体
溶液里立即产生无色无味的气体
向盐酸中慢慢滴加碳酸钠溶液
CO32-+H+====HCO3-
HCO3-+H+====H2O+CO2↑
Na2CO3+2HCl====2NaCl+CO2↑+H2O
【拓展提高】
【实验】向试管中加1mL 0.1mol/L NaHCO3溶液,然后加1mL 0.01mol/L BaCl2溶液, 观察现象。再向其中逐滴滴加NaOH溶液,振荡,观察现象。
【结论】
NaHCO3+NaOH====Na2CO3 +H2O
Na2CO3+BaCl2====BaCO3↓+2NaCl
NaHCO3+Ba(OH)2
BaCO3↓
【交流与讨论】
得到的白色沉淀是什么?
沉淀是如何形成的?
友情提醒:
①小试管中1mL溶液大约高1cm。
②用指定的胶头滴管取用溶液。
探究实验四 碳酸氢钠与盐、碱反应
你能想出用哪些方法鉴别Na2CO3与NaHCO3固体?
小组内交流,然后与同学分享。
1.加热,观察能否产生使澄清石灰水变浑浊的气体。
2.等质量固体加等体积水观察溶解情况。
3.配制饱和溶液测定pH。
4.固体与盐酸反应观察剧烈程度。
……
【交流讨论】
碳酸钠的用途
碳酸氢钠的用途
疏松剂
胃药
灭火剂
NaHCO3常作为食品制作过程中的膨松剂、发酵剂。
决定于
类别
转
化
转
化
碳酸钠
碳酸氢钠
物理性质
化学性质
白色粉末状物质
盐类
与酸反应
与碱反应
与盐反应
物理性质
化学性质
细小白色晶体,稳定性差
鉴别方法
1.为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )
A.加热,观察是否有气体放出
B.溶于水后加入BaCl2溶液,看有无沉淀
C.溶于水后加入澄清石灰水,看有无沉淀
D.取固体试样加入盐酸,看是否有气泡产生
A
2.不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
A.加热这两种固体物质,并将生成的气体通入澄清
的石灰水中
B.在这两种物质的溶液中加入CaCl2溶液
C.在这两种固体中加入同浓度的稀盐酸
D.在这两种物质的溶液中加入少量澄清的石灰水
C
注意啦!B项:Ca2++CO32-==== CaCO3↓,而HCO3-与Ca2+不反应,故可用氯化钙溶液鉴别碳酸钠和碳酸氢钠。
若改为加入BaCl2溶液,是否可以鉴别?
遵守诺言,可以使别人对你建立起信心;违背诺言,不仅动摇了信心,同时可能伤了别人的心。
镜子只能照出你的外貌,而生活却能洞察你的心灵。
第二单元 金属钠及钠的化合物
第2课时 碳酸钠 碳酸氢钠
“苏打水”为什么用的是“小苏打”,而不是“苏打”?
小苏打
苏打水
1.了解碳酸钠和碳酸氢钠的性质和重要用途。
2.掌握碳酸钠和碳酸氢钠的性质和鉴别方法。
1.通过观察、实验等方法对比研究解碳酸钠、碳酸氢钠的性质,并知道它们在生产生活中的用途。(宏观辨识与微观探析)
2.通过实验探究碳酸钠、碳酸氢钠的化学性质,初步形成基于物质构成对物质性质进行预测和检验的认识模型。(证据推理与模型认知)
3.通过体验实验探究和问题讨论的过程,了解实验研究化学物质的一般方法,初步形成分析推理、综合归纳的能力。(科学探究与创新意识)
4.通过对侯氏制碱法的学习,培养科学态度与社会责任核心素养。(科学态度与社会责任)
体会课堂探究的乐趣,
汲取新知识的营养,
让我们一起 吧!
进
走
课
堂
【试一试】你能填出表格中的内容吗?
Na2CO3
NaHCO3
白色、固态
白色、固态
纯碱、苏打
小苏打
碳酸钠和碳酸氢钠
俗名
颜色、状态
化学式
物 质
碳酸钠
碳酸氢钠
【拓展延伸】化学上的“苏氏三兄弟”:大苏打Na2S2O3、苏打Na2CO3、小苏打NaHCO3。
探究实验一 碳酸钠和碳酸氢钠的溶解性及碱性
序号 探究步骤 Na2CO3(1g) NaHCO3(1g)
1 加几滴水
2 加10 mL水
3 加2滴酚
酞溶液
初步结论
白色粉末,加水
结块变成晶体;
放热
细小白色粉末,加
水部分溶解;感受
不到热量变化
振荡时间长时
可溶解
固体量减小
溶液变红(较深)
溶液变微红色
Na2CO3溶解性较NaHCO3大;
碱性比NaHCO3强
【理论分析】
你能根据知识背景进行科学假设,猜测碳酸钠与碳酸氢钠的热稳定性差异吗?
知识背景:
1.碳酸钙在高温下才分解;
2.碳酸氢钙受热分解生成碳酸钙、二氧化碳和水。
探究实验二 碳酸钠和碳酸氢钠的热稳定性
【验证猜想】
现 象 发生反应的化学方程式 结 论
Na2CO3
NaHCO3
△
2NaHCO3====
Na2CO3+H2O+CO2↑
澄清的石灰
水不变浑浊
澄清的石灰
水变浑浊
受热不分解
受热易分解
在试管中分别加热Na2CO3和NaHCO3,连接装有澄清石灰水的烧杯,观察现象。
Na2CO3和NaHCO3的热稳定性比较
【方法点拨】利用此性质可以鉴别固体Na2CO3和NaHCO3 ,还可以除去Na2CO3固体中混有的NaHCO3 。
【结论】
①Na2CO3受热难分解。
②2NaHCO3====Na2CO3 + H2O + CO2↑
△
【交流讨论】你能设计出一套装置比较热稳定性吗?
现象:
结论:
两只气球都鼓起来,但是装碳酸氢钠的气球鼓起得更快
都能和盐酸反应产生二氧化碳,但是碳酸氢钠和盐酸反应更快
探究实验三 Na2CO3和NaHCO3与盐酸的反应
在两只试管中分别加入足量且等物质
的量浓度的稀盐酸,将两只各装有等
量Na2CO3和NaHCO3固体的小气球分
别套在两只试管口,同时把固体粉末
抖入试管,观察现象。
为什么NaHCO3与酸反应比Na2CO3剧烈呢?
CO32-
H+
HCO3-
H+
CO2 ↑ + H2O
H2CO3
【深度分析】
提示:
试写出Na2CO3和NaHCO3与盐酸反应的方程式。
Na2CO3与盐酸反应的方程式:
Na2CO3 + HCl ==== NaCl + NaHCO3
NaHCO3 + HCl ==== NaCl + H2O + CO2↑
总反应方程式:
Na2CO3 + 2HCl ==== 2NaCl + H2O + CO2↑
NaHCO3与盐酸反应的方程式:
NaHCO3 + HCl ==== NaCl + H2O + CO2↑
Na2CO3、NaHCO3均可与胃酸(盐酸)反应,为何不选用Na2CO3作抗酸药 ?
原因:碱性 Na2CO3>NaHCO3
注意:
胃溃疡患者不能过多服用碳酸氢钠治疗胃酸,产生的CO2会导致胃穿孔!
【学以致用】
向盐酸中逐滴加入碳酸钠溶液与向碳酸钠溶液中逐滴加入盐酸现象一样吗?
向碳酸钠溶液中滴加盐酸
开始没有明显现象,后来从溶液里产生无色无味的气体
溶液里立即产生无色无味的气体
向盐酸中慢慢滴加碳酸钠溶液
CO32-+H+====HCO3-
HCO3-+H+====H2O+CO2↑
Na2CO3+2HCl====2NaCl+CO2↑+H2O
【拓展提高】
【实验】向试管中加1mL 0.1mol/L NaHCO3溶液,然后加1mL 0.01mol/L BaCl2溶液, 观察现象。再向其中逐滴滴加NaOH溶液,振荡,观察现象。
【结论】
NaHCO3+NaOH====Na2CO3 +H2O
Na2CO3+BaCl2====BaCO3↓+2NaCl
NaHCO3+Ba(OH)2
BaCO3↓
【交流与讨论】
得到的白色沉淀是什么?
沉淀是如何形成的?
友情提醒:
①小试管中1mL溶液大约高1cm。
②用指定的胶头滴管取用溶液。
探究实验四 碳酸氢钠与盐、碱反应
你能想出用哪些方法鉴别Na2CO3与NaHCO3固体?
小组内交流,然后与同学分享。
1.加热,观察能否产生使澄清石灰水变浑浊的气体。
2.等质量固体加等体积水观察溶解情况。
3.配制饱和溶液测定pH。
4.固体与盐酸反应观察剧烈程度。
……
【交流讨论】
碳酸钠的用途
碳酸氢钠的用途
疏松剂
胃药
灭火剂
NaHCO3常作为食品制作过程中的膨松剂、发酵剂。
决定于
类别
转
化
转
化
碳酸钠
碳酸氢钠
物理性质
化学性质
白色粉末状物质
盐类
与酸反应
与碱反应
与盐反应
物理性质
化学性质
细小白色晶体,稳定性差
鉴别方法
1.为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )
A.加热,观察是否有气体放出
B.溶于水后加入BaCl2溶液,看有无沉淀
C.溶于水后加入澄清石灰水,看有无沉淀
D.取固体试样加入盐酸,看是否有气泡产生
A
2.不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
A.加热这两种固体物质,并将生成的气体通入澄清
的石灰水中
B.在这两种物质的溶液中加入CaCl2溶液
C.在这两种固体中加入同浓度的稀盐酸
D.在这两种物质的溶液中加入少量澄清的石灰水
C
注意啦!B项:Ca2++CO32-==== CaCO3↓,而HCO3-与Ca2+不反应,故可用氯化钙溶液鉴别碳酸钠和碳酸氢钠。
若改为加入BaCl2溶液,是否可以鉴别?
遵守诺言,可以使别人对你建立起信心;违背诺言,不仅动摇了信心,同时可能伤了别人的心。
镜子只能照出你的外貌,而生活却能洞察你的心灵。
