沪教版化学九年级上册课课练:基础强化:化学方程式 (word版有答案)
文档属性
| 名称 | 沪教版化学九年级上册课课练:基础强化:化学方程式 (word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 92.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-13 00:00:00 | ||
图片预览


文档简介
基础强化:化学方程式
1.常见化学方程式的书写
回忆与下列物质相关的化学反应,将每个化学反应“立体模型化”(即联想该反应的实验现象、反应原理、应用、基本反应类型等,记住该反应的反应物和生成物),然后写出反应的化学方程式,并关注各物质之间相互转化的关系。写完后要记得检查书写是否正确:一查化学式、二查配平、三查反应条件、四查沉淀与气体符号。
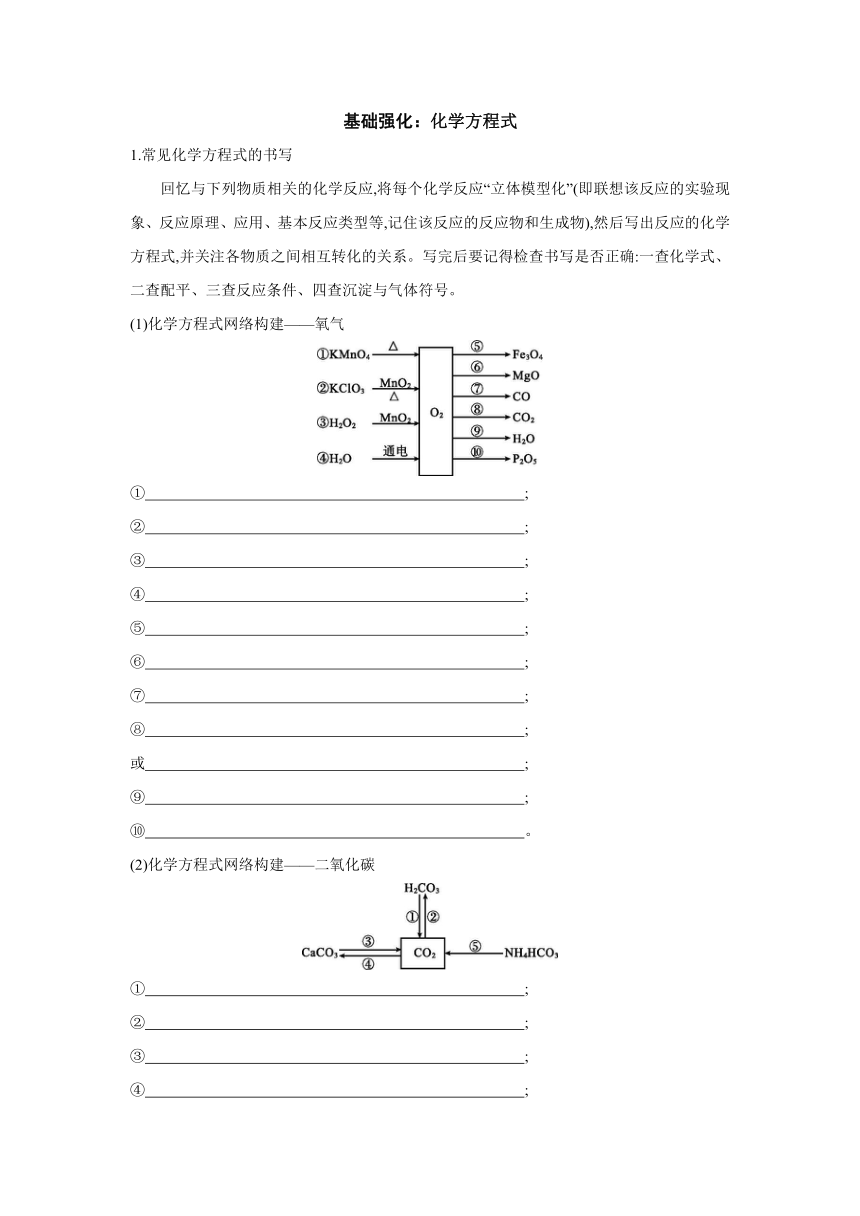
(1)化学方程式网络构建——氧气
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ ;
⑦ ;
⑧ ;
或 ;
⑨ ;
⑩ 。
(2)化学方程式网络构建——二氧化碳
① ;
② ;
③ ;
④ ;
⑤ 。
[定向练习]
按题目要求写出下列反应的化学方程式。
(1)有水生成的化合反应: 。
(2)有氧气生成的分解反应: 。
(3)用镁粉制照明弹: 。
(4)一氧化碳用作燃料: 。
(5)用红磷制烟幕弹: 。
(6)用二氧化碳制碳酸饮料: 。
(7)条件是“高温”的分解反应: 。
(8)条件是“通电”的分解反应: 。
(9)实验室制取二氧化碳的原理: 。
(10)反应物和某一生成物是组成元素相同的液体:
。
(11)检验二氧化碳的原理:
。
(12)某银白色金属在氧气中剧烈燃烧,火星四射,生成一种黑色固体:
。
2.根据化学方程式的计算
下面是一道根据化学方程式进行计算的题,请将其补充完整,注意解题格式的规范。
用68 g过氧化氢溶液和2 g二氧化锰的混合物来制取氧气,充分反应后,称量剩余溶液和滤渣的质量为68.4 g。求:
(1)充分反应后,生成氧气的质量为68 g+2 g-( )g=1.6 g。
(2)参加反应的过氧化氢的质量。
解:设产生1.6 g氧气需要过氧化氢的质量为( )。
2H2O22H2O+O2↑
2×( ) 32
x ( )
=
x=( )
答:参加反应的过氧化氢的质量为( )。
答案
1.(1)①2KMnO4K2MnO4+MnO2+O2↑
②2KClO32KCl+3O2 ↑
③2H2O22H2O+O2↑
④2H2O2H2↑+O2↑
⑤3Fe+2O2 Fe3O4
⑥2Mg+O2 2MgO
⑦2C+O2 2CO
⑧2CO+O22CO2
C+O2 CO2(合理即可)
⑨2H2+O2 2H2O(合理即可)
⑩4P+5O2 2P2O5
(2)①H2CO3 CO2 ↑+ H2O
②CO2+H2OH2CO3
③CaCO3+2HClCaCl2+H2O+CO2↑(合理即可)
④Ca(OH)2+CO2CaCO3 ↓+H2O
⑤NH4HCO3H2O+CO2↑+NH3↑
[定向练习]
(1)2H2+O22H2O
(2)2KMnO4K2MnO4+MnO2+O2↑(合理即可)
(3)2Mg+O2 2MgO
(4)2CO+O22CO2
(5)4P+5O2 2P2O5
(6)H2O+CO2H2CO3
(7)CaCO3CaO+CO2↑
(8)2H2O2H2↑+O2↑
(9)CaCO3+2HClCaCl2+H2O+CO2↑
(10)2H2O2 2H2O+O2↑
(11)Ca(OH)2+CO2CaCO3 ↓+H2O
(12)3Fe+2O2Fe3O4
2.(1)68.4
(2)x 34 1.6 g 2×34 1.6 g 3.4 g 3.4 g
1.常见化学方程式的书写
回忆与下列物质相关的化学反应,将每个化学反应“立体模型化”(即联想该反应的实验现象、反应原理、应用、基本反应类型等,记住该反应的反应物和生成物),然后写出反应的化学方程式,并关注各物质之间相互转化的关系。写完后要记得检查书写是否正确:一查化学式、二查配平、三查反应条件、四查沉淀与气体符号。
(1)化学方程式网络构建——氧气
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ ;
⑦ ;
⑧ ;
或 ;
⑨ ;
⑩ 。
(2)化学方程式网络构建——二氧化碳
① ;
② ;
③ ;
④ ;
⑤ 。
[定向练习]
按题目要求写出下列反应的化学方程式。
(1)有水生成的化合反应: 。
(2)有氧气生成的分解反应: 。
(3)用镁粉制照明弹: 。
(4)一氧化碳用作燃料: 。
(5)用红磷制烟幕弹: 。
(6)用二氧化碳制碳酸饮料: 。
(7)条件是“高温”的分解反应: 。
(8)条件是“通电”的分解反应: 。
(9)实验室制取二氧化碳的原理: 。
(10)反应物和某一生成物是组成元素相同的液体:
。
(11)检验二氧化碳的原理:
。
(12)某银白色金属在氧气中剧烈燃烧,火星四射,生成一种黑色固体:
。
2.根据化学方程式的计算
下面是一道根据化学方程式进行计算的题,请将其补充完整,注意解题格式的规范。
用68 g过氧化氢溶液和2 g二氧化锰的混合物来制取氧气,充分反应后,称量剩余溶液和滤渣的质量为68.4 g。求:
(1)充分反应后,生成氧气的质量为68 g+2 g-( )g=1.6 g。
(2)参加反应的过氧化氢的质量。
解:设产生1.6 g氧气需要过氧化氢的质量为( )。
2H2O22H2O+O2↑
2×( ) 32
x ( )
=
x=( )
答:参加反应的过氧化氢的质量为( )。
答案
1.(1)①2KMnO4K2MnO4+MnO2+O2↑
②2KClO32KCl+3O2 ↑
③2H2O22H2O+O2↑
④2H2O2H2↑+O2↑
⑤3Fe+2O2 Fe3O4
⑥2Mg+O2 2MgO
⑦2C+O2 2CO
⑧2CO+O22CO2
C+O2 CO2(合理即可)
⑨2H2+O2 2H2O(合理即可)
⑩4P+5O2 2P2O5
(2)①H2CO3 CO2 ↑+ H2O
②CO2+H2OH2CO3
③CaCO3+2HClCaCl2+H2O+CO2↑(合理即可)
④Ca(OH)2+CO2CaCO3 ↓+H2O
⑤NH4HCO3H2O+CO2↑+NH3↑
[定向练习]
(1)2H2+O22H2O
(2)2KMnO4K2MnO4+MnO2+O2↑(合理即可)
(3)2Mg+O2 2MgO
(4)2CO+O22CO2
(5)4P+5O2 2P2O5
(6)H2O+CO2H2CO3
(7)CaCO3CaO+CO2↑
(8)2H2O2H2↑+O2↑
(9)CaCO3+2HClCaCl2+H2O+CO2↑
(10)2H2O2 2H2O+O2↑
(11)Ca(OH)2+CO2CaCO3 ↓+H2O
(12)3Fe+2O2Fe3O4
2.(1)68.4
(2)x 34 1.6 g 2×34 1.6 g 3.4 g 3.4 g
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
