第二单元课题1空气-2021-2022学年九年级化学人教版上册(共56张PPT内嵌视频)
文档属性
| 名称 | 第二单元课题1空气-2021-2022学年九年级化学人教版上册(共56张PPT内嵌视频) |
|
|
| 格式 | zip | ||
| 文件大小 | 92.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-15 00:00:00 | ||
图片预览











文档简介
(共56张PPT)
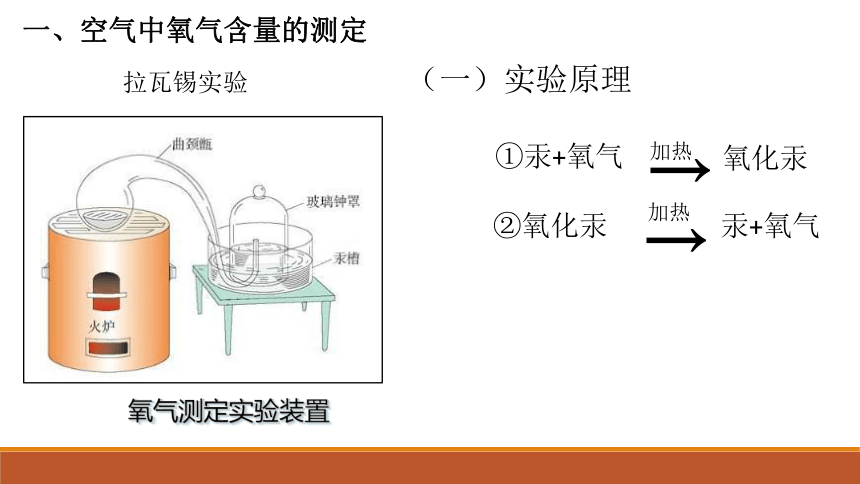
试管
试管夹
玻璃棒
酒精灯
胶头滴管
滴瓶
铁架台(包括铁夹和铁圈)
烧杯
量筒
集气瓶
水槽
复习巩固
一、常用仪器
1、药品的取用
镊子、药匙、量筒、胶头滴管
2、物质加热
固体:略向下倾斜,均匀加热
液体:≤,45°,不对人,均匀加热
3、洗涤标准
试管刷、水既不聚成水滴,也不成股流下
二、化学实验操作
酒精灯:三禁止,一用
谜 语
一物到处有,用棒赶不走;
眼睛看不见,手摸也没有;
咀嚼无滋味,没它活不久。 (打一物质)
第二单元 我们周围的空气
课题1 空气
目录
二、空气成分及其用途
一、空气中氧气含量的测定
三、纯净物与混合物
了解固态空气
拉瓦锡
一、空气中氧气含量的测定
氧气测定实验装置
一、空气中氧气含量的测定
拉瓦锡实验
①汞+氧气
加热
氧化汞
→
②氧化汞
加热
汞+氧气
→
(一)实验原理
(二)实验结论
拉瓦锡根据实验结果提出了新的燃烧理论:
他认为燃烧决不是物质燃素的外逸,而是物质跟氧气的剧烈作用,放出光和热。他又对空气的成份作了正确的分析:空气中有五分之一的氧气,可以帮助燃烧;还有五分之四的氮气(拉瓦锡称为窒息空气),不能帮助燃烧。
红色粉末,有剧毒
HgO 氧化汞
Hg 汞
俗称:水银
常温下可蒸发,汞蒸气有剧毒。
(三)实验缺点
1、时间长,12天
2、实验药品有毒
红磷燃烧测定空气中氧气含量实验
1、实验原理
红磷在封闭的容器内充分燃烧,消耗了空气中的氧气,生成五氧化二磷固体,容器内压强减小,水面上升约1/5,从而确定空气中氧气的体积分数。
1、实验原理(文字表达式)
P O2 P2O5
五氧化二磷
点燃
磷 + 氧气
2、实验步骤
(1)连接装置,并检查装置气密性
(2)点燃燃烧匙内的红磷,迅速伸入集气瓶中,并塞紧塞子
(3)待温度冷却到室温时,打开弹簧夹
3、实验现象
(1)产生黄色火焰,放出热量;
(3)等到燃烧停止,冷却后,集气瓶内水面上升了约1/5
4、实验结论
①氧气约占空气总体积的1/5
(2)产生大量白烟;
②氮气不支持燃烧,也不溶于水
(1)点燃前,打开止水夹,水会不会倒流,为什么?
点燃前不会倒流,点燃前集气瓶内外没有压强差。
(2)燃烧停止后,烧杯的水进入集气瓶说明了什么?
说明集气瓶内外存在压强差,说明集气瓶中气体减少。
(3)是什么导致了集气瓶中气体减少?减少的气体是什么?
红磷燃烧消耗氧气导致了集气瓶中的气体减少,减少了氧气。
5、实验误差分析
如果测出来的数据,小于1/5,可能的原因有哪些?
(1)装置气密性不好,装置漏气。
(2)红磷量不足,未将集气瓶中的
氧气耗完。
(3)未等冷却到室温就打开止水夹。
5、实验误差分析
如果测出来的数据,大于1/5,可能的原因有哪些?
(1)弹簧夹没有夹紧
(2)点燃红磷后伸入集气瓶的速度过慢
5、实验误差分析
(2)装置漏气;
(5)燃烧一定程度时,瓶内氧气含量小, 红磷不能继续燃烧。
偏大
(水面上升大于1/5)
偏小
(水面上升小于1/5)
弹簧夹没有夹紧;
红磷量不足;
装置漏气;
未冷却到室温就打开了弹簧夹;
点燃红磷后伸入广口瓶的速度过慢;
6、药品的选择
药品 可燃物 只与氧气反应 生成物的状态 是否选择
木炭
硫
镁带
红磷
是
是
是
是
是
是
是
否
气体
气体
固体
固体
×
×
×
√
药品需满足的条件:
①在空气中能燃烧
②在点燃条件下,只与氧气反应
③生成物只有固体
采用燃烧的方法除去密闭容器中空气里的氧气,以测定空气中氧气的含量,选用下列哪种物质最为适宜( )
A.红磷 B.硫磺 C.木炭 D.铁丝
例题1
A
例题2
在测定空气中氧气含量的实验时,甲同学的集气瓶内水面上升明显小于瓶内空气的1/5,乙同学的结果明显大于1/5.下列对这两种现象原因分析合理的是( )
A.甲同学插入燃烧匙太慢
B.甲同学使用的红磷量不足
C.甲同学实验前弹簧夹未夹紧
D.乙同学没冷却到室温就打开弹簧夹
B
二、空气成分及其用途
在小学《科学》中我们已经学过了空气的组成,同学们还记得空气中含有哪些成分吗?
(一)空气成分
空气主要由氮气、氧气、稀有气体(氦、氖、氩、氪、氙、氡),二氧化碳以及其他物质(如水蒸气、杂质等)组合而成。
氮气的体积分数约为78%
氧气的体积分数约为21%
稀有气体(氦、氖、氩、氪、氙、氡)的体积分数约为0.934%,
二氧化碳的体积分数约为0.03%
其他物质(如水蒸气、杂质等)的体积分数约为0.003%。
空气的成分不是固定的,随着高度的改变、气压的改变,空气的组成比例也会改变。但是长期以来人们一直认为空气是一种单一的物质,直到后来法国科学家拉瓦锡通过实验首先得出了空气是由氧气和氮气组成的结论。19世纪末,科学家们又通过大量的实验发现,空气里还有氦、氩、氙等稀有气体。
1、氧气
每天吸入15 kg 空气
真空环境下不超过5分钟就会死亡
(1)医疗:供给呼吸
(潜水、登山、航天)
(2)国防工业:液氧做助燃剂
(3)冶金:富氧炼钢(缩短反应时间,提高钢产品质量)
液氮了解一下
2、氮气
物理性质:无色、无味、气体、难溶于水
N2
化学性质:不活泼
↓
用途
保护气
(1)充灌灯泡
(2)保护粮食(薯片)
(3)液氮(冷冻剂)
3、稀有气体(惰性气体)
物理性质:无色、无味
氦
He
氖
Ne
氩
Ar
氪
Kr
氙
Xe
化学性质:不活泼
稀有气体
氡Rn
(1)霓虹灯
用途
(2)保护气
用途
4、二氧化碳
物理性质:无色、无味、能溶于水
CO2
用途:灭火、光合作用
了解大气污染的成因
5、大气污染及防治
5、大气污染及防治
(1)污染物
粉尘
有害气体:CO、SO2、NO2
空气污染指数
三大环境问题
(1)酸雨:二氧化硫
(2)温室效应:二氧化碳
(3)臭氧空洞:氟氯烃(氟氯昂)
(2)大气的保护
植树造林
绿色出行
使用清洁能源
例题1
空气是一种宝贵的自然资源.如图为空气成分示意图,其中R指的是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
B
例题2
下列有关空气中各成分说法不正确的是( )
A.氮气的化学性质不活泼,可在食品包装时充入防腐
B.氧气化学性质比较活泼,能支持燃烧
C.二氧化碳不能燃烧,一般也不支持燃烧,可用于灭火
D.稀有气体一定不能与其他物质发生反应
D
例题3
我们每时每刻都要吸入空气,关于空气的下列说法正确的是( )
A.空气中有很多物质,其中只有氧气是有用的,其他成分都有害
B.空气中氧气能供给呼吸,而氮气不能供给呼吸,但对人呼吸无害
C.空气中的其他成分都分离出去,只留下氧气,对人类的生存更有宜
D.空气是由多种物质组成的,各气体含量永远不会发生变化
B
练习3-2
下列措施符合“生态柳州”理念的是( )
①将垃圾分类处理; ②禁止尾气排放不达标的机动车上路;
③提倡使用一次性筷子; ④大力提倡植树造林.
A.①②③ B.①②④ C.①③④ D.②③④
有人患咽喉炎或鼻炎,医生常用“冷冻法”治疗,其冷冻剂是下列物质中的( )
A.液态氧气 B.液态空气 C.液化石油气 D.液态氮气
练习3-1
D
B
三、纯净物与混合物
1、纯净物:由一种物质组成(可以用专门的化学符号表示)
如:N2、O2、CO2、P、P2O5、H2O
2、混合物:由两种或两种以上物质混合而成的物质
如:空气、溶液、矿泉水、泥沙
下列属于混合物的是( )
A.洁净的空气 B.水 C.氢氧化钙 D.硫酸
例题1
例题2
下列物质属于纯净物的是( )
A.空气 B.冰水混合物
C.氯化钠溶液 D.75%的医用酒精
A
B
下列物质属于纯净物的是( )
A.钢 B.空气 C.干冰 D.海水
练习2-1
例题3
下列各组物质中,前者属于纯净物,后者属于混合物的是( )
A.洁净的空气 氮气 B.稀有气体 人体呼出气体
C.二氧化碳 冰水混合物 D.蒸馏水 海水
C
D
总结
空气成分别忘记,主要成分氮氧气;
氮七八,氧二一,零点九四是稀气;
还有两个零点三,二氧化碳和杂气 ;
百分体积要记清,莫要当成质量比 。
总结
空气
组成
氮气(N2):78%
氧气(O2):21%
稀有气体(He、Ne、Ar、Kr、Xe):0.94%
二氧化碳(CO2):0.03%
其他气体和杂质:0.03%
污染
污染物
粉尘
有害气体:CO、SO2、NO2
大气的保护:植树造林、绿色出行、使用清洁能源
纯净物:由一种物质组成(可以用专门的化学符号表示)
混合物:由两种或两种以上物质组成
试管
试管夹
玻璃棒
酒精灯
胶头滴管
滴瓶
铁架台(包括铁夹和铁圈)
烧杯
量筒
集气瓶
水槽
复习巩固
一、常用仪器
1、药品的取用
镊子、药匙、量筒、胶头滴管
2、物质加热
固体:略向下倾斜,均匀加热
液体:≤,45°,不对人,均匀加热
3、洗涤标准
试管刷、水既不聚成水滴,也不成股流下
二、化学实验操作
酒精灯:三禁止,一用
谜 语
一物到处有,用棒赶不走;
眼睛看不见,手摸也没有;
咀嚼无滋味,没它活不久。 (打一物质)
第二单元 我们周围的空气
课题1 空气
目录
二、空气成分及其用途
一、空气中氧气含量的测定
三、纯净物与混合物
了解固态空气
拉瓦锡
一、空气中氧气含量的测定
氧气测定实验装置
一、空气中氧气含量的测定
拉瓦锡实验
①汞+氧气
加热
氧化汞
→
②氧化汞
加热
汞+氧气
→
(一)实验原理
(二)实验结论
拉瓦锡根据实验结果提出了新的燃烧理论:
他认为燃烧决不是物质燃素的外逸,而是物质跟氧气的剧烈作用,放出光和热。他又对空气的成份作了正确的分析:空气中有五分之一的氧气,可以帮助燃烧;还有五分之四的氮气(拉瓦锡称为窒息空气),不能帮助燃烧。
红色粉末,有剧毒
HgO 氧化汞
Hg 汞
俗称:水银
常温下可蒸发,汞蒸气有剧毒。
(三)实验缺点
1、时间长,12天
2、实验药品有毒
红磷燃烧测定空气中氧气含量实验
1、实验原理
红磷在封闭的容器内充分燃烧,消耗了空气中的氧气,生成五氧化二磷固体,容器内压强减小,水面上升约1/5,从而确定空气中氧气的体积分数。
1、实验原理(文字表达式)
P O2 P2O5
五氧化二磷
点燃
磷 + 氧气
2、实验步骤
(1)连接装置,并检查装置气密性
(2)点燃燃烧匙内的红磷,迅速伸入集气瓶中,并塞紧塞子
(3)待温度冷却到室温时,打开弹簧夹
3、实验现象
(1)产生黄色火焰,放出热量;
(3)等到燃烧停止,冷却后,集气瓶内水面上升了约1/5
4、实验结论
①氧气约占空气总体积的1/5
(2)产生大量白烟;
②氮气不支持燃烧,也不溶于水
(1)点燃前,打开止水夹,水会不会倒流,为什么?
点燃前不会倒流,点燃前集气瓶内外没有压强差。
(2)燃烧停止后,烧杯的水进入集气瓶说明了什么?
说明集气瓶内外存在压强差,说明集气瓶中气体减少。
(3)是什么导致了集气瓶中气体减少?减少的气体是什么?
红磷燃烧消耗氧气导致了集气瓶中的气体减少,减少了氧气。
5、实验误差分析
如果测出来的数据,小于1/5,可能的原因有哪些?
(1)装置气密性不好,装置漏气。
(2)红磷量不足,未将集气瓶中的
氧气耗完。
(3)未等冷却到室温就打开止水夹。
5、实验误差分析
如果测出来的数据,大于1/5,可能的原因有哪些?
(1)弹簧夹没有夹紧
(2)点燃红磷后伸入集气瓶的速度过慢
5、实验误差分析
(2)装置漏气;
(5)燃烧一定程度时,瓶内氧气含量小, 红磷不能继续燃烧。
偏大
(水面上升大于1/5)
偏小
(水面上升小于1/5)
弹簧夹没有夹紧;
红磷量不足;
装置漏气;
未冷却到室温就打开了弹簧夹;
点燃红磷后伸入广口瓶的速度过慢;
6、药品的选择
药品 可燃物 只与氧气反应 生成物的状态 是否选择
木炭
硫
镁带
红磷
是
是
是
是
是
是
是
否
气体
气体
固体
固体
×
×
×
√
药品需满足的条件:
①在空气中能燃烧
②在点燃条件下,只与氧气反应
③生成物只有固体
采用燃烧的方法除去密闭容器中空气里的氧气,以测定空气中氧气的含量,选用下列哪种物质最为适宜( )
A.红磷 B.硫磺 C.木炭 D.铁丝
例题1
A
例题2
在测定空气中氧气含量的实验时,甲同学的集气瓶内水面上升明显小于瓶内空气的1/5,乙同学的结果明显大于1/5.下列对这两种现象原因分析合理的是( )
A.甲同学插入燃烧匙太慢
B.甲同学使用的红磷量不足
C.甲同学实验前弹簧夹未夹紧
D.乙同学没冷却到室温就打开弹簧夹
B
二、空气成分及其用途
在小学《科学》中我们已经学过了空气的组成,同学们还记得空气中含有哪些成分吗?
(一)空气成分
空气主要由氮气、氧气、稀有气体(氦、氖、氩、氪、氙、氡),二氧化碳以及其他物质(如水蒸气、杂质等)组合而成。
氮气的体积分数约为78%
氧气的体积分数约为21%
稀有气体(氦、氖、氩、氪、氙、氡)的体积分数约为0.934%,
二氧化碳的体积分数约为0.03%
其他物质(如水蒸气、杂质等)的体积分数约为0.003%。
空气的成分不是固定的,随着高度的改变、气压的改变,空气的组成比例也会改变。但是长期以来人们一直认为空气是一种单一的物质,直到后来法国科学家拉瓦锡通过实验首先得出了空气是由氧气和氮气组成的结论。19世纪末,科学家们又通过大量的实验发现,空气里还有氦、氩、氙等稀有气体。
1、氧气
每天吸入15 kg 空气
真空环境下不超过5分钟就会死亡
(1)医疗:供给呼吸
(潜水、登山、航天)
(2)国防工业:液氧做助燃剂
(3)冶金:富氧炼钢(缩短反应时间,提高钢产品质量)
液氮了解一下
2、氮气
物理性质:无色、无味、气体、难溶于水
N2
化学性质:不活泼
↓
用途
保护气
(1)充灌灯泡
(2)保护粮食(薯片)
(3)液氮(冷冻剂)
3、稀有气体(惰性气体)
物理性质:无色、无味
氦
He
氖
Ne
氩
Ar
氪
Kr
氙
Xe
化学性质:不活泼
稀有气体
氡Rn
(1)霓虹灯
用途
(2)保护气
用途
4、二氧化碳
物理性质:无色、无味、能溶于水
CO2
用途:灭火、光合作用
了解大气污染的成因
5、大气污染及防治
5、大气污染及防治
(1)污染物
粉尘
有害气体:CO、SO2、NO2
空气污染指数
三大环境问题
(1)酸雨:二氧化硫
(2)温室效应:二氧化碳
(3)臭氧空洞:氟氯烃(氟氯昂)
(2)大气的保护
植树造林
绿色出行
使用清洁能源
例题1
空气是一种宝贵的自然资源.如图为空气成分示意图,其中R指的是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
B
例题2
下列有关空气中各成分说法不正确的是( )
A.氮气的化学性质不活泼,可在食品包装时充入防腐
B.氧气化学性质比较活泼,能支持燃烧
C.二氧化碳不能燃烧,一般也不支持燃烧,可用于灭火
D.稀有气体一定不能与其他物质发生反应
D
例题3
我们每时每刻都要吸入空气,关于空气的下列说法正确的是( )
A.空气中有很多物质,其中只有氧气是有用的,其他成分都有害
B.空气中氧气能供给呼吸,而氮气不能供给呼吸,但对人呼吸无害
C.空气中的其他成分都分离出去,只留下氧气,对人类的生存更有宜
D.空气是由多种物质组成的,各气体含量永远不会发生变化
B
练习3-2
下列措施符合“生态柳州”理念的是( )
①将垃圾分类处理; ②禁止尾气排放不达标的机动车上路;
③提倡使用一次性筷子; ④大力提倡植树造林.
A.①②③ B.①②④ C.①③④ D.②③④
有人患咽喉炎或鼻炎,医生常用“冷冻法”治疗,其冷冻剂是下列物质中的( )
A.液态氧气 B.液态空气 C.液化石油气 D.液态氮气
练习3-1
D
B
三、纯净物与混合物
1、纯净物:由一种物质组成(可以用专门的化学符号表示)
如:N2、O2、CO2、P、P2O5、H2O
2、混合物:由两种或两种以上物质混合而成的物质
如:空气、溶液、矿泉水、泥沙
下列属于混合物的是( )
A.洁净的空气 B.水 C.氢氧化钙 D.硫酸
例题1
例题2
下列物质属于纯净物的是( )
A.空气 B.冰水混合物
C.氯化钠溶液 D.75%的医用酒精
A
B
下列物质属于纯净物的是( )
A.钢 B.空气 C.干冰 D.海水
练习2-1
例题3
下列各组物质中,前者属于纯净物,后者属于混合物的是( )
A.洁净的空气 氮气 B.稀有气体 人体呼出气体
C.二氧化碳 冰水混合物 D.蒸馏水 海水
C
D
总结
空气成分别忘记,主要成分氮氧气;
氮七八,氧二一,零点九四是稀气;
还有两个零点三,二氧化碳和杂气 ;
百分体积要记清,莫要当成质量比 。
总结
空气
组成
氮气(N2):78%
氧气(O2):21%
稀有气体(He、Ne、Ar、Kr、Xe):0.94%
二氧化碳(CO2):0.03%
其他气体和杂质:0.03%
污染
污染物
粉尘
有害气体:CO、SO2、NO2
大气的保护:植树造林、绿色出行、使用清洁能源
纯净物:由一种物质组成(可以用专门的化学符号表示)
混合物:由两种或两种以上物质组成
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
