物质的分离和提纯
图片预览






文档简介
课件24张PPT。 第二单元
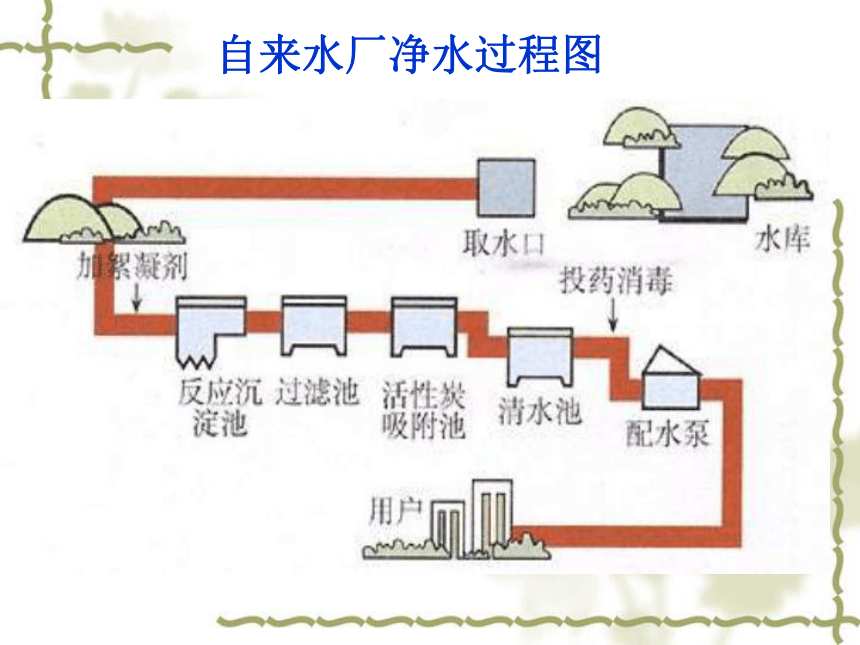
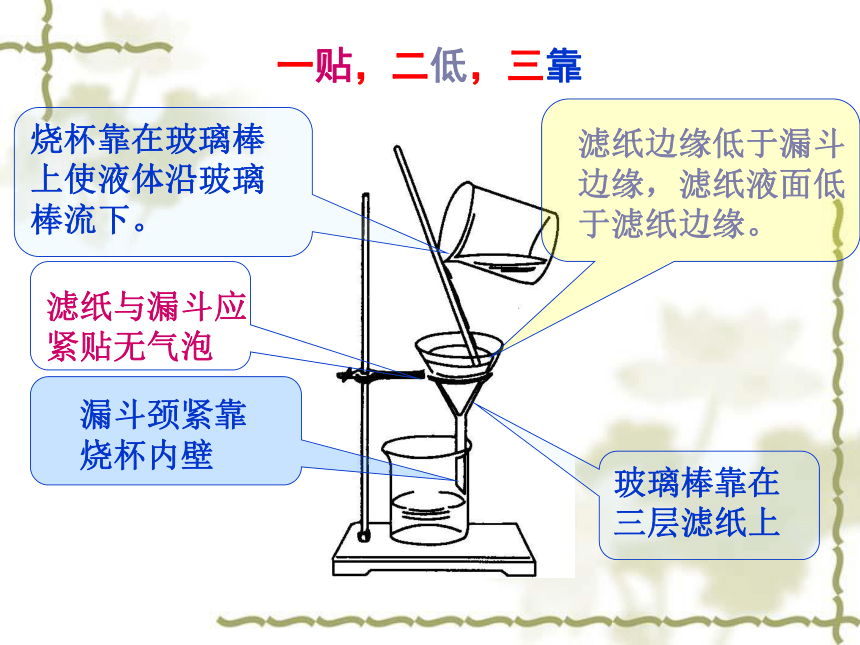
研究物质的实验方法第一课时 物质的分离与提纯自来水厂净水过程图蒸馏:可以得到比较纯的蒸馏水分离和提纯有什么不同? 分离 把混合物中的几种物质分开,每一组分都要保留下来,即分别得到纯净的物质,且各物质要恢复到原来的状态 。 提纯 指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去,以得到纯净的物质。 实验室中用KClO3在MnO2催化下受热分解制取氧气。如何从反应后的KCl和MnO2的混合物中分离这两种物质?该过程中都用到了哪些分离方法?过滤、蒸发、结晶实例1方法一:过滤(1)适用除去溶液里混有不溶于溶剂的杂质(固液混合物的分离)(2)主要仪器:漏斗、烧杯、玻璃棒、铁架台(带铁圈)、滤纸等。滤纸边缘低于漏斗边缘,滤纸液面低于滤纸边缘。 烧杯靠在玻璃棒上使液体沿玻璃棒流下。一贴,二低,三靠 实例2海水通过日晒得到粗盐,其中使用了什么分离方法?方法二:结晶(蒸发结晶、冷却结晶)(1)结晶适用:分离可溶性固体混合物。
(2)蒸发结晶原理:通过蒸发溶剂,使溶质以晶体析出的分离方法(3)主要仪器:
蒸发皿、铁架台、
酒精灯、玻璃棒。现有混有少量氯化钾的硝酸钾粉末,请参照右图的溶解度曲线,设计实验方案提纯硝酸钾。实例3冷却结晶冷却结晶实验方案①溶解:在较高温度下将混合物溶于水形成浓溶液②冷却结晶:迅速冷却,析出大量KNO3晶体③过滤:固体为KNO3,滤液中含KNO3和KCl④如提纯效果不理想,重复以上操作1、某地区的自来水中混有少量Fe3+,实验室如何获得少量纯净的水?实例42、已知醋酸的沸点是118℃,乙醇的沸点是78.5 ℃,如何将二者分离?蒸馏-物质的分离和提纯方法之三(1)适用:
沸点相差较大的液体,
或除去水中难挥发或不挥发的物质
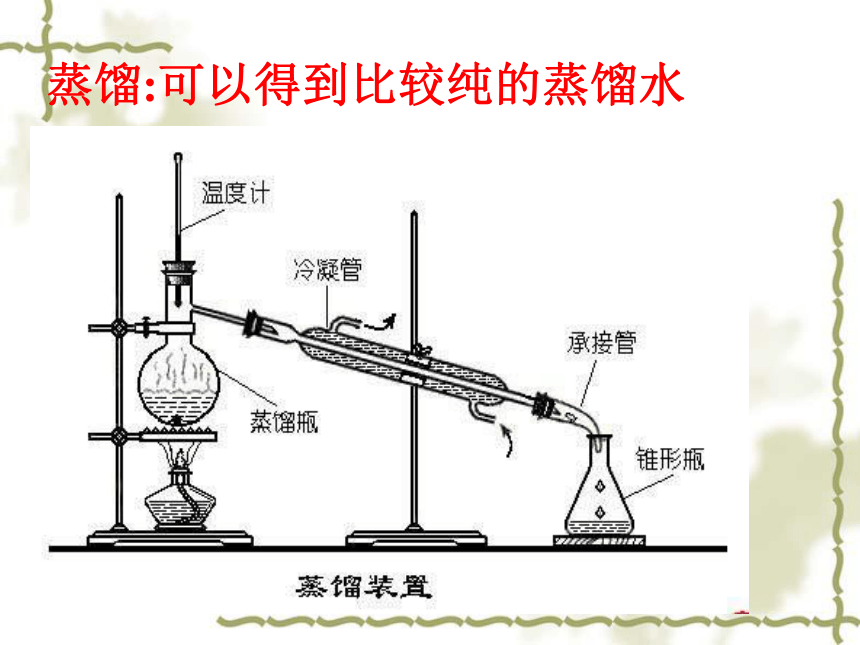
(2)仪器蒸馏实验示意图注意点:①实验前在蒸馏烧瓶中先加入几粒沸石(或碎瓷片)—防止液体暴沸③冷凝水的方向:
用CCl4萃取溴水现象液体分层
上层液体显( )色
下层液体显( )色黄橙红用CCl4萃取碘水现象液体分层
上层液体显( )色
下层液体显( )色黄紫红实例5 (1)萃取原理:利用物质在互不相溶的溶剂中溶解度的不同,将物质从一种溶剂转移到另一种溶剂中,从而实现分离的方法方法四:萃取、分液(2)萃取仪器:
分液漏斗,铁架台(铁圈),烧杯(3)萃取、分液操作要点:1、检漏2、振荡
并不时旋开活塞,放出易挥 发物质的蒸气。4、分液3、静置分层 4、分液:两种互不相溶液体的分离 操作注意:
a.分液时保持漏斗内与大气压一致;
b.下层溶液下口出,上层溶液上口出
----“上走上,下走下”(4)萃取剂的选择:1、萃取剂与原溶剂不混溶、不反应2、溶质在萃取剂中有较大的溶解度3、溶质不与萃取剂发生任何反应玫瑰(Rose)分离提纯玫瑰精油萃取的生活应用【小结】物质的分离、提纯现需要分离下列物质,请用直线将分离实例、分离方法和选择分离方法的依据连接起来。 实 例 分离方法 选择的依据
除去澄清石灰水中的碳酸钙 蒸馏 溶解度随温度变化的差异
用CCl4提取溴水中溴单质 过滤 在不同溶剂中溶解度的差异
分离醋酸 与 乙醇 分液 沸点的差异较大
(沸点118℃) (沸点78.5℃)
分离汽油和水 结晶 两溶剂互不相溶
从含有氯化钠的硝酸钾溶液中 萃取 物质在水中溶解度的不同
提取硝酸钾练习泥沙、Mg2+、Cl- 、Na+MgCl2、泥沙、NaClNaCl晶体提纯含少量氯化镁和泥沙等杂质 的粗食盐实验方案实验方案:加水溶解加入稍过量的NaOH溶液泥沙、Mg(OH)2↓、OH-、Cl- 、Na+过滤泥沙、Mg(OH)2↓OH-、 Cl- 、Na+蒸发结晶加入适量盐酸中和 过量的NaOH溶液H+、Cl- 、Na+实例6
研究物质的实验方法第一课时 物质的分离与提纯自来水厂净水过程图蒸馏:可以得到比较纯的蒸馏水分离和提纯有什么不同? 分离 把混合物中的几种物质分开,每一组分都要保留下来,即分别得到纯净的物质,且各物质要恢复到原来的状态 。 提纯 指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去,以得到纯净的物质。 实验室中用KClO3在MnO2催化下受热分解制取氧气。如何从反应后的KCl和MnO2的混合物中分离这两种物质?该过程中都用到了哪些分离方法?过滤、蒸发、结晶实例1方法一:过滤(1)适用除去溶液里混有不溶于溶剂的杂质(固液混合物的分离)(2)主要仪器:漏斗、烧杯、玻璃棒、铁架台(带铁圈)、滤纸等。滤纸边缘低于漏斗边缘,滤纸液面低于滤纸边缘。 烧杯靠在玻璃棒上使液体沿玻璃棒流下。一贴,二低,三靠 实例2海水通过日晒得到粗盐,其中使用了什么分离方法?方法二:结晶(蒸发结晶、冷却结晶)(1)结晶适用:分离可溶性固体混合物。
(2)蒸发结晶原理:通过蒸发溶剂,使溶质以晶体析出的分离方法(3)主要仪器:
蒸发皿、铁架台、
酒精灯、玻璃棒。现有混有少量氯化钾的硝酸钾粉末,请参照右图的溶解度曲线,设计实验方案提纯硝酸钾。实例3冷却结晶冷却结晶实验方案①溶解:在较高温度下将混合物溶于水形成浓溶液②冷却结晶:迅速冷却,析出大量KNO3晶体③过滤:固体为KNO3,滤液中含KNO3和KCl④如提纯效果不理想,重复以上操作1、某地区的自来水中混有少量Fe3+,实验室如何获得少量纯净的水?实例42、已知醋酸的沸点是118℃,乙醇的沸点是78.5 ℃,如何将二者分离?蒸馏-物质的分离和提纯方法之三(1)适用:
沸点相差较大的液体,
或除去水中难挥发或不挥发的物质
(2)仪器蒸馏实验示意图注意点:①实验前在蒸馏烧瓶中先加入几粒沸石(或碎瓷片)—防止液体暴沸③冷凝水的方向:
用CCl4萃取溴水现象液体分层
上层液体显( )色
下层液体显( )色黄橙红用CCl4萃取碘水现象液体分层
上层液体显( )色
下层液体显( )色黄紫红实例5 (1)萃取原理:利用物质在互不相溶的溶剂中溶解度的不同,将物质从一种溶剂转移到另一种溶剂中,从而实现分离的方法方法四:萃取、分液(2)萃取仪器:
分液漏斗,铁架台(铁圈),烧杯(3)萃取、分液操作要点:1、检漏2、振荡
并不时旋开活塞,放出易挥 发物质的蒸气。4、分液3、静置分层 4、分液:两种互不相溶液体的分离 操作注意:
a.分液时保持漏斗内与大气压一致;
b.下层溶液下口出,上层溶液上口出
----“上走上,下走下”(4)萃取剂的选择:1、萃取剂与原溶剂不混溶、不反应2、溶质在萃取剂中有较大的溶解度3、溶质不与萃取剂发生任何反应玫瑰(Rose)分离提纯玫瑰精油萃取的生活应用【小结】物质的分离、提纯现需要分离下列物质,请用直线将分离实例、分离方法和选择分离方法的依据连接起来。 实 例 分离方法 选择的依据
除去澄清石灰水中的碳酸钙 蒸馏 溶解度随温度变化的差异
用CCl4提取溴水中溴单质 过滤 在不同溶剂中溶解度的差异
分离醋酸 与 乙醇 分液 沸点的差异较大
(沸点118℃) (沸点78.5℃)
分离汽油和水 结晶 两溶剂互不相溶
从含有氯化钠的硝酸钾溶液中 萃取 物质在水中溶解度的不同
提取硝酸钾练习泥沙、Mg2+、Cl- 、Na+MgCl2、泥沙、NaClNaCl晶体提纯含少量氯化镁和泥沙等杂质 的粗食盐实验方案实验方案:加水溶解加入稍过量的NaOH溶液泥沙、Mg(OH)2↓、OH-、Cl- 、Na+过滤泥沙、Mg(OH)2↓OH-、 Cl- 、Na+蒸发结晶加入适量盐酸中和 过量的NaOH溶液H+、Cl- 、Na+实例6
