化学人教版(2019)必修第二册7.1认识有机化合物(共30张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.1认识有机化合物(共30张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-21 00:00:00 | ||
图片预览




文档简介
(共30张PPT)
认识有机化合物
第七章 有机化合物
第一节
知道有机化合物的键线式。
2
知道什么是有机化合物。
1
知道烷烃的结构。
3
会对有机物进行简单的命名
4
掌握同分异构体的概念
5
讨论:有机物的定义?
一、有机化合物中碳原子的成键特点
1.有机物的定义
大多数含有碳元素的化合物为有机物化合物,简称有机物。
( 但CO、CO2、H2CO3及其盐、氰化物、硫氰化物等看作无机物。)
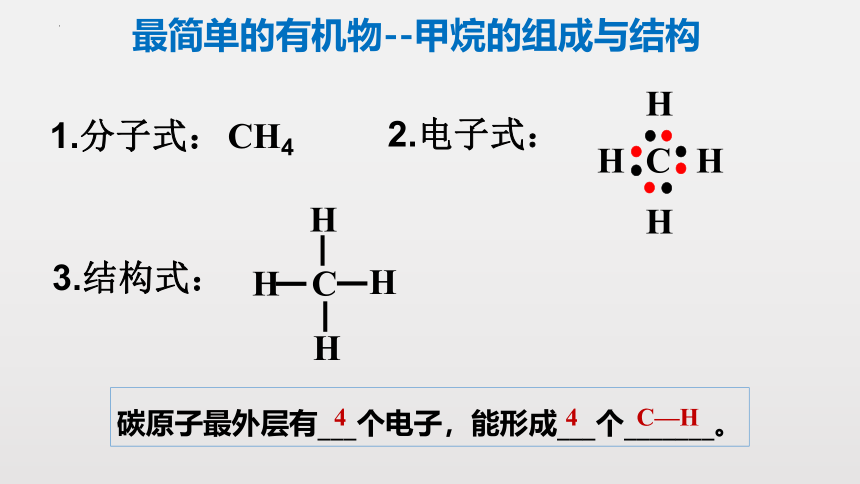
最简单的有机物--甲烷的组成与结构
1.分子式:
CH4
2.电子式:
H
H
H
C
H
3.结构式:
C
H
H
H
H
碳原子最外层有___个电子,能形成___个_______。
4
4
C—H
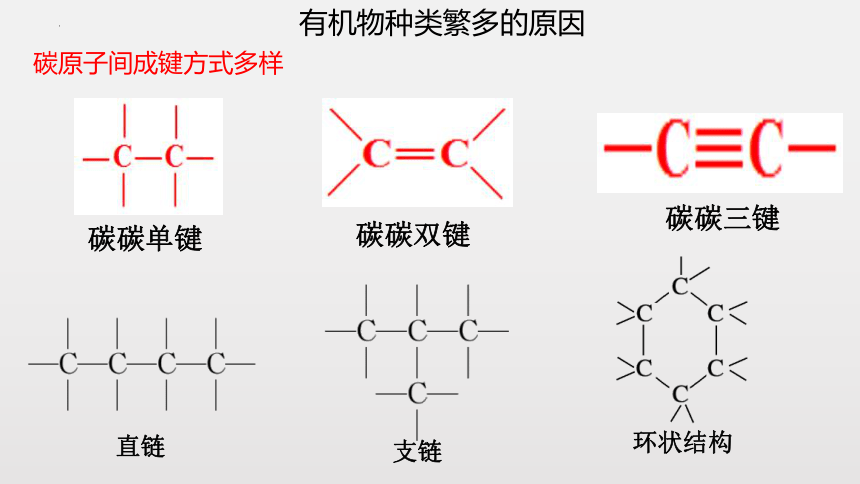
有机物种类繁多的原因
碳原子间成键方式多样
碳碳单键
碳碳双键
碳碳三键
直链
支链
环状结构
体会以碳为骨架的有机物种类繁多的原因
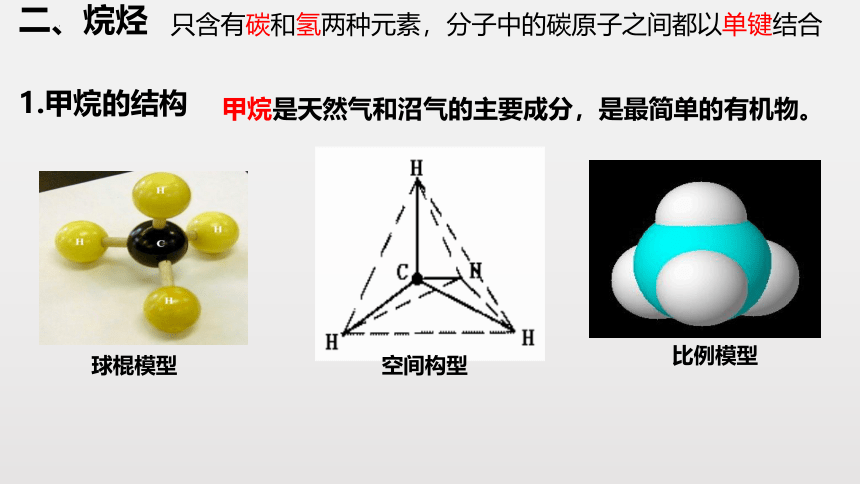
球棍模型
比例模型
二、烷烃
空间构型
1.甲烷的结构
甲烷是天然气和沼气的主要成分,是最简单的有机物。
只含有碳和氢两种元素,分子中的碳原子之间都以单键结合
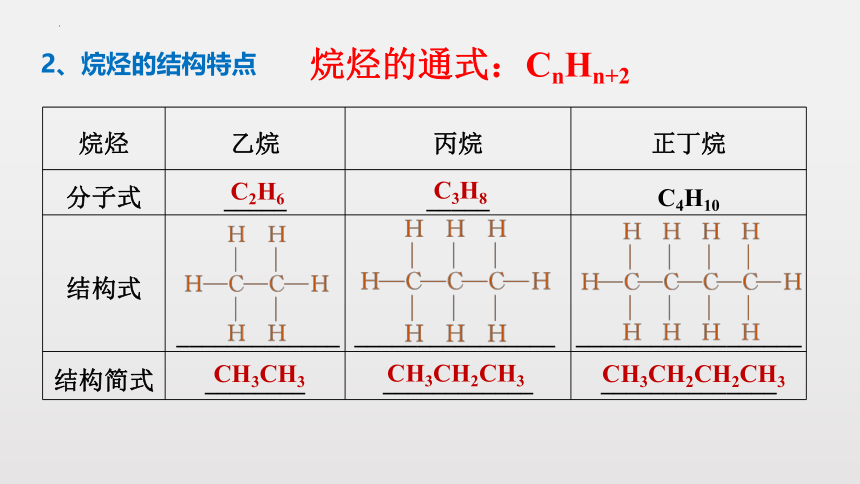
烷烃 乙烷 丙烷 正丁烷
分子式 _____ _____ C4H10
结构式 _____________ ________________
__________________
结构简式 ________ ____________ ______________
2、烷烃的结构特点
C2H6
C3H8
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
烷烃的通式:CnHn+2
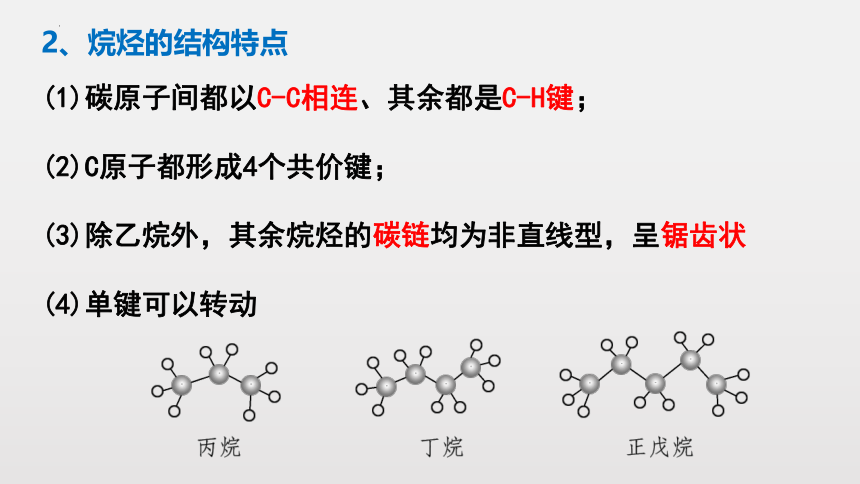
(1)碳原子间都以C-C相连、其余都是C-H键;
(2)C原子都形成4个共价键;
(3)除乙烷外,其余烷烃的碳链均为非直线型,呈锯齿状
(4)单键可以转动
2、烷烃的结构特点
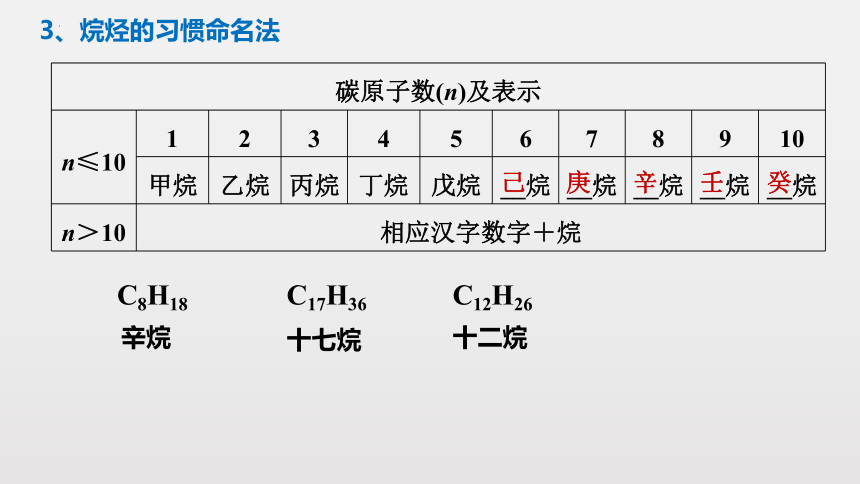
3、烷烃的习惯命名法
碳原子数(n)及表示
n≤10 1 2 3 4 5 6 7 8 9 10
甲烷 乙烷 丙烷 丁烷 戊烷 __烷 __烷 __烷 __烷 __烷
n>10 相应汉字数字+烷
己
庚
辛
壬
癸
C17H36
十七烷
C8H18
C12H26
辛烷
十二烷
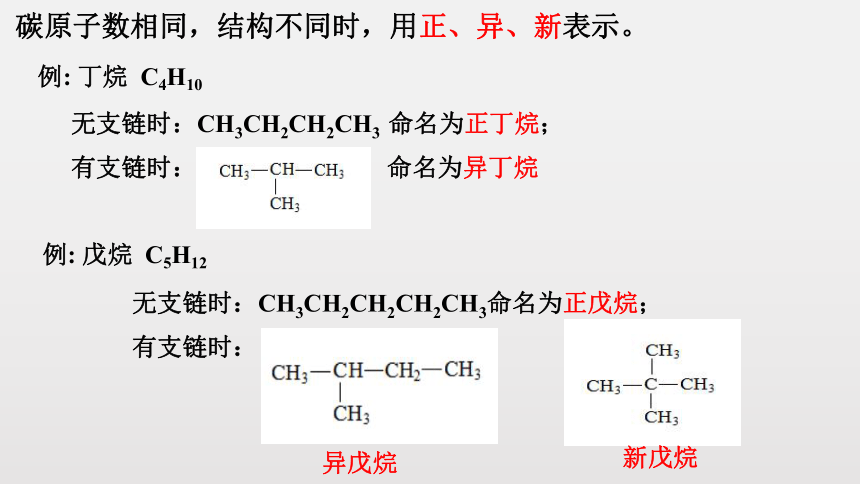
碳原子数相同,结构不同时,用正、异、新表示。
无支链时:CH3CH2CH2CH3 命名为正丁烷;
有支链时: 命名为异丁烷
例: 丁烷 C4H10
例: 戊烷 C5H12
无支链时:CH3CH2CH2CH2CH3命名为正戊烷;
新戊烷
有支链时:
异戊烷
4、同分异构体
分子式相同,结构不同
例如C5H12有3种同分异构体
正戊烷
异戊烷
新戊烷
CH3CH2CH2CH2CH3
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物。
例:CH4、C2H6、C3H8、C17H36互为同系物。
同一类物质,官能团的种类和数目一样。
结构相似,碳骨架的链接方式相同。
分子组成上差一个或多个CH2
5、同系物
E、CH3CH2CH2CH3 和 CH3CHCH3
判断:下列物质是否为同系物?
A、CH3CH3 和 CH2=CH2-CH3
C、CH3CH3 和
D、CH3CH2Br 和 CH3CH2CH2Cl
B、CH2=CH2 和
CH2
CH2
CH2
不是
不是
是
不是
不是
CH3
CH3CHCH3
CH3
3.下列有机物中和甲烷互为同系物的为____________(填序号,下同),和
CH2==CH2互为同系物的为_____,和 互为同分异构体的为___。
①CH3CH2CH3 ② ③CH2==CH—CH3
④ ⑤ ⑥
①②④
③⑥
③
A、CH3CH2CH2CH3 CH3CH(CH3)CH3
B、CH3CH3 CH3CH(CH3)CH3
C、CH3-CH=CH2 CH3=CH—CH=CH2
D、CH3-CH2—CH=CH2 CH3CH2CH2CH2CH3
4、下列哪组是同系物( )
B
5、. 下列说法中正确的一组是( )
A. 和 C(CH3)4 是同一种物质
C. 正丁烷和异丁烷是同系物
互为同分异构体
B. H2 和 D2互为同位素
D.
A
二、烷烃性质
几种烷烃的物理性质
名称 分子式 常温状态 熔点/℃ 沸点/℃ 相对密度
甲烷 CH4 气 -182 -162
乙烷 C2H6 气 -183 -89
丙烷 C3H8 气 -188 -42 0.5005
丁烷 C4H10 气 -138 0 0.5788
戊烷 C5H12 液 -130 36 0.5572
癸烷 C10H22 液 -95 69 0.7298
十六烷 C16H34 液 -91 98 0.7733
十七烷 C18H38 固 -57 126 0.7767
C5H12的三种同分异构体的结构简式
链状、无支链
链状、有支链
链状、多支链
36.07℃
27.9℃
9.5℃
结构特点
沸点
CH3CH2CH2CH2CH3
CH3CH2CHCH3
CH3
CH3-C-CH3
CH3
CH3
同分异构体,物理性质不同(支链越多沸点越低),化学性质相似。
二、烷烃性质
1、物理性质
①熔、沸点随碳原子数增加而升高,当碳原子数相同时,支链越多,熔沸点越低。
②状态:气态 液态 固态(碳原子数≤4的烷烃为气态)。
③密度:随碳原子数增加而增大,但均比水的密度小,难溶于水。
练习1. 以下物质的沸点由高到低的排列顺序是
①正丁烷 ②异丁烷 ③正戊烷 ④异戊烷 ⑤新戊烷 ⑥丙烷
。
③> ④> ⑤ >① >②> ⑥
通常情况下,烷烃比较稳定,不与强酸、强碱或高锰酸钾等强氧化剂反应。
2、烷烃的化学性质
①. 稳定性
②.可燃性— 氧化反应
例:甲烷燃烧
( 淡蓝色火焰,放大量热 )
CH4 + 2O2 CO2 + 2H2O
点燃
注意: 点燃甲烷前必须验纯否则会爆炸。
烷烃燃烧通式:
nCO2 + (n+1) H2O
点燃
③. 取代反应
以甲烷为例探究烷烃的取代反应
实验装置
实验现象 装置A:
装置B:
试管内气体颜色逐渐变浅;
内壁上有油状液体出现;
试管内液面上升;
有白雾出现;
无明显现象
实验结论:CH4与Cl2在光照时才能发生化学反应。
③. 取代反应
甲烷和氯气的取代反应
CH4
Cl2
C
H
Cl
HCl
CH3Cl
甲烷和氯气的取代反应
光照
CH4
Cl2
CH3Cl
C
H
Cl
HCl
一氯甲烷
物理性质:气态(g)、难溶于水
③. 取代反应
在光照条件下,烷烃与Cl2、Br2等卤素单质发生取代反应(与氯水、溴水不反应)。
特点:
下一上一、有进有出
③. 取代反应
注意:产物最多的为HCl,烷烃中的一个H消耗1个Cl2
(1) CH4+Cl2 CH3Cl+HCl
(一氯甲烷)
光
(2) CH3Cl+Cl2 CH2Cl2+HCl
(二氯甲烷)
光
(4) CHCl3+Cl2 CCl4+HCl
(四氯化碳)
光
(3) CH2Cl2+Cl2 CHCl3+HCl
(三氯甲烷)
光
甲烷的各种氯代物比较:
一氯甲烷 二氯甲烷 三氯甲烷 四氯甲烷
俗 名 —— ——
分子式
状 态
用 途
氯仿
四氯化碳
CH3Cl
CH2Cl2
CHCl3
CCl4
气态
液态
液态
液态
局部麻
醉剂
溶剂
溶剂、
全身麻醉剂
溶剂、
灭火剂
A.CH2Cl2 + Br2 CHBrCl2 + HBr
B.CH3OH + HCl CH3Cl + H2O
C.2Na + 2H2O === 2NaOH + H2↑
D.CH3-CH2-Br + H2O CH3-CH2-OH + HBr
光照
光照
练习1.下列化学反应中不属于取代反应的是( )
C
B
C
认识有机化合物
第七章 有机化合物
第一节
知道有机化合物的键线式。
2
知道什么是有机化合物。
1
知道烷烃的结构。
3
会对有机物进行简单的命名
4
掌握同分异构体的概念
5
讨论:有机物的定义?
一、有机化合物中碳原子的成键特点
1.有机物的定义
大多数含有碳元素的化合物为有机物化合物,简称有机物。
( 但CO、CO2、H2CO3及其盐、氰化物、硫氰化物等看作无机物。)
最简单的有机物--甲烷的组成与结构
1.分子式:
CH4
2.电子式:
H
H
H
C
H
3.结构式:
C
H
H
H
H
碳原子最外层有___个电子,能形成___个_______。
4
4
C—H
有机物种类繁多的原因
碳原子间成键方式多样
碳碳单键
碳碳双键
碳碳三键
直链
支链
环状结构
体会以碳为骨架的有机物种类繁多的原因
球棍模型
比例模型
二、烷烃
空间构型
1.甲烷的结构
甲烷是天然气和沼气的主要成分,是最简单的有机物。
只含有碳和氢两种元素,分子中的碳原子之间都以单键结合
烷烃 乙烷 丙烷 正丁烷
分子式 _____ _____ C4H10
结构式 _____________ ________________
__________________
结构简式 ________ ____________ ______________
2、烷烃的结构特点
C2H6
C3H8
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
烷烃的通式:CnHn+2
(1)碳原子间都以C-C相连、其余都是C-H键;
(2)C原子都形成4个共价键;
(3)除乙烷外,其余烷烃的碳链均为非直线型,呈锯齿状
(4)单键可以转动
2、烷烃的结构特点
3、烷烃的习惯命名法
碳原子数(n)及表示
n≤10 1 2 3 4 5 6 7 8 9 10
甲烷 乙烷 丙烷 丁烷 戊烷 __烷 __烷 __烷 __烷 __烷
n>10 相应汉字数字+烷
己
庚
辛
壬
癸
C17H36
十七烷
C8H18
C12H26
辛烷
十二烷
碳原子数相同,结构不同时,用正、异、新表示。
无支链时:CH3CH2CH2CH3 命名为正丁烷;
有支链时: 命名为异丁烷
例: 丁烷 C4H10
例: 戊烷 C5H12
无支链时:CH3CH2CH2CH2CH3命名为正戊烷;
新戊烷
有支链时:
异戊烷
4、同分异构体
分子式相同,结构不同
例如C5H12有3种同分异构体
正戊烷
异戊烷
新戊烷
CH3CH2CH2CH2CH3
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物。
例:CH4、C2H6、C3H8、C17H36互为同系物。
同一类物质,官能团的种类和数目一样。
结构相似,碳骨架的链接方式相同。
分子组成上差一个或多个CH2
5、同系物
E、CH3CH2CH2CH3 和 CH3CHCH3
判断:下列物质是否为同系物?
A、CH3CH3 和 CH2=CH2-CH3
C、CH3CH3 和
D、CH3CH2Br 和 CH3CH2CH2Cl
B、CH2=CH2 和
CH2
CH2
CH2
不是
不是
是
不是
不是
CH3
CH3CHCH3
CH3
3.下列有机物中和甲烷互为同系物的为____________(填序号,下同),和
CH2==CH2互为同系物的为_____,和 互为同分异构体的为___。
①CH3CH2CH3 ② ③CH2==CH—CH3
④ ⑤ ⑥
①②④
③⑥
③
A、CH3CH2CH2CH3 CH3CH(CH3)CH3
B、CH3CH3 CH3CH(CH3)CH3
C、CH3-CH=CH2 CH3=CH—CH=CH2
D、CH3-CH2—CH=CH2 CH3CH2CH2CH2CH3
4、下列哪组是同系物( )
B
5、. 下列说法中正确的一组是( )
A. 和 C(CH3)4 是同一种物质
C. 正丁烷和异丁烷是同系物
互为同分异构体
B. H2 和 D2互为同位素
D.
A
二、烷烃性质
几种烷烃的物理性质
名称 分子式 常温状态 熔点/℃ 沸点/℃ 相对密度
甲烷 CH4 气 -182 -162
乙烷 C2H6 气 -183 -89
丙烷 C3H8 气 -188 -42 0.5005
丁烷 C4H10 气 -138 0 0.5788
戊烷 C5H12 液 -130 36 0.5572
癸烷 C10H22 液 -95 69 0.7298
十六烷 C16H34 液 -91 98 0.7733
十七烷 C18H38 固 -57 126 0.7767
C5H12的三种同分异构体的结构简式
链状、无支链
链状、有支链
链状、多支链
36.07℃
27.9℃
9.5℃
结构特点
沸点
CH3CH2CH2CH2CH3
CH3CH2CHCH3
CH3
CH3-C-CH3
CH3
CH3
同分异构体,物理性质不同(支链越多沸点越低),化学性质相似。
二、烷烃性质
1、物理性质
①熔、沸点随碳原子数增加而升高,当碳原子数相同时,支链越多,熔沸点越低。
②状态:气态 液态 固态(碳原子数≤4的烷烃为气态)。
③密度:随碳原子数增加而增大,但均比水的密度小,难溶于水。
练习1. 以下物质的沸点由高到低的排列顺序是
①正丁烷 ②异丁烷 ③正戊烷 ④异戊烷 ⑤新戊烷 ⑥丙烷
。
③> ④> ⑤ >① >②> ⑥
通常情况下,烷烃比较稳定,不与强酸、强碱或高锰酸钾等强氧化剂反应。
2、烷烃的化学性质
①. 稳定性
②.可燃性— 氧化反应
例:甲烷燃烧
( 淡蓝色火焰,放大量热 )
CH4 + 2O2 CO2 + 2H2O
点燃
注意: 点燃甲烷前必须验纯否则会爆炸。
烷烃燃烧通式:
nCO2 + (n+1) H2O
点燃
③. 取代反应
以甲烷为例探究烷烃的取代反应
实验装置
实验现象 装置A:
装置B:
试管内气体颜色逐渐变浅;
内壁上有油状液体出现;
试管内液面上升;
有白雾出现;
无明显现象
实验结论:CH4与Cl2在光照时才能发生化学反应。
③. 取代反应
甲烷和氯气的取代反应
CH4
Cl2
C
H
Cl
HCl
CH3Cl
甲烷和氯气的取代反应
光照
CH4
Cl2
CH3Cl
C
H
Cl
HCl
一氯甲烷
物理性质:气态(g)、难溶于水
③. 取代反应
在光照条件下,烷烃与Cl2、Br2等卤素单质发生取代反应(与氯水、溴水不反应)。
特点:
下一上一、有进有出
③. 取代反应
注意:产物最多的为HCl,烷烃中的一个H消耗1个Cl2
(1) CH4+Cl2 CH3Cl+HCl
(一氯甲烷)
光
(2) CH3Cl+Cl2 CH2Cl2+HCl
(二氯甲烷)
光
(4) CHCl3+Cl2 CCl4+HCl
(四氯化碳)
光
(3) CH2Cl2+Cl2 CHCl3+HCl
(三氯甲烷)
光
甲烷的各种氯代物比较:
一氯甲烷 二氯甲烷 三氯甲烷 四氯甲烷
俗 名 —— ——
分子式
状 态
用 途
氯仿
四氯化碳
CH3Cl
CH2Cl2
CHCl3
CCl4
气态
液态
液态
液态
局部麻
醉剂
溶剂
溶剂、
全身麻醉剂
溶剂、
灭火剂
A.CH2Cl2 + Br2 CHBrCl2 + HBr
B.CH3OH + HCl CH3Cl + H2O
C.2Na + 2H2O === 2NaOH + H2↑
D.CH3-CH2-Br + H2O CH3-CH2-OH + HBr
光照
光照
练习1.下列化学反应中不属于取代反应的是( )
C
B
C
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
