第三单元 物质构成的奥秘 单元过关测试题 九年级化学人教版上册 (word版 有答案)
文档属性
| 名称 | 第三单元 物质构成的奥秘 单元过关测试题 九年级化学人教版上册 (word版 有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 190.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-22 00:00:00 | ||
图片预览



文档简介
第三单元 物质构成的奥秘 单元过关测试题
一、单选题
1.下表是生物细胞中的部分元素及其组成,其中属于金属元素的是
选项 元素符号 质量分数
A N 3%
B P 1%
C K 0.35%
D S 0.25%
A.A B.B C.C D.D
2.化学符号具有独特的学科内涵。下列各项对相关符号含义的说法正确的是
A.2H2O2:只能表示2个过氧化氢分子
B.:只能表示硫酸根离子
C.只能表示氩原子的结构示意图:
D.Ag:只能表示金属银
3.推理是学习化学的一种重要方法,必须严谨、科学。下列推理正确的是
A.溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
B.同种元素的原子具有相同的质子数,所以具有相同质子数的原子属于同种元素
C.燃烧都伴有发光、放热现象,所以有发光、放热现象的一定是燃烧
D.单质是由同种元素组成的物质,所以由同种元素组成的物质一定是单质
4.宏观辨识与微观探析是化学学科的核心素养之一、下列宏观事实的微观解释错误的是
A.自然界中水的天然循环一水分子不断运动的结果
B.氧气经压缩储存在钢瓶中一氧气分子体积变小了
C.一滴水中大约含有1.67×1021个水分子一水分子很小
D.氧气和液氧都能支持燃烧一物质的分子相同,其化学性质相同
5. 元素在元素周期表中的相关信息如图所示。下列关于该元素说法错误的是
A.元素符号为Bh B.原子的中子数为270
C.属于金属元素 D.原子序数为107
6.钛和钛合金被认为是21世纪的重要金属材料。下图是钛元素在元素周期表中的部分信息,下列说法正确的是
A.钛原子的电子数为22 B.钛为非金属元素
C.钛原子的中子数为22 D.钛原子的相对原子质量为47.87g
7.“结构决定性质”是化学的核心观念。下列有关钠原子结构与性质的说法错误的是
A.钠原子次外层有8个电子 B.一个钠原子变成钠离子失去1个电子
C.钠离子的结构示意图为 D.钠呈+1价与钠原子的最外层电子有关
8.拉瓦锡在研究空气成分时,将氧化汞(HgO)收集后加强热,反应的微观示意图如下。下列说法错误的是
A.该反应的基本反应类型为分解反应 B.该反应的化学方程式为
C.该反应中,分子的种类发生了变化 D.分子和原子均可构成物质
9.人体中有50多种元素,含量如图。下列说法正确的是
A.人体中氢元素含量约为10%
B.含量最高的金属元素是钠
C.人体中微量元素共有10种
D.缺铁会引起骨质疏松
10.荷叶中含有的荷叶碱(化学式为C19H21NO2)具有降脂、抑菌等作用。下列有关荷叶碱的说法,正确的是
A.含有O2 B.由四种非金属元素组成
C.属于氧化物 D.其中氢元素的质量分数最大
11.下列粒子结构示意图中,表示阳离子的是
A. B. C. D.
12.构建化学基本观念是学好化学的基础。下列对化学基本观念的认识中,不正确的是
A.微粒观:过氧化氢是由氢分子和氧分子构成的
B.元素观:过氧化氢和水都是由氢元素和氧元素组成的
C.结构观:过氧化氢和水的化学性质不同是因为两者的分子构成不同
D.转化观:过氧化氢在一定条件下可以转化为水
13.一个碳-12原子的实际质量是mg,钙的相对原子质量是40,则一个钙原子的实际质量是
A.10g B. C.10 m g D.
14.下列关于空气的说法中正确的是
A.空气是由空气分子组成的
B.空气里氮气、氧气等分子均匀地混合在一起
C.空气中的氮气、氧气经混合,它们的化学性质都已改变
D.经过液化、蒸发从空气中得到氧气和氮气的过程,属于化学变化
二、填空题
15.下表是几种常见原子的原子结构,请完成表格中的空白
原子种类 质子数 中子数 核外电子数 相对原子质量
钠 11 12 ________ 23
碳 ________ ________ 6 12
硫 16 16 ________ ________
钙 20 ________ ________ 40
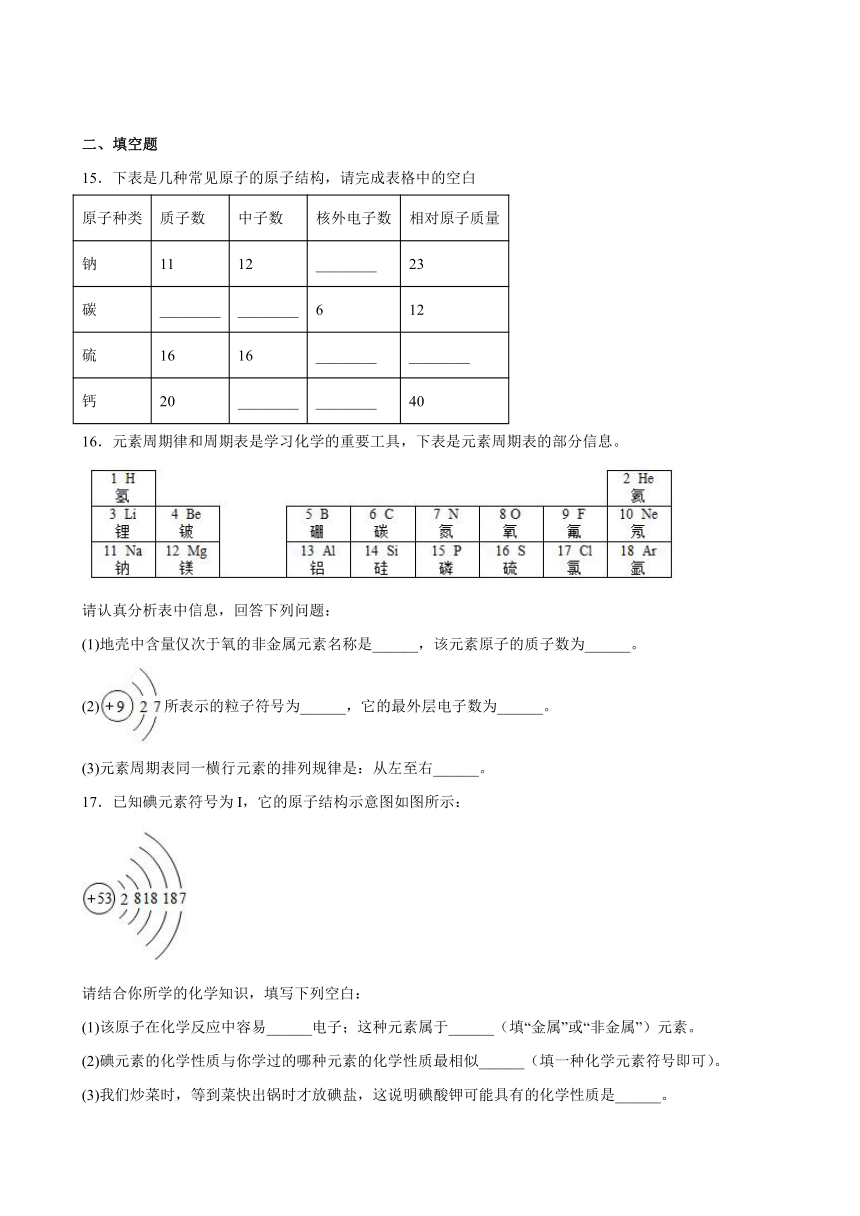
16.元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是______,该元素原子的质子数为______。
(2)所表示的粒子符号为______,它的最外层电子数为______。
(3)元素周期表同一横行元素的排列规律是:从左至右______。
17.已知碘元素符号为I,它的原子结构示意图如图所示:
请结合你所学的化学知识,填写下列空白:
(1)该原子在化学反应中容易______电子;这种元素属于______(填“金属”或“非金属”)元素。
(2)碘元素的化学性质与你学过的哪种元素的化学性质最相似______(填一种化学元素符号即可)。
(3)我们炒菜时,等到菜快出锅时才放碘盐,这说明碘酸钾可能具有的化学性质是______。
18.某粒子(原子或离子)的结构示意图如右,请回答下列问题:
(1)若m=11和n=1,则该粒子为______(填“原子”、“阳离子”或“阴离子”);
(2)若该粒子带两个单位负电荷,且n=8,则该粒子的符号为______;
(3)若m-n<10,则该粒子是一个______(填“原子”、“阳离子”或“阴离子”)。
19.观察如图,你可以得出的信息有
(1)______;
(2)______;
(3)______;
(4)______。
三、计算题
20.已知碳12原子的质量为1.993×10-26 kg,若A 原子的质量为4.5539×10-26 kg,且A原子核内质子数比中子数少1个。求: ①A原子的相对原子质量。(结果为整数) ②A原子的核外电子数
21.若1个A原子的质量为akg,1个碳12原子(含有6个质子和6个中子的碳原子)的质量为bkg.请计算:
(1)A原子的相对原子质量为__________.
(2)1个碳12原子的核外电子数为________.
22.实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的______都没有发生变化;
(2)反应生成氧气的质量为________g。
(3)参加反应过氧化氢溶液的质量分数是____________
参考答案:
1.C
2.A
3.B
4.B
5.B
6.A
7.C
8.B
9.A
10.B
11.A
12.A
13.B
14.B
15. 11 6 6 16 32 20 20
16.(1) 硅 14
(2) F 7
(3)最外层电子数依次增加1
17.(1) 得到 非金属元素
(2)Cl
(3)不稳定性
18.(1)原子
(2)S2-
(3)阴离子
19.(1)苯分子很小
(2)苯分子是真实存在的
(3)苯分子之间有间隔
(4)苯是由苯分子构成的
20.①27 ②13
21.(1)(2)6
22.(1)质量和化学性质(2)1.6(3)5%
一、单选题
1.下表是生物细胞中的部分元素及其组成,其中属于金属元素的是
选项 元素符号 质量分数
A N 3%
B P 1%
C K 0.35%
D S 0.25%
A.A B.B C.C D.D
2.化学符号具有独特的学科内涵。下列各项对相关符号含义的说法正确的是
A.2H2O2:只能表示2个过氧化氢分子
B.:只能表示硫酸根离子
C.只能表示氩原子的结构示意图:
D.Ag:只能表示金属银
3.推理是学习化学的一种重要方法,必须严谨、科学。下列推理正确的是
A.溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
B.同种元素的原子具有相同的质子数,所以具有相同质子数的原子属于同种元素
C.燃烧都伴有发光、放热现象,所以有发光、放热现象的一定是燃烧
D.单质是由同种元素组成的物质,所以由同种元素组成的物质一定是单质
4.宏观辨识与微观探析是化学学科的核心素养之一、下列宏观事实的微观解释错误的是
A.自然界中水的天然循环一水分子不断运动的结果
B.氧气经压缩储存在钢瓶中一氧气分子体积变小了
C.一滴水中大约含有1.67×1021个水分子一水分子很小
D.氧气和液氧都能支持燃烧一物质的分子相同,其化学性质相同
5. 元素在元素周期表中的相关信息如图所示。下列关于该元素说法错误的是
A.元素符号为Bh B.原子的中子数为270
C.属于金属元素 D.原子序数为107
6.钛和钛合金被认为是21世纪的重要金属材料。下图是钛元素在元素周期表中的部分信息,下列说法正确的是
A.钛原子的电子数为22 B.钛为非金属元素
C.钛原子的中子数为22 D.钛原子的相对原子质量为47.87g
7.“结构决定性质”是化学的核心观念。下列有关钠原子结构与性质的说法错误的是
A.钠原子次外层有8个电子 B.一个钠原子变成钠离子失去1个电子
C.钠离子的结构示意图为 D.钠呈+1价与钠原子的最外层电子有关
8.拉瓦锡在研究空气成分时,将氧化汞(HgO)收集后加强热,反应的微观示意图如下。下列说法错误的是
A.该反应的基本反应类型为分解反应 B.该反应的化学方程式为
C.该反应中,分子的种类发生了变化 D.分子和原子均可构成物质
9.人体中有50多种元素,含量如图。下列说法正确的是
A.人体中氢元素含量约为10%
B.含量最高的金属元素是钠
C.人体中微量元素共有10种
D.缺铁会引起骨质疏松
10.荷叶中含有的荷叶碱(化学式为C19H21NO2)具有降脂、抑菌等作用。下列有关荷叶碱的说法,正确的是
A.含有O2 B.由四种非金属元素组成
C.属于氧化物 D.其中氢元素的质量分数最大
11.下列粒子结构示意图中,表示阳离子的是
A. B. C. D.
12.构建化学基本观念是学好化学的基础。下列对化学基本观念的认识中,不正确的是
A.微粒观:过氧化氢是由氢分子和氧分子构成的
B.元素观:过氧化氢和水都是由氢元素和氧元素组成的
C.结构观:过氧化氢和水的化学性质不同是因为两者的分子构成不同
D.转化观:过氧化氢在一定条件下可以转化为水
13.一个碳-12原子的实际质量是mg,钙的相对原子质量是40,则一个钙原子的实际质量是
A.10g B. C.10 m g D.
14.下列关于空气的说法中正确的是
A.空气是由空气分子组成的
B.空气里氮气、氧气等分子均匀地混合在一起
C.空气中的氮气、氧气经混合,它们的化学性质都已改变
D.经过液化、蒸发从空气中得到氧气和氮气的过程,属于化学变化
二、填空题
15.下表是几种常见原子的原子结构,请完成表格中的空白
原子种类 质子数 中子数 核外电子数 相对原子质量
钠 11 12 ________ 23
碳 ________ ________ 6 12
硫 16 16 ________ ________
钙 20 ________ ________ 40
16.元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是______,该元素原子的质子数为______。
(2)所表示的粒子符号为______,它的最外层电子数为______。
(3)元素周期表同一横行元素的排列规律是:从左至右______。
17.已知碘元素符号为I,它的原子结构示意图如图所示:
请结合你所学的化学知识,填写下列空白:
(1)该原子在化学反应中容易______电子;这种元素属于______(填“金属”或“非金属”)元素。
(2)碘元素的化学性质与你学过的哪种元素的化学性质最相似______(填一种化学元素符号即可)。
(3)我们炒菜时,等到菜快出锅时才放碘盐,这说明碘酸钾可能具有的化学性质是______。
18.某粒子(原子或离子)的结构示意图如右,请回答下列问题:
(1)若m=11和n=1,则该粒子为______(填“原子”、“阳离子”或“阴离子”);
(2)若该粒子带两个单位负电荷,且n=8,则该粒子的符号为______;
(3)若m-n<10,则该粒子是一个______(填“原子”、“阳离子”或“阴离子”)。
19.观察如图,你可以得出的信息有
(1)______;
(2)______;
(3)______;
(4)______。
三、计算题
20.已知碳12原子的质量为1.993×10-26 kg,若A 原子的质量为4.5539×10-26 kg,且A原子核内质子数比中子数少1个。求: ①A原子的相对原子质量。(结果为整数) ②A原子的核外电子数
21.若1个A原子的质量为akg,1个碳12原子(含有6个质子和6个中子的碳原子)的质量为bkg.请计算:
(1)A原子的相对原子质量为__________.
(2)1个碳12原子的核外电子数为________.
22.实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的______都没有发生变化;
(2)反应生成氧气的质量为________g。
(3)参加反应过氧化氢溶液的质量分数是____________
参考答案:
1.C
2.A
3.B
4.B
5.B
6.A
7.C
8.B
9.A
10.B
11.A
12.A
13.B
14.B
15. 11 6 6 16 32 20 20
16.(1) 硅 14
(2) F 7
(3)最外层电子数依次增加1
17.(1) 得到 非金属元素
(2)Cl
(3)不稳定性
18.(1)原子
(2)S2-
(3)阴离子
19.(1)苯分子很小
(2)苯分子是真实存在的
(3)苯分子之间有间隔
(4)苯是由苯分子构成的
20.①27 ②13
21.(1)(2)6
22.(1)质量和化学性质(2)1.6(3)5%
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
