人教版选修三 2.3.1 气体的等压变化和等容变 课件(48张PPT)
文档属性
| 名称 | 人教版选修三 2.3.1 气体的等压变化和等容变 课件(48张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2022-08-23 00:00:00 | ||
图片预览










文档简介
(共48张PPT)
第二章 气体、固体和液体
2.3.1 气体的等压变化和等容变化
人教版(2019)高中物理选择性必修第三册
烧瓶上通过橡胶塞连接一根玻璃管,向玻璃管中注入一段水柱。用手捂住烧瓶,会观察到水柱缓慢向外移动,这说明了什么?
新课导入
1.等压变化:一定质量的某种气体,在压强不变时,体积随温度的变化叫做等压变化.
在等压变化中,气体的体积与温度可能存在着什么关系?
想一想
一、气体的等压变化
法国科学家盖—吕萨克通过实验发现:一定质量的某种气体,在压强不变的情况下,其体积V与热力学温度T之间呈线性关系,把它盖—吕萨克定律。
0
V
t/0C
A
B
甲
结论:当压强不太大,温度不太低时,一定质量的气体,在压强不变时,体积V和温度T成正比.
0
V
T/K
A
B
乙
273.15
气体体积为0时,温度为0
V与摄氏温度t是一次函数关系
V与热力学温度T是正比关系
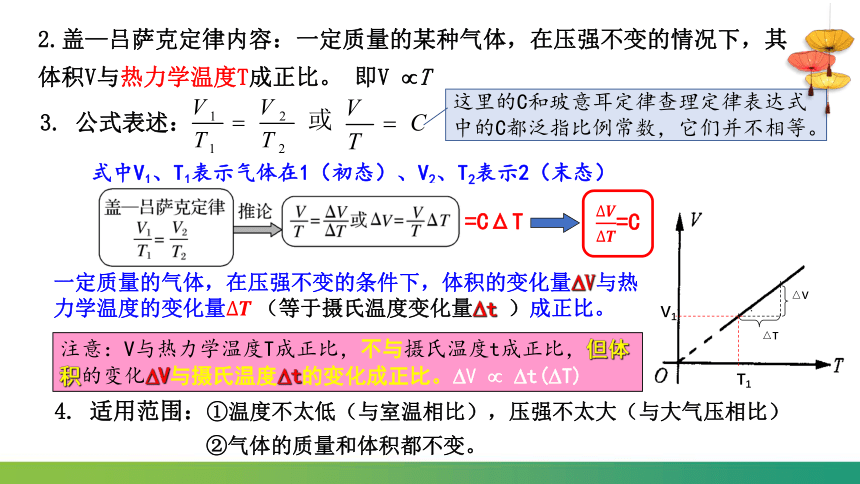
2.盖—吕萨克定律内容:一定质量的某种气体,在压强不变的情况下,其体积V与热力学温度T成正比。 即V T
式中V1、T1表示气体在1(初态)、V2、T2表示2(末态)
3. 公式表述:
这里的C和玻意耳定律查理定律表达式中的C都泛指比例常数,它们并不相等。
4. 适用范围:①温度不太低(与室温相比),压强不太大(与大气压相比)
②气体的质量和体积都不变。
=CΔT
=C
一定质量的气体,在压强不变的条件下,体积的变化量 V与热力学温度的变化量(等于摄氏温度变化量 t )成正比。
注意:V与热力学温度T成正比,不与摄氏温度t成正比,但体积的变化 V与摄氏温度 t的变化成正比。 V t( T)
或
△V
△T
T1
V1
盖·吕萨克(UosephLollis Gay—lussac,1778—1850年)法国化学家、物理学家.
盖—吕萨克生平介绍
盖·吕萨克1778年9月6日生于圣·莱昂特。1800年毕业于巴黎理工学校. 1850年5月9日,病逝于巴黎,享年72岁.
1802年,盖·吕萨克发现气体热膨胀定律(即盖·吕萨克定律)压强不变时,一定质量气体的体积跟热力学温度成正比.即V1/T1=V2/T2=……=C恒量.
其实查理早就发现体积与温度的关系,只是当时未发表,也未被人注意。直到盖-吕萨克重新提出后,才受到重视。早年都称“查理定律”,但为表彰盖-吕萨克的贡献而称为“查理-盖吕萨克定律”.
5、图象——等压线
(1)等压线:一定质量的某种气体在等压变化过程中,体积随温度变化关系的直线,叫做等压线。
(2)等压线的特点:一定质量的气体的V—T图线其延长线过坐标原点(过原点的倾斜直线)。
答:热力学绝对零度不可能达到。
想一想:为什么O点附近用虚线?
等压线
V-t图像
V-T图像
V0
V
V
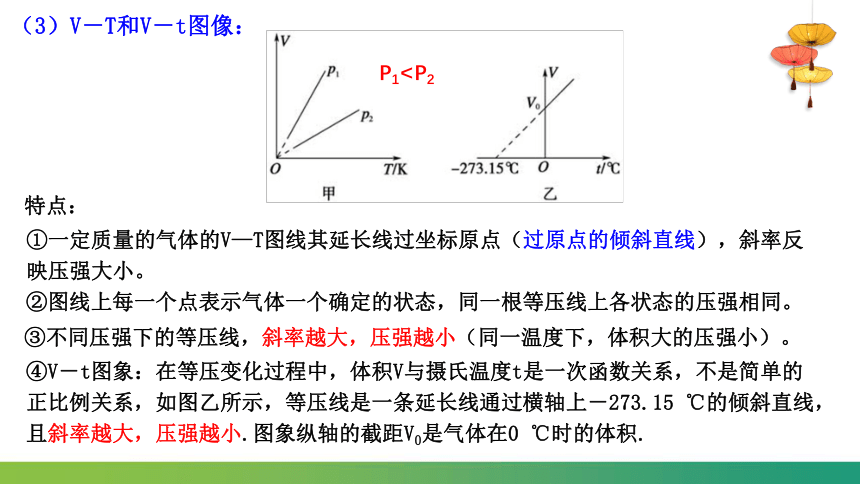
(3)V-T和V-t图像:
④V-t图象:在等压变化过程中,体积V与摄氏温度t是一次函数关系,不是简单的正比例关系,如图乙所示,等压线是一条延长线通过横轴上-273.15 ℃的倾斜直线,且斜率越大,压强越小.图象纵轴的截距V0是气体在0 ℃时的体积.
特点:
①一定质量的气体的V—T图线其延长线过坐标原点(过原点的倾斜直线),斜率反映压强大小。
②图线上每一个点表示气体一个确定的状态,同一根等压线上各状态的压强相同。
③不同压强下的等压线,斜率越大,压强越小(同一温度下,体积大的压强小)。
P1⑤盖—吕萨克定律的微观解释:
——实验定律
一定质量(m)的理想气体的总分子数(N)是一定的,要保持压强(p)不变,当温度(T)升高时,全体分子运动的平均速率V会增加,那么单位体积内的分子数(n)一定要减小(否则压强不可能不变),因此气体体积一定增大;反之当温度降低时,同理可推出气体体积一定减小。
注意:
条件中的“温度不太低(与室温相比),压强不太大(与大气压相比)”的含义: 相当于大气压几倍的压强都可以算作“压强不太大”,零下几十摄氏度的温度也可以算作“温度不太低”。
【例题1】一容器中装有某种气体,且容器上有一个小口与外界大气相通,原来容器内的温度为27℃,若把它加热到127℃,从容器中溢出的空气质量是原来质量的多少倍呢?
解析:
初态 T1=300K V1=V P1=P
分析:容器上有一个小口与外界大气相通,即气体的压强始终等于外界大气压,气体状态变化可以看作是等压变化。本题解题的关键不是气体状态的确定,而是研究对象的选取。
末态 T2=400K V2=? P2=P
由盖-吕萨克定律 :
就容器而言,里面气体质量变了,但可视容器中气体出而不走,以原来容器中的气体为研究对象,就可以运用气体的等压变化规律求解。气体状态变化如图所示。
法一:
解析:
以后来容器中的气体为研究对象。气体状态变化如图所示。
法二:
【例题1】一容器中装有某种气体,且容器上有一个小口与外界大气相通,原来容器内的温度为27℃,若把它加热到127℃,从容器中溢出的空气质量是原来质量的多少倍呢?
初态 T1=400K V1=V P1=P
末态 T2=300K V2=? P2=P
由盖-吕萨克定律 :
夏天汽车轮胎打气太足,容易爆胎。
利用高压锅可以很快把饭煮熟。
轮胎和高压锅都是气体体积不变,温度升高,压强增大。
相传三国时期著名的军事家、政治家诸葛亮被司马懿困于平阳,无法派兵出城求救。就在此关键时刻,诸葛亮发明了一种可以升空的信号灯——孔明灯,并成功进行了信号联络,其后终于顺利脱险。你知道孔明灯为什么能够升空吗
简答:孔明灯是利用火焰的热量使容器内的气体膨胀,使部分气体从孔明灯内溢出,进而使孔明灯内气体的质量减少,当大气对孔明灯的浮力恰好等于孔明灯的重力时,即达到孔明灯升空的临界条件,若继续升温,孔明灯就能升空了。
1.等容变化:一定质量的某种气体,在体积不变时,压强随温度的变化叫做等容变化.
在等容变化中,气体的压强与温度可能存在着什么关系?
想一想
二、气体的等容变化
法国科学家查理在分析了实验事实后发现:当气体的体积一定时,各种气体的压强与温度之间都有线性关系,把它叫做查理定律。
0
P
t/0C
A
B
甲
结论:当压强不太大,温度不太低时,一定质量的气体,在体积不变时,压强p和温度T成正比.
0
P
T/K
A
B
乙
273.15
气体压强为0时,温度为0
P与摄氏温度t是一次函数关系
P与热力学温度T是正比关系
2.查理定律内容:一定质量的某种气体,在体积不变的情况下,压强P与热力学温度T成正比。 即p T
或
式中p1、T1表示气体在1(初态)、p2、T2表示2(末态)
3. 公式表述:
这里的C和玻意耳定律表达式中的C都泛指比例常数,它们并不相等。
4. 适用范围:①温度不太低,压强不太大
②气体的质量和体积都不变。
=CΔT
=C
一定质量的气体,在体积不变的条件下,压强的变化量与热力学温度的变化量(等于摄氏温度变化量 t )成正比。
△p
△T
T1
p1
注意:p与热力学温度T成正比,不与摄氏温度t成正比,但压强的变化 P与摄氏温度 t的变化成正比。 P t( T)
5、图象——等容线
(1)等容线:一定质量的某种气体在等容变化过程中,压强随温度变化关系的直线,叫做等容线。
p0
P-t图像
P-T图像
等容线
(2)等容线的特点:一定质量的气体的p—T图线其延长线过坐标原点(过原点的倾斜直线)。
答:热力学绝对零度不可能达到。
想一想:为什么O点附近用虚线?
P-t图象变化为P-T图象
把交点作为坐标原点,建立新的坐标系,那么,这时的压强与温度的关系就是正比例关系了。
在等容变化过程中,p-t是一次函数关系,不是简单的正比例关系。
如果把直线AB延长至与横轴相交,交点坐标是-273.150C
0
P
t
-273.15
273.15
A
B
0
P
t
A
B
0
P
A
B
-273.15
T
绝对零度
(3)p-T和p-t图像:
④p-t图象:在等容变化过程中,压强p与摄氏温度t是一次函数关系,不是简单的正比例关系,如图乙所示,等容线是一条延长线通过横轴上-273.15 ℃的倾斜直线,且斜率越大,体积越小.图象纵轴的截距p0是气体在0 ℃时的压强.
特点:
①一定质量的气体的P—T图线其延长线过坐标原点(过原点的倾斜直线),斜率反映体积大小。
②图线上每一个点表示气体一个确定的状态,同一根等容线上各状态的体积相同。
③不同体积下的等容线,斜率越大,体积越小(同一温度下,压强大的体积小)。
V1一定质量(m)的气体的总分子数(N)是一定的,体积(V)保持不变时,其单位体积内的分子数(n)也保持不变,当温度(T)升高时,其分子运动的平均速率(v)也增大,则气体压强(p)也增大;反之当温度(T)降低时,气体压强(p)也减小。
⑤查理定律的微观解释:
——实验定律
注意:
条件中的“温度不太低(与室温相比),压强不太大(与大气压相比)”的含义: 相当于大气压几倍的压强都可以算作“压强不太大”,零下几十摄氏度的温度也可以算作“温度不太低”。
6、应用
(1)高压锅内的食物易熟;
(2)打足了气的车胎在阳光下曝晒会胀破;
(3)使凹进的乒乓球恢复原状。
我国民间常用“拔火罐”来治疗某些疾病,即用一个小罐,将纸燃烧后放入罐内,然后迅速将火罐开口端紧压在人体的皮肤上,待火罐冷却后,火罐就被紧紧地“吸”在皮肤上。你知道其中的道理吗?
答案:火罐内的气体体积一定,冷却后气体的温度降低,压强减小,故在大气压力作用下被“吸”在皮肤上。
想一想
【例题】密闭在容积不变的容器中的气体,当温度降低时( )
A、压强减小,密度减小;
B、压强减小,密度增大;
C、压强不变,密度减小;
D、压强减小,密度不变
D
【例题】下列关于一定质量的气体的等容变化的说法中正确的是( )
A、气体压强的改变量与摄氏温度成正比;
B、气体的压强与摄氏温度成正比;
C、气体压强的改变量与热力学温度成正比;
D、气体的压强与热力学温度成正比。
D
【例题】某种气体在状态A时压强2×105Pa,体积为1m3,温度为200K,
(1)它在等温过程中由状态A变为状态B,状态B的体积为2m3,求状态B的压强。
(2)随后,又由状态B在等容过程中变为状态C,状态C的温度为300K,求状态C的压强。
A B C
以气体为研究对象。
解:
初态:
PA=2×105Pa
VA=1m3
末态:
PB=?
VB=2m3
等温变化,根据 pAVA=pBVB
代入得:
2×105×1=PB×2
解得:
(1)
PB=105Pa
TA=200K
TB=200K
初态:
PB=105Pa
VB=2m3
末态:
PC=?
VC=2m3
等容变化,根据
代入得:
解得:
(2)
PC=1.5×105Pa
TB=200K
TC=300K
总结:利用查理定律解题的一般步骤
(1)确定研究对象,即被封闭的气体。
(2)分析被研究气体在状态变化时是否符合定律成立的条件,即是否是质量和体积保持不变。
(3)确定初、末两个状态的温度、压强。
(4)按查理定律公式列式求解,并对结果进行讨论。
A
【例题】某种气体的压强为2×105Pa,体积为1m3,温度为200K。它经过等温过程后体积变为2m3。随后又经过等容过程,温度变为300K,求此时气体的压强?
根据查理定律,有
状态1:p1=2×105Pa,V1=1m3,T1=200K
根据玻意耳定律,有p1V1=p2V2
等温后状态2: p2= , V2=2m3,T2=200K
等容后状态3: p3= ,V3=2m3,T3=300K
可得
可得
解析:
P3=1.5×105Pa
T1=T2
V1=V2
因为
所以
即
查理定律与盖·吕萨克定律的比较
气体实验定律
玻意耳定律
查理定律
盖-吕萨克定律
压强不太大(相对大气压),温度不太低(相对室温)
这些定律的适用范围:
p1V1=p2V2
『判一判』
(1)现实生活中,自行车轮胎在烈日下暴晒,车胎内气体的变化是等容过程。
( )
(2)一定质量的气体,等容变化时,气体的压强和温度不一定成正比。
( )
(3)气体的温度升高,气体的体积一定增大。 ( )
×
√
×
×
√
×
『选一选』
(多选)(2020·安徽省淮北市第一中学高二下学期期中)在下列图中,可能反映理想气体经历了等压变化→等温变化→等容变化后,又回到原来状态的有( )
解析:由图可看出经历了“等压变化”→“等温变化”→“等容变化”后,又回到原来状态的是A、C。
AC
例.(多选)下列关于盖·吕萨克定律的说法中正确的是( )
A、对于一定质量的气体,在保持压强不变的情况下,温度每升高1℃时,其体积的增量是原来体积的1/273
B、对于一定质量的气体.在保持压强不变的情况下,温度每升高1℃时,其体积的增量是它在0℃时体积的1/273
C、对于一定质量的气体,在保持压强不变的情况下,其体积与温度成正比
D、对于一定质量的气体,在保持压强不变的情况下,其体积与热力学温度成正比
BD
【例题】如图所示,封闭有一定质量理想气体的汽缸开口向下竖直固定放置,活塞的截面积为S,质量为m0,活塞通过轻绳连接了一个质量为m的重物。若开始时汽缸内理想气体的温度为T0,轻绳刚好伸直且对活塞无拉力作用,外界大
气压强为p0,一切摩擦均不计且m0g(1)重物刚离地时汽缸内气体的压强;
(2)重物刚离地时汽缸内气体的温度。
解析:
(1)当轻绳刚好伸直且对活塞无拉力作用时,设此时汽缸内气体的压强为p1,
由力的平衡条件可得m0g+p1S=p0S 所以
当重物刚好离开地面时,设此时汽缸内气体的压强为p2,
则有p2S+(m+m0)g=p0S 所以
(2)设重物刚好离开地面时汽缸内气体的温度为T1,
此过程气体发生等容变化,由查理定律可得
解得
解析:
【例题】如图所示,两端封闭、粗细均匀、竖直放置的玻璃管内,有一长为h的水银柱,将管内气体分为两部分,已知l2=2l1。若使两部分气体同时升高相同的温度,管内水银柱将如何运动?(设原来温度相同)
水银柱原来处于平衡状态,所受合外力为零,即此时两部分气体的压强差Δp=p1-p2=ph。温度升高后,两部分气体的压强都增大,若Δp1>Δp2,水银柱所受合外力方向向上,应向上移动,若Δp1<Δp2,水银柱向下移动,若Δp1=Δp2,水银柱不动。所以判断水银柱怎样移动,就是分析其合外力方向,即判断两部分气体的压强哪一个增大得多。
假设水银柱不动,两部分气体都做等容变化,分别对两部分气体应用查理定律:
上段
同理,下段
所以Δp1>Δp2,即水银柱上移。
例.如图所示,气缸内封闭有一定质量的理想气体,当时温度为0℃,大气压为1atm(设其值为105Pa)、气缸横截面积为500cm2,活塞重为5000N。则:
(1)气缸内气体压强为多少?
(2)如果开始时内部被封闭气体的总体积为 汽缸上部体积为 ,并且汽缸口有个卡环可以卡住活塞,使之只能在汽缸内运动,所有摩擦不计。现在使气缸内的气体加热至273℃,求气缸内气体压强又为多少?
30°
解:
(1)由受力平衡可知:
(2)缸内气体先做等压变化,活塞将运动到卡环处就不再运动,设此时温度为T1 ,有
所以
接下来继续升温,气缸内气体将做等体积变化,设所求压强为p2,故有
代入可得
30°
第二章 气体、固体和液体
2.3.1 气体的等压变化和等容变化
人教版(2019)高中物理选择性必修第三册
烧瓶上通过橡胶塞连接一根玻璃管,向玻璃管中注入一段水柱。用手捂住烧瓶,会观察到水柱缓慢向外移动,这说明了什么?
新课导入
1.等压变化:一定质量的某种气体,在压强不变时,体积随温度的变化叫做等压变化.
在等压变化中,气体的体积与温度可能存在着什么关系?
想一想
一、气体的等压变化
法国科学家盖—吕萨克通过实验发现:一定质量的某种气体,在压强不变的情况下,其体积V与热力学温度T之间呈线性关系,把它盖—吕萨克定律。
0
V
t/0C
A
B
甲
结论:当压强不太大,温度不太低时,一定质量的气体,在压强不变时,体积V和温度T成正比.
0
V
T/K
A
B
乙
273.15
气体体积为0时,温度为0
V与摄氏温度t是一次函数关系
V与热力学温度T是正比关系
2.盖—吕萨克定律内容:一定质量的某种气体,在压强不变的情况下,其体积V与热力学温度T成正比。 即V T
式中V1、T1表示气体在1(初态)、V2、T2表示2(末态)
3. 公式表述:
这里的C和玻意耳定律查理定律表达式中的C都泛指比例常数,它们并不相等。
4. 适用范围:①温度不太低(与室温相比),压强不太大(与大气压相比)
②气体的质量和体积都不变。
=CΔT
=C
一定质量的气体,在压强不变的条件下,体积的变化量 V与热力学温度的变化量(等于摄氏温度变化量 t )成正比。
注意:V与热力学温度T成正比,不与摄氏温度t成正比,但体积的变化 V与摄氏温度 t的变化成正比。 V t( T)
或
△V
△T
T1
V1
盖·吕萨克(UosephLollis Gay—lussac,1778—1850年)法国化学家、物理学家.
盖—吕萨克生平介绍
盖·吕萨克1778年9月6日生于圣·莱昂特。1800年毕业于巴黎理工学校. 1850年5月9日,病逝于巴黎,享年72岁.
1802年,盖·吕萨克发现气体热膨胀定律(即盖·吕萨克定律)压强不变时,一定质量气体的体积跟热力学温度成正比.即V1/T1=V2/T2=……=C恒量.
其实查理早就发现体积与温度的关系,只是当时未发表,也未被人注意。直到盖-吕萨克重新提出后,才受到重视。早年都称“查理定律”,但为表彰盖-吕萨克的贡献而称为“查理-盖吕萨克定律”.
5、图象——等压线
(1)等压线:一定质量的某种气体在等压变化过程中,体积随温度变化关系的直线,叫做等压线。
(2)等压线的特点:一定质量的气体的V—T图线其延长线过坐标原点(过原点的倾斜直线)。
答:热力学绝对零度不可能达到。
想一想:为什么O点附近用虚线?
等压线
V-t图像
V-T图像
V0
V
V
(3)V-T和V-t图像:
④V-t图象:在等压变化过程中,体积V与摄氏温度t是一次函数关系,不是简单的正比例关系,如图乙所示,等压线是一条延长线通过横轴上-273.15 ℃的倾斜直线,且斜率越大,压强越小.图象纵轴的截距V0是气体在0 ℃时的体积.
特点:
①一定质量的气体的V—T图线其延长线过坐标原点(过原点的倾斜直线),斜率反映压强大小。
②图线上每一个点表示气体一个确定的状态,同一根等压线上各状态的压强相同。
③不同压强下的等压线,斜率越大,压强越小(同一温度下,体积大的压强小)。
P1
——实验定律
一定质量(m)的理想气体的总分子数(N)是一定的,要保持压强(p)不变,当温度(T)升高时,全体分子运动的平均速率V会增加,那么单位体积内的分子数(n)一定要减小(否则压强不可能不变),因此气体体积一定增大;反之当温度降低时,同理可推出气体体积一定减小。
注意:
条件中的“温度不太低(与室温相比),压强不太大(与大气压相比)”的含义: 相当于大气压几倍的压强都可以算作“压强不太大”,零下几十摄氏度的温度也可以算作“温度不太低”。
【例题1】一容器中装有某种气体,且容器上有一个小口与外界大气相通,原来容器内的温度为27℃,若把它加热到127℃,从容器中溢出的空气质量是原来质量的多少倍呢?
解析:
初态 T1=300K V1=V P1=P
分析:容器上有一个小口与外界大气相通,即气体的压强始终等于外界大气压,气体状态变化可以看作是等压变化。本题解题的关键不是气体状态的确定,而是研究对象的选取。
末态 T2=400K V2=? P2=P
由盖-吕萨克定律 :
就容器而言,里面气体质量变了,但可视容器中气体出而不走,以原来容器中的气体为研究对象,就可以运用气体的等压变化规律求解。气体状态变化如图所示。
法一:
解析:
以后来容器中的气体为研究对象。气体状态变化如图所示。
法二:
【例题1】一容器中装有某种气体,且容器上有一个小口与外界大气相通,原来容器内的温度为27℃,若把它加热到127℃,从容器中溢出的空气质量是原来质量的多少倍呢?
初态 T1=400K V1=V P1=P
末态 T2=300K V2=? P2=P
由盖-吕萨克定律 :
夏天汽车轮胎打气太足,容易爆胎。
利用高压锅可以很快把饭煮熟。
轮胎和高压锅都是气体体积不变,温度升高,压强增大。
相传三国时期著名的军事家、政治家诸葛亮被司马懿困于平阳,无法派兵出城求救。就在此关键时刻,诸葛亮发明了一种可以升空的信号灯——孔明灯,并成功进行了信号联络,其后终于顺利脱险。你知道孔明灯为什么能够升空吗
简答:孔明灯是利用火焰的热量使容器内的气体膨胀,使部分气体从孔明灯内溢出,进而使孔明灯内气体的质量减少,当大气对孔明灯的浮力恰好等于孔明灯的重力时,即达到孔明灯升空的临界条件,若继续升温,孔明灯就能升空了。
1.等容变化:一定质量的某种气体,在体积不变时,压强随温度的变化叫做等容变化.
在等容变化中,气体的压强与温度可能存在着什么关系?
想一想
二、气体的等容变化
法国科学家查理在分析了实验事实后发现:当气体的体积一定时,各种气体的压强与温度之间都有线性关系,把它叫做查理定律。
0
P
t/0C
A
B
甲
结论:当压强不太大,温度不太低时,一定质量的气体,在体积不变时,压强p和温度T成正比.
0
P
T/K
A
B
乙
273.15
气体压强为0时,温度为0
P与摄氏温度t是一次函数关系
P与热力学温度T是正比关系
2.查理定律内容:一定质量的某种气体,在体积不变的情况下,压强P与热力学温度T成正比。 即p T
或
式中p1、T1表示气体在1(初态)、p2、T2表示2(末态)
3. 公式表述:
这里的C和玻意耳定律表达式中的C都泛指比例常数,它们并不相等。
4. 适用范围:①温度不太低,压强不太大
②气体的质量和体积都不变。
=CΔT
=C
一定质量的气体,在体积不变的条件下,压强的变化量与热力学温度的变化量(等于摄氏温度变化量 t )成正比。
△p
△T
T1
p1
注意:p与热力学温度T成正比,不与摄氏温度t成正比,但压强的变化 P与摄氏温度 t的变化成正比。 P t( T)
5、图象——等容线
(1)等容线:一定质量的某种气体在等容变化过程中,压强随温度变化关系的直线,叫做等容线。
p0
P-t图像
P-T图像
等容线
(2)等容线的特点:一定质量的气体的p—T图线其延长线过坐标原点(过原点的倾斜直线)。
答:热力学绝对零度不可能达到。
想一想:为什么O点附近用虚线?
P-t图象变化为P-T图象
把交点作为坐标原点,建立新的坐标系,那么,这时的压强与温度的关系就是正比例关系了。
在等容变化过程中,p-t是一次函数关系,不是简单的正比例关系。
如果把直线AB延长至与横轴相交,交点坐标是-273.150C
0
P
t
-273.15
273.15
A
B
0
P
t
A
B
0
P
A
B
-273.15
T
绝对零度
(3)p-T和p-t图像:
④p-t图象:在等容变化过程中,压强p与摄氏温度t是一次函数关系,不是简单的正比例关系,如图乙所示,等容线是一条延长线通过横轴上-273.15 ℃的倾斜直线,且斜率越大,体积越小.图象纵轴的截距p0是气体在0 ℃时的压强.
特点:
①一定质量的气体的P—T图线其延长线过坐标原点(过原点的倾斜直线),斜率反映体积大小。
②图线上每一个点表示气体一个确定的状态,同一根等容线上各状态的体积相同。
③不同体积下的等容线,斜率越大,体积越小(同一温度下,压强大的体积小)。
V1
⑤查理定律的微观解释:
——实验定律
注意:
条件中的“温度不太低(与室温相比),压强不太大(与大气压相比)”的含义: 相当于大气压几倍的压强都可以算作“压强不太大”,零下几十摄氏度的温度也可以算作“温度不太低”。
6、应用
(1)高压锅内的食物易熟;
(2)打足了气的车胎在阳光下曝晒会胀破;
(3)使凹进的乒乓球恢复原状。
我国民间常用“拔火罐”来治疗某些疾病,即用一个小罐,将纸燃烧后放入罐内,然后迅速将火罐开口端紧压在人体的皮肤上,待火罐冷却后,火罐就被紧紧地“吸”在皮肤上。你知道其中的道理吗?
答案:火罐内的气体体积一定,冷却后气体的温度降低,压强减小,故在大气压力作用下被“吸”在皮肤上。
想一想
【例题】密闭在容积不变的容器中的气体,当温度降低时( )
A、压强减小,密度减小;
B、压强减小,密度增大;
C、压强不变,密度减小;
D、压强减小,密度不变
D
【例题】下列关于一定质量的气体的等容变化的说法中正确的是( )
A、气体压强的改变量与摄氏温度成正比;
B、气体的压强与摄氏温度成正比;
C、气体压强的改变量与热力学温度成正比;
D、气体的压强与热力学温度成正比。
D
【例题】某种气体在状态A时压强2×105Pa,体积为1m3,温度为200K,
(1)它在等温过程中由状态A变为状态B,状态B的体积为2m3,求状态B的压强。
(2)随后,又由状态B在等容过程中变为状态C,状态C的温度为300K,求状态C的压强。
A B C
以气体为研究对象。
解:
初态:
PA=2×105Pa
VA=1m3
末态:
PB=?
VB=2m3
等温变化,根据 pAVA=pBVB
代入得:
2×105×1=PB×2
解得:
(1)
PB=105Pa
TA=200K
TB=200K
初态:
PB=105Pa
VB=2m3
末态:
PC=?
VC=2m3
等容变化,根据
代入得:
解得:
(2)
PC=1.5×105Pa
TB=200K
TC=300K
总结:利用查理定律解题的一般步骤
(1)确定研究对象,即被封闭的气体。
(2)分析被研究气体在状态变化时是否符合定律成立的条件,即是否是质量和体积保持不变。
(3)确定初、末两个状态的温度、压强。
(4)按查理定律公式列式求解,并对结果进行讨论。
A
【例题】某种气体的压强为2×105Pa,体积为1m3,温度为200K。它经过等温过程后体积变为2m3。随后又经过等容过程,温度变为300K,求此时气体的压强?
根据查理定律,有
状态1:p1=2×105Pa,V1=1m3,T1=200K
根据玻意耳定律,有p1V1=p2V2
等温后状态2: p2= , V2=2m3,T2=200K
等容后状态3: p3= ,V3=2m3,T3=300K
可得
可得
解析:
P3=1.5×105Pa
T1=T2
V1=V2
因为
所以
即
查理定律与盖·吕萨克定律的比较
气体实验定律
玻意耳定律
查理定律
盖-吕萨克定律
压强不太大(相对大气压),温度不太低(相对室温)
这些定律的适用范围:
p1V1=p2V2
『判一判』
(1)现实生活中,自行车轮胎在烈日下暴晒,车胎内气体的变化是等容过程。
( )
(2)一定质量的气体,等容变化时,气体的压强和温度不一定成正比。
( )
(3)气体的温度升高,气体的体积一定增大。 ( )
×
√
×
×
√
×
『选一选』
(多选)(2020·安徽省淮北市第一中学高二下学期期中)在下列图中,可能反映理想气体经历了等压变化→等温变化→等容变化后,又回到原来状态的有( )
解析:由图可看出经历了“等压变化”→“等温变化”→“等容变化”后,又回到原来状态的是A、C。
AC
例.(多选)下列关于盖·吕萨克定律的说法中正确的是( )
A、对于一定质量的气体,在保持压强不变的情况下,温度每升高1℃时,其体积的增量是原来体积的1/273
B、对于一定质量的气体.在保持压强不变的情况下,温度每升高1℃时,其体积的增量是它在0℃时体积的1/273
C、对于一定质量的气体,在保持压强不变的情况下,其体积与温度成正比
D、对于一定质量的气体,在保持压强不变的情况下,其体积与热力学温度成正比
BD
【例题】如图所示,封闭有一定质量理想气体的汽缸开口向下竖直固定放置,活塞的截面积为S,质量为m0,活塞通过轻绳连接了一个质量为m的重物。若开始时汽缸内理想气体的温度为T0,轻绳刚好伸直且对活塞无拉力作用,外界大
气压强为p0,一切摩擦均不计且m0g
(2)重物刚离地时汽缸内气体的温度。
解析:
(1)当轻绳刚好伸直且对活塞无拉力作用时,设此时汽缸内气体的压强为p1,
由力的平衡条件可得m0g+p1S=p0S 所以
当重物刚好离开地面时,设此时汽缸内气体的压强为p2,
则有p2S+(m+m0)g=p0S 所以
(2)设重物刚好离开地面时汽缸内气体的温度为T1,
此过程气体发生等容变化,由查理定律可得
解得
解析:
【例题】如图所示,两端封闭、粗细均匀、竖直放置的玻璃管内,有一长为h的水银柱,将管内气体分为两部分,已知l2=2l1。若使两部分气体同时升高相同的温度,管内水银柱将如何运动?(设原来温度相同)
水银柱原来处于平衡状态,所受合外力为零,即此时两部分气体的压强差Δp=p1-p2=ph。温度升高后,两部分气体的压强都增大,若Δp1>Δp2,水银柱所受合外力方向向上,应向上移动,若Δp1<Δp2,水银柱向下移动,若Δp1=Δp2,水银柱不动。所以判断水银柱怎样移动,就是分析其合外力方向,即判断两部分气体的压强哪一个增大得多。
假设水银柱不动,两部分气体都做等容变化,分别对两部分气体应用查理定律:
上段
同理,下段
所以Δp1>Δp2,即水银柱上移。
例.如图所示,气缸内封闭有一定质量的理想气体,当时温度为0℃,大气压为1atm(设其值为105Pa)、气缸横截面积为500cm2,活塞重为5000N。则:
(1)气缸内气体压强为多少?
(2)如果开始时内部被封闭气体的总体积为 汽缸上部体积为 ,并且汽缸口有个卡环可以卡住活塞,使之只能在汽缸内运动,所有摩擦不计。现在使气缸内的气体加热至273℃,求气缸内气体压强又为多少?
30°
解:
(1)由受力平衡可知:
(2)缸内气体先做等压变化,活塞将运动到卡环处就不再运动,设此时温度为T1 ,有
所以
接下来继续升温,气缸内气体将做等体积变化,设所求压强为p2,故有
代入可得
30°
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
