第五单元课题1质量守恒律-2022-2023学年九年级化学人教版上册(共47张PPT)
文档属性
| 名称 | 第五单元课题1质量守恒律-2022-2023学年九年级化学人教版上册(共47张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-24 00:00:00 | ||
图片预览








文档简介
(共47张PPT)
1
课题1:
质量守恒律
?
化学反应的实质:
知识回顾
有新物质生成
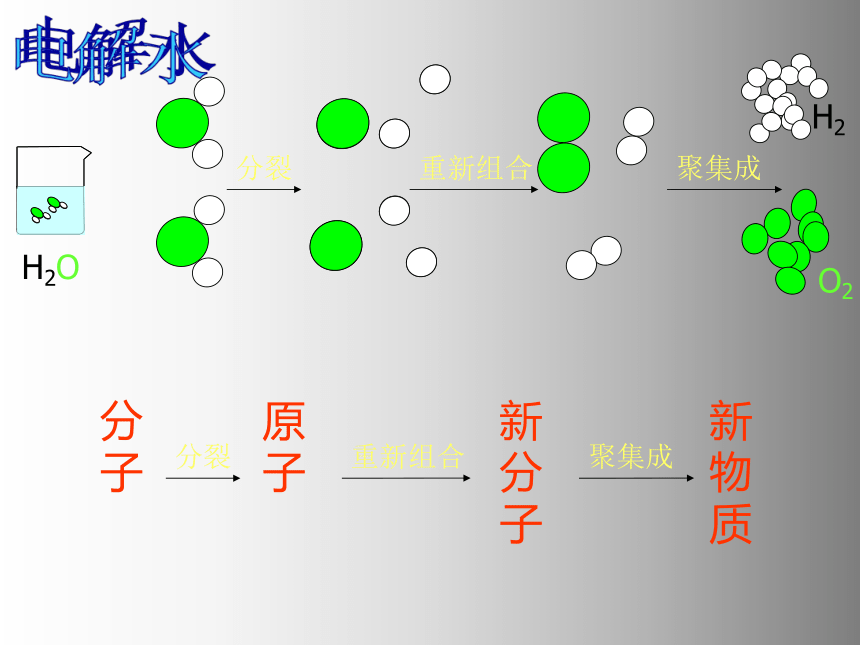
由分子构成的物质发生化学变化时
分 子
分裂
原 子
聚集成
新物质
新分子
重新组合
分裂
重新组合
聚集成
H2
O2
H2O
电解水
4
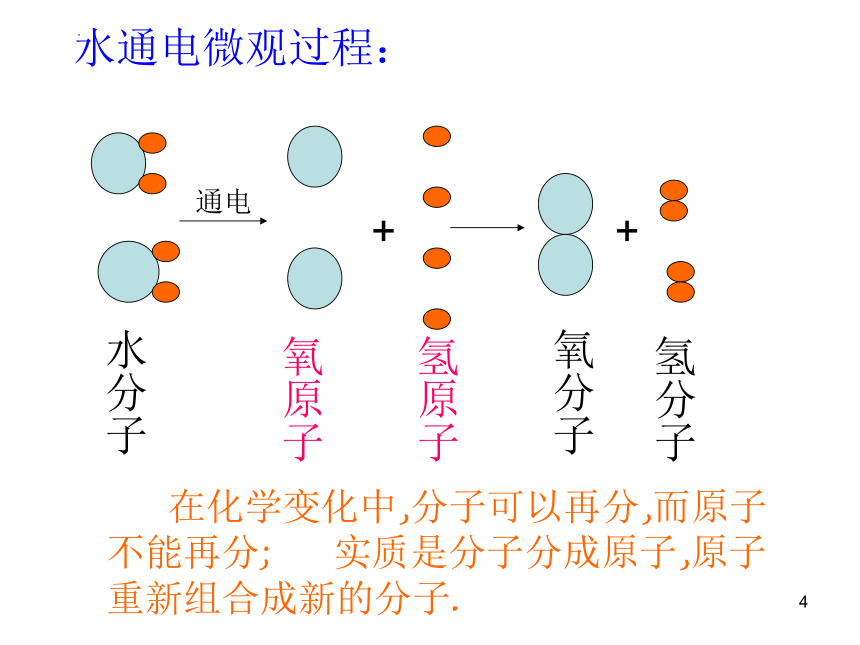
通电
+
+
氧原子
氢原子
氧分子
氢分子
水分子
水通电微观过程:
在化学变化中,分子可以再分,而原子不能再分; 实质是分子分成原子,原子重新组合成新的分子.
5
思考
在生成新物质以后,物质的总质量,跟反应前相比,是否发生改变呢?请同学们大胆的猜想……
反应物的质量总和 生成物的质量总和
等于
大于
小于
7
分组实验
方案一:白磷燃烧
方案二:铁钉与硫酸铜溶液反应
注意观察(1)反应物和生成物状态及变化、现象(2)质量的变化
8
演示实验1:
白磷燃烧前后质量的测定:
(1)在锥形瓶中放一小块白磷
(2)称量锥形瓶内物质的总质量
(3)点燃白磷,观察产生的现象为:
产生大量白烟,放热
(4)冷却后称量锥形瓶内物质的总质量
9
白磷在燃烧前后质量没发生变化,你能解释原因吗?
白磷燃烧前后质量的测定
10
对比思考:
反应前物质(或物体)
反应后物质(或物体)
锥形瓶
细砂
橡皮塞
玻璃管、气球
(空气)
氧气
氮气
白磷
锥形瓶
细砂
橡皮塞
玻璃管、气球
五氧化二磷
(剩余气体)
氮气
白磷质量+氧气质量=五氧化二磷质量
稀有气体等
稀有气体等
白磷
五氧化二磷
氧气
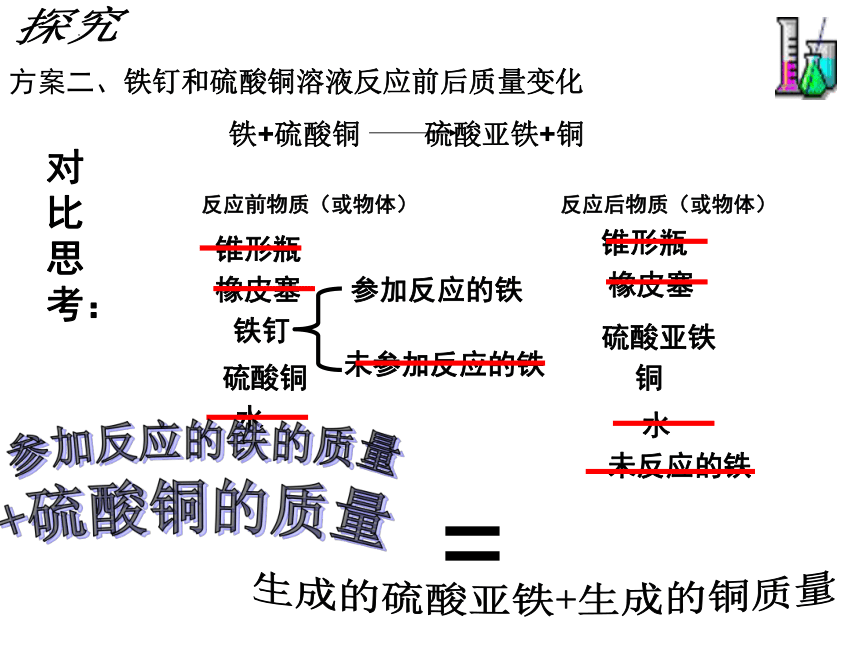
方案二、铁钉和硫酸铜溶液反应前后质量变化
探究
对比思考:
反应前物质(或物体)
反应后物质(或物体)
锥形瓶
橡皮塞
铁钉
硫酸铜
水
锥形瓶
橡皮塞
铁+硫酸铜 硫酸亚铁+铜
硫酸亚铁
铜
水
未反应的铁
未参加反应的铁
参加反应的铁
=
参加反应的铁的质量
生成的硫酸亚铁+生成的铜质量
+硫酸铜的质量
12
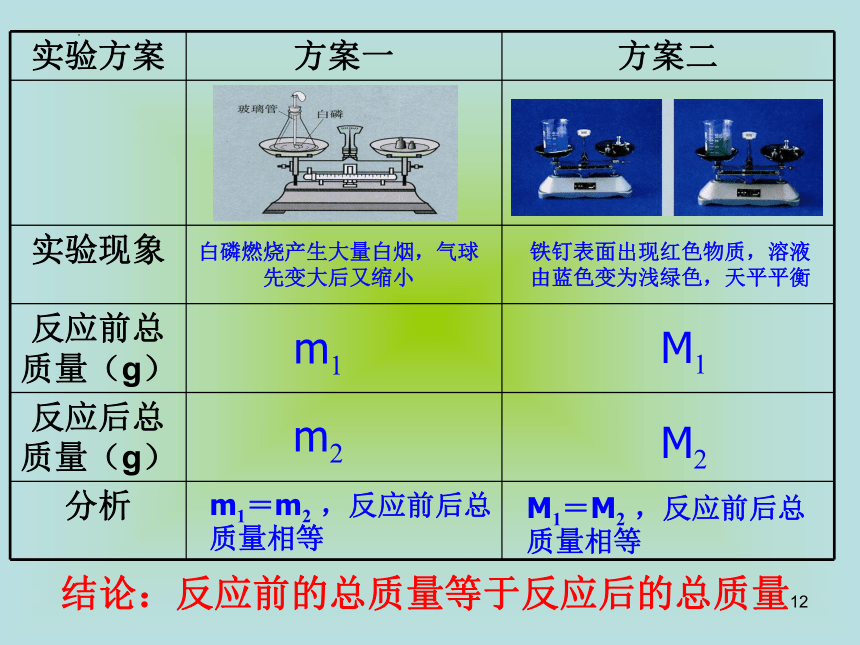
实验方案 方案一 方案二
实验现象
反应前总质量(g)
反应后总质量(g)
分析
m1
铁钉表面出现红色物质,溶液
由蓝色变为浅绿色,天平平衡
m2
M1
M2
m1=m2 ,反应前后总质量相等
M1=M2 ,反应前后总质量相等
白磷燃烧产生大量白烟,气球先变大后又缩小
结论:反应前的总质量等于反应后的总质量
13
一、质量守恒定律:
1、内容:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
板书
你能写出吗?
P+O2 P2O5
点燃
Fe+CuSO4 Cu+FeSO4
分析讨论:该定律内容有几处关键词?
1. 适用于 “一切化学反应”,不适用于物理变化。
2. 仅是指“质量”守恒,而不指其它物理量。如体积是不一定守恒。
指反应或生成的“各种物质”,包括固体、 液体、气体都要考虑。
指“参加”反应的物质,未反应完的物质不计算在内。
温馨小提示
再次探究:
二、镁条燃烧
一、碳酸钠跟稀盐酸反应
16
2. 取一根用砂纸打磨干净的长镁条和一个石棉网,将它们一起放在托盘天平上称量,记录所盛的质量。
在石棉网上方将镁条点燃,将镁条燃烧后的产物与石棉网一起放在托盘天平上称量,比较反应前后的质量。
17
2 如果在燃着镁条上方罩上玻璃罩,使生成物全部收集起来称量,会出现什么实验结果?
1 上述两个实验为什么会出现这样的实验结果?
讨论
名称 ③镁条燃烧 ④碳酸钠粉末与稀盐酸反应
现象
表达式
结果
分析
发出耀眼的白光,生成一种白色固体,天平不平衡
有气泡出现,天平不平衡
镁 + 氧气 → 氧化镁
点燃
碳酸钠+盐酸→氯化钠+水+二氧化碳
反应后物质的总质量改变了
反应后物质的总质量减少
参加反应的氧气的质量没有称量,有少量的氧化镁粉末散发到空气中
生成的二氧化碳气体跑掉了
讨论:
1、以上两个反应是否遵守质量守恒定律?
2、如何改进装置,才能把生成的气体也收集起来进行称量呢?
汇报交流、展示
优化实验方案、再次探究
改进后的装置
结 果
分 析
对有气体参与或有气体生成的反应,作定量研究时,需用密闭装置。
天平仍平衡,物质总质量不变
参加反应的镁和氧气的质量等于反应后生成的氧化镁的质量;
参加反应的碳酸钠和盐酸的质量等于反应后生成的氯化钠、水和二氧化碳的质量。
21
见课本实验图中,
玻璃管上不套气球,天平仍会平衡吗?为什么?
不平衡,因为白磷与氧气的总质量与生成的五氧化二磷的质量相等,但有部分五氧化二磷跑到空气中去了,所以不平衡。
22
板书
Na2CO3+HCl
Mg+O2 MgO
点燃
2、适用范围:适用于一切化学反应。
一切化学变化都可以用质量守恒定律来解释!
NaCl+CO2+H2O
想一想
想一想
为什么化学反应前后的各物质的质量总和相等呢?
24
从分子和原子观点来看
在一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。
25
原子数目没有增减
原子种类没有改变
原子质量没有变化
化学反应前后质量守恒的原因
26
元素种类变了吗?
元素质量变了吗?
物质的总质量呢?
化学反应前后
物质种类呢?
分子种类呢?
动动脑
不变
改变
27
原子数目
原子质量
原子种类
微观
物质的总质量
元素质量
元素种类
六不变
物质的种类
分子的种类
改变
宏观
分子个数可能发生改变
质量守恒定律参加化学反应前后
28
练习:1.在化学反应前后,下列粒子的总数可能变的是( )
A.质子 B.原子
C.电子 D.分子
2:在化学反应前后下列微粒可能变的是( )
A:分子个数 B:原子种类
C:元素种类 D原子个数
D
A
29
3:参加反应的各物质质量总和等于反应后生成的各物质质量总和,是因为 [ ]。
A.反应后物质的种类没有变化
B.反应后分子的种类没有变化
C.反应后原子的种类、数目和质量没有变化
D.反应后分子的种类、数目和质量没有变化
C
说明了反应前后原子种类,数目和质量没有变化,物质种类和分子个数可能要发生变化
30
4:质量守恒定律成立的原因是( )
① 原子的数目没有增减 ② 原子的种类没有改变③ 化学反应前后物质总质量相等 ④ 原子的质量没有改变
A.①②③④
B.①②③
C.②③④
D.①②④
A
31
质量守恒定律的使用范围是什么?学了该定律,对我们有什么用?
质量守恒定律适用于一切化学反应
可运用定律 1. 进行有关的计算
2. 推测一些物质的组成
3. 解释一些实验事实
质量守恒定律的应用
32
已知蜡烛的的主要成分是石蜡。由蜡烛燃烧后生成水和二氧化碳的实验事实,判断石蜡中一定含有哪些元素?
答案:蜡烛燃烧后生成了H2O和CO2,根据质量守恒定律,产物中有C、H、O三种元素,说明反应物中也应含有这三种元素。反应物是石蜡和氧气,氧气由氧元素组成,那么石蜡中肯定含有碳和氢两种元素。
一:推断出一些物质的组成
1.某大师说他能发功使铝(Al)发生化学变化变成黄金(Au)。他的说法是否有科学道理?
没有。化学反应前后,原子和元素种类不变。
34
二:根据质量守恒定律解释下列实验现象
例:(1)镁条在空气中燃烧后,生成的白色粉末的质量比原来镁条的质量增加。
答:(1)镁条燃烧后生成物的质量增加,是由于镁条在空气中燃烧时与空气中的氧气发生了化学反应,生成了白色固体物质氧化镁:Mg+O2
点燃
MgO
显然,依据质量守恒定律生成物氧化镁的质量应等于反应物镁条与氧气的质量之和。所以,氧化镁的质量要比镁条的质量大。
35
生活空间 化学无限
二、你能用质量守恒定律解释吗
1、 细铁丝在氧气中燃烧后,生成物的质量
比细铁丝的质量大。
2、加热氯酸钾与二氧化锰的混合物,剩余
的固体质量减少了。
因为细铁丝与氧气的质量和才等于生成的四氧化三铁的质量,所以生成物比细铁丝的质量大。
因为剩余的固体与生成的氧气质量和才等于反应前的质量,而氧气是气体跑掉,所以剩余的固体质量减少了。
36
随堂练习:
3、下列现象可用质量守恒定律解释的是( )
A、10g水受热变成10g水蒸气
B、纸在空气中燃烧后化为灰烬.灰烬的质量比纸的质量小
C、铁在空气中灼烧后,质量增加
D、蜡烛受热熔化,冷却后质量不变
4、根据质量守恒定律可以推知,铁丝在氧气中燃烧后,生成物的质量( )
A、一定等于铁丝的质量 B、—定小于铁丝的质量
C、—定大于铁丝的质量 D、无法确定质量大小
BC
C
5、A+B=C+D, 已知12gA和18gB恰好完全反应生成28gC,则生成的D的质量是( )
A、30g B、58g C、2g D、无法确定
C
37
6: 不能用质量守恒定律解释的是( )
A. 潮湿的衣服在阳光下晒干
B. 蜡烛燃烧越来越短
C. 铁丝烧后质量增加
D. 高锰酸钾受热后质量减小
A
38
随堂练习:
7、如右图所示,每两个甲分子反应后生成两个乙分子和一个丙分子,已知甲、乙、丙分别为不同种类的纯净物,则乙物质的化学式为( )
A、A2 B
B、AB2
C、AB
D、A4B2
A
+
甲
乙
丙
A原子
B原子
8、
39
判断题:
1:氯酸钾受热分解后,剩余固体比原反应物
轻,这不符合质量守恒定律 。 ( )
练习:
×
2:
根据质量守恒定律,水变成水蒸气,
质量保持不变。 ( )
Χ
3:煤球燃烧后质量减轻,这不符合质量守恒定律( )
×
40
练习:
则生成氧化镁
的质量为____克
24克镁与16克氧气恰好完全反应,
40
2. 6克碳与一定量的氧气恰好完全反应,
生成二氧化碳22克,有______克氧气
参加了反应。
16
三:根据质量守定律进行有关计算
41
1,加热10克氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52克,则生成氧气的质量为_____。
2,在化学反应A+B=C中,5克A的足量的B反应生成8克C,则参加反应的B的质量是______。
A 8克 B 5克, C 3克 D 2克
课堂发散题
0.48克
C
42
想一想:可要利用质量守恒定律
1、在A+B=C+D反应中,5克A和4克B恰好完全反应生成3克C,则生成D的质量为( ) A 5克 B.3克 C.6克 D.4克 2、蜡烛在空气中燃烧后只生成CO2和H2O,试推断蜡烛一定由( ) A.碳元素组成 B.氢元素组成 C.碳氢氧元素组成 D.碳氢元素组成
43
2. 根据质量守恒定律,在4A+5B2=2X的反应中,X的化学式为( )
A.A2B5 B.AB2
C.A3B2 D.A4B5
3,已知一反应:2A2+3B2→2C,A,B为两元素符号,则C的化学式为( )
A. AB B. A2B3 C. A4B6 D. A3B2
A
D
44
无数实验证明:______________的
各物质的________,等于反应后生成的
各物质的_________,这个规律叫做
质量守恒定律。这是因为化学反应前后,
_______没有改变,______没有增减,
______没有变化,只有反应中的____
重新组。合成其它物质
参加化学反应
巩固练习:
质量总和
质量总和
原子种类
原子数目
原子质量
原子
45
原子数目没有增减
原子种类没有改变
原子质量没有变化
推测一些物质的组成
进行有关的计算
解释一些实验事实
内容
内容
原因
原因
应用
应用
质量守恒定律
质量守恒定律
小结
小结
参加化学反应的各物质
生成的各物质的质量总和
的质量总和等于反应后
46
活动与探究
1.取一支蜡烛粘在一小块玻璃片上,将玻璃片和蜡烛一起放在托盘天平上称量。点燃蜡烛,天平会发生什么变化?
1.小明说蜡烛燃烧后质量变小,这一事实不符合质量守恒定律,你认为对吗?为什么?
不对。蜡烛燃烧后生成的CO2和H2O跑掉了,所以蜡烛燃烧后质量变小,仍符合质量守恒定律。
47
讨论
(1)上面两个实验的结果与你实验前的预测相同吗?为什么会出现这样的实验结果?
(2)如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?
(3)以碳在氧气中燃烧生成二氧化碳为例,从化学反应中分子、原子的变化情况说明化学反应必定符合质量守恒定律。
1
课题1:
质量守恒律
?
化学反应的实质:
知识回顾
有新物质生成
由分子构成的物质发生化学变化时
分 子
分裂
原 子
聚集成
新物质
新分子
重新组合
分裂
重新组合
聚集成
H2
O2
H2O
电解水
4
通电
+
+
氧原子
氢原子
氧分子
氢分子
水分子
水通电微观过程:
在化学变化中,分子可以再分,而原子不能再分; 实质是分子分成原子,原子重新组合成新的分子.
5
思考
在生成新物质以后,物质的总质量,跟反应前相比,是否发生改变呢?请同学们大胆的猜想……
反应物的质量总和 生成物的质量总和
等于
大于
小于
7
分组实验
方案一:白磷燃烧
方案二:铁钉与硫酸铜溶液反应
注意观察(1)反应物和生成物状态及变化、现象(2)质量的变化
8
演示实验1:
白磷燃烧前后质量的测定:
(1)在锥形瓶中放一小块白磷
(2)称量锥形瓶内物质的总质量
(3)点燃白磷,观察产生的现象为:
产生大量白烟,放热
(4)冷却后称量锥形瓶内物质的总质量
9
白磷在燃烧前后质量没发生变化,你能解释原因吗?
白磷燃烧前后质量的测定
10
对比思考:
反应前物质(或物体)
反应后物质(或物体)
锥形瓶
细砂
橡皮塞
玻璃管、气球
(空气)
氧气
氮气
白磷
锥形瓶
细砂
橡皮塞
玻璃管、气球
五氧化二磷
(剩余气体)
氮气
白磷质量+氧气质量=五氧化二磷质量
稀有气体等
稀有气体等
白磷
五氧化二磷
氧气
方案二、铁钉和硫酸铜溶液反应前后质量变化
探究
对比思考:
反应前物质(或物体)
反应后物质(或物体)
锥形瓶
橡皮塞
铁钉
硫酸铜
水
锥形瓶
橡皮塞
铁+硫酸铜 硫酸亚铁+铜
硫酸亚铁
铜
水
未反应的铁
未参加反应的铁
参加反应的铁
=
参加反应的铁的质量
生成的硫酸亚铁+生成的铜质量
+硫酸铜的质量
12
实验方案 方案一 方案二
实验现象
反应前总质量(g)
反应后总质量(g)
分析
m1
铁钉表面出现红色物质,溶液
由蓝色变为浅绿色,天平平衡
m2
M1
M2
m1=m2 ,反应前后总质量相等
M1=M2 ,反应前后总质量相等
白磷燃烧产生大量白烟,气球先变大后又缩小
结论:反应前的总质量等于反应后的总质量
13
一、质量守恒定律:
1、内容:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
板书
你能写出吗?
P+O2 P2O5
点燃
Fe+CuSO4 Cu+FeSO4
分析讨论:该定律内容有几处关键词?
1. 适用于 “一切化学反应”,不适用于物理变化。
2. 仅是指“质量”守恒,而不指其它物理量。如体积是不一定守恒。
指反应或生成的“各种物质”,包括固体、 液体、气体都要考虑。
指“参加”反应的物质,未反应完的物质不计算在内。
温馨小提示
再次探究:
二、镁条燃烧
一、碳酸钠跟稀盐酸反应
16
2. 取一根用砂纸打磨干净的长镁条和一个石棉网,将它们一起放在托盘天平上称量,记录所盛的质量。
在石棉网上方将镁条点燃,将镁条燃烧后的产物与石棉网一起放在托盘天平上称量,比较反应前后的质量。
17
2 如果在燃着镁条上方罩上玻璃罩,使生成物全部收集起来称量,会出现什么实验结果?
1 上述两个实验为什么会出现这样的实验结果?
讨论
名称 ③镁条燃烧 ④碳酸钠粉末与稀盐酸反应
现象
表达式
结果
分析
发出耀眼的白光,生成一种白色固体,天平不平衡
有气泡出现,天平不平衡
镁 + 氧气 → 氧化镁
点燃
碳酸钠+盐酸→氯化钠+水+二氧化碳
反应后物质的总质量改变了
反应后物质的总质量减少
参加反应的氧气的质量没有称量,有少量的氧化镁粉末散发到空气中
生成的二氧化碳气体跑掉了
讨论:
1、以上两个反应是否遵守质量守恒定律?
2、如何改进装置,才能把生成的气体也收集起来进行称量呢?
汇报交流、展示
优化实验方案、再次探究
改进后的装置
结 果
分 析
对有气体参与或有气体生成的反应,作定量研究时,需用密闭装置。
天平仍平衡,物质总质量不变
参加反应的镁和氧气的质量等于反应后生成的氧化镁的质量;
参加反应的碳酸钠和盐酸的质量等于反应后生成的氯化钠、水和二氧化碳的质量。
21
见课本实验图中,
玻璃管上不套气球,天平仍会平衡吗?为什么?
不平衡,因为白磷与氧气的总质量与生成的五氧化二磷的质量相等,但有部分五氧化二磷跑到空气中去了,所以不平衡。
22
板书
Na2CO3+HCl
Mg+O2 MgO
点燃
2、适用范围:适用于一切化学反应。
一切化学变化都可以用质量守恒定律来解释!
NaCl+CO2+H2O
想一想
想一想
为什么化学反应前后的各物质的质量总和相等呢?
24
从分子和原子观点来看
在一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。
25
原子数目没有增减
原子种类没有改变
原子质量没有变化
化学反应前后质量守恒的原因
26
元素种类变了吗?
元素质量变了吗?
物质的总质量呢?
化学反应前后
物质种类呢?
分子种类呢?
动动脑
不变
改变
27
原子数目
原子质量
原子种类
微观
物质的总质量
元素质量
元素种类
六不变
物质的种类
分子的种类
改变
宏观
分子个数可能发生改变
质量守恒定律参加化学反应前后
28
练习:1.在化学反应前后,下列粒子的总数可能变的是( )
A.质子 B.原子
C.电子 D.分子
2:在化学反应前后下列微粒可能变的是( )
A:分子个数 B:原子种类
C:元素种类 D原子个数
D
A
29
3:参加反应的各物质质量总和等于反应后生成的各物质质量总和,是因为 [ ]。
A.反应后物质的种类没有变化
B.反应后分子的种类没有变化
C.反应后原子的种类、数目和质量没有变化
D.反应后分子的种类、数目和质量没有变化
C
说明了反应前后原子种类,数目和质量没有变化,物质种类和分子个数可能要发生变化
30
4:质量守恒定律成立的原因是( )
① 原子的数目没有增减 ② 原子的种类没有改变③ 化学反应前后物质总质量相等 ④ 原子的质量没有改变
A.①②③④
B.①②③
C.②③④
D.①②④
A
31
质量守恒定律的使用范围是什么?学了该定律,对我们有什么用?
质量守恒定律适用于一切化学反应
可运用定律 1. 进行有关的计算
2. 推测一些物质的组成
3. 解释一些实验事实
质量守恒定律的应用
32
已知蜡烛的的主要成分是石蜡。由蜡烛燃烧后生成水和二氧化碳的实验事实,判断石蜡中一定含有哪些元素?
答案:蜡烛燃烧后生成了H2O和CO2,根据质量守恒定律,产物中有C、H、O三种元素,说明反应物中也应含有这三种元素。反应物是石蜡和氧气,氧气由氧元素组成,那么石蜡中肯定含有碳和氢两种元素。
一:推断出一些物质的组成
1.某大师说他能发功使铝(Al)发生化学变化变成黄金(Au)。他的说法是否有科学道理?
没有。化学反应前后,原子和元素种类不变。
34
二:根据质量守恒定律解释下列实验现象
例:(1)镁条在空气中燃烧后,生成的白色粉末的质量比原来镁条的质量增加。
答:(1)镁条燃烧后生成物的质量增加,是由于镁条在空气中燃烧时与空气中的氧气发生了化学反应,生成了白色固体物质氧化镁:Mg+O2
点燃
MgO
显然,依据质量守恒定律生成物氧化镁的质量应等于反应物镁条与氧气的质量之和。所以,氧化镁的质量要比镁条的质量大。
35
生活空间 化学无限
二、你能用质量守恒定律解释吗
1、 细铁丝在氧气中燃烧后,生成物的质量
比细铁丝的质量大。
2、加热氯酸钾与二氧化锰的混合物,剩余
的固体质量减少了。
因为细铁丝与氧气的质量和才等于生成的四氧化三铁的质量,所以生成物比细铁丝的质量大。
因为剩余的固体与生成的氧气质量和才等于反应前的质量,而氧气是气体跑掉,所以剩余的固体质量减少了。
36
随堂练习:
3、下列现象可用质量守恒定律解释的是( )
A、10g水受热变成10g水蒸气
B、纸在空气中燃烧后化为灰烬.灰烬的质量比纸的质量小
C、铁在空气中灼烧后,质量增加
D、蜡烛受热熔化,冷却后质量不变
4、根据质量守恒定律可以推知,铁丝在氧气中燃烧后,生成物的质量( )
A、一定等于铁丝的质量 B、—定小于铁丝的质量
C、—定大于铁丝的质量 D、无法确定质量大小
BC
C
5、A+B=C+D, 已知12gA和18gB恰好完全反应生成28gC,则生成的D的质量是( )
A、30g B、58g C、2g D、无法确定
C
37
6: 不能用质量守恒定律解释的是( )
A. 潮湿的衣服在阳光下晒干
B. 蜡烛燃烧越来越短
C. 铁丝烧后质量增加
D. 高锰酸钾受热后质量减小
A
38
随堂练习:
7、如右图所示,每两个甲分子反应后生成两个乙分子和一个丙分子,已知甲、乙、丙分别为不同种类的纯净物,则乙物质的化学式为( )
A、A2 B
B、AB2
C、AB
D、A4B2
A
+
甲
乙
丙
A原子
B原子
8、
39
判断题:
1:氯酸钾受热分解后,剩余固体比原反应物
轻,这不符合质量守恒定律 。 ( )
练习:
×
2:
根据质量守恒定律,水变成水蒸气,
质量保持不变。 ( )
Χ
3:煤球燃烧后质量减轻,这不符合质量守恒定律( )
×
40
练习:
则生成氧化镁
的质量为____克
24克镁与16克氧气恰好完全反应,
40
2. 6克碳与一定量的氧气恰好完全反应,
生成二氧化碳22克,有______克氧气
参加了反应。
16
三:根据质量守定律进行有关计算
41
1,加热10克氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52克,则生成氧气的质量为_____。
2,在化学反应A+B=C中,5克A的足量的B反应生成8克C,则参加反应的B的质量是______。
A 8克 B 5克, C 3克 D 2克
课堂发散题
0.48克
C
42
想一想:可要利用质量守恒定律
1、在A+B=C+D反应中,5克A和4克B恰好完全反应生成3克C,则生成D的质量为( ) A 5克 B.3克 C.6克 D.4克 2、蜡烛在空气中燃烧后只生成CO2和H2O,试推断蜡烛一定由( ) A.碳元素组成 B.氢元素组成 C.碳氢氧元素组成 D.碳氢元素组成
43
2. 根据质量守恒定律,在4A+5B2=2X的反应中,X的化学式为( )
A.A2B5 B.AB2
C.A3B2 D.A4B5
3,已知一反应:2A2+3B2→2C,A,B为两元素符号,则C的化学式为( )
A. AB B. A2B3 C. A4B6 D. A3B2
A
D
44
无数实验证明:______________的
各物质的________,等于反应后生成的
各物质的_________,这个规律叫做
质量守恒定律。这是因为化学反应前后,
_______没有改变,______没有增减,
______没有变化,只有反应中的____
重新组。合成其它物质
参加化学反应
巩固练习:
质量总和
质量总和
原子种类
原子数目
原子质量
原子
45
原子数目没有增减
原子种类没有改变
原子质量没有变化
推测一些物质的组成
进行有关的计算
解释一些实验事实
内容
内容
原因
原因
应用
应用
质量守恒定律
质量守恒定律
小结
小结
参加化学反应的各物质
生成的各物质的质量总和
的质量总和等于反应后
46
活动与探究
1.取一支蜡烛粘在一小块玻璃片上,将玻璃片和蜡烛一起放在托盘天平上称量。点燃蜡烛,天平会发生什么变化?
1.小明说蜡烛燃烧后质量变小,这一事实不符合质量守恒定律,你认为对吗?为什么?
不对。蜡烛燃烧后生成的CO2和H2O跑掉了,所以蜡烛燃烧后质量变小,仍符合质量守恒定律。
47
讨论
(1)上面两个实验的结果与你实验前的预测相同吗?为什么会出现这样的实验结果?
(2)如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?
(3)以碳在氧气中燃烧生成二氧化碳为例,从化学反应中分子、原子的变化情况说明化学反应必定符合质量守恒定律。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
